
- •ФІЗИЧНА ТА КОЛОЇДНА ХІМІЯ
- •КИЇВ НУХТ 2012
- •ВСТУП
- •Лабораторна робота № 1
- •Теоретичні відомості
- •Поверхневий натяг розчинів оцтової кислоти
- •Лабораторна робота № 8
- •Прилади, лабораторний посуд та реактиви
- •Опрацювання результатів
- •Таблиця 8.1
- •Результати розрахунку адсорбції на межі поділу тверде тіло – рідина
- •Номери
- •Лабораторна робота № 9
- •Теоретичні відомості
- •Прилади, лабораторний посуд, реактиви
- •Перевірка на ефект Тіндаля
- •Одержання емульсії типу М/В
- •Одержання емульсії типу В/М
- •Одержання емульсій, стабілізованих порошками
- •Емульсії соняшникової олії у воді
- •Опрацювання результатів
- •Лабораторна робота № 10
- •Теоретичні відомості
- •Швидкість електрофоретичного перенесення визначають за рівнянням:
- •Градієнт потенціалу дорівнює:
- •Прилади, лабораторний посуд, реактиви
- •Опрацювання результатів
- •Лабораторна робота № 11
- •Теоретичні відомості
- •Опрацювання результатів
- •Лабораторна робота № 12
- •Теоретичні відомості
- •Лабораторна робота № 12.1
- •Прилади, лабораторний посуд, реактиви
- •Опрацювання результатів
- •Лабораторна робота № 12.2
- •Опрацювання результатів
- •Результати дослідження кінетики набухання желатину
- •Залежність граничного набухання желатину від рН розчину
- •Порядок виконання роботи
- •Опрацювання результатів
- •Залежність граничного ступеня набухання желатину від рН розчину
- •Прилади, лабораторний посуд та реактиви
- •Опрацювання результатів
Таблиця 12.4
Залежність граничного набухання желатину від рН розчину
|
|
|
Концентрація соляної |
|
Буферні |
||
№ |
Дані |
|
|
кислоти |
|
|
суміші |
|
|
|
(нормальність) |
|
|
||
|
|
10-1 |
10-2 |
10-3 |
10-4 |
10-5 |
|
1 |
рН розчину |
1 |
2 |
3 |
4 |
5 |
6,8 9,18 |
2Граничний ступінь набухання
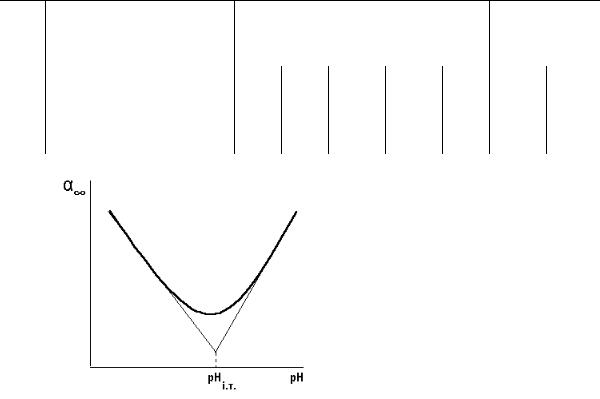
Рис. 12.2. Визначення ізоелектричної точки желатину
Варіант 2
Порядок виконання роботи
1.Шість близьких за масою платівок желатину зважують на торсійних терезах і записують їх початкову масу m0.
2.Кожну зважену платівку желатину опускають в бюкс, заповнений на 2/3 розчином з певним значенням рН. Платівку залишають для подальшого набухання на 40 хвилин.
3.Після набухання платівки виймають, висушують між листами фільтрувального паперу і знову зважують. Записують масу платівки желатину після набухання m.
Опрацювання результатів
1. Експериментальні дані заносять в таблицю 12.5.
Таблиця 12.5
Залежність граничного ступеня набухання желатину від рН розчину
|
|
|
Концентрація соляної |
|
Буферні суміші |
||||||
№ |
Дані |
|
|
|
кислоти |
|
|
|
|
|
|
|
|
|
|
(нормальність) |
|
|
|
||||
|
|
10-1 |
|
10-2 |
10-3 |
|
10-4 |
|
10-5 |
|
|
85

1 |
рН розчину |
1 |
2 |
3 |
4 |
5 |
6,8 |
9,18 |
2 |
Маса платівок до |
|
|
|
|
|
|
|
|
набухання, m0, мг |
|
|
|
|
|
|
|
3Маса платівок після набухання, m, мг
4Граничний ступінь набухання,
a¥ = m - m0 m0
2. Будують криву залежності граничного ступеня набухання від. рН Ізотерма набухання в ізоелектричній точці проходить через мінімум. Проводять дотичні до початкової та кінцевої ділянок графіка. Перпендикуляр, опущений на вісь абсцис з точки перетину двох дотичних кривої набухання, вказує ізоелектричну точку рН желатину (рНіт) (рис. 12.2).
Питання для самоперевірки
1.Дайте визначення високомолекулярних речовин. Природні та синтетичні ВМС, приклади.
2.Які особливості будови молекул ВМС?
3.Які властивості розчинів ВМС притаманні істинним, а які колоїдним розчинам? Які специфічні властивості розчинів ВМС?
4.Що таке набухання? Обмежене та необмежене набухання, приклади.
5.Що називається ступенем набухання? Як його можна розрахувати?
6.Охарактеризуйте чотири стадії набухання.
7. Наведіть рівняння, що описує швидкість набухання. Охарактеризуйте графічний метод знаходження граничного ступеня набухання та константи швидкості набухання.
8.Що таке граничний ступінь набухання? Як його можна визначити?
9.Ваговий метод визначення ступеня набухання.
10.Як розраховують швидкість набухання?
11.Які чинники впливають на набухання ВМС?
12.Охарактеризувати вплив на набухання ВМС природи полімера та розчинника, в’язкості розчинника, молекулярної маси ВМС.
13.Як впливає температура на швидкість та ступінь набухання?
14.Як впливає рН середовища на набухання ВМС?
15.Що таке ізоелектричний стан білка? Як визначити ізоелектричну точку желатину за ступенем набухання?
16.Що називається висолюванням? Його вплив на набухання ВМС.
17.Охарактеризувати вплив додавання спирту в розчин на ступінь набухання желатину.
86
Лабораторна робота № 13
ВИЗНАЧЕНЯ ЗВ`ЯЗАНОЇ ВОДИ ІНДИКАТОРНИМ РЕФРАКТОМЕТРИЧНИМ МЕТОДОМ
Мета роботи – ознайомлення з методикою визначення кількості води, що зв`язується гідрофільними ВМС.
Теоретичні відомості
Зв`язаною вважається вода, розташована на межі поділу фаз і приєднана до макромолекул ВМС за механізмом водневого зв. ’язкуГідрофільними називають ВМС, що утворюють водневий зв`язок з водою. З усіх видів міжмолекулярної взаємодії Н-зв`язок є найміцнішим і його енергія досягає20– 30 кДж/моль води. Тому властивості води, зв`язаної ВМС, відрізняються від властивостей вільної води.
Властивості ВМС значною мірою залежать від вмісту зв’язаної та вільної води, тобто від наявних форм зв’язку води з полімерами. Вода має різні види зв’язку із високомолекулярними речовинами: від самого міцного, обумовленого молекулярними силами, до чисто механічного утримання вологи на поверхні дисперсних частинок.
Зв’язана вода має наступні відмінні властивості. Вона замерзає при більш низьких температурах, які можуть досягати–15¸–20 0С. Густина і в’язкість зв’язаної води більші, ніж у вільної води, а діелектрична проникність – менша. Зв’язана вода не може бути розчинником для інших речовин.
Особливою властивістю зв’язаної води є її дуже слабка рухливість, що обумовлює здатність набухлих білкових драглів зберігати форму.
Кількість зв’язаної води визначається гідрофільністю ВМС. Гідрофільність – це кількість зв’язаної води, що припадає на100 г
абсолютно сухої речовини ВМС.
Чим вища спорідненість макромолекули ВМС до води, т м вища їх гідрофільність і тим більше зв’язаної води містить ВМС. Так, в желатині кількість зв’язаної води у два рази вище маси сухої речовини, а в агар-агарі – в чотири рази.
Методи визначення кількості зв`язаної води базуються на використанні її властивостей. Зв`язану воду визначають за теплотою змочування ВМС, за густиною зв`язаної води, за діелектричною проникністю, за зниженням температури замерзання, за властивістю зв’язаної води не бути розчинником для інших речовин.
Найбільш розповсюдженим методом визначення зв’язаної води є індикаторно-рефрактометричний. Суть цього методу полягає в тому, що вода, зв`язана гідрофільними ВМС, не є розчинником для інших речовин. Якщо в розчин сахарози концентрацієюС0 внести наважку сухого крохмалю, концентрація розчину підвищиться до концентраціїСр внаслідок вибіркової адсорбції крохмалю до води. Отже, розчин сахарози показує (індукує) на цю
87
