
- •Львівський національний медичний університет
- •Загальні правила техніки безпеки при роботі студентів у навчальній хімічній лабораторії
- •Модуль 2. Загальні закономірності метаболізму Тематичний план практичних занять з модуля 2
- •Тематичний план лекцій з модуля 2
- •Завдання для самостійної роботи студентів (срс)
- •Вимоги до виконання та перевірки самостійної роботи студентів (срс)
- •Методика проведення та критерії оцінювання підсумкового модульного контролю
- •Модуль 2. Загальні закономірності метаболізму.
- •Теоретичні питання
- •Наукові напрями роботи кафедри біохімії
- •Характеристика фізико-хімічних методів дослідження
- •Загальні принципи клініко-біохімічної оцінки результатів досліджень
- •Помилки, що трапляються під час проведення лабораторних досліджень
- •Практична робота Визначення оптичної густини забарвлених розчинів у залежності від їх концентрації.
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Дослід 2. Дослідження термолабільності амілази слини.
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •1/16 Мл сечі розщеплює 2 мл 0,1 %-го розчину крохмалю;
- •1Мл сечі розщеплює - х мл 0,1 %-го розчину крохмалю,
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •А. Амілази, ліпази, фосфатази
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •А. Ацетил-КоА
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •1. Дослідження дії якого з перерахованих ферментів базується на знебарвленні бензидину при його окисненні?
- •3. За яких умов відбувається забарвлення пірокатехіну при окисненні його молекулярним киснем в присутності фенолоксидази:
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів.
- •Література
- •Теоретичні питання
- •Практична робота Дослід 1. Вивчення окисного фосфорилування в мітохондріях та дії роз’єднувача – 2,4-динітрофенолу на цей процес.
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •2. Універсальність хеміоосмотичної теорії для живих систем. Література
- •Теоретичні питання
- •Приклади тестового контролю знань.
- •А. Аконітатгідратази
- •Приклади тестів та ситуаційних задач по засвоєнню практичних навичок
- •Література Основна:
- •Модуль 3. Метаболізм Вуглеводів, ліпідів, амінокислот та його регуляція
- •Тематичний план лекцій з модуля 3
- •Завдання для самостійної роботи студентів (срс)
- •Критерії оцінювання поточної навчальної діяльності студента
- •Методика проведення та критерії оцінювання підсумкового модульного контролю
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок -1”
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Принцип методу. В результаті реакції креатиніну і пікринової кислоти в лужному середовищі утворюється кольорова сполука, інтенсивність забарвлення якої прямопропорційна концентрації креатиніну.
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Тема № 9. Дослідження процесів детоксикації аміаку та біосинтезу сечовини.
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Самостійна індивідуальна робота студентів
- •Література
- •Теоретичні питання
- •Приклади тестового контролю знань „Крок 1”
- •Приклади тестів та ситуаційних задач по засвоєнню практичних навичок
- •Література
Теоретичні питання
Біологічне окиснення субстратів в клітинах.
Реакції біологічного окиснення та їх функціональне значення:
дегідрогеназні,
оксидазні,
оксигеназні (моно- та діоксигеназні).
Піридинзалежні дегідрогенази. Будова НАД+ і НАДФ+. Їх значення у реакціях окиснення та відновлення.
Флавінзалежні дегідрогенази. Будова ФАД і ФМН. Їх роль у реакціях окиснення та відновлення.
Убіхінон, будова та його роль у реакціях окиснення та відновлення.
Цитохроми та їх роль у тканинному диханні. Будова їх простетичної групи.
Молекулярна організація ланцюга транспорту електронів (дихального ланцюга) мітохондрій:
компоненти дихального ланцюга мітохондрій;
послідовність переносників електронів в дихальному ланцюгу;
роль редокс-потенціалів у транспорті електронів і протонів.
Надмолекулярні комплекси дихального ланцюга внутрішніх мембран мітохондрій.
Шляхи включення відновлювальних еквівалентів (електронів та протонів) у дихальний ланцюг мітохондрій (повний та вкорочений дихальні ланцюги).
Шляхи утворення АТФ в клітинах – субстратне та окисне фосфорилування (визначення, приклади).
Практична робота
Дослід 1. Дослідження дії фенолоксидази.
Принцип методу. Метод базується на явищі забарвлення пірокатехіну в разі окиснення його молекулярним киснем за присутності фенолоксидази.
Матеріальне забезпечення: розчин пірокатехіну, 2 г свіжої картоплі (джерело фенолоксидази), дистильована вода, розчин натрію сульфіду, ступка, штатив із пробірками, піпетки, водяна баня, термометр, газовий пальник.
Хід роботи. Одержання свіжого соку з картоплі: 1 – 2 г свіжої картоплі розтирають у ступці, додають 25 мл води, перемішують і зливають розчин у пробірку (ножем подрібнювати картоплю не можна, тому що іони заліза спричинюють потемніння).
У 4 пронумеровані пробірки наливають по 0,5 мл свіжого картопляного соку. У першу пробірку додають 0,5 мл пірокатехіну, у другу – 1 – 2 краплі інгібітора натрію сульфіду та 0,5 мл пірокатехіну. Вміст третьої пробірки кип’ятять, а потім вміщують 0,5 мл пірокатехіну. У четверту пробірку доливають 0,5 мл дистильованої води.
Усі пробірки ставлять на водяну баню на 30 хв при температурі 37° С. Вміст пробірок перемішують для кращого доступу кисню. Розчин першої пробірки забарвлюється внаслідок окиснення пірокатехіну киснем за присутності фенолоксидази. Колір розчинів у другій, третій, четвертій пробірках не змінюється.
Пояснити отриманий результат. Зробити висновок.
Дослід 2. Дослідження дії альдегіддегідрогенази.
Принцип методу. Метод базується на знебарвленні метиленового синього за умови його відновлення альдегідом у присутності ферменту альдегіддегідрогенази. Дегідрогеназа, що міститься в молоці, легко окиснює формальдегід у мурашину кислоту. При цьому відбувається перенесення водню на метиленовий синій, який знебарвлюється:
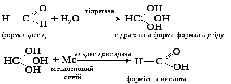
Матеріальне забезпечення: нейтралізований альдегід, розчин метиленового синього, молоко, штатив із пробірками, піпетки, водяна баня, термометр, газовий пальник.
Хід роботи. Готують 3 пронумеровані пробірки. В першу наливають 1 мл молока, 1 – 2 краплі нейтралізованого альдегіду і 2 краплі розчину метиленового синього. У другу пробірку – 1 мл молока та 2 краплі метиленового синього. В третю пробірку – 1 мл прокип'яченого молока, 1 – 2 краплі нейтралізованого альдегіду і 2 краплі розчину метиленового синього. Вміст усіх трьох пробірок перемішують і ставлять на водяну баню на 30 хв при температурі 37°С.
У першій пробірці розчин метиленового синього знебарвлюється. У другій і третій знебарвлення не спостерігають.
Пояснити отриманий результат. Зробити висновок.
Дослід 3. Дослідження дії пероксидази.
Принцип методу. Метод базується на здатності пероксидази за присутності гідрогену пероксиду каталізувати окиснення бензидину, яке супроводжується його наступним забарвленням.
Матеріальне забезпечення: витяжка з хрону (джерело пероксидази), 3 %-ний розчин гідрогену пероксиду, розчин бензидину в ацетатній кислоті, інгібітор пероксидази, штатив із пробірками, піпетки, газовий пальник.
Хід роботи. Готують 3 пронумеровані пробірки. В першу вливають 3-4 краплі розчину бензидину в ацетатній кислоті, 3-4 краплі 3 %-го розчину гідрогену пероксиду та 3-4 краплі витяжки з хрону. В другу пробірку вносять 3-4 краплі розчину бензидину в ацетатній кислоті, 3-4 краплі 3 %-го розчину гідрогену пероксиду та 3-4 краплі прокип’яченої витяжки з хрону. В третю пробірку до 3-4 крапель розчину бензидину додають інгібітор пероксидази, витяжку з хрону, після перемішування додають 3-4 краплі гідрогену пероксиду.
У першій пробірці спостерігають появу синього забарвлення. В другій та третій пробірках забарвлення відсутнє.
Пояснити отриманий результат. Зробити висновок.
Клініко-діагностичне значення. Ферменти, які беруть участь у транспортуванні електронів у процесах тканинного дихання, відносяться до окисно-відновних. Зокрема, до них належать цитохроми - залізопорфіринові ферменти, простетична група яких містить різні похідні гему. Атом феруму в гемі може змінювати валентність, приєднуючи або віддаючи електрони. Препарат цитохрому с використовують для покращення тканинного дихання асфіксії новонароджених, при астматичних станах, хронічній пневмонії, серцевій недостатності, ішемічній хворобі серця, інфекційному гепатиті при інтоксикаціях та інших станах, що супроводжуються порушенням окиснювальних процесів в організмі.
