
- •1. Терминология,
- •2. Энергетика процессов
- •3. Критерии направленности процессов и равновесия
- •4. Химическое равновесие
- •1. Терминология, основные понятия и определения
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры
- •1.3. Термодинамический процесс и термодинамическое равновесие
- •1.4. Функции пути осуществления процесса и функции состояния
- •1.5. Химический процесс и химическая переменная
- •1.6. Модели идеальных систем в химической термодинамике. Реальные системы
- •2. Энергетика процессов
- •2.1. Первое начало термодинамики (постулат о существовании внутренней энергии)
- •2.2. Термодинамическая работа
- •2.3. Внутренняя энергия и теплота
- •2.4. Энтальпия
- •2.5. Взаимосвязь работы и теплоты с изменениями внутренней энергии и энтальпии в изопроцессах с участием идеального газа
- •2.6. Теплоёмкость
- •2.7. Фазовые переходы I рода
- •2.8. Зависимость теплоёмкости от температуры
- •Простых веществ
- •2.9. Зависимость внутренней энергии и энтальпии от температуры
- •2.10. Зависимость внутренней энергии, энтальпии и теплоемкости от давления
- •2.11. Изменение внутренней энергии и энтальпии в химических реакциях
- •2.12. Экспериментальные методы определения тепловых эффектов химических реакций
- •2.13. Стандартные тепловые эффекты
- •2.14. Зависимость теплового эффекта от температуры. Уравнение Кирхгофа
- •Температуры:
- •2.15. Интегрирование уравнения Кирхгофа
- •2.16. Зависимость энтальпии реакции от давления
- •3. Критерии направленности процессов и равновесия в системах постоянного и переменного составов
- •3.1. Второе начало термодинамики (постулат о существовании энтропии)
- •3 .1.1.С в о и ств а энтропии. Энтропия как критерий направленности самопроизвольных процессов и равновесия в изолированных системах
- •3.1.2. Связь энтропии с параметрами
- •3.1.4. Изменение энтропии при обратимых фазовых переходах I рода
- •3.1.5. Статистическое толкование энтропии. Уравнение б ольцма иа -Пл анка
- •3.1.7. Расчет абсолютных значений энтропии
- •Абсолютной энтропии
- •3.1.8. Изменение энтропии в химических
- •3.2. Критерии направленности процессов и равновесия в неизолированных системах
- •3.2.1. Объединенное уравнение первого и второго начал термодинамики
- •3.2.4. Зависимости энергии Гиббса и энергии Гельмгольца от основных параметров состояния
- •Веществ
- •Веществ
- •Веществ
- •Веществ
- •При наличии фазовых превращений
- •3.2.7. Уравнения г и б б с а-г е л ь м г о л ь ц а
- •3.2.8. Вывод уравнений для зависимостей термодинамических функций от давления и объема
- •3.2.9. О "сложности" преобразований при выводе уравнений химической термодинамики
- •Функций по параметрам состояния
- •3.3. Критерии направленности процессов и равновесия в системах переменного состава
- •3.3.1. Химический потенциал
- •3.3.2. Свойства химического потенциала
- •3.3.3. Химический потенциал моля идеального газа
- •3.3.4. Химический потенциал компонента смеси идеальных газов
- •4. Химическое равновесие
- •4.1. Химическое равновесие в смеси идеальных
- •4.2. Расчет стандартного химического сродства
- •4.3. Стандартное химическое сродство и термодинамическая константа равновесия как характеристики равновесного состояния
- •4.4. Химическое сродство как критерий направленности процесса
- •4.5. Зависимость константы равновесия от температуры
- •4.5.1. Дифференциальная форма уравнений изобары и изохоры химической реакции
- •4.6. Расчет термодинамической константы равновесия
- •4.6.1. Общая характеристика фонда справочных данных
- •4.6.2. Способы расчета термодинамической константы равновесия
- •4 . 7 . 1.Реа к ц и и в смесях газов.
- •Связь термодинамической константы равновесия с
- •Эмпирическими (концентрационными) константами
- •Равновесия:Кр', кх,кп,кс
- •4.7.2.Реакции в гомогенной конденсированной фазе (реакции в растворах)
- •4.7.3. Реакции в гетерогенных системах
- •4.8. Расчет состава равновесной смеси по величине термодинамической константы равновесия
- •4.8.1.Химическое превращение представлено единственным уравнением
- •4.8.2.Химическое превращение представлено двумя уравнениями
- •4.8.3. Множественные реакции
- •4.9. Влияние различных факторов на состав
3.3. Критерии направленности процессов и равновесия в системах переменного состава
3.3.1. Химический потенциал
В системах переменного состава происходят изменения, связанные либо с протеканием химических реакций, либо с перераспределением вещества между сосуществующими фазами. Чтобы учесть эти эффекты и определить критерии направленности самопроизвольных процессов и равновесия в системах переменного состава, необходимо представить величину характеристического свойства системы (G, A, U, Н) не только как функцию двух "естественных" переменных: но и как функцию числа молей всех веществ, присутствующих в системе, т.е.:

С учетом сказанного полный дифференциал энергии Гиббса, выраженный через частные производные, следует записать в виде:
![]()
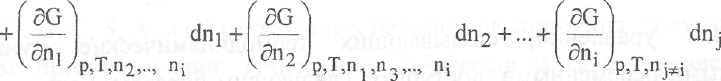
Все слагаемые, которые относятся к производным по числу молей компонентов, можно объединить в сумму

112
[p# 118]
Набор подстрочных индексов учитывает, что производная берется по числу молей 1-го компонента в условиях, когда числа молей всех остальных компонентов остаются постоянными.
Каждая из производных под знаком ^ получила название химического
потенциала, соответственно, 1-го, 2-го, .,.., i-ro компонента:

Эта функция была введена Гиббсом в 1875 году для описания равновесия в системах переменного состава. По своему смыслу химический потенциал показывает, как изменяется энергия Гиббса при добавлении одного моля 1-го компонента к системе бесконечно большой массы при постоянных давлении и температуре. Оговорка, касающаяся массы, имеет целью исключить возможность изменения состава системы при проведении указанной процедуры.
Аналогичным образом для A, U и Н могут быть получены выражения, подобные громоздкому уравнению, записанному выше для полного дифференциала энергии Гиббса. Преобразование их приводит к равенству:
![]()
Чтобы установить критерий направленности процессов и равновесия в системах переменного состава, запишем фундаментальное уравнение Гиббса в виде:
![]()
В условиях р,Т = const оно преобразуется к виду:
![]()
Поскольку всегда nj > 0 и, следовательно, dnj > 0, то можно заключить, что самопроизвольные процессы в системах переменного состава сопровождаются убылью химического потенциала, а состояние равновесия достигается, когда
3. Критерии (ц.)
[p# 119]
![]()
Обобщение изложенного об условиях направленности процессов и равновесия в системах различных типов дано в табл.5.
Таблица 5 Критерии направленности процессов и равновесия в различных системах
Условия существования системы
Критерий направленности Процесса
Критерий Равновесия системы
Изолированные системы
![]()
Увеличение энтропии
dS>0
Максимум энтропии
![]()
Закрытые системы Постоянного состава
a) T^const, V^const
б) T~const, p-const
Уменьшение энергии Гельмгольца
dA<0
Уменьшение энергии Гиббса
dG<0
Минимум энергии Гельмгольца
dA = 0: d2A>0
Минимум энергии Гиббса
dG-0; d2G>0
![]()
переменного состава
T=const, p^const
Уменьшение химического потенциала
![]()
dnj =
114
[p# 120]
