
- •Министерство образования и науки Российской Федерации
- •Научный редактор
- •Введение
- •1. Основные термические параметры состояния
- •Удельный объем
- •Давление
- •Соотношения единиц измерения давления
- •Температура
- •1.1. Задачи
- •1.2. Контрольные вопросы
- •2. Законы и уравнения состояния идеальных газов. Смеси идеальных газов
- •2.1. Задачи
- •2.2. Контрольные вопросы
- •3. Теплоемкости газов и газовых смесей
- •3.1. Задачи
- •3.2. Контрольные вопросы
- •4. Первый закон термодинамики для закрытой системы
- •4.1. Задачи
- •4.2. Контрольные вопросы
- •5. Политропные процессы изменения состояния идеальных газов
- •5.1. Задачи
- •5.2. Особенности расчета процессов идеальных газов при учете влияния температуры на их изобарную и изохорную теплоемкости
- •5.3. Задачи
- •5.4. Контрольные вопросы
- •6. Термодинамические свойства воды и водяного пара. Процессы водяного пара
- •6.1. Задачи
- •6.2. Контрольные вопросы
- •7. Влажный воздух
- •Основные характеристики влажного воздуха
- •Характеристики атмосферного влажного воздуха
- •Область влажного ненасыщенного воздуха h,d- диаграммы
- •Область перенасыщенного влажного воздуха h,d- диаграммы
- •Пример пользования h,d- диаграммой
- •7.1. Задачи
- •7.2. Контрольные вопросы
- •8. Второй закон термодинамики
- •8.1. Задачи
- •8.2. Контрольные вопросы
- •9. Первый закон термодинамики для потока. Работа изменения давления в потоке. Эксергия в потоке
- •Работа изменения давления в потоке для адиабатных процессов
- •Эксергия в потоке
- •9.1. Задачи
- •9.2. Контрольные вопросы
- •10. Истечение газа и пара через сопловые каналы
- •Особенности расчета процесса истечения через сопло реальных веществ
- •Необратимое истечение газов и паров через сопло
- •Процессы торможения. Параметры заторможенного потока
- •Методика расчета соплового канала при истечении через него газа или пара с начальной скоростью больше нуля
- •10.1. Задачи
- •10.2. Контрольные вопросы
- •11. Дросселирование газов, паров и жидкостей
- •11.1. Задачи
- •11.2. Контрольные вопросы
- •12. Процессы смешения газов и паров
- •Смешение в объёме
- •Смешение в потоке
- •Смешение при заполнении объёма
- •12.1. Задачи
- •12.2. Контрольные вопросы
- •13. Циклы двигателей внутреннего сгорания
- •Цикл двс с подводом теплоты к рабочему телу при постоянном объеме
- •Цикл двс с подводом теплоты к рабочему телу при постоянном давлении
- •Цикл двс со смешанным подводом теплоты к рабочему телу
- •13.1. Задачи
- •13.2. Контрольные вопросы
- •14. Циклы воздушных реактивных двигателей
- •Цикл прямоточного врд
- •Цикл турбокомпрессорного врд
- •14.1. Задачи
- •14.2. Контрольные вопросы
- •15. Циклы газотурбинных установок
- •Методика расчета тепловой экономичности обратимого цикла гту
- •Тепловая экономичность реального цикла гту
- •Регенеративный цикл гту
- •Регенеративный цикл гту с двухступенчатым сжатием и расширением рабочего тела
- •15.1. Задачи
- •15.2. Контрольные вопросы
- •16. Циклы паротурбинных установок
- •16.1. Базовый цикл пту – цикл Ренкина
- •Расчет простого обратимого цикла пту
- •Расчет необратимого цикла простой пту
- •Система кпд цикла пту
- •16.2. Цикл пту с вторичным перегревом пара
- •16.3. Регенеративный цикл пту
- •Выбор оптимальных давлений отборов пара турбины на регенеративные подогреватели пту
- •Особенности расчета регенеративных пту с подогревателями поверхностного типа
- •16.4. Теплофикационные циклы пту
- •Теплофикационные пту с отборами пара на тепловые потребители
- •16.5. Термодинамические особенности расчета циклов аэс на насыщенном водяном паре
- •16.6. Задачи
- •16.7. Контрольные вопросы
- •17. Циклы парогазовых установок
- •17.1. Цикл пгу с котлом-утилизатором
- •17.2. Циклы пгу со сжиганием топлива в паровом котле
- •Цикл пгу с низконапорным парогенератором
- •Цикл пгу с высоконапорным парогенератором
- •Полузависимая пгу
- •17.3. Задачи
- •17.4. Контрольные вопросы
- •18. Циклы холодильных установок и тепловых насосов
- •18.1. Цикл воздушной холодильной установки (вху)
- •Методика расчета вху
- •18.2. Цикл парокомпрессорной холодильной установки
- •Методика расчета цикла пкху
- •18.3. Парокомпрессорный цикл теплового насоса
- •Методика расчета цикла парокомпрессорного теплового насоса
- •18.4. Задачи
- •18.5. Контрольные вопросы
- •Заключение
- •Библиографический список
- •Приложения
- •Оглавление
- •Чухин Иван Михайлович
- •Редактор н.Б. Михалева
- •153003, Г. Иваново, ул. Рабфаковская, 34.
7.2. Контрольные вопросы
1. Дайте определение парциального давления водяного пара во влажном воздухе.
2. Дайте определение и расчетное выражение абсолютной влажности воздуха, поясните, какие допущения делаются для влажного атмосферного воздуха и какую формулу при этом используют для расчета его абсолютной влажности.
3. Дайте определение и расчетное выражения относительной влажности воздуха, поясните, какую формулу используют для расчета относительной влажности атмосферного воздуха.
4. Назовите основные состояния влажного воздуха и соответствующие этим состояниям параметры и характеристики влажного воздуха. Покажите состояния водяного пара в этом воздухе в р,v- диаграмме.
5. Дайте определение температуры точки росы влажного воздуха и покажите эту изотерму в р,v- диаграмме для водяного пара. Поясните практическое значение температуры точки росы.
6. Дайте определение влагосодержания воздуха и приведите расчетное выражение влагосодержания пара для атмосферного влажного воздуха.
7. Напишите расчетное выражение энтальпии влажного воздуха при наличии в нем паровой, жидкой и твердой фаз воды. Поясните, какие требования предъявляются к удельным энтальпиям, входящим в это уравнение.
8. Напишите расчетное выражение энтальпии для влажного атмосферного воздуха при наличии в нем паровой, жидкой и твердой фаз воды. Поясните, какие допущения приняты при получении расчетных выражений удельных энтальпий, входящих в это уравнение.
9. Поясните принцип работы психрометра и его практическое предназначение.
10. Поясните принцип построения изотерм в области ненасыщенного влажного воздуха в H,d- диаграмме.
11. Поясните принцип построения линий постоянных относительных влажностей для влажного атмосферного воздуха в H,d- диаграмме.
12. Поясните принцип построения изотерм в области перенасыщенного влажного воздуха и изотерм влажного термометра психрометра в области ненасыщенного воздуха в H,d- диаграмме.
13. Поясните особенность линий постоянных относительных влажностей атмосферного воздуха при температурах больше 100 оС.
14. На основании какого выражения строится зависимость парциального давления пара от влагосодержания в H,d- диаграмме?
15. Поясните назначение калорифера в сушильной установке.
16. Почему процесс идеальной сушки идет при постоянной энтальпии?
17. Как определяется парциальное давление пара в области перенасыщенного влажного воздуха в H,d- диаграмме?
18. Как определяется температура точки росы в области перенасыщенного влажного воздуха в H,d- диаграмме?
19. Как определяются влагосодержания паровой и жидкой фаз воды в области перенасыщенного влажного воздуха в H,d- диаграмме?
8. Второй закон термодинамики
Второй закон термодинамики так же, как и первый, не имеет никаких доказательств, кроме человеческого опыта в земных условиях. Если первый закон термодинамики количественно характеризует термодинамические процессы, то второй закон термодинамики дает качественную их оценку. Он отвечает на вопросы, в каком направлении и до какого предела может идти тот или иной процесс, при каких условиях возможно преобразование теплоты в работу, что необходимо для передачи теплоты от холодного тела к горячему, что характеризует реальные процессы и т.п. [1 - 6].
Поскольку в природе происходит множество термодинамических процессов, то единой формулировки второго закона термодинамики быть не может. Однако к каждому классу этих процессов можно дать свою трактовку второго закона термодинамики.
Второй закон термодинамики дает не только качественную, но и количественную оценку процессов, используя такую характеристику, как изменение энтропии тела или системы.
Математическая запись второго закона термодинамики для тела может быть представлена выражением
![]() .
(8.1)
.
(8.1)
В соответствии с выражением (8.1) можно дать следующую формулировку второго закона термодинамики: необратимость термодинамического процесса для тела приводит к увеличению изменения энтропии необратимого процесса по сравнению с изменением энтропии аналогичного обратимого процесса, при том же количестве подведенной внешней теплоты.
Для замкнутой изолированной системы второй закон термодинамики характеризует закономерность изменения ее энтропии:
![]() .
(8.2)
.
(8.2)
При этом если в системе происходят обратимые процессы, то ΔSС=0, если необратимые – ΔSС>0.
Поскольку все реальные процессы необратимы, то в случае их прохождения в замкнутой изолированной системе ее энтропия всегда будет увеличиваться.
В изолированной системе возможно получить полезную работу только в том случае, если она не находится в состоянии термодинамического равновесия. Работоспособность системы исчерпывается при достижении в ней равновесного состояния.
Наибольшая возможная полезная работа может быть получена при переходе системы из неравновесного состояния в равновесное, при протекании в ней только обратимых процессов.
В технической термодинамике наибольший интерес представляет возможность получения полезной работы в системе, состоящей из тел и внешней среды, находящихся в неравновесном состоянии. Окружающая среда в большинстве энергетических установок выступает в качестве холодного источника теплоты.
Для оценки максимально-возможного количества полезной работы, которое может быть получено в таких системах, в 1955 г. югославским ученым З. Рантом было введено понятие эксергии [5, 6].
Понятие эксергии относится к закрытам и открытым системам, а также к источникам теплоты.
Эксергией в объеме называется максимально возможная полезная работа постоянной массы вещества в закрытой системе, которая может быть получена при переходе данного вещества (тела) из неравновесного состояния в состояние равновесия с окружающей средой только по обратимым процессам.
Расчетное выражение удельной эксергии тела, находящегося в закрытой системе, соответствует уравнению
![]() ,
(8.3)
,
(8.3)
где u1, s1, v1 – параметры тела, находящегося в неравновесном состоянии с внешней средой;
Тос, рос, uос, sос, vос – параметры тела при давлении и температуре окружающей среды.
Расчетного выражения эксергии источника теплоты изолированной системы нет, но есть универсальная закономерность второго закона термодинамики, позволяющая рассчитать эту эксергию:
![]() ,
(8.4)
,
(8.4)
где Sc, Sит, Sос – изменение энтропии системы, источника теплоты и окружающей среды соответственно.
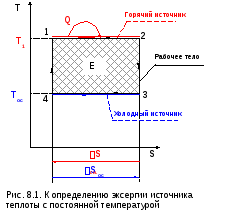
Например, эксергия источника теплоты Q с постоянной температурой Т1=const (рис.8.1) в соответствии с выражением (8.4) будет равна работе обратимого цикла Карно в интервале температур Т1 и Тос :
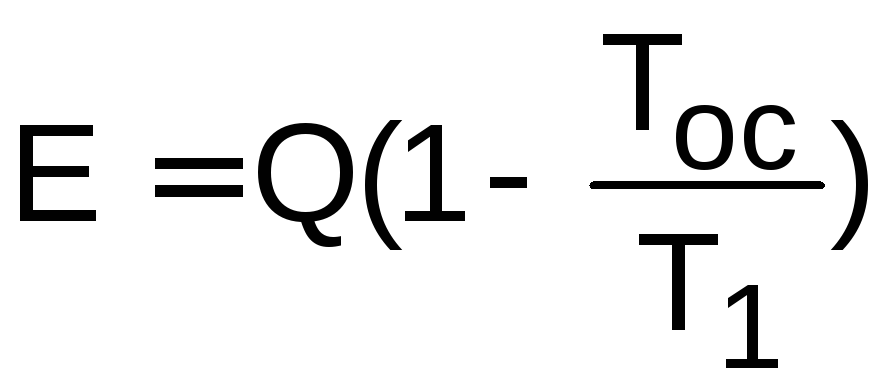 .
.
Потери потенциально возможной полезной работы (эксергии) при протекании необратимых процессов определяются по универсальному выражению, называющемуся теоремой Гюи–Стодолы [1, 2],
![]() ,
(8.5)
,
(8.5)
где -Lмп=E=Е1-Е2 – потери потенциально возможной работы (эксергии);
Тос – температура внешней среды;
SС – возрастание энтропии системы.
Термодинамический анализ эффективности работы любой теплоэнергетической установки выполняется при совместном использовании первого и второго законов термодинамики.
