
- •1. Отличительные особенности поведения полимеров
- •2. Строение полимеров
- •3. Классификация полимеров
- •1. Природные, искусственные и синтетические полимеры
- •2. Органические и неорганические полимеры
- •3. Термопласты и реактопласты
- •4. Пластики, эластомеры, волокна и смолы
- •4. Химия полимеризации
- •4.1. Цепная полимеризация
- •4.1.1. Свободнорадиакальная полимеризация
- •4.1.2. Ионная полимеризация
- •4.1.3. Координационная полимеризация
- •4.2. Ступенчатая полимеризация
- •4.2.1. Поликонденсация
- •4.2.2. Полиприсоединение
- •4.2.3. Полимеризация с раскрытием цикла
- •4.3. Особые типы полимеризационных реакций
- •4.3.1. Электрохимическая полимеризация
- •4.3.2. Полимеризация по механизму метатезиса
- •5. Способы проведения процессов полимеризации
- •6. Средняя молекулярная масса полимеров
- •6.1. Полидисперсность и кривые
- •7. Выделение и очистка полимеров
- •8. Фракционирование полимеров
- •9. Определение молекулярных масс полимеров
- •9.1. Криоскопия
- •9.2. Эбуллиоскопия
- •9.3. Мембранная осмометрия
- •9.4. Парофазная осмометрия
- •9.5. Вискозиметрия
- •9.6. Ультрацентрифугирование
- •9.7. Светорассеяние
- •10. Структура полимерных молекул
- •10.1. Микроструктуры, связанные с химическим строением полимеров
- •10.1.1. Гомоцепные и гетероцепные полимеры.
- •10.1.2. Гомополимеры и сополимеры.
- •10.2. Микроструктуры, связанные с геометрическим
- •10.3. Стереорегулярные полимеры
- •10.4. Геометрическая изомерия
- •11. Стеклообразное состояние полимеров
- •11.1 Агрегатные состояния веществ
- •11.2. Фазовые состояния веществ
- •11.3. Факторы, влияющие на температуру стеклования
- •11.4 Температура стеклования и молекулярная масса полимеров
- •11.5. Влияние пластификаторов на температуру стеклования
- •11.6. Значение температуры стеклования
- •12. Кристаллические полимеры
- •12.1. Полимерные монокристаллы
- •12.2. Влияние степени кристалличности на свойства полимеров
- •13. Химические превращения полимеров
- •14. Деструкция полимеров
- •14.1. Термическая деструкция
- •14.2. Механическая деструкция
- •14.3. Фотодеструкция
- •14.4. Радиационная деструкция
- •14.5. Окислительная деструкция
- •15. Переработка полимеров
4.2. Ступенчатая полимеризация
При ступенчатой полимеризации построение полимерной цепи происходит за счет взаимодействия функциональных групп мономеров. Реакция протекает по ступенчатому механизму, т.е. последовательными, независимыми актами, и рост цепи происходит весьма медленно, в отличие от цепной полимеризации, которая заканчивается практически мгновенно.
Имеется огромное количество реакций между функциональными группами органических соединений, которые в принципе могут лежать в основе ступенчатой полимеризации, однако на практике чаще всего используют лишь:
-
поликонденсацию,
-
полиприсоединение,
-
раскрытие циклов,
-
амидирование,
-
переэтерификацию.
Ступенчатая полимеризация может идти с выделением низкомолекулярных продуктов или без него. Соответственно состав мономера может совпадать с составом элементарных звеньев полимера или же может отличаться от него.
Примером ступенчатой полимеризации, сопровождающейся выделением низкомолекулярных продуктов, является реакция поликонденсации. В результате реакции поликонденсации состав элементарного звена полимера всегда отличается от состава молекул мономеров.
4.2.1. Поликонденсация
В поликонденсации участвуют мономеры, молекулы которых содержат не менее двух функциональных групп, способных химически взаимодействовать друг с другом. Чаще всего это бывают гидроксильные, карбоксильные и аминогруппы.
В основе поликонденсации лежат те же химические реакции, которые известны для низкомолекулярных органических соединений. Примером может служить реакция этерификации, приводящая к образованию сложных эфиров.
CH3COOH + C2H5OH CH3COOC2H5 + H2O
Если в эту реакцию взять бифункциональную кислоту, например адипиновую, и бифункциональный спирт, например этиленгликоль, то получится тоже сложный эфир:
HOOC-(CH2)4-COOH + HO-CH2-CH2-OH HOOC-(CH2)4-COO-CH2-CH2-OH
-H2O
В этом продукте кроме неактивной эфирной группы есть активная карбоксильная и активная спиртовые группы. Следовательно, он может присоединить еще одну молекулу адипиновой кислоты со стороны спиртового гидроксила и еще одну молекулу этиленгликоля со стороны карбоксильной группы:
HO-CH2-CH2-OOC-(CH2)4-COO-CH2-CH2- OOC-(CH2)4-COOH + 2 H2O
Полученная на этой стадии молекула вновь содержит две функциональные группы и по-прежнему способна к реакции как с адипиновой кислотой, так и с этиленгликолем. В общем виде уравнение реакции можно записать так:
n HO-CH2-CH2-OH + n HOOC-(CH2)4-COOH
H
 O
[
CH2-CH2-OOC-(CH2)4-COO
]n
H
+ (2n-1) H2O
O
[
CH2-CH2-OOC-(CH2)4-COO
]n
H
+ (2n-1) H2O
На этом примере можно сделать некоторые выводы, касающиеся как поликонденсации, так и вообще ступенчатой полимеризации:
1). Для осуществления реакции необходимо использовать мономеры, имеющие не менее двух активных функциональных групп.
2). Реакция протекает ступенчато, путем последовательного взаимодействия этих функциональных групп.
3). К образованию полимера приводит только один тип реакции между двумя функциональными группами.
4). Образующиеся макромолекулы содержат на своих концах активные функциональные группы обоих типов и поэтому в любой момент готовы к продолжению реакции. То есть образуются живые, а не мертвые цепи.
В рассмотренном примере две разные молекулы содержали по две одинаковые группы. Это пример гетерополиконденсации. Примером гетерополиконденсации является также получение полиамида-6,6 (другие названия: анид, найлон-6,6) из гексаметилендиамина и адипиновой кислоты:

Естественно, возможен случай, когда две разные функциональные группы содержатся на концах одной молекулы мономера. В этом случае протекает реакция гомополиконденсации. Примером гомополиконденсации может служить получение поликапроамида (другие названия: капрон, найлон-6, перлон) из ε-аминокапроновой кислоты:

Необходимо отметить, что растущая цепь содержит на концах функциональные группы, которые могут взаимодействовать между собой. Поэтому межмолекулярная конденсация, приводящая к росту цепи, может соседствовать с внутримолекулярной конденсацией, дающей побочные низкомолекулярные циклические продукты.
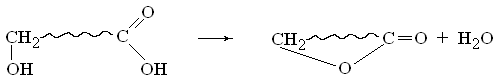
Такого рода продукты с различной величиной цикла довольно часто присутствуют наряду с полимером.
В рассмотренных примерах поликонденсация бифункциональных мономеров приводит к образованию линейных макромолекул и называется линейной поликонденсацией. В результате реакции получается термопласт – плавкий линейный полимер, растворимый в органических растворителях. При наличии в мономерах трех и более функциональных групп образуются разветвленные и сетчатые полимеры, а процесс их образования называется трехмерной поликонденсацией. В ходе такого процесса поликонденсации образуется реактопласт – неплавкий полимер пространственного строения, нерастворимый в органических растворителях. Например, при реакции глицерина с двухосновными кислотами быстро образуется трехмерная макромолекула практически бесконечно большой молекулярной массы. При образовании такой бесконечно большой трехмерной структуры весь образец полимера, называемый гелем, теряет способность растворяться и плавиться.
Реакция поликонденсации идет ступенчато с постепенным нарастанием молекулярной массы полимера. Растущие цепи могут реагировать не только с мономерами, но и между собой. Каждый акт взаимодействия сопровождается отщеплением низкомолекулярных побочных продуктов, и поэтому состав элементарного звена полимера отличается от состава мономеров. Промежуточные продукты реакции поликонденсации (димеры, тримеры, тетрамеры и т.д.) вполне устойчивы и могут быть выделены на любой стадии процесса в качестве самостоятельных продуктов.
Достаточно высокомолекулярный продукт образуется только при очень высокой степени завершенности реакции (обычно более 98%), а выход и молекулярная масса полимера зависят от продолжительности реакции.
При линейной поликонденсации двух разных мономеров (гетерополиконденсации) для получения полимера с высокой молекулярной массой исходные мономеры необходимо брать в строго эквимолярных количествах. Увеличение количества одного из них резко снижает степень поликонденсации, т.к. функциональные группы избыточного мономера действуют как ингибиторы и останавливают реакцию на ранних стадиях, то есть до образования полимера. Рост полимерной цепи прекращается, поскольку при исчерпании одного мономера однотипные функциональные группы второго не могут реагировать между собой. Так, например, установлено, что при поликонденсации адипиновой кислоты с гексаметилендиамином избыток одного из мономеров всего в 0,09% снижает молекулярную массу полимера в 10 раз.
Кинетически поликонденсация является обратимой реакцией, т.е. полимер может реагировать с побочными низкомолекулярными веществами с образованием исходных мономеров. Наряду с ростом макромолекулы протекает обратный процесс – ее деструкция, которую можно ослабить, удаляя низкомолекулярные соединения или полимер из сферы реакции.
В случае образования полимеров сетчатой структуры требования равенства концентраций мономеров и удаления побочных продуктов не являются такими жесткими, как при линейной поликонденсации.
Скорость реакции поликонденсации можно регулировать, изменяя температуру реакционной среды. Увеличение температуры ускоряет реакцию в целом и благоприятствует удалению низкомолекулярных продуктов, смещая тем самым равновесие в сторону образования полимера. Вместе с тем повышение температуры ускоряет ряд нежелательных побочных реакций, приводящих к исчезновению функциональных групп или изменению их химической природы (декарбоксилирование, окисление и др.) и, следовательно, к прекращению роста полимерной цепи. Одновременно возрастает и опасность термодеструкции полимера.
На практике для ускорения реакции поликонденсации широко используют катализаторы: минеральные кислоты, кислые соли, органические сульфокислоты, галогениды металлов, щелочи и т. д., а также вещества, взаимодействующие с низкомолекулярными продуктами реакции.
