
- •1 Билет
- •2 Билет
- •Количество электричества равное одному Фарадею всегда изменяет электрохимически 1 г-экв любого вещества независимо от его природы.
- •3. Билет
- •Ванна для электролитического получения цинка
- •4. Процесс взаимодействия продуктов электродных реакций между собой (вторичные реакции).
- •3.Закономерности роста крист фазы.
- •4 Билет
- •1. Удельная электропроводность
- •2.Равновесн электородный потенц.Ур-е Нернста.Стандрт электрод потенц
- •3Поляризациооные кривые в усл-ях электрохим перенапряжения
- •5 Билет
- •6 Билет
- •7 Билет
- •2 Диффузион перенапр в усл-ях молекулярн диффузии
- •8 Билет
- •3.Кинетика электрод-х пр-в в расплавл-х солях
- •9 Билет
- •Билет 10
- •1 Вывд т/д выраж для равновесн эдс
- •2 Влияние адсорбции на форму экк.
- •3Обр-е новой мет фазы на эл-де.
- •11 Билет
- •1. Уравнение Гиббса-Гельмгольца
- •2. Частные случаи электрохим перенапряжения
- •Билет 12
- •1 Знак эдс.
- •3. Концентрационные цепи с расплавленными солями.
- •Билет 13
- •Билет 14
- •15 Билет
- •Билет 16
- •2 Совмесное восст-е ме и водорода
Билет 12
1 Знак эдс.
Е = п - л.
Следовательно, знак ЭДС устанавливается по положению потенциала правого электрода относительно левого и может быть как положительным, так и отрицательным.
За направление тока принимают движение положит. зарядов
ЭДС считается положительной, если при замыкании гальванического элемента на внешнее сопротивление электрический ток, за направление которого принимается движение положительных зарядов, течет в электролите (по внутренней цепи) от левого электрода к правому. (ЭДС «+»)
Электрохимический ряд напр. в 12ВОПРОСЕ (Можно отметить, что более отрицат. нах в окисленном состоянии и более активны,на катоде восст. более полож. элементы, все кто стоит до Н будут окисляться Н)
2электрохим восст-е мет.катодные р-и. катодные р-и:
Mez+ x H2O + ze = Me + x H2O
MeAx (z-x) + ze = Me + xA-
Катодное выделение металла имеет ряд особенностей:
В ходе электролиза поверхность катода не постоянна, а непрерывно изменяется вследствие осаждения металла. Надо различать кажущуюся плотность тока, то есть силу тока на единицу геометрической видимой поверхности и истинную, то есть отношение силы тока к активной поверхности осадка.
Неустойчивость во времени потенциала катода. Изменения потенциала могут быть связаны с изменением активной поверхности катода (истинной плотностью тока), с изменением перенапряжения при осаждении металла.
Примеси ПАВ различных окислителей (например, растворённого кислорода) в электролите изменяют характер роста осадка, величину поляризации.
Наличие сопряжённых процессов, например, выделение водорода, изменяют рН раствора вблизи поверхности электрода, что может привести к гидролизу солей и влиять на ход электроосаждения металла.
При осаждении металла на инертном катоде зависимость поляризации от времени при постоянной силе тока может иметь следующий вид:
В нач потенц быстро сдвиг-ся в отриц сторону от равновесного знач,проходит ч/з макс(точ А) затем устанавл
На некотором знач-и.После отключ тока(точВ) потенц приним равновесн знач.В(точ А) м/но увид обр-е зародыша.
3. Концентрационные цепи с расплавленными солями.
В концентрационных цепях токообразующий процесс обусловлен различием в концентрациях соответствующего компонента в полуэлементах цепи.
(+) Ag|AgNO3, (NaNO3) | | AgNO3, (NaNO3) | Ag, (-)
α1 α2
Пусть
α1
> α2;
E =
ln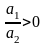
Токообразующим процессом будет переход AgNO3 из раствора с большей С в раствор с меньшей С.
Ток будет течь пока α не станут одинаковыми и ЭДС = 0
Если α1 и ЭДС известно, тогда α2 можно найти из E = - ln α2
Если два сплава Ме различной С поместить в качестве электродов в расплавленный электролит, содержащий ионы одного из Ме, то получится цепь амальгамного типа
(-) Cd(Pb) | CdCl2 | Cd(Pb) (+)
α1 > α2
то
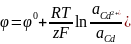 φл
> φп
(т.к. активность Cd
одинаковы)
φл
> φп
(т.к. активность Cd
одинаковы)
Е
= φправ
– φлев
=

будет переход Cd из сплава с большей α1 в сплав с меньшей α2
α1=1, то найдем α2 из E = - ln α2 > 0
