
- •1 Билет
- •2 Билет
- •Количество электричества равное одному Фарадею всегда изменяет электрохимически 1 г-экв любого вещества независимо от его природы.
- •3. Билет
- •Ванна для электролитического получения цинка
- •4. Процесс взаимодействия продуктов электродных реакций между собой (вторичные реакции).
- •3.Закономерности роста крист фазы.
- •4 Билет
- •1. Удельная электропроводность
- •2.Равновесн электородный потенц.Ур-е Нернста.Стандрт электрод потенц
- •3Поляризациооные кривые в усл-ях электрохим перенапряжения
- •5 Билет
- •6 Билет
- •7 Билет
- •2 Диффузион перенапр в усл-ях молекулярн диффузии
- •8 Билет
- •3.Кинетика электрод-х пр-в в расплавл-х солях
- •9 Билет
- •Билет 10
- •1 Вывд т/д выраж для равновесн эдс
- •2 Влияние адсорбции на форму экк.
- •3Обр-е новой мет фазы на эл-де.
- •11 Билет
- •1. Уравнение Гиббса-Гельмгольца
- •2. Частные случаи электрохим перенапряжения
- •Билет 12
- •1 Знак эдс.
- •3. Концентрационные цепи с расплавленными солями.
- •Билет 13
- •Билет 14
- •15 Билет
- •Билет 16
- •2 Совмесное восст-е ме и водорода
15 Билет
1 напряж на электролиз ванне. Количество электроэнергии, затраченное на получение единицы количества металла (или другого продукта электролиза).
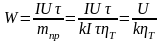 [кВтч/кг]
U
= Er
+ Eом
+ к
+ а
U
– напряжение на электролизной ванне,
Er
– равновесная ЭДС, Eом
–омические падения напряжения во всех
токоведущих частях электролизёра, к
, а
поляризация катода и анода.
[кВтч/кг]
U
= Er
+ Eом
+ к
+ а
U
– напряжение на электролизной ванне,
Er
– равновесная ЭДС, Eом
–омические падения напряжения во всех
токоведущих частях электролизёра, к
, а
поляризация катода и анода.
Напряжение можно найти по закону Ома. Удельный расход электроэнергии-расход электроэнергии отнесен к массе получен пр-та при эл-зе
2механизм масса переноса. Перенос реагирующих веществ в условиях электрохимической реакции может осуществляться по трём механизмам. Первый механизм – молекулярная диффузия, то есть перемещение частиц вещества под действием градиента концентрации. При прохождении через границу электрод-электролит электрического тока концентрация реагирующих веществ у поверхности падает и одновременно растёт концентрация продуктов реакции.
Прилегающая к электроду область раствора, в которой происходит изменение концентрации раствора, но сохраняется условие электронейтральности, называется диффузионным слоем. Этот слой нужно отличать от диффузной части двойного электрического слоя. Обычно толщина диффузионного слоя на порядок и более превышает толщину диффузной части двойного электрического слоя, а поэтому при решении задач массопереноса полагают, что в первом приближении начало диффузионного слоя соответствует координате x = 0 (ось x направлена вдоль нормали к поверхности электрода).
Второй механизм массопереноса –миграция – связан с перемещением заряженных частиц под действием электрического поля, которое возникает в диффузионном слое при прохождении через него электрического тока.
Третий механизм массопереноса – конвекция, то есть перенос вещества вместе с потоком движущейся жидкости. В естественных условиях конвекция возникает в результате градиента плотности раствора, который, в свою очередь, является следствием концентрационных или температурных изменений в приэлектродном пространстве. Искусственную (вынужденную) конвекцию создают перемешиванием электролита или вращением самого электрода.
Изменение скорости совершается в некотором слое, который называется пограничным слоем гр, или слоем Прандтля. Передача движения от одного слоя к другому определяется кинематической вязкостью жидкости . Передача растворённого вещества диффузией определяется коэффициентом диффузии D.
10-2
см2/с;
D
10-5
см2/с
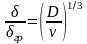
0,1 гр
0,1 гр
Для случая естественной конвекции для вертикального расположения электрода
 k0,6;
h
– высота электрода;
- плотность раствора; g
- ускорение силы тяжести.
k0,6;
h
– высота электрода;
- плотность раствора; g
- ускорение силы тяжести.

Для вынужденной конвекции, когда ламинарный поток жидкости набегает с одной стороны на пластинчатый электрод id определяется из уравнения
 x
– расстояние вдоль электрода.
x
– расстояние вдоль электрода.
Третий случай конвективной диффузии реализуется при применении вращающегося дискового электрода. Особенностью дискового электрода является постоянство толщины диффузионного слоя в любых точках его поверхности. Предельный ток на дисковом электроде описывается уравнением
 id
= 0,62 z
F
1/2-1/6D1/2c0
- скорость вращения дискового
id
= 0,62 z
F
1/2-1/6D1/2c0
- скорость вращения дискового
электрода.
3 электропроводн и числа переноса расплавлен солей. Расплавленные соли близки по строение к твердому веществу.
Электропроводность. Величина электропроводности соли связана с природой химической связи в ней структурными изменениями при плавлении.
λ=
χ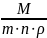
M – молекулярная масса соли, г/моль.
m – число атомов металла в молекуле соли.
n – валентность катиона.
ρ – плотность соли
λ – зависит от заряда, подвижности ионов, их количества в единице объема.
χ – для бинарных смесей плавно меняется при изменении их состава
Электропроводность связана с движением ионов и зависит от их природы и взаимодействия между ними.
Числа переноса.
В бинарных смесях с общим ионом один сорт покоится например ионы Х- в смесях АХ-ВХ. Это позволяет определить числа переноса А+ и В+ по отношению к ионам Х. Это дает возможность характеризовать свойства ионов одного знака в расплавленных смесях с общими катионами или анионами. (внутренние числе переноса)
Числа переноса (t- , t+) можно рассматривать относительно покоящейся массы электролита. Тогда в это время малая часть ионов переносит электричество. ( внешние числа переноса)
