
- •1 Билет
- •2 Билет
- •Количество электричества равное одному Фарадею всегда изменяет электрохимически 1 г-экв любого вещества независимо от его природы.
- •3. Билет
- •Ванна для электролитического получения цинка
- •4. Процесс взаимодействия продуктов электродных реакций между собой (вторичные реакции).
- •3.Закономерности роста крист фазы.
- •4 Билет
- •1. Удельная электропроводность
- •2.Равновесн электородный потенц.Ур-е Нернста.Стандрт электрод потенц
- •3Поляризациооные кривые в усл-ях электрохим перенапряжения
- •5 Билет
- •6 Билет
- •7 Билет
- •2 Диффузион перенапр в усл-ях молекулярн диффузии
- •8 Билет
- •3.Кинетика электрод-х пр-в в расплавл-х солях
- •9 Билет
- •Билет 10
- •1 Вывд т/д выраж для равновесн эдс
- •2 Влияние адсорбции на форму экк.
- •3Обр-е новой мет фазы на эл-де.
- •11 Билет
- •1. Уравнение Гиббса-Гельмгольца
- •2. Частные случаи электрохим перенапряжения
- •Билет 12
- •1 Знак эдс.
- •3. Концентрационные цепи с расплавленными солями.
- •Билет 13
- •Билет 14
- •15 Билет
- •Билет 16
- •2 Совмесное восст-е ме и водорода
Билет 16
1 Электроды 1 рода. систему, в которой восстановленной формой является металл электрода, а окисленной формой – простые ионы этого же металла. Примером может служить система
Cu2+
+ 2e
Cu
= 0Cu2+/Cu
+
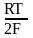 ln
aCu2+
ln
aCu2+
относятся
амальгамные электроды, в которых
восстановленной формой служит амальгама
какого-либо металла, а окисленной формой
– ионы этого же металлаTl+
+ e(Hg)
Tl(Hg)
= 0Tl+/Tl
+
ln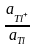 aTl
– активность таллия в амальгаме.общую
формулу для потенциала электрода 1 рода
1
= 01
+
aTl
– активность таллия в амальгаме.общую
формулу для потенциала электрода 1 рода
1
= 01
+
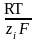 ln
ln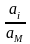 где ai
– активность потенциалопределяющих
ионов в растворе; zi
– число электронов, участвующих в
электродной реакции; аМ
– активность соответствующего металла.
где ai
– активность потенциалопределяющих
ионов в растворе; zi
– число электронов, участвующих в
электродной реакции; аМ
– активность соответствующего металла.
Электроды 2 рода.система, в которой металл покрыт слоем трудно растворимой соли, а раствор содержит анионы этой соли. Окисленной формой здесь является трудно растворимая соль, а восстановленная форма представлена металлом и анионом. Примеры.
Хлорсеребряный электрод
AgCl + e Ag + Cl- = 0 - ln aCl-
Каломельный электрод Hg2Cl2 + 2 e 2Hg + 2Cl- = 0 - ln aCl-
2 Совмесное восст-е ме и водорода
1-поляризац кривая,отвеч-щая восст ме
2- поляризац кривая,отвеч-щая восст водорода
При потен положительнее равновесоного потенц водорода на эл-де(К) не воз/но выделение ни водорода ни мет.до равновесн потенц мет возм восст тол водорода при потенц отриц-е равновесого потенц мет происх-т совместное выдел ме и водорода.выдел водорода хар-ся бол перенапр,чем выделен мет поэтому кривая 2 положе кривой 1
С помощью диаграммы видно как мо-но измен выход по току в нужную сторону,измен-е концентр ионов мет и вод-да измен-ет равновесное знач потенц след изм-ся полож ПК и след равновесное знач сдвиг в торону «-« что приводит к увел выхода по току мет,если РН в прикатодном слое достигает РН гидр то на пов-ть катода выпадает осадок NaOH возм\НО РАССЛАИВАНИЕ КАТОДА И РАССЕИВАНИЕ ОСАДКА
3электродные потенц в расплпвлен соляхДля индивидуальных солей ряды потенц-в могут б-ть составлены из величин напряж и разлож.Для смеси солей электрод потенц мет обратимый по отношею к ионам этого мет.подчин ур-ю нернста
При невыс крнцентр активность линейно завичит от концентр те в некотором диапозоне подчин закону Генри тогда
-условный стандарт потенц,он м/т б/ть тол экспер Эл.ряды мет-в в индивидуально расплавленных солях составлены на основе вел станд потенц,кот опре-ется величиной напряжения разложения в смесях солей электрохим ряды составлены на основе условного станд потенц
