
- •1 Билет
- •2 Билет
- •Количество электричества равное одному Фарадею всегда изменяет электрохимически 1 г-экв любого вещества независимо от его природы.
- •3. Билет
- •Ванна для электролитического получения цинка
- •4. Процесс взаимодействия продуктов электродных реакций между собой (вторичные реакции).
- •3.Закономерности роста крист фазы.
- •4 Билет
- •1. Удельная электропроводность
- •2.Равновесн электородный потенц.Ур-е Нернста.Стандрт электрод потенц
- •3Поляризациооные кривые в усл-ях электрохим перенапряжения
- •5 Билет
- •6 Билет
- •7 Билет
- •2 Диффузион перенапр в усл-ях молекулярн диффузии
- •8 Билет
- •3.Кинетика электрод-х пр-в в расплавл-х солях
- •9 Билет
- •Билет 10
- •1 Вывд т/д выраж для равновесн эдс
- •2 Влияние адсорбции на форму экк.
- •3Обр-е новой мет фазы на эл-де.
- •11 Билет
- •1. Уравнение Гиббса-Гельмгольца
- •2. Частные случаи электрохим перенапряжения
- •Билет 12
- •1 Знак эдс.
- •3. Концентрационные цепи с расплавленными солями.
- •Билет 13
- •Билет 14
- •15 Билет
- •Билет 16
- •2 Совмесное восст-е ме и водорода
Билет 10
1 Вывд т/д выраж для равновесн эдс
AA + BB = LL + MM
Электрическая работа (энергия) будет равна произведению Е zF (перемещение заряда по замкнутому контуру под действием ЭДС). Тогда
G = - Е zF
G = ii
i = i0 + RT ln ai
G = i0i + RT ln ai
G
= i0i
+
RT ln
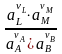
i0I = - RT ln Kр – связь i0i с Кр
Используя все уравнения получаем:
E
=
 ln
Kр
-
ln
ln
Kр
-
ln
E = E0 - ln
E0
–стандартная ЭДС электрохимической
системы.
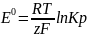 (ур-е
Нернста)
(ур-е
Нернста)
2 Влияние адсорбции на форму экк.
Налич пав изменяет форму экк,адсорбир-е пав пр-с самопроиз след работа этого пр-са+ и приводит к уменш пов-го наяжения.влияние анионов:макс снижается и смещ-ся в сторону отриц потенц.Сдвиг потенц н.з связван с возник скачка потенц м/ду слоем адсорбированных анионов и притянутых к ним катионам.Влияние орг в-в:макс сниж-ся ,снижение бол чем выше концентр пав,в области выс зарядо экк совпадают.вл-е катионов:смещ макс в сторону пол зарядов.
3Обр-е новой мет фазы на эл-де.
Это откл-е-фазовое перенапряж или перенапряж-е критсталлизации.оно возник потому что необходимы затраты энергии на обр-е кристалла в первые моменты времени.Зависимость фазового перенапр от плотности тока м/т иметь разный вид в зависимости от вида обр-ся зародыша.Обр-е электролит осадков ме опр-ся скоростями 2–х параллельно протек-х пр-в:1)появл-е центров критс на катоде хар-ся скоростью появл центров крист-ции2) рост обр-ся зародышей хар-ся скоростью роста.скор ЦК больше скор ре-и-мелко крист-е осадки,наоборот_ккрупнокрист-е осадки
11 Билет
1. Уравнение Гиббса-Гельмгольца
G
= Н
- ТS
Н
= G
+ ТS
S
= -
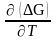
уравнение Гиббса-Гельмгольца:
Е
= -
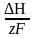 +Т
+Т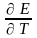 S
= zF
S
= zF
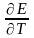 ,
-температурный
коэффициент ЭДС. характеризует
изменение энтропии в ходе соответствующей
химической реакции
,
-температурный
коэффициент ЭДС. характеризует
изменение энтропии в ходе соответствующей
химической реакции
2. Частные случаи электрохим перенапряжения
1.
Потенциал электрода равен его равновесному
значению
= r.
Тогдаi
= 0;
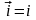 ;
;
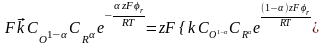
Решение
последнего уравнения относительно r
даёт уравнение Нернста для обратимого
электродного потенциала
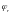 =
=
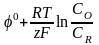
2.
Система незначительно отклоняется от
равновесия, перенапряжение невелико
(
< 25 мВ) zF
< RT.
В этом случае каждую экспоненту можно
разложить в ряд и ограничится двумя
первыми его членами
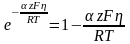
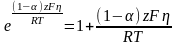 тогда
тогда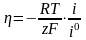
3.
Система существенно отклоняется от
равновесия и через неё проходит
значительный ток. Если
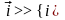 ,
то есть протекает катодный процесс, то
вторым частным током можно пренебречь
i
=
,
то есть протекает катодный процесс, то
вторым частным током можно пренебречь
i
=
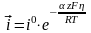
откуд
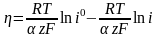
= a
+ b
lg
i
уравнение Тафеля.
Для случая когда
= a
+ b
lg
i
уравнение Тафеля.
Для случая когда
 i
= ia
=
i
= ia
=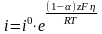 получим
уравнение Тафеля для анодного процесса
= aa
+ ba
lg
i
получим
уравнение Тафеля для анодного процесса
= aa
+ ba
lg
i
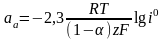
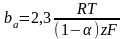
3 влияние природы мет,анионного и катионного со-ва эл-та на хар катодного осадка мет.
Все металлы можно условно разделить на три группы:
1) выделяющиеся из водных растворов с очень малым перенапряжением. Для них характерны неустойчивость потенциала во времени, сложный характер роста катодного осадка и другие особенности, свойственные процессу катодного выделения металла. При промышленных плотностях тока эти металлы дают грубые осадки с крупными зёрнами. Ток обмена для этих металлов очень велик. Скорость реакции лимитируется стадией диффузии.
2) образуют более тонкие осадки, имеют меньшие токи обмена и большее перенапряжение.
3)Наибольшая величина перенапряжения и наим токи обмена. Они выделяются на катоде в виде плотных тонкокристаллических осадков. В стационарных условиях общее перенапряжение обусловлено перенапряжением разряда и диффузии.
