
- •1 Билет
- •2 Билет
- •Количество электричества равное одному Фарадею всегда изменяет электрохимически 1 г-экв любого вещества независимо от его природы.
- •3. Билет
- •Ванна для электролитического получения цинка
- •4. Процесс взаимодействия продуктов электродных реакций между собой (вторичные реакции).
- •3.Закономерности роста крист фазы.
- •4 Билет
- •1. Удельная электропроводность
- •2.Равновесн электородный потенц.Ур-е Нернста.Стандрт электрод потенц
- •3Поляризациооные кривые в усл-ях электрохим перенапряжения
- •5 Билет
- •6 Билет
- •7 Билет
- •2 Диффузион перенапр в усл-ях молекулярн диффузии
- •8 Билет
- •3.Кинетика электрод-х пр-в в расплавл-х солях
- •9 Билет
- •Билет 10
- •1 Вывд т/д выраж для равновесн эдс
- •2 Влияние адсорбции на форму экк.
- •3Обр-е новой мет фазы на эл-де.
- •11 Билет
- •1. Уравнение Гиббса-Гельмгольца
- •2. Частные случаи электрохим перенапряжения
- •Билет 12
- •1 Знак эдс.
- •3. Концентрационные цепи с расплавленными солями.
- •Билет 13
- •Билет 14
- •15 Билет
- •Билет 16
- •2 Совмесное восст-е ме и водорода
6 Билет
1.скачки на потенц на границе разд фаз. Электродным потенциалом называют ЭДС электрохимической цепи, в которой слева находится стандартный водородный электрод, потенциал которого условно принят за нуль, а справа - данный электрод.
 Е-
суммарный эффект скачков потенциала
на границах раздела фаз
Е-
суммарный эффект скачков потенциала
на границах раздела фаз
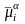 = i
ziFg;
–
электрохимический
потенциал
частиц сорта i
в фазе ;
g
– внутренний
потенциал,
который представляет собой разность
потенциалов между точкой внутри фазы
и бесконечно удалённой точкой в вакууме;
zi
– заряд частиц сорта i.
Условием равновесия для заряженных
частиц с фазами
и
будет равенство их электрохимических
потенциалов.
=
= i
ziFg;
–
электрохимический
потенциал
частиц сорта i
в фазе ;
g
– внутренний
потенциал,
который представляет собой разность
потенциалов между точкой внутри фазы
и бесконечно удалённой точкой в вакууме;
zi
– заряд частиц сорта i.
Условием равновесия для заряженных
частиц с фазами
и
будет равенство их электрохимических
потенциалов.
=
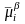
Работа перенесения заряженной частицы из фазы в фазу будет равна разности её электрохимических потенциалов в этих фазах, то есть - = (i - i) ziF(g - g)
Электрохимический потенциал частицы i в фазе равен работе перенесения моля данного компонента i из бесконечности в вакууме внутрь данной фазы.
g - g - разность внутренних потенциалов называется гальвани потенциалом и обозначается как g.В условиях равновесия g = (i - i)/ ziF ЭДС электрохимической системы, которая представляет собой сумму скачков потенциала на границах раздела фаз, является в то же время суммой всех гальвани потенциалов. Е = gМ1L1 + gL1L2 + gL2M2 + gМ2M1
Если в электрохимической системе потенциал gL1L2 отсутствует, то Е = gМ1L1 - g M2L2 - gМ1M2
С другой стороны ЭДС представляет собой разность двух электродных потенциалов, то есть
Е = п - л
2. Концентрационные электрохим. цепи Оба электрода идентичны по физическому состоянию и по химической природе. Они отличаются концентрацией компонентов Ox и Red.
Источником электрической энергии является разность свободных энергий Гиббса, обусловленная различными активностями одних и тех же химических компонентов.
Концентрационные цепи можно приготовить следующим образом:
1.Из амальгам разных концентраций в одном и том же растворе;
2.Из одинаковых электродов 1 и 2 рода, находящихся в растворах разной концентрации (активности);
3.Из одинаковых газовых электродов, работающих при разных давлениях.
Различают концентрационные цепи без переноса и с переносом. При работе концентрационных цепей идёт выравнивание активностей или давлений. Cu Zn (Hg)(a1) ZnSO4 Zn (Hg)(a2) Cu цепь без переноса Если а1 > а2, то левый электрод – анод, а правый – катод. E = к - а = RT/2F ln a1/a2Zn ZnSO4 (а’) ZnSO4 (a’’) Zn цепь с переносом Если а’ < а’’, то левый электрод – анод, а правый – катод. E = к - а = RT/2F ln a’’/a’ К: Cu2++2e=Cu0 А: Cu0-2e=Cu2+
3. электролиз расплавленных солей широко используется для получения легких, тугоплавких, редких металлов, сплавов, фтора, хлора, для рафинирования металлов. Применение электролиза расплавленных солей весьма перспективно для получения сплавов и соединений, а так же для нанесения гальванических покрытий и обработки поверхности металлов.
высокая интенсивность процесса, которая может в 25-100 раз превышать интенсивность электролиза водных растворов;
возможность работы в широком диапазоне температур и концентрацией электролита; значительное сокращение расхода воды.
значительный удельный расход электроэнергии,
повышенные капитальные и эксплуатационные затраты на охрану окружающей среды,
В настоящее время считается, что расплавленные соли близки по своему строению к твердому веществу. Расплавленные соли при температурах, близких к температуре плавления, наследуют структуру твердого в-ва. Структура твердого кристалла характеризуется дальним порядком, т.е. правильным расположением частиц одна около другой во всем объеме кристалла.Но имеются разл дефекты.они увел-ся с увел-ем темп-ры,тем самым уменьшают дальний порядок.При переоде в жидкое сост-е дальний порядок полностью нар-ся,но созр ближний порядок.ряд солей имеют молекулярную стр-ру при их нагревании стр-ра сохр,расплав становится непроводящим.Для некоторых солей характерна слоистая стр-ра, в этом случае кристалл состоит из отдел-х пакетов.
