
- •II член
- •Глава 26 рак пищевода
- •Глава 27 нагноительные заболевания лёгких и плевры
- •Глава 28 рак легкого
- •Глава 20 врождённые пороки сердца и крупных сосудов
- •Глава 30 приобретенные пороки сердца
- •Глава 31 перикардиты
- •Глава 33 хрургическое лечение аритмий
- •Глава 34 острая артериальная непроходимость
- •Глава 35 хронические облитерирующие заболевания аорты и её ветвей
- •Глава 36
- •Глава 37 острые венозные тромбозы
- •38 Глава
- •I. Локализация
- •II. Степень нарушения перфузии лёгких
- •III. Характер гемодинамических расстройств
- •IV. Осложнения
- •39 Глава хроническая венозная
- •Эндокринная хирургия
- •Глава 41 опухоли надпочечников
- •Хирургия молочных желёз
- •Глава 42 острый мастит
- •Глава 43 дисгормональные
- •Глава 44 рак молочной железы
- •Рекомендуемая литература
II член
ТОРАКАЛЬНАЯ ХИРУРГИЯ 24 глава
ТРАВМА ГРУДИ
Травма груди включает в себя повреждения грудной клетки и органов грудной полости. Учение об этом разделе хирургии как самостоятельной проблеме сформировалось лишь в последние десятилетия XX века, хотя интерес к ней прослеживается на протяжении всей истории медицины. Особенности современного травматизма в условиях роста дорожно-транспортных происшествий, падений с высоты, техногенных катастроф, локальных военных конфликтов, террористических актов с использованием взрывных устройств выдвигают травму груди, в особенности сочетанную, на одно из первых мест по тяжести течения и числу неблагоприятных исходов.
Основные черты патологии
Патологические изменения, возникающие при травме груди, включают весь спектр механических повреждений тканей грудной клетки и органов грудной полости: от сотрясения и ушиба до разрывов, переломов, размозжений и ранений (мягкие ткани грудной стенки, рёбра, лёгкие, бронхи, перикард и сердце, крупные сосуды, диафрагма, нервные стволы и др.). Эти изменения в тканях и органах относятся как к прямым повреждениям, возникающим в месте приложения силы, так и к травме рёбер, лёгочной ткани, сосудов, возникающим в отдалении. Они могут быть изолированными (один орган или одно ребро) или множественными (несколько рёбер, ранение лёгкого и перикарда, лёгкого и диафрагмы и т.п.).
Анатомические особенности грудной клетки, органов средостения и лёгких в определённой мере отражаются на характере их повреждений, диагностике и лечебной тактике. По строению рёбра имеют вид дуг, слегка наклонённых книзу. Сдавление грудной клетки в передне-заднем направлении нередко вызывает переломы как в области прямого приложения силы, так и в зоне сгибания или даже с противоположной стороны (рис. 24-1). Все рёбра взрослых, кроме I и II, на всём протяжении имеют губчатое строение, заполнены красным костным

Рис. 24-1. Варианты переломов рёбер в зависимости от места приложения силы при закрытой травме груди.
мозгом. Поэтому в месте перелома всегда возникает гематома, даже если межрёберные сосуды не повреждены. Объём такой гематомы составляет в среднем 100 мл. Это позволяет легко рассчитать общую кровопотерю при множественных переломах рёбер.
Особенностью травмы груди является и то, что рёберный каркас, защищающий органы груди от внешних воздействий, в ряде случаев становится источником вторичных их повреждений отломками рёбер, при этом чаще всего страдают лёгкие. Состояние лёгких после травмы во многом определяется стороной повреждения (правое или левое лёгкое) и обусловлено шириной бронхов, начиная с главного, углами их отхождения и длиной. Слева условия для вентиляции всегда хуже, чем справа, так же, как и для эвакуации крови и мокроты из просвета бронхов, поэтому опасность развития ателектаза и пневмонии всегда больше.
Органы средостения достаточно хорошо защищены от травматических воздействий. И всё-таки характерная горизонтальная конфигурация груди с позвоночным столбом, выступающим кпереди почти на треть передне заднего поперечника грудной клетки, иногда создаёт условия для типичных повреждений главных бронхов и начального отдела нисходящей аорты как раз у позвоночного столба. Это чаще случается у молодых людей при «локальных», но достаточно интенсивных ударах (дети — на качелях, молодые люди — в дорожно-транспортных происшествиях).
Функции органов, заключённых в грудной полости, многообразны, но главными из них являются дыхание и кровообращение. В основе всех патофизиологических нарушений при травме груди лежат кардиореспираторные расстройства, они требуют неотложной профилактики и лечения. При торакальной травме эти нарушения чаще всего являются взаимообусловленными. Они и сегодня остаются главными причинами смерти каждого третьего пострадавшего с сочетан-ными повреждениями груди, хотя 15% погибших не имеют абсолютно смертельных поражений. Расстройства дыхания, возникающие при травме груди, развиваются в результате нарушения дыхательных экскурсий рёбер и диафрагмы, коллабирования лёгочной ткани за счёт крови или воздуха, скопившегося в плевре, непосредственного поражения лёгких или бронхов. Во всех случаях это сопровождается гипоксией, значительным повышением лёгочного сосудистого сопротивления и гипертензией малого круга кровообращения, что ограничивает венозный возврат к левому предсердию. Страдает диастолическая, а затем и систолическая функция левого и правого желудочков. Непосредственное повреждение сердца ещё более снижает СВ.
Одним из самых серьёзных синдромов, развивающихся при травме груди, является шок. Он обусловлен, прежде всего, множественным характером поражения органов. Прямое травматическое воздействие на широкую сеть нервно-сосудистых образований, включая структуры вегетативной нервной системы, регулирующие функции кардиореспираторного комплекса, ещё более увеличивает «шоко-генность» травмы. Наиболее выраженные изменения гемодинамики отмечаются на 2-е и 3-й сутки после травмы. Именно в этот период достигают максимума расстройства вентиляции и газообмена, обусловленные поражениями лёгких и бронхов.
Независимо от причины поражения, у пострадавших при травме груди формируется несколько типичных синдромов, определяющих диагностику, тактику лечения и характер типичных осложнений. Главными среди них являются пневмоторакс, гемоторакс, подкожная эмфизема и эмфизема средостения. Они имеют свои особенности при различном характере травмы.
Гемоторакс — скопление крови в плевральной полости. Источником кровотечения могут быть сосуды межреберий или повреждённого лёгкого. Принято различать малый гемоторакс — кровь в пределах рёберно-диафрагмального синуса, средний — скопление крови от угла до уровня середины лопатки, большой — уровень крови выше середины лопатки. Гемоторакс, возникающий в связи с повреждением лёгких или бронхов, почти всегда сопровождается скоплением воздуха в плевральной полости и коллапсом лёгкого, т.е. развитием ге-мопневмоторакса. Только при нетяжёлых закрытых травмах возникает пневмоторакс без гемоторакса. Основная опасность этого осложнения при закрытой травме — возможность формирования клапанного пневмоторакса. Он развивается тогда, когда дефект в лёгком не слишком велик и воздух поступает в плевральную полость лишь при кашле, разговоре, реже — при вдохе. На выдохе же путь выхода воздуха из плевральной полости в бронхи оказывается закрытым своеобразным клапаном (спадающаяся рана лёгкого или лоскут плевры, который прикрывает дефект в момент выдоха). В результате лёгкое кол-лабируется за счёт избыточного давления воздуха в плевральной полости, органы средостения смещаются в противоположную сторону, происходит сдавление крупных сосудов, прежде всего полых вен, что является основной причиной тяжёлых кардиореспираторных расстройств, возникающих в этот момент.
Проявлениями травмы лёгкого или крупных бронхов являются также эмфизема средостения и подкожная эмфизема. Они развиваются чаще при заращённой плевральной полости (вследствие предшествующих болезней или травм) и возникают тогда, когда повреждение лёгкого или бронха расположено близко к корню, на участках, прикрытых медиастинальной плеврой, или в зоне переломов рёбер, отломками которых повреждаются внутригрудная фасция, плевральные листки и лёгкое. При массивном и быстром поступлении воздуха может возникнуть ситуация, обозначаемая как «напряжённая медиастинальная эмфизема», чреватая сдавлением крупных венозных стволов (лёгочные и полые вены) и уменьшением притока крови к сердцу.
Подкожная эмфизема может быть ограниченной, распространённой и тотальной. Распространённая подкожная эмфизема и эмфизема средостения без напряжения серьёзной угрозы для жизни больного не представляют, так как не вызывают существенных кардиореспираторных расстройств.
Открытые повреждения груди подразделяют на непроникающие и проникающие. Последние характеризуются нарушением целостности париетальной плевры, независимо от того, имеются сращения лёгкого с грудной стенкой в зоне ранения или нет. При непроникающих ранениях повреждаются лишь мягкие ткани грудной стенки. Они относятся чаще всего к категории лёгких, хотя иногда и могут сопровождаться значительной наружной кровопотерей. Проникающие ранения всегда опасны в связи с возможностью травмы органов грудной клетки, брюшной полости и забрюшинного пространства. Для проникающих ранений патогномоничны те же синдромы, что и при закрытых травмах. Однако механизмы их возникновения, клиническая картина и тактика лечения несколько иные.
Источником кровотечения и формирования гемоторакса при открытой травме груди могут быть межрёберные сосуды, внутренняя грудная артерия, сосуды лёгкого, средостения и раны сердца. Следует отметить, что количество определяемой в момент исследования крови не всегда даёт основание определить источник кровотечения и сформулировать тактику лечения. Решающее значение иногда приобретает темп кровопотери, определяемый по количеству крови, вытекающей по дренажам за 1 ч.
Характерным признаком проникающего ранения груди является открытый пневмоторакс. Он возникает, когда рана груди достаточно широка, раневой ход идёт в зонах груди с относительно небольшой толщиной мышц (нижняя передняя и нижняя задняя области груди), а по отношению к грудной стенке — в радиальном направлении. Воздух в плевральную полость попадает на вдохе через рану, на выдохе он частично выходит обратно. С каждым вдохом давление в плевральной полости стремится к выравниванию с атмосферным давлением за счёт коллабирования лёгкого. Расстройства дыхания и кровообращения при этой ситуации также могут стать угрожающими, хотя они менее выражены, чем при напряжённом пневмотораксе. Возможно формирование и клапанного механизма, когда воздух в плевру поступает через рану, которая приоткрывается на вдохе и оказывается «прикрытой» в момент выдоха за счёт смещения слоев мышц вслед за экскурсией рёбер. Формирование клапанного пневмоторакса возможно и при ранении лёгкого, когда воздух в плевре накапливается по тому же механизму, что и при закрытой травме.
Классификация
Характер травмы груди:
закрытая;
открытая (проникающая): ранения колото-резаные, огнестрельные; слепые, сквозные. Состояние костного скелета:
повреждения рёбер, грудины или позвоночника;
без повреждений. Повреждение внутренних органов:
• ранения лёгкого, трахеи, бронхов, сердца, крупных сосудов, не парной вены, грудного протока, пищевода;
отсутствуют. Осложнения:
пневмоторакс: открытый, закрытый, клапанный, напряжённый;
эмфизема: подкожная, медиастинальная;
ателектаз лёгкого;
пневмония;
респираторный дистресс-синдром;
гемоторакс: малый, средний, большой (тотальный);
тампонада сердца;
хилоторакс;
абсцесс лёгкого, эмпиема плевры, гнойный медиастенит.
Диагностика
Определение характера повреждений при травме груди основывается на планомерном и тщательном физикальном обследовании больного, применении необходимых инструментальных методик, использовании лабораторных исследований и средств медицинской визуализации (рентгенологических, ультразвуковых и др.). Всё это должно обеспечить правильную диагностику в период первичного обследования больного или в максимально короткие сроки и установление всех характеристик полученной больным травмы.
При клиническом обследовании следует обратить внимание на обстоятельства травмы и динамику развития болезненных проявлений. При этом врачу следует быть наиболее внимательным в случаях раннего обращения пострадавшего и относительно нетяжёлого его состояния, так как многие опасные синдромы могли просто ещё не сформироваться.
Жалобы на боли в груди, усиливающиеся при вдохе, движениях и кашле, характерны для повреждений рёберного каркаса. Появление нелокализованных болей на стороне поражения, не стихающих при изменении положения тела, и беспокойное поведение больного чаще свидетельствуют о наличии крови в плевральной полости. Острое начало боли и постепенное её «притупление» наряду с нарастающей на этом фоне одышкой заставляют предположить наличие пневмоторакса. Одышка и затруднённое дыхание имеют место практически всегда, их стихание спустя 2-3 сут не должно успокаивать внимание врача, т.к. и в этом случае необходимо полноценное обследование больного.
Нарушения гемодинамики идентичны при различных видах поражений, они требуют к себе самого пристального внимания. Очень важны использование и комплексная оценка физикальных, электрофизиологических и ультразвуковых методик.
При обнаружении подкожной эмфиземы всегда следует обращать внимание на локализацию её в яремной ямке, на шее, появление осиплости голоса, что свидетельствует о развитии эмфиземы средостения. Несмотря на сложность оценки результатов перкуссии и аускульта-ции, особенно при обширной подкожной эмфиземе, они должны проводиться. Особое внимание следует уделять границам средостения, характеру изменений тонов сердца и дыхания не только на стороне поражения, но и на контрлатеральной.
У 15% госпитализированных в стационар по поводу травмы груди имеются повреждения органов брюшной полости, поэтому физикаль-ное обследование живота также обязательно. Необходимо внимательное изучение локализации ран, однако расположение раны само по себе не может быть основополагающим для исключения тех или иных внутригрудных или сочетанных поражений внутренних органов, так как характер использующихся сегодня средств и приёмов нанесения ран нередко непредсказуем. Тем более это невозможно при огнестрельном характере ранения.
Широкое использование лабораторных методов повышает точность диагностики. Речь идёт не только о стандартном определении количественных показателей крови, позволяющих оценить кровопотерю. Имеющиеся сегодня в клиниках приборы дают возможность объективно оценить степень насыщения крови кислородом, следить за быстро меняющимися пульсом и АД. Методы мониторного наблюдения позволяют зарегистрировать изменения сократительной способности миокарда и нарушения центральной гемодинамики.
Обследование больного обязательно включает рентгенологическое исследование. Начинать его следует с рентгенографии грудной клетки в двух проекциях (обзорный снимок и боковые снимки правой и левой сторон). Этого в большинстве случаев бывает достаточно, чтобы установить диагноз или обосновать необходимость дополнительных исследований. Обширную информацию о характере поражения внутренних органов при множественных повреждениях даёт КТ. Ею иногда и завершают обследование.
В последние годы всё шире стали использовать УЗИ. Оно позволяет неинвазивным способом выявить, прежде всего, наличие и характер скоплений крови (и сгустков) в плевральной полости, их локализацию, сопутствующий пневмоторакс. Методика применима даже у больных, находящихся в бессознательном состоянии, когда провести полипозиционное рентгенологическое обследование сложно. Ещё более информативен этот метод для выявления скоплений крови в полости перикарда.
В экстренных ситуациях при стремительном ухудшении состояния больного и клинической картине пневмоторакса полезной оказывается плевральная пункция, которая носит в этом случае не только диагностический, но и лечебный характер. При подозрении на тампонаду сердца вследствие кровотечения в полость перикарда, что проявляется резким снижением АД, быстрым и значительным повышением центрального венозного давления и значительным ослаблением тонов сердца, пункция перикарда становится совершенно необходимой. Место для пункции плевральной полости выбирают с учётом данных физикального и рентгенологического исследований. Пункции перикарда проводятся в типичных точках (рис. 24-2).
Торакоскопия необходима для установления факта продолжающегося кровотечения в плевральную полость и выявления источника кровотечения. Её также используют в качестве способа хирургической остановки кровотечения путём электрокоагуляции или клипиро-вания сосудов. При невозможности выполнить подобные манипуляции эндоскопическим способом торакоскопия позволяет чётко аргументировать показания к торакотомии. Торакоскопия всегда заканчивается эвакуацией крови и дренированием плевральной полости.
Бронхоскопия и эзофагоскопия в диагностике внутригрудных поражений показаны при обоснованных подозрениях на разрыв главных бронхов и повреждение пищевода.
Необходимость дифференциальной диагностики основных патологических синдромов травмы груди в остром периоде возникает редко. Наиболее часто в этой стадии допускаются ошибки в распознавании разрыва левого купола диафрагмы с перемещением желудка в грудную полость в связи с тем, что воздушный пузырь желудка над уровнем жидкости, иногда располагающийся на уровне угла лопатки и выше, принимают за гемопневмоторакс. У больных, перенёсших ранее травмы или плевриты с обширными плевральными изменениями, рентгенологическая картина иногда напоминает малый или даже средний гемоторакс. Методически правильно выполненное рентгенологическое исследование, контрастирование пищевода и желудка позволяют устранить все сомнения.
Лечение
Лечебная тактика при травме груди определяется тяжестью состояния пострадавшего, выраженностью нарушений дыхания и кровообращения, характером повреждений, прежде всего рёберного каркаса и органов грудной полости. Во всех случаях основными задачами являются ликвидация опасных для жизни состояний, восстановле- ние целостности и функций поражённых органов, профилактика осложнений. Дискуссия о тактике лечения (консервативные методы или «максимально хирургические») разрешилась в последние годы в пользу всё более широкого использования эндоскопических методик. Это позволяет сформулировать основной тактический принцип: лечение пострадавших при травме груди должно быть активным, с применением малотравматичных способов устранения основных патологических синдромов и своевременным выполнением по обоснованным показаниям торакотомии. Обязательным должно быть строгое обоснование как показаний к торакотомии, так и отказа от неё. Особенности патологических синдромов, возникающих при закрытой и открытой травмах груди, требуют лечебных мероприятий, ориентированных на каждый из этих видов поражений.
Закрытая травма груди
При закрытой травме груди, особенно сочетанной, жизнеугрожа-ющие состояния обусловлены нарушениями проходимости верхних дыхательных путей вследствие скопления в них мокроты, рвотных масс или крови, компрессией лёгких при скоплении в плевре крови и воздуха или из-за нарушений экскурсии грудной клетки в связи с множественными переломами рёбер. Во всех случаях имеет место выраженный болевой синдром. При развёрнутой картине сердечнососудистой и дыхательной недостаточности лечение начинается с восстановления проходимости дыхательных путей путём интубации трахеи и бронхоскопии.
Обязательно проводится обезболивание. При переломе одного или двух рёбер это возможно путём введения местных анестетиков в место перелома или за счёт паравертебральной блокады межреберий выше и ниже повреждённого ребра (рёбер) либо с помощью вагосимпати-ческой блокады. При множественных переломах рёбер эта методика не даёт надёжного результата. Её применяют только в период транспортировки больного в специализированный стационар, где может быть осуществлена перидуральная блокада с оставлением катетера в перидуральном пространстве для повторного введения анестетиков.
Клинические проявления напряжённого пневмоторакса диктуют необходимость выполнения пункции и дренирования плевральной полости. Кардиореспираторные нарушения в остром периоде купируют введением сердечных средств и дыхательных аналептиков, плаз-мозамещающих растворов, ингаляцией кислорода. Лечение гемоторакса и пневмоторакса может быть осуществлено повторными пункциями или дренированием плевральной полости. Лучшие результаты удаётся получить путём выполнения лечебной торакоскопии уже в момент госпитализации пострадавшего в стационар. В процессе выполнения этой процедуры можно осуществить остановку кровотечения, герметизацию небольших дефектов лёгкого, удалить все сгустки крови и установить дренажи таким образом, чтобы они наиболее эффективно обеспечивали эвакуацию воздуха и экссудата из плевральной полости.
Широкая торакотомия при закрытой травме груди должна быть выполнена в связи со следующими обстоятельствами.
I. Гемостатические показания: 1) продолжающееся внутриплевральное кровотечение; 2) внутриперикардиальное кровотечение с развитием тампонады сердца; 3) кровоизлияния в клетчатку средостения со сдавлением воздухопроводящих путей, смещением и сдав- лением магистральных кровеносных сосудов.
II. Аэростатические показания возникают при безуспешном откачивании пневмоторакса и беспрерывном его восстановлении, несмотря на дренажи и постоянно действующую эндоплевральную аспирацию. В особо срочном порядке надо оперировать пострадавших с напряжённым пневмотораксом, сопровождающимся смещением средостения, нарастающей эмфиземой последнего и развитием экстраперикардиальной тампонады сердца.
III. Дополнительные показания: 1) повреждение диафрагмы; 2)прогрессивное ухудшение состояния пострадавшего, несмотря на применение комплекса консервативных мероприятий.
Из «частных» проблем лечения закрытой травмы груди следует отметить переломы рёбер и грудины, травмы лёгких, сердца, разрывы крупных сосудов и бронхов.
Переломы рёбер и грудины
Основное требование при лечении пострадавших с переломами рёбер — эффективное обезболивание. Это необходимое условие даже при одиночных переломах, особенно у лиц, страдающих хроническим бронхитом. Неустранённая боль и вследствие этого неэффективный кашель способны в очень короткие сроки осложнить течение травмы обострением гнойно-воспалительных процессов в бронхах и лёгких. Сложную проблему представляет лечение «флотирующих переломов». Как правило, они являются показанием к длительной ИВЛ.
Переломы грудины обычно редко требуют специальных приёмов репозиции или оперативных вмешательств. При эффективном обезболивании путём введения анестетиков в место перелома и укладывании больного на валик отломки «встают» на место.
Повреждения лёгких
Повреждения лёгких при закрытой травме груди представлены ушибами, гематомами и разрывами. Первые две формы требуют проведения всех мероприятий, улучшающих проходимость бронхов. Для этого необходимы ингаляции аэрозолей, содержащих бронхолитики, муко-литики и антисептики. Показаны периодические санационные бронхоскопии с введением в просвет бронхов смесей этих же препаратов.
Более сложной проблемой лечения являются разрывы лёгкого. Наличие разрывов само по себе ещё не является показанием к торакото-мии, так как раны лёгкого склонны закрываться достаточно быстро самостоятельно или вследствие применения менее травматичных методик (коагуляция, клипирование, наложение швов через торакопорт под контролем торакоскопии). Лечение начинают с эффективного дренирования плевральной полости и контроля за восстановлением её герметичности. Степень герметичности плевры оценивают по сбросу воздуха через дренажи. Возможны три варианта: а) воздух выходит при каждом вдохе; б) воздух выходит при разговоре; в) воздух выходит только при кашле. По изменению условий «продувания» можно сделать заключение: идёт процесс восстановления герметичности лёгкого или нет. При отсутствии каких-либо положительных сдвигов или при отрицательной динамике используют методику расправления лёгкого путём временной окклюзии поролоновым обтуратором долевого или главного бронха негерметичного лёгкого с активной аспирацией воздуха из плевры. Обтуратор вводят в бронх и извлекают посредством бронхоскопии жёстким бронхоскопом под наркозом. В течение 2— 3 сут дефекты на лёгком успевают прикрыться фибрином, грануляциями, и после удаления обтуратора у большинства больных пневмоторакс не возобновляется. Если этого не происходит, становится необходимой торакотомия, особенно у пострадавших с исходно нарушенными показателями вентиляции лёгкого. Обычно выполняют боковую или переднебоковую торакотомию в V—VII межреберье. Объём вмешательства определяется обширностью дефектов лёгочной ткани и может заключаться в ушивании ран или резекции разрушенных участков лёгкого.
Разрывы трахеи и крупных бронхов
Разрывы трахеи и крупных бронхов относятся к редким повреждениям при закрытой травме груди. Разрывы бронхов могут быть полными (отрыв), частичными или в виде переломов хрящевого каркаса без повреждения слизистой оболочки. Диагностика их в остром периоде травм основывается на неэффективности всех мероприятий по восстановлению герметичности плевральной полости и на данных бронхоскопического обследования. При своевременно установленном диагнозе возможно выполнение восстановительных операций в остром периоде. Между тем, чаще повреждения бронхов выявляют на более поздних стадиях при уже формирующихся Рубцовых стенозах или окклюзиях бронхов в месте их повреждения. Резекция суженного участка бронха с наложением межбронхиального анастомоза обычно даёт хорошие результаты.
Травма сердца
Травма сердца встречается довольно часто - у 8% больных, госпитализированных по поводу закрытой травмы груди. Патомор-фологические исследования показывают, что тяжёлая травма груди сопровождается структурными и метаболическими нарушениями в миокарде даже при отсутствии видимых его повреждений. Для уточнения диагноза иногда необходимы специальные исследования. Лечебная тактика при закрытой травме сердца определяется характером повреждения и тяжестью расстройств сердечной деятельности. При ушибах проводят в основном консервативное лечение, напоминающее терапию коронарной недостаточности или инфаркта миокарда. Оно предполагает создание покоя, нормализацию ритма, проводимости, электрической активности и сократительной способности миокарда, купирование болевого синдрома, нормализацию гемодинамики, противовоспалительную терапию. Продолжительность постельного режима зависит от тяжести состояния и составляет 2—3 нед. Необходимо проводить санацию верхних дыхательных путей, оксигенотерапию. Назначают седативные и болеутоляющие средства. Переливание крови или кровезаменяющих жидкостей должно быть ограниченным и проводиться строго по показаниям.
Необходимость оперативного лечения при ушибах сердца возникает только в случаях поздних осложнений — нарастании сердечной
недостаточности в связи с формированием аневризмы или наличием сдавливающего перикардита.
При разрывах мышечной стенки сердца, в том числе сквозных, смерть не всегда наступает моментально. Некоторые такие больные поступают в стационар и подлежат срочному оперативному вмешательству, независимо от времени, прошедшего с момента травмы. Показания к операции — гемоперикард, подтверждённый клинически, рентгенологически или пункцией; тампонада сердца; внутриплев-ральное кровотечение.
При внутренних травматических разрывах (например, повреждение клапанов) вначале проводят консервативную терапию, направленную на лечение сердечной недостаточности. В случаях прогрес-сирования нарушений гемодинамики показана первичная реконструктивная операция.
Разрывы аорты
Разрывы аорты относятся к наиболее тяжёлым повреждениям при закрытой травме груди. Большая часть пострадавших погибают, вместе с тем до 20% из них поступают в стационар живыми. Клинические проявления возможны в двух вариантах: 1) массивное кровотечение в плевральную полость; 2) неясная клиническая картина, дефицит пульса на сонных артериях слева, расширение средостения на рентгенограмме, смещение пищевода и трахеи вправо. При первом варианте разрыв аорты обнаруживают обычно во время операции, предпринятой по поводу массивного внутригрудного кровотечения. Диагностика при втором типе, соответствующем повреждению аорты без разрыва адвентиции, основывается на данных КТ и аорто-графии. Во всех случаях выявления повреждений аорты (или при обоснованных подозрениях) показаны немедленная торакотомия и выполнение восстановительных операций.
Повреждения диафрагмы
Установленный диагноз закрытого разрыва диафрагмы должен считаться основанием для срочной операции. Нельзя предвидеть время опасного для жизни ущемления и некроза переместившихся в плевральную полость органов. Операцию выгоднее производить чрез-плеврально. Оптимальным является разрез по VII или VIII межреберью из бокового доступа. Неушитые раны диафрагмы, как правило, приводят к образованию диафрагмальной грыжи.
Открытая травма груди
Лечение раненых при открытых травмах груди во многом определяется характером ранящего снаряда (огнестрельные ранения, взрывные поражения, колото-резаные ранения), а объём хирургической помощи определяется обширностью и особенностями поражения внутренних органов. Лечебные мероприятия при непроникающих ранениях включают в себя хирургическую обработку раны, профилактику инфекционных осложнений, оперативные способы закрытия раневых дефектов и пластические операции в более позднем периоде при формировании стойких изменений в мягких тканях и рёберном каркасе грудной стенки.
Проникающие ранения
Проникающие ранения, сопровождающиеся открытым пневмотораксом, требуют ушивания раны грудной стенки. Полезно в этот момент выполнить торакоскопию для обнаружения возможных ранений органов груди, диафрагмы и источника кровотечения, если оно продолжается. Операцию всегда заканчивают дренированием плевральной полости. Оно включает в себя установку двух дренажей: нижнего, ближе к синусу, направленного кзади, и верхнего, дренирующего пе-реднебоковые отделы плевральной полости. Первый дренаж обеспечивает отток экссудата, появление которого возможно вследствие инфицированности плевральной полости, а второй создаёт условия для эвакуации воздуха и максимально быстрого расправления лёгкого.
Показания к срочной торакотомии при проникающих ранениях груди возникают при: 1) большом гемотораксе; 2) продолжающемся внутриплевральном кровотечении, когда по дренажу выделяется 250-300 мл крови в час; 3) ранениях сердца и диафрагмы; 4) ухудшении состояния больного на фоне комплексной терапии и в связи с возникающим подозрением на повреждение органов груди. В комплексе лечебных мероприятий при проникающих ранениях груди должны быть предусмотрены меры по адекватному обезболиванию, восполнению кровопотери, борьбе с дыхательными и циркуляторными расстройствами, а также антимикробная терапия.
Ранение лёгкого
Хирургическая тактика при ранении лёгкого, которое не сопровождается продолжающимся к моменту госпитализации кровотечением, принципиально не отличается от таковой при закрытой травме груди. Показания к торакотомии возникают при отсутствии тенденции к восстановлению герметичности плевральной полости и повторных коллапсах лёгкого.
Повреждения трахеи и бронхов
Повреждения трахеи и бронхов чаще наблюдают при огнестрельных ранениях. Это очень тяжёлые ранения, диагностика которых строится на тех же принципах, что и в случаях закрытой травмы груди. В связи с одновременными ранениями крупных сосудов факт ранения трахеи или крупных бронхов чаще выявляют в процессе неотложной торакотомии, предпринятой по поводу кровотечения. К сожалению, в связи с особенностями течения огнестрельной раны первичное восстановление целостности трахеи или бронхов часто осложняется несостоятельностью анастомозов и швов, что в последующем, если удаётся ликвидировать гнойно-септические осложнения, требует проведения ряда реконструктивно-восстанови-тельных операций.
Ранения перикарда и сердца
Ранения перикарда и сердца стоят на втором месте по частоте. При этом только у трети пострадавших имеется изолированное повреждение перикарда, а у остальных одновременно поражается и сердце. Клиническая картина и хирургическая тактика обусловлены локализацией раны на сердце, её размером и глубиной. Диагностика строится с учётом локализации раны на грудной стенке, общего состояния больного, особенностей кровотечения и признаков тампонады сердца. Чем ближе рана к проекции сердца на переднюю стенку груди, тем более вероятно его ранение. Обращают на себя внимание стремительное нарастание бледности, появление холодного пота на лице, обморочного состояния. При этом чаще всего определяют большой гемоторакс, набухание шейных вен, глухие тоны сердца, парадоксальный пульс (рис. 24-3), что свидетельствует о скоплении крови в перикарде и сдавлении сердца.
Лечение ранений сердца должно быть только хирургическим, пункция перикарда преследует цель временной декомпрессии его на этапе вводного наркоза и торакотомии. Раны сердца ушивают отдельными швами, иногда используют «прокладки» из аутоперикарда. Следует обратить внимание на обязательный осмотр и ревизию задней поверхности сердца, так как ранение может быть сквозным.
Повреждения пищевода и грудного лимфатического протока
Повреждения пищевода и грудного лимфатического протока встречаются достаточно редко, не имеют чётко очерченной клинической симптоматики в остром периоде травмы и выявляются или в момент операции, предпринятой по другим показаниям, или в связи с формирующимися осложнениями (медиастинит, хилоторакс). Выявленная во время операции рана пищевода должна быть ушита двухрядным швом, который дополнительно укрывают лоскутом плевры или прядью большого сальника. Средостение и плевральную полость следует дренировать, а пищевод «выключить» из пассажа по нему пищи путём гастростомии или введения назогастрального зонда. К сожалению, у многих больных повреждение пищевода выявляется лишь после возникновении медиастинита и других воспалительных осложнений. В таких случаях показаны дренирующие средостение вмешательства, а при прорыве гнойника в плевру — торакотомия. Что касается повреждений грудного протока, то хирургическое лечение должно быть предпринято при неэффективности повторных пункций плевральной полости в течение 8—10 дней. Операция чаще всего заключается в лигировании протока выше и ниже повреждения.
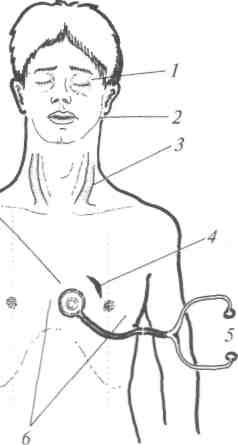
— рана в проекции сердца;
— глухие стоны сердца; 6 — расширение границ сердца; 7— снижение АД; 8 — урежение сердечного ритма и снижение вольтажа на ЭКГ.
Осложнения
У пострадавших с травмой груди имеется определённая закономерность возникновения ближайших и отдалённых осложнений. В остром периоде наиболее частой причиной гибели больных служит острая кровопотеря. В раннем постшоковом периоде на первое место выходят лёгочные осложнения, причинами которых могут быть неадекватное дренирование плевральной полости, плохое обезболивание, и недостаточная вентиляция лёгких. Наиболее частое и опасное осложнение этого периода — формирование респираторного дистресс-синдрома взрослых. Он сопровождается нарушением функций сердечно-сосудистой системы, ЦНС и жизненно важных паренхиматозных органов. Исход его характеризуется очень высокой летальностью (до 50%), но ранняя диагностика и своевременно начатое лечение позволяют получить обнадёживающие результаты. Методы профилактики респираторного дистресс-синдрома взрослых при травме груди включают адекватное обезболивание, устранение гемоп-невмоторакса, восстановление каркасной функции грудной клетки и обеспечение адекватной вентиляции лёгких.
Пневмония — типичное раннее осложнение травм груди. В основе этого осложнения лежат микроэмболии сосудов малого круга кровообращения, поражение сурфактантной системы и нарушения дренажной функции бронхов. С учётом перечисленных факторов должны строиться мероприятия по профилактике и лечению пневмонии.
В более позднем периоде возможно развитие острой и хронической эмпиемы плевры, причиной которой является неполное устранение гемоторакса, длительно существующая негерметичность лёгкого, неадекватное дренирование плевральной полости и подавление механизмов иммунной защиты.
По мере роста числа пострадавших сформировалась устойчивая группа пациентов с поздними осложнениями: стенозами и окклюзи-ями трахеи и бронхов, пищеводно-бронхиальными свищами, диаф-рагмальными грыжами и др. Часто они требуют проведения сложных реконструктивных вмешательств.
ДОБРОКАЧЕСТВЕННЫЕ
ЗАБОЛЕВАНИЯ
И ПОВРЕЖДЕНИЯ ПИЩЕВОДА
В этой главе рассматриваются разнообразные по своей природе патологические состояния, которые обусловливают нарушения функционирования пищевода, по которому пища поступает в ЖКТ. Это, в первую очередь, нервно-мышечные заболевания, грыжи пищеводного отверстия диафрагмы и дивертикулы пищевода, последствия ожогов и травм.
Основные черты патологии
Физиологическая роль пищевода заключается в проведении пищи из полости глотки в желудок. Основную роль в этом процессе играют три механизма: впрыскивающий эффект глотки, сила тяжести и гидростатическое давление пищи, а также перистальтика пищевода. В зависимости от характера пищи тот или иной механизм имеет преобладающее значение в продвижении пищи по пищеводу. Так, глоток воды быстро, за 2—3 сек, попадает в желудок, значительно опережая активную перистальтику пищевода. Считают, что прохождение жидкой пищи обеспечивается в основном силой тяжести, гидростатическим давлением и впрыскивающим эффектом глотки. При прохождении по пищеводу плотного пищевого комка (оно продолжается от 8 до 12 сек) ведущая роль принадлежит перистальтической волне.
В спокойном состоянии в пищеводе поддерживается относительно стабильное давление. Верхний и нижний пищеводные сфинктеры отделяют зону слабо отрицательного давления от положительного давления в глотке и желудке. Тоническое напряжение циркулярных волокон этих сфинктеров создаёт в норме верхнюю и нижнюю зоны повышенного давления покоя, что является довольно мощным ан-тирефлюксным барьером, благодаря, в основном, односторонней проходимости зоны нижнего пищеводного жома. Для того, чтобы пища из пищевода попала в желудок, достаточно повышения давления на 4 мм рт.ст. Для регургитации необходим подъём давления на 80 мм рт.ст. В предотвращении заброса содержимого желудка в пищевод имеют значение несколько механизмов: нижний пищеводный сфинктер, создающий зону повышенного давления; острый угол Хиса, образованный стенкой пищевода и дном желудка; клапан, представляющий собой складку слизистой оболочки в месте перехода многослойного плоского неороговевающего эпителия пищевода в цилиндрический эпителий желудка, и связка, удерживающая пищевод в одноимённом отверстии диафрагмы.
Различные заболевания нарушают этот стройный механизм. Они характеризуются в основном симптомами, связанными с затруднением прохождения пищи по пищеводу, а также рефлюксом в пищевод содержимого желудка.
Дисфагия — ощущение замедления или препятствия при продвижении пищи по глотке и пищеводу в желудок. Дисфагия может быть органической и функциональной. Органическая дисфагия возникает при раке (см. главу 26), постожоговых и пептических стриктурах пищевода, обтурации просвета пищевода инородным телом, остром эзофагите, дивертикулах, доброкачественных новообразованиях пищевода, наружном сдавлении органа (опухолями лёгких и средостения, заглоточным или медиастинальным абсцессом, увеличенной щитовидной железой, аневризмой грудной аорты).
Функциональная дисфагия развивается при ахалазии кардии, кардиоспазме, диффузном спазме пищевода, может наблюдаться при нарушении глотательного рефлекса вследствие поражения глотательного центра, миастении, сахарном диабете, а также быть следствием острого нарушения мозгового кровообращения или полиомиелита.
Одинофагия — болезненное проглатывание или появление боли при прохождении пищи по пищеводу, часто наблюдается совместно с дисфагией. Одинофагия — признак воспаления слизистой оболочки пищевода.
Изжога — специфическое ощущение жжения за грудиной, которое распространяется снизу вверх из надчревья до шеи. Изжога усиливается в положении лёжа, после еды, при наклонах туловища, напряжении мышц брюшного пресса. Изжога — характерный симптом гастроэзофагеальной рефлюксной болезни.
Регургитация — появление содержимого пищевода или желудка во рту. Наблюдается при ахалазии кардии и кардиоспазме, больших дивертикулах, органических стенозах пищевода, гастроэзофагеальной рефлюксной болезни. Регургитация может привести к аспирации содержимого в верхние дыхательные пути.
Боли в грудной клетке некоронарного происхождения в большинстве случаев связаны с патологией пищевода. Они наиболее часто встречаются при нервно-мышечных заболеваниях, гастроэзофагеаль-ной рефлюксной болезни, раке пищевода.
Нервно-мышечные заболевания пищевода
К этой группе заболеваний относят кардиоспазм, ахалазию пищевода (кардии), диффузный эзофагоспазм (синдром Барсони—Тешен-дорфа) и некоторые другие моторные расстройства, связанные с нарушением иннервации пищевода.
Ахалазия пищевода и кардиоспазм
Ахалазия пищевода (кардии) заключается в отсутствии расслабления нижнего пищеводного сфинктера во время акта глотания. Выключение физиологического рефлекса его раскрытия приводит к нарушению тонуса и моторики пищевода, что вызывает задержку пищи.
Кардиоспазм — стойкое спастическое сужение терминального отдела пищевода, проявляющееся дисфагией и в далеко зашедших стадиях сопровождающееся органическими изменениями его вышележащих отделов.
Этиология и патогенез
Этиология и патогенез нервно-мышечных заболеваний пищевода окончательно не выяснены. Существуют теории врождённого спазма, патологических изменений в окружающих органах, инфекционная, рефлекторная, психогенная теории и др. В последнее время большое значение в их развитии придают нарушениям синтеза оксида азота, что приводит к нарушениям обмена ионов кальция и передачи нервно-мышечного импульса. В настоящее время кардиоспазм и ахалазию кардии рассматривают как два различных патологических состояния.
• При кардиоспазме наблюдается повышенное давление в области нижнего пищеводного сфинктера, градиент пищеводно-желудочно-го давления может достигать 20 мм рт.ст. и более. Для начальных стадий кардиоспазма характерна усиленная непропульсивная моторика пищевода. Морфологически находят дегенеративно-дистрофические изменения в преганглионарных нейронах дорсальных ядер блуждающих нервов и в меньшей степени — постганглионарных нейронах ауэрбахова сплетения пищевода. Считают, что в связи с нарушением центральной иннервации при кардиоспазме гладкая мускулатура нижнего пищеводного сфинктера становится более, чем обычно, чувствительной к своему физиологическому регулятору — эндогенному гастрину. Таким образом, при данном варианте течения заболевания возникает истинный спазм кардии. Длительные спастические сокращения ведут к нарушению кровоснабжения и рубцовому перерождению гладкой мускулатуры, формированию органического стеноза кардиоэзофагеальной зоны. • При ахалазии кардии, напротив, поражаются преимущественно постганглионарные нейроны, в результате выпадает рефлекс раскрытия кардии на глоток. Манометрически находят нормальный или даже сниженный градиент пищеводно-желудочного давления, наблюдают значительное ослабление моторики пищевода. При ахалазии нет условий для возникновения повышенной чувствительности гладкой мускулатуры нижнего пищеводного сфинктера к гастрину — сохраняется центральная иннервация. Необходимо отметить, что нарушение рефлекса раскрытия кардии и нарушение моторики пищевода — два параллельных процесса, идущих одновременно.
Классификация
Согласно наиболее распространённой классификации (рис. 25-1.), различают четыре стадии ахалазии и кардиоспазма.
• I стадия — пищевод не расширен, рефлекс раскрытия кардии сохранён, но моторика пищевода усилена и дискоординирована.
II стадия — рефлекс раскрытия кардии отсутствует, отмечается расширение пищевода до 4—5 см.
III стадия — значительное расширение пищевода до 6—8 см, задержка в нём жидкости и пищи, отсутствие пропульсивной моторики.
IV стадия — резкое расширение, удлинение и искривление пищевода с атонией стенок, длительной задержкой жидкости и пищи.
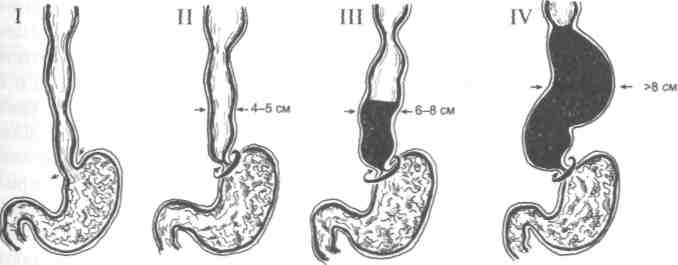
Рис. 25-1. Стадии ахалазии кардии (пищевода) и кардиоспазма.
Клиническая картина и диагностика
Ахалазия кардии и кардиоспазм проявляются дисфагией, регур-гитацией, болями в груди.
Дисфагия часто носит интермиттирующий характер, может усиливаться при волнении, нередко имеет парадоксальный характер: хорошо проходит твёрдая пища, жидкость задерживается. Больные отмечают, что для того чтобы пища проходила, им приходится запивать её водой или прибегать к другим приёмам, например, повторным глотательным движениям.
Регургитация возникает вначале сразу после еды, а при прогресси-ровании заболевания через более или менее значительное время после приёма пищи. Она может наблюдаться во время сна (симптом «мокрой подушки»), что грозит опасностью аспирации и развитием лёгочных осложнений.
Боль обычно носит распирающий характер, появляется во время или после еды по ходу пищевода, иррадиирует в спину, между лопатками. Иногда сильный спазм пищевода во время приёма пищи может быть расценён как приступ стенокардии.
Рентгенологическое исследование (рис. 25-2) позволяет в большинстве случаев правильно поставить диагноз. Характерный рентгенологический признак — расширение пищевода в той или иной степени с наличием узкого сегмента в терминальном его отделе (симптом «перевёрнутого пламени свечи»). Стенки пищевода, в том числе и в суженной части, сохраняют эластичность. Газовый пузырь желудка обычно отсутствует. При эзофагоскопии в начальных стадиях заболевания каких-либо характерных изменений в пищеводе не находят. В далеко зашедших стадиях болезни виден большой зияющий просвет пищевода, иногда с жидкостью, слизью, остатками пищи. Слизистая оболочка пищевода обычно воспалена, утолщена, могут выявляться эрозии, язвы, участки лейкоплакии, изменения нарастают в дистальном направлении. Эндоскоп практически всегда проходит в желудок. Если этого не происходит, следует думать об органическом стенозе (пептическая стриктура, рак).
Дифференциально-диагностические критерии ахалазии пищевода (кардии) и кардиоспазма представлены рис 25-1
Таблица 25-1. Критерии диагностики кардиоспазма и ахалазии пищевода
Кардиоспазм |
Ахалазия пищевода (кардии) |
1 |
2 |
Клиническая симптоматика
Обычно дисфагия проявляется неожиданно |
В большинстве случаев дисфагия развивается постепенно |
Характерна парадоксальная дисфагия |
Парадоксальная дисфагия не наблюдается |
Характерна интенсивная спастическая боль за грудиной |
Распирающая боль за грудиной возникает редко |
Регургитация во время или сразу после еды |
Регургитация возникает в горизонтальном положении или при наклоне туловища вперёд, через несколько часов после еды |
Рентгенологическая симптоматика
Пищеводная моторика усилена, выражены сегментарные сокращения пищевода |
Моторная активность пищевода снижена, сегментарные сокращения отсутствуют |
Терминальная часть пищевода имеет конусовидную форму |
Терминальная часть пищевода закруглена, сужение часто расположено эксцентрично |
Пищевод опорожняется путём продавливания контраста через узкий сегмент — симптом «шприца» |
Начало опорожнения определяется высотой столба бариевой взвеси и наблюдается при повышении гидростатического давления по типу «провала» |
Расслабление нижнего пищеводного сфинктера в ответ на введение холинолитиков |
Отрицательный фармакологический тест на холинолитики |
Большое значение в диагностике нервно-мышечных заболеваний пищевода придают эзофагоманометрии, позволяющей провести окончательную дифференциальную диагностику между ахалазией кардии и кардиоспазмом (в I и IV стадиях клиническая и рентгенологическая картина не позволяют чётко дифференцировать эти патологические процессы). При кардиоспазме градиент пищеводно-желудочного давления составляет более 20 мм рт.ст. При ахалазии кардии он меньше 20 мм рт.ст., отсутствует рефлекс раскрытия нижнего пищеводного сфинктера на глотание.
Лечение
В начальных стадиях ахалазии пищевода (кардии) и кардиоспазма возможно применение консервативного лечения. В настоящее время наибольшее распространение получили препараты из группы нитратов (нитроглицерин, изосорбида динитрат) и антагонистов кальция (верапамил, нифедипин), в ряде случаев используют седативные препараты. Необходимо обращать внимание на соблюдение больными чёткого режима питания с 4- или 5-разовым приёмом пищи, а при необходимости и более частым. Есть необходимо медленно, тщательно пережёвывая пищу.
В последние годы появилось новое перспективное направление в лечении больных ахалазией (пищевода) кардии и кардиоспазмом — применение препаратов ботулотоксина, которые вводят через фиб-роэзофагогастроскоп в зону нижнего пищеводного сфинктера, что способствует его расслаблению.
Основной метод лечения ахалазии кардии (пищевода) и кардиоспазма в настоящее время — кардиодилатация, которая при повторных проведениях приводит к разрыву рубцовой ткани, уменьшая тем самым градиент пищеводно-желудочного давления и обеспечивая восстановление пассивного (за счёт силы тяжести) пассажа пищи. Пневматический кардиодилататор состоит из резинового или пластмассового зонда с баллоном, укреплённым на конце, диаметром 25, 35 и 45 мм. Кардиодилатацию проводят под рентгеновским контролем, начиная с дилататора диаметром 25 мм и давления в нём от 180 до 240 мм рт.ст. Сеансы подобного лечения обычно проводят через день, постепенно увеличивая диаметр баллона и повышая давление до 320 мм рт.ст. В среднем курс лечения состоит из 5—6 процедур, в некоторых случаях число кардиодилатаций приходится увеличивать до 10—12. Об эффективности кардиодилатации судят по клиническим проявлениям (исчезновение дисфагии) и снижению градиента пищеводно-желудочно-го давления (градиент давления не следует уменьшать ниже 7—8 мм рт.ст., так как это может привести к развитию рефлюкс-эзофагита).
Показания к оперативному лечению ахалазии кардии и кардиоспазма — невозможность проведения кардиодилататора через кардию, неуверенность в правильном диагнозе при обоснованном подозрении на рак кардиоэзофагеальнои зоны, неадекватное восстановление проходимости кардии после законченного курса пневматической кардиодилатации, неэффективность трёх курсов кардиодилатации, сочетание с другими заболеваниями, требующими оперативного лечения.
В настоящее время оптимальной операцией считают экстрамукозную (внеслизис-тую) эзофагокардиомиотомию по Хеллеру (рис. 25-3) с неполной фундопликацией. Операция может быть выполнена как открытым, так и видеоэндоскопическим способом. Производят рассечение продольных и циркулярных мышечных волокон передне-левой стенки пищевода на протяжении 6— 7 см, разрез на 1,5-2 см переходит на кар-диальный отдел желудка, что ведёт к расши- рИс. 25-3. Схема операции рению области пищеводно-желудочного эзофагокардиомиотомии.
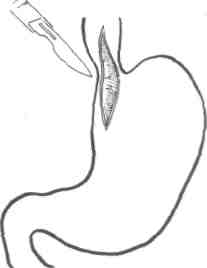
Рис 25-3 Схема операции эзофагокардиомиотомии
перехода. Важное условие — пересечение как продольных, так и циркулярных мышечных волокон пищевода, что служит профилактикой рецидива заболевания. Операцию дополняют передней фундопликаци-ей, которая не требует пересечения связочного аппарата и коротких сосудов желудка, её производят путём подшивания стенки дна желудка к краям разреза мышечной оболочки тремя-четырьмя отдельными узловыми швами с предварительно введённым в просвет пищевода зондом. При IV стадии заболевания, особенно у больных, уже перенёсших неудачные операции, осложнившиеся развитием рефлюкс-эзофаги-та и пептической стриктуры, операцией выбора является субтотальная резекция пищевода с одномоментной эзофагопластикой.
Диффузный спазм пищевода
Диффузный спазм пищевода, или синдром Барсони—Тешендор-фа, — заболевание пищевода, обусловленное спастическими сокращениями его стенки при сохранении нормальной сократительной способности нижнего пищеводного сфинктера. Выделяют первичный и вторичный эзофагоспазм. Под вторичным понимают эзофагоспазм, развившийся на фоне других заболеваний пищевода. Ведущими клиническими симптомами диффузного спазма пищевода являются дис-фагия и боль в грудной клетке. Реже встречаются регургитация, похудание, общая слабость.
Диагностика
Рентгенологически при диффузном эзофагоспазме выявляют «чёт-кообразный», а в других случаях «штопорообразный» пищевод, задержки в пищеводе контрастного вещества и сужения дистального отдела пищевода не бывает (рис. 25-4). Эндоскопическое исследование не выявляет характерных признаков заболевания. При эзофаго-манометрии по всему длиннику пищевода наблюдают сегментарные непропульсивные сократительные волны, возникающие одновременно на разных уровнях независимо от глотка, цифры градиента пище-водно-желудочного давления нормальные.
Лечение
Лечение первичного эзофагоспазма консервативное, кардиодила-тация не даёт выраженного эффекта. Комплексная консервативная терапия включает в себя назначение антагонистов кальция (верапамил, нифедипин), нитратов, седативных препаратов, витаминов, спазмолитических препаратов (дротаверин, платифиллин, папаверин), физиопроцедур (электрофорез с прокаином, сульфатом магния, хлоридом калия).
При неэффективности консервативного лечения выполняют операцию — экстрамукозную эзофагомиотомию (рассечение адвентици-ального и мышечного слоев пищевода) на протяжении от дуги аорты до нижнего пищеводного сфинктера. К оперативному лечению диффузного спазма пищевода прибегают достаточно редко. Операция может быть выполнена эндоскопическим путём из правостороннего торакального доступа.
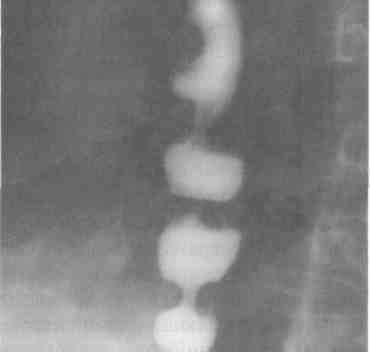
Рис. 25-4. Рентгенограмма при диффузном эзофагоспазме.
Грыжи пищеводного отверстия диафрагмы и рефлюкс-эзофагит
Грыжами пищеводного отверстия диафрагмы называют смещение какого-либо органа брюшной полости, покрытого брюшиной, через это отверстие в заднее средостение. Выделяют скользящие (аксиальные) и параэзофагеальные грыжи. Содержимым скользящей грыжи пищеводного отверстия диафрагмы могут быть не только кардиаль-ный отдел желудка и его дно, но и большая часть этого органа. В состав параэзофагеальных грыж могут входить как часть желудка (обычно его дно), так и участки кишечника, большой сальник.
Этиология
Причины образования приобретённых грыж пищеводного отверстия диафрагмы — инволюционные и дистрофические процессы в связочном аппарате пищеводного отверстия диафрагмы, в результате чего оно расширяется и образуются своего рода грыжевые ворота. Эти изменения наиболее часто встречают у стариков, беременных, больных, страдающих ожирением. Непосредственной причиной, вызывающей возникновение грыж пищеводного отверстия диафрагмы, служит повышение внутрибрюшного давления. Подобные грыжи в ряде случаев сочетаются с другими заболеваниями пищеварительной системы. Сочетание с хроническим холециститом и язвенной болезнью двенадцатиперстной кишки носит название триады Касте-на, а сочетание с хроническим холециститом и дивертикулёзом толстой кишки — триады Сайнта.
Рефлюкс-эзофагит — наиболее частое осложнение скользящей грыжи пищеводного отверстия диафрагмы. Причинами возникновения рефлюкс-эзофагита могут быть также язвенный стеноз привратника, состояние после резекции желудка и гастроэнтеростомии, предшествующие операции в области пищеводно-желудочного перехода, тяжёлая рвота, длительное трансназальное дренирование желудка. В основе развития этого осложнения лежит недостаточность кардии, нарушение функций нижнего пищеводного сфинктера. При тяжёлом рефлюкс-эзофагите может развиться пептическая стриктура пищевода.
В развитии пептических стриктур большое значение придают также синдрому Баррета — эктопии слизистой оболочки желудка в пищевод. При рефлюкс-эзофагите в зоне воспаления может полностью разрушаться плоскоклеточный эпителий, регенерация слизистой оболочки происходит за счёт кардиальных желёз, что приводит к замещению плоскоклеточного эпителия цилиндрическим. В некоторых случаях встречается врождённая эктопия желудочного эпителия. Одно из возможных осложнений грыж пищеводного отверстия диафрагмы — ущемление.
Клиническая картина
Клиническая картина грыж пищеводного отверстия диафрагмы очень разнообразна. Симптомами грыж пищеводного отверстия диафрагмы могут быть изжога, боль, отрыжка, регургитация, дисфагия, икота. Изжога возникает обычно после еды, при перемене положения тела, чаще в ночное время. Боли за грудиной появляются и усиливаются при горизонтальном положении или наклоне туловища вперёд, часто сопровождаются регургитацией желудочного содержимого («симптом шнурка»). При грыжах пищеводного отверстия диафрагмы нередко возникает рефлекторная стенокардия. Боли могут локализоваться также в подложечной и межлопаточной областях. Иногда при грыжах пищеводного отверстия диафрагмы возникает кровотечение, обычно незначительное. Развитие пептической стриктуры пищевода проявляется стойкой дисфагией. При грыжах небольших размеров клинические проявления могут отсутствовать.
Диагностика
Основной метод выявления грыж пищеводного отверстия диафрагмы — рентгенологическое исследование (рис. 25-5). Рентгенологические симптомы определяются типом грыжи. При аксиальной грыже в грудную полость смещена вся область желудочно-пище-водного перехода и часть желудка пролабирует в заднее средостение. Кардия находится над диафрагмой. При параэзофагеальной грыже пищеводно-желудочный переход располагается в брюшной полости, а часть желудка выходит через пищеводное отверстие диафрагмы в грудную полость рядом с пищеводом. Большие грыжи распознают сравнительно легко, для выявления небольших грыж необходимо исследование как в вертикальном, так и в горизонтальном положении больного, а также в положении Тренделенбурга. Рентгенологическое исследование играет важную роль в распознавании осложнений хиатальной грыжи и, прежде всего, рефлюкс-эзофагита.

Рис. 25-5. Рентгенограмма больного с грыжей пищеводного отверстия диафрагмы. Часть желудка находится выше диафрагмы (указана стрелкой).
Эндоскопическое исследование также весьма важно, так как позволяет выявить недостаточность кардии, оценить тяжесть эзофагита, обнаружить осложнения и сопутствующие заболевания. По эндоскопической классификации различают четыре степени рефлюкс-эзофагита: 1) лёгкий; 2) средней тяжести; 3) тяжёлый; 4) пептическая стриктура пищевода.
Ценный функциональный метод диагностики скользящих грыж пищеводного отверстия диафрагмы — эзофагоманометрия, позволяющая определить зону повышенного давления в области пищевод-но-желудочного перехода, смещённого выше уровня диафрагмы.
Важным методом диагностики представляется рН-метрия, особенно 24-часовая, которая даёт возможность получить достоверную информацию о частоте и длительности эпизодов эзофагеального заброса, их зависимости от положения тела, приёма пищи, времени суток и т.п.
Лечение
Лечение скользящих грыж пищеводного отверстия диафрагмы начинают с консервативных мероприятий. Необходимо соблюдать режим приёма пищи, избегать переедания, не рекомендуются тяжёлые физические нагрузки, ношение тугой одежды. Из лекарственных препаратов используют блокаторы Н -гистаминовых рецепторов (ранитидин, фамотидин и др.), ингибиторы протонного насоса (омеп-разол, лансопразол и др.), прокинетики (например, домперидон), антацидные средства (алгелдрат + магния гидроксид, алюминия фосфат и др.).
При сформировавшейся пептической стриктуре на фоне проводимых консервативных мероприятий проводят бужирование пищевода, чаще всего в качестве предоперационной подготовки. Оперативное вмешательство необходимо проводить при осложнённых формах и безуспешности предшествующих медикаментозных мероприятий. Наиболее целесообразная операция — фундопликация по Ниссену (рис. 25-6). При этой операции производят выделение правой и левой стенок пищевода, клетчатку позади него тупо разделяют, ножки диафрагмы сводят отдельными узловыми швами, накладываемыми позади пищевода с предварительно введённым в его просвет толстым зондом. Затем выполняют мобилизацию дна и верхней части большой кривизны желудка, короткие желудочные артерии пересекают. Стенку желудка захватывают введённым позади пищевода зажимом и протягивают слева направо вперёд, образуя циркулярную манжетку. Задний лоскут подшивают двумя—тремя узловыми швами к дну желудка, выведенному спереди от пищевода, с обязательным захватыванием в шов стенки пищевода для предотвращения соскальзывания созданной манжетки. Подобную операцию в настоящее время выполняют путём лапароскопии.

Рис. 25-6. Схема операции фундопликации по Ниссену, применяющейся при скользящих грыжах пищеводного отверстия диафрагмы и рефлюкс-эзофа-гите: а — низведение пищевода и наложение швов на переднюю и заднюю стенки дна желудка с захватыванием его стенки; б — после завязывания швов сформирована манжета вокруг абдоминального отдела пищевода.
При протяжённых стриктурах выполняют резекцию пищевода. Параэзофагеальные грыжи подлежат оперативному вмешательству в связи с опасностью тяжёлых осложнений. Производят низведение грыжевого содержимого в брюшную полость, иссечение грыжевого мешка, крурорафию. Операцию завершают фундопликапией.
Дивертикулы пищевода
Дивертикулы пищевода представляют собой мешковидные выпячивания стенки данного органа в полость средостения. По результатам массового рентгенологического обследования населения они встречается у 2% взрослых людей.
Классификация
Происхождение дивертикулов: врождённые, приобретённые. Механизм развития: пульсионные, тракционные. Локализация: глоточно-пищеводные (ценкеровские), бифуркационные, наддиафрагмальные. Строение: истинные, ложные.
Патогенез
В подавляющем большинстве случаев эзофагеальные дивертикулы носят приобретённый характер, врождёнными они бывают чрезвычайно редко.
Пульсионные дивертикулы возникают за счёт выбухания стенки пищевода, обусловленного повышением внутрипищеводного давления по тем или иным причинам (гипермоторная дискинезия органа).
Тракционный механизм возникновения заболевания предполагает наличие сращений, в основном воспалительного характера, между пищеводом и окружающими органами (в первую очередь лимфатическими узлами корня лёгкого или бифуркации трахеи). Перистальтика пищевода в условиях фиксации его к лимфатическим узлам вызывает локальное выпячивание стенки пищевода.
Глоточно-пищеводные и наддиафрагмальные дивертикулы по механизму своего возникновения являются пульсионными, их развитие связано с повышением давления в области верхнего и нижнего пищеводных сфинктеров, бифуркационные дивертикулы обычно тракпионные. Вместе с тем, в возникновении любого дивертикула играют роль оба указанных механизма развития, лишь на начальных этапах их формирования тракционный или пульсионный механизм встречают в чистом виде.
Истинными называют такие дивертикулы, стенка которых состоит из всех слоев пищевода, ложные дивертикулы не содержат мышечного слоя.
Клиническая картина и диагностика
Ценкеровские (глоточно-пищеводные) дивертикулы в течение длительного времени могут ничем себя не проявлять. По мере увеличения их размеров попадание в него пищи ведёт к сдавлению пищевода и появлению характерных симптомов — дисфагии (вплоть до полной непроходимости пищи), срыгиванию, неприятному запаху изо рта. При больших дивертикулах в области левой половины шеи может появляться эластическое выпячивание, при надавливании на которое определяется характерное урчание. В редких случаях наблюдают такие симптомы, как одышка, сердцебиение, набухание шейных вен, осиплость голоса, синдром Хорнера. Срыгивание и заброс содержимого глоточно-пищеводного дивертикула в трахеобронхиаль-ное дерево могут приводить к развитию аспирационных пневмоний, зачастую абсцедирующих.
Бифуркационные и эпифренальные дивертикулы небольших размеров протекают обычно бессимптомно, их выявляют случайно при выполнении эзофагоскопии или рентгенологического исследования. При увеличении размеров дивертикулов и затруднении их опорожнения появляются боль за грудиной и в спине, гиперсаливация, отрыжка. Дисфагия развивается редко и связана со спазмом пищевода.
К осложнениям дивертикулов пищевода относят дивертикулит, который может привести к изъязвлению и перфорации дивертикула с развитием медиастинита или пишеводно-респираторных свищей. Дивертикулит может приводить и к кровотечению. В редких случаях перфорация дивертикула может произойти в верхнюю полую вену, лёгочную артерию, аорту, вызвав смертельное кровотечение. Описаны случаи малигнизации дивертикулов.
Ведущая роль в диагностике дивертикулов пищевода принадлежит полипозиционному рентгеноконтрастному исследованию (рис. 25-7), позволяющему выявить локализацию, форму, размеры дивертикула, сопутствующие заболевания. При задержке бариевой взвести дивертикула более 2 мин можно предположить развитие дивер-тикулита. Эзофагоскопическое исследование способствует уточнению диагноза, позволяет выявить различные осложнения

.
Лечение
Консервативное лечение показано при небольших неосложнён-ных дивертикулах, а также при наличии противопоказаний к операции. Оно направлено на уменьшение либо ликвидацию явлений ди-вертикулита. Больному рекомендуют неторопливый приём пищи, диета должна быть механически, термически и химически щадящей, но полноценной по аминокислотному и витаминному составу. Целесообразно периодическое промывание полости дивертикула растворами антисептиков (перманганат калия, нитрофурал и др.).
Оперативное вмешательство выполняют у больных с выраженной клинической симптоматикой. Оперативному лечению обычно подвергают больных с большими дивертикулами пищевода, в которых длительно задерживается бариевая взвесь и возникают явления ди-вертикулита. Дивертикул размером до 3 см инвагинируют: после
выделения его погружают в просвет пищевода кисетным или одиночными узловыми швами, наложенными в продольном направлении. При наличии осложнений и при размерах дивертикула более 3 см необходима дивертикулэктомия. Для этого его выделяют из окружающих тканей до шейки, отсекают и удаляют. Образовавшийся дефект ушивают непрерывным или узловыми швами. Дивертикулэктомию (особенно при видеоэндохирургических операциях) осуществляют с помощью линейных сшивающих аппаратов.
Повреждения пищевода
Изолированные открытые и закрытые повреждения пищевода встречаются достаточно редко из-за глубокого залегания органа и тесных взаимоотношений с другими структурами. Чаще такие повреждения бывают сочетанными и сопровождаются опасными для жизни кровотечениями и нарушениями проходимости дыхательных путей. Это может привести к несвоевременной диагностике повреждений пищевода и развитию медиастинита.
Классификация
• Уровень повреждения: шейный, грудной, абдоминальный отделы пищевода.
Локализация: передняя, задняя, левая или правая стенка, противоположные стенки, циркулярные.
Причина повреждения: внешняя травма (ранения колотые, резаные, рваные, огнестрельные), инородные тела, хирургические операции или инструментальные манипуляции (ятрогенные повреждения), спонтанные разрывы.
• Сопутствующие повреждения: медиастинальной плевры, трахеоб- ронхиального дерева, крупных сосудов; ложный ход в средостении.
Клиническая диагностика
Помимо ранений пищевода, в последние годы значительно чаще наблюдают повреждения пищевода, связанные с проведением различных диагностических и лечебных манипуляций (эзофагогастроско-пия, бужирование пищевода, кардиодилатация, интубация трахеи во время проведения наркоза). При рвоте из-за значительного повышения внутрибрюшного давления может произойти спонтанный (гидравлический) разрыв нижнегрудного отдела пищевода.
Клинически повреждения пищевода проявляются болью, дисфа-гией, кровотечением из пищевода, образованием подкожной эмфиземы. При развитии медиастинита ухудшается общее состояние больного, возникают боли за грудиной, в грудной клетке и надчревье, появляются признаки системной воспалительной реакции.
Для диагностики повреждений пищевода и их осложнений применяют обзорное рентгенологическое исследование шеи, грудной клетки и брюшной полости, рентгеноконтрастное исследование пищевода, при необходимости — фиброэзофагоскопию. Для уточнения диагноза могут быть использованы УЗИ плевральных полостей и сердца, КТ средостения, торакоскопия и лапароскопия.
Лечение
Консервативное лечение проникающих повреждений пищевода проводят лишь при малых дефектах стенки пищевода (до 0,5 см), небольших затёках контрастного вещества (до 2 см) за контуры пищевода в условиях их хорошего опорожнения, а также при отсутствии гнойного процесса в средостении, плевральных полостях, околопищеводной клетчатке на шее. Лечение заключается в исключении питания через рот (проводят зондовое или парентеральное питание), назначении массивной антибактериальной терапии. Ежедневно проводят лабораторный и рентгенологический контроль.
Для хирургического лечения повреждений пищевода используют несколько доступов. Чресшейный доступ применяют во время операций на шейном и верхнегрудном отделах пищевода, а также на верхней части средостения (чресшейная медиастинотомия). Разрез производят по переднему краю грудино-ключично-сосцевидной мышцы, начиная от яремной ямки, чаще слева. К нижнегрудному и абдоминальному отделам пищевода, а также к заднему средостению наиболее удобен чрезбрюшинный доступ, дополненный сагиттальной ди-афрагмотомией. Операции на среднегрудном отделе пищевода производят через торакотомный разрез. При необходимости применяют сочетание нескольких доступов.
Оперативное лечение при повреждениях шейного отдела пищевода заключается в ушивании раны с укреплением линии швов мышцей на ножке и дренированием области вмешательства. Операции на шейном отделе менее опасны, ушивание повреждения можно производить даже в поздние сроки, так как образование свища в этой области не является обычно серьёзной проблемой. При свежих повреждениях грудного отдела выполняют ушивание раны с укреплением линии швов лоскутом плевры или перикарда, а также диафрагмаль-ным лоскутом на ножке. В случаях повреждений абдоминального отдела пищевода оперативное вмешательство производят через ла-паротомный доступ, линию швов укрепляют стенкой желудка, выполнив фундопликацию. Для питания пациента необходимо проведение в желудок зонда (при травме на уровне шейного отдела) либо наложение гастростомы в сочетании с фундопликацией (при повреждениях грудного отдела пищевода).
При свежих обширных повреждениях у сравнительно крепких пациентов может быть выполнена экстирпация пищевода. Пластику трансплантатом из желудка или толстой кишки производят обычно вторым этапом, спустя несколько месяцев.
При общем тяжёлом состоянии пациента, поступлении в поздние сроки после повреждения выполняют минимальные оперативные вмешательства, направленные на спасение жизни. Широко дренируют клетчаточные пространства шеи, средостение, плевральные полости, накладывают гастростому в сочетании с фундопликацией с целью исключения питания через рот и профилактики заброса в пищевод содержимого желудка.
Успех лечения больных с повреждениями пищевода во многом зависит от эффективности дренирования зоны повреждения. В последнее время с успехом применяют метод закрытого аспирационно-промывного лечения повреждений пищевода, в том числе осложнённых медиастинитом.
Инородные тела пищевода
Причиной попадания инородных тел могут быть привычка держать различные предметы во рту, поспешная еда, алкогольное опьянение, преднамеренное проглатывание предметов психически больными. Более чем в 50% случаев инородные тела свободно проходят по пищеводу и другим отделам ЖКТ и выходят естественным путём. Обычно они задерживаются в местах физиологических сужений, наиболее часто (около 70%) в области глоточно-пищеводного перехода. При Рубцовых и опухолевых стриктурах, дивертикулах пищевода инородные тела могут локализоваться в месте патологического процесса.
Клиническая симптоматика
Клиническая симптоматика может быть обусловлена как самим инородным телом, так и вызванными им осложнениями. Обычно пациенты предъявляют жалобы на боль в горле, дисфагию, неприятные ощущения при глотании, повышенное слюноотделение (гиперсаливацию). При длительном нахождении инородных тел вышеописанные симптомы становятся более выраженными из-за нарастания реактивного отёка вокруг инородного тела. Вместе с тем, описаны случаи длительного бессимптомного нахождения инородных тел в пищеводе. Чаще удалённое не сразу инородное тело вызывает тяжёлые осложнения: некроз и перфорацию стенки пищевода с развитием флегмоны шеи, медиастинита, плеврита, остеомиелита позвонков, сепсиса, аррозионных кровотечений из крупных сосудов.
Для диагностики инородных тел применяют эндоскопическое и рентгенологическое исследования (обзорные снимки и исследование с водорастворимым контрастом). При перфорации пищевода отмечают затекание контрастного вещества за его контуры, наличие ме-диастинальной эмфиземы, при образовании свищей — попадание контраста в трахеобронхиальное дерево.
Лечение
В настоящее время методом выбора удаления инородных тел пищевода служит эндоскопия. Инородное тело захватывают специальными щипцами и удаляют из пищевода вместе с фиброэзофагоско-пом. При необходимости инородное тело (булавку, кость и т.д.) поворачивают в пищеводе для того, чтобы захватить его за тупой конец. Если развернуть инородное тело в пищеводе не представляется возможным, то его сначала низводят в желудок тупым концом вниз, а затем разворачивают на 180°. В ряде случаев приходится прибегать к фрагментации и поэтапному удалению инородного тела.
После удаления инородного тела проводят контрольную эзофагоскопию для исключения повреждения стенки пищевода, кровотечения, других инородных тел, а при сомнении — рентгенологическое исследование с водорастворимым контрастом. Из-за опасности развития осложнений все больные с инородными телами пищевода должны быть госпитализированы.
Если извлечь инородное тело с помощью эндоскопа невозможно, проводят оперативное вмешательство. При отсутствии осложнений
выполняют рассечение стенки пищевода, извлекают инородное тело и ушивают рану с укреплением линии швов. В случаях гнойных осложнений широко дренируют клетчаточные пространства шеи, плевральные полости, средостение, выполняют гастростомию в сочетании с фундопликацией.
Свищи пищевода
Приобретённые свищи как осложнение различных повреждений и заболеваний пищевода могут располагаться в любом его отделе. Они могут возникать вследствие опухолей, травм, специфического и неспецифического воспаления. Различают наружные и внутренние свищи. Внутренние свищи могут сообщаться с органами дыхания, средостением, плевральной и брюшной полостями.
Клинические проявления
Клинические проявления зависят от этиологии, локализации, размеров свища. Часто на первый план выходят симптомы основного заболевания (рак или тяжёлая рубцовая стриктура). Пищеводно-рес-пираторные свищи проявляются мучительным кашлем во время еды. Аспирация пищи может приводить к развитию пневмонии и абсцесса лёгкого. Пищеводно-плевральные свищи приводят к эмпиеме плевры. При пищеводно-медиастинальных свищах (без нарушения целостности плевры) клиника менее отчётлива, свищи могут выявляться только при рентгеноконтрастном исследовании.
Диагностика
Диагноз наружных пищеводных свищей подтверждают пробой с красящим веществом (метилтионина хлорид). Окрашенная жидкость, принятая через рот, выделяется через некоторое время из наружного отверстия свища или по дренажу. Проводят также полипозиционное рентгенологическое исследование с водорастворимым контрастом, а при необходимости и фистулографию. Диагностику пищеводно-респираторных свищей производят при рентгеноконтрастном и эндоскопическом исследованиях (выполняют трахеобронхо-скопию с одновременным введением в пищевод по зонду метилтионина хлорида).
Лечение
Наружные пищеводные свищи обычно лечат консервативно, проводя антибактериальную, общеукрепляющую и дезинтоксикационную терапию. Питание осуществляют через зонд или гастростому (при её наличии). Такое лечение приводит к заживлению свища в течение 7-14 дней.
Для лечения пищеводно-респираторных свищей накладывают гастростому с целью полноценного энтерального питания больного. Её целесообразно сочетать с фундопликацией для предотвращения заброса содержимого желудка в пищевод. Если свищ после гастросто-мии и интенсивной терапии не закрывается, то необходимо выполнение радикальной операции. Доступ осуществляют в зависимости от локализации свища. Операция заключается в выделении и пересечении свища, ушивании дефекта трахеи или бронха и отверстия в стенке пищевода с обязательным укрытием линии швов лоскутом из мышцы, плевры, диафрагмы, большого сальника, плевро-надкост-ничным лоскутом и т.д. При тяжёлых органических изменениях в лёгких, возникших из-за длительного существования пищеводно-респираторных свищей, может потребоваться сочетанная операция — атипичная резекция лёгкого, лобэктомия или даже пневмонэктомия. При пищеводно-респираторных свищах, возникших вследствие Рубцовых стриктур пищевода, целесообразно выполнять полное удаление (экстирпацию) пищевода. При свищах пищевода опухолевого происхождения выполнение радикальной операции возможно лишь в единичных случаях из-за распространённости опухолевого процесса.
Ожоги и рубцовые сужения пищевода
Чаще всего приходится сталкиваться с химическими ожогами пищевода, гораздо реже наблюдают термические его повреждения. Химические ожоги возникают при случайном или преднамеренном (суицидальная попытка) приёме различных химических веществ, чаще всего концентрированных кислот или щелочей. Ожоги пищевода могут вызывать и некоторые другие соединения (соли тяжёлых металлов, перманганат калия, фенол, ацетон и т.д.).
Тяжесть химического ожога, а также его общее токсическое воздействие на организм зависят от концентрации принятого вещества, его количества, химической природы, времени воздействия на слизистые оболочки пищеварительного тракта, сроков оказания первой помощи, реактивности организма.
Щёлочи вызывают глубокий и обширный колликвационный некроз (мягкое омертвение) тканей пищеварительного тракта, сопровождающийся растворением белков и омылением жиров, что приводит к диффузии принятого вещества в глубже лежащие ткани.
Кислоты обладают прижигающим и денатурирующим действием и ведут к возникновению менее глубокого коагуляционного некроза. В связи с длительной задержкой химических веществ наиболее выраженные изменения обычно отмечаются в местах физиологических сужений пищевода.
В зависимости от глубины поражения тканей различают три степени химического ожога пищевода:
I степень (лёгкая) — повреждение поверхностных слоев эпителия слизистой оболочки;
II степень (средней тяжести) — поражение слизистой оболочки на всю глубину с распространением процесса на подслизистый слой;
III степень (тяжёлая) — распространение повреждения на все слои пищевода, нередко с вовлечением околопищеводной клетчатки и соседних структур (плевра, перикард, трахея).
В клиническом течении ожогов пищевода различают четыре периода:
острый период, который длится до 2 нед и характеризуется выраженными воспалительными и дегенеративно-дистрофическими изменениями в стенке пищевода;
период мнимого благополучия продолжительностью 2-3 нед, в течение которого происходят отторжение некротических масс и образование грануляционной ткани, что приводит к уменьшению или полному исчезновению дисфагии;
период формирования рубцовой стриктуры (начиная с 4-5-й недели), когда происходит замещение грануляций плотной фиброзной соединительной тканью, вновь возникает дисфагия (при химических ожогах I степени заживление происходит без формирования рубца);
период поздних осложнений (облитерация просвета пищевода, развитие рака и др.).
Клиническая картина
Сразу после проглатывания химического вещества (острый период) отмечается многократная рвота, часто с примесью крови, возникает сильная боль в полости рта, за грудиной, в надчревье, появляется рефлекторная дисфагия. Во время рвоты возможна аспирация, в результате развивается ожог гортани, трахеи, бронхов, что может привести к тяжёлой пневмонии. У пострадавшего возникают страх, возбуждение, характерны бледность кожи, обильное слюноотделение, часто наблюдают осиплость голоса (вследствие распространения отёка с глотки на гортань), появляются одышка, тахикардия, артериальная гипотензия. При тяжёлых ожогах пищевода общее состояние больного быстро ухудшается, возбуждение сменяется адинамией, появляются холодный пот, акроцианоз, нарастают тахикардия, одышка, могут возникнуть спутанное сознание, бред. К концу первого дня температура тела повышается до 38-39 °С, уменьшается количество мочи, гемолитическое действие некоторых химических веществ может привести к почечной недостаточности. При глубоких некрозах возможна перфорация пищевода с развитием медиастинита. В наиболее тяжёлых случаях пострадавшие погибают в первые часы или дни вследствие шока или полиорганной недостаточности (летальность в остром периоде достигает 10%).
Через 7-14 дней после ожога дисфагия и боль при глотании уменьшаются (период мнимого благополучия), начинается отторжение не-кротизированных тканей пищевода. В случае глубокого некроза возможно возникновение кровотечения или перфорации пищевода. Этот опасный для жизни больного период обычно длится 2-3 нед, после чего острое воспаление стихает и начинается процесс регенерации за счёт развития грануляционной ткани. Общее состояние больного стабилизируется, дисфагия уменьшается или даже исчезает вовсе, больной начинает осторожно принимать пищу через рот, что может ввести в заблуждение врачей, которые ошибочно прекращают лечение в эту стадию патологического процесса.
Через 4—5 нед после ожога пищевода грануляции начинают замещаться плотной фиброзной соединительной тканью, которая постепенно превращается в рубец (период формирования рубцовой стриктуры). Стриктуры пищевода чаще всего локализуются в области физиологических сужений. Выше рубцового сужения стенка пищевода со временем расширяется, истончается и склеротически изменяется в результате длительной задержки пищи, поддерживающей воспалительный процесс. Рубцовые сужения могут быть полными и неполными, короткими (до 3—5 см) и протяжёнными.
Длительно существующая стриктура пищевода может привести к развитию рака (период поздних осложнений), частота которого в обожжённом пищеводе превышает таковую у здоровых людей. Клинические проявления рубцовой стриктуры зависят от степени нарушения проходимости пищевода. Основным симптомом служит дисфагия, которая обычно сопровождается гиперсаливацией и регургитацией. Если пациент своевременно не обращается за медицинской помощью, рубцовая стриктура пищевода приводит к алиментарному истощению. Указание в анамнезе на приём химического вещества, появление через некоторое время дисфагии позволяют заподозрить образование рубцового сужения пищевода.
Диагностика
Для определения локализации, протяжённости и выраженности стриктуры проводят рентгеноконтрастное исследование пищевода и желудка с использованием жидкой взвеси сульфата бария или водорастворимого контрастного вещества. Основные рентгенологические признаки рубцовой стриктуры пищевода — неравномерное сужение его просвета вплоть до полной облитерации, неровный зазубренный контур на протяжении стриктуры, деформация рельефа слизистой оболочки, ригидность стенок, наличие супрастенотического расширения (рис. 25-8). Рентгенологическое исследование также позволяет выявить сопутствующие ожоговые деформации желудка. При полной облитерации пищевода желудок и отрезок пищевода ниже сужения заполняют контрастным веществом через гастростому.
Эзофагоскопия даёт возможностьопределить степень и форму сужения, ха рактер расширения пищевода над участком стеноза, локализацию рубцов, гра ницы неизменённой слизистой оболочки. Ретроградная эзофагоскопия (через гастростому) позволяет уточнить нижнюю границу сужения, состояние пост- нижней третей пищеводастенотического отдела пищевода и желудка
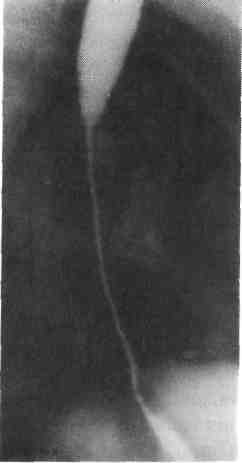
Рис.25-8 Протяженная рубцовая стриктура средней и нижней третей пищевода (рентгенограмма в боковой проекции).
Лечение
Неотложная помощь заключается в обезболивании, удалении остатков химических веществ, попавших в пищевод и желудок, и их нейтрализации. Это достигается путём введения анальгетиков, вплоть до наркотических, а также промыванием пищевода и желудка большим количеством (не менее 10 л) тёплой воды или слабого раствора нейтрализующего соединения.
Лечение химических ожогов пищевода должно быть комплексным и проводиться в специализированных отделениях. Необходимо применение инфузионно-трансфузионной, противошоковой терапии, парентерального питания, антибактериальных средств. Назначают глюкокортикоиды (гидрокортизон, преднизолон), обеспечивающие противовоспалительный эффект и лучшую регенерацию тканей. Значительно улучшают репаративные процессы сеансы гипербарической оксигенации, местное облучение через эндоскоп ожоговой поверхности гелий-неоновым лазером. При сопутствующем ожоге дыхательных путей необходимы аспирация слизи из трахеи и бронхов и поддержание проходимости дыхательных путей, при необходимости производят трахеостомию. Развитие печёночно-почечной недостаточности диктует необходимость применения эфферентных методов лечения (гемодиализ, плазмаферез).
С первых дней после ожога рекомендуют приём жидких масел (подсолнечное, оливковое, облепиховое, рыбий жир). Если в течение 5—7 дней после ожога пациент не в состоянии принимать хотя бы жидкую пищу и отсутствуют условия для проведения длительного парентерального питания, необходимо выполнять гастростомию.
Спустя 8—10 дней с момента ожога начинают бужирование пищевода, которое проводят на протяжении 1—1,5 мес. Использование раннего бужирования в 90% случаев предупреждает образование рубцового стеноза. Существует несколько методик проведения этой процедуры. Бужирование вслепую через рот представляется самой опасной из них, так как наиболее часто осложняется перфорацией пищевода. В современных условиях его обычно проводят полыми рен-тгеноконтрастными бужами по металлической струне-проводнику, который проводят под рентгенологическим контролем или под контролем фиброэзофагоскопа. Бужирование показано всем больным, которым удаётся провести через сужение в желудок металлический проводник, и абсолютно противопоказано при стриктурах, осложнившихся образованием свищей пищевода.
В результате заживления образовавшихся во время бужирования надрывов в зоне рубцового поражения у большинства больных в последующем в различные сроки развивается рестеноз, поэтому после первичного курса подобного лечения требуется проведение поддерживающих курсов бужирования в течение 1—1,5 лет для получения стойкого длительного расширения просвета в зоне сужения. При неэффективности поддерживающего лечения в течение этого времени необходимо решать вопрос о хирургической операции.
Оперативное лечение показано при полной облитерации просвета пищевода, невозможности провести буж из-за плотных рубцов, быстро возникающих после повторных курсов бужирования рецидивах стриктуры (через 3—6 мес), сочетании ожоговой стриктуры пищевода, глотки и желудка; ожоговых стриктурах, осложнённых пищеводными свищами, перфорации пищевода во время бужирования.
Выбор метода операции зависит от локализации, протяжённости и степени стриктуры, наличия осложнений, сопутствующих поражений глотки и желудка, предыдущих операций, общего состояния больного. Оперативное вмешательство может производиться в один или несколько этапов. У ослабленных пациентов первым этапом накладывают гастростому для полноценного питания. При постожоговом стенозе выходного отдела желудка вначале выполняют пилоро-пластику, гастроэнтеростомию или резекцию желудка в сочетании с гастростомией. Соединение трансплантата с пищеводом или глоткой чаще всего осуществляют одномоментно, но оно может быть отложено на второй этап при сомнении в адекватности кровоснабжения трансплантата или при недостаточной его длине.
В зависимости от локализации и протяжённости стриктуры, длины выкраиваемого трансплантата производят местную, сегментарную, субтотальную и тотальную пластику пищевода. Местная пластика может быть выполнена при коротких (протяжённостью до 3 см) стриктурах. Производят циркулярную резекцию суженного отдела пищевода с эзофагоанастомозом «конец в конец» или продольное рассечение стриктуры с ушиванием разреза пищевода в поперечном направлении.
При ограниченном рубцовом поражении пищевода может быть выполнена так называемая сегментарная пластика, для которой используют короткие трансплантаты из тонкой или толстой кишки. При протяжённых сужениях пищевода показана субтотальная или тотальная пластика пищевода трансплантатом из толстой кишки, желудка или тонкой кишки. В зависимости от локализации и протяжённости
стриктуры анастомоз между пищеводом и трансплантатом может быть сформирован или в грудной полости, или на шее.
Для субтотальной и тотальной пластики пищевода часто используют трансплантат из толстой кишки. Он может быть сформирован как из правой, так и из левой половины толстой кишки, располагаться либо в изоперистальтическом, либо в антиперистальтическом направлении. Трансплантат из толстой кишки проводят позади желудка, а затем на шею, чаще всего в загрудинном тоннеле в переднем средостении. Нижний конец трансплантата соединяют с желудком (в некоторых случаях с двенадцатиперстной или тощей кишкой), верхний конец — с пищеводом или глоткой. Непрерывность кишечника восстанавливают путём наложения анастомоза.
В настоящее время для пластики пищевода широко применяют желудок (рис. 25-9), используя как трубчатые трансплантаты, располатающиеся изоперистальтически, так и целый желудок. Пассаж пищи после желудочной пластики считают более физиологичным, так как он обеспечивает участие в акте пищеварения всех отделов ЖКТ. Кроме того, при желудочной пластике формируют лишь один анастомоз (между пищеводом или глоткой и желудком), что позволяет избежать многих осложнений. К сожалению, для пластики пищевода желудок удаётся использовать не всегда из-за выполненных ранее операций (резекция, гастроэнтеростомия, гастростомия).
В последние годы достаточно широко применяют метод удаления рубцово изменённого пищевода. Данная операция является наиболее радикальной, но к выполнению этого вмешательства необходимо подходить индивидуально, так как оно достаточно травматично и значительно отягощает течение послеоперационного периода. Трансплантат проводят в заднем средостении в ложе удалённого пищевода.
При стриктурах нижней трети пищевода может быть выполнена резекция поражённого участка с наложением анастомоза между пищеводом и желудком в грудной полости. Несостоятельность анастомоза в грудной полости приводит к развитию медиастинита, сопровождающегося высокой летальностью, поэтому большинство хирургов предпочитают тотальную и субтотальную пластику пищевода, при которых формирование анастомоза между пищеводом и трансплантатом производят на шее. Несостоятельность анастомоза на шее обычно не приводит к тяжёлым осложнениям.
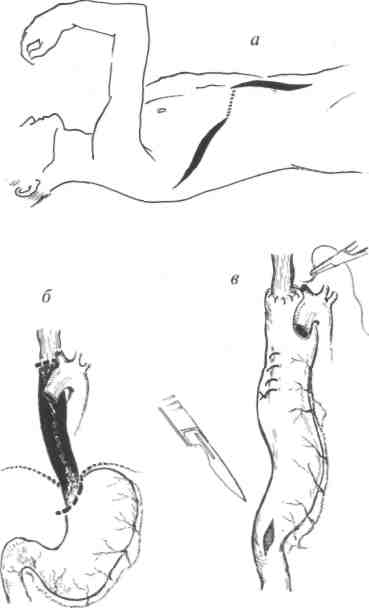
Рис. 25-9. Схема формирования искусственного пищевода из большой кривизны желудка: а — используемые доступы; б — объём удаления изменённого пищевода; в — желудок перемещён в плевральную полость и анастомо-зирован с проксимальной порцией пищевода. Выполнена внеслизистая пилоротомия для предотвращения гастростаза.
