
- •Содержание
- •Глава 1. Обзор литературы 11
- •Глава 2. Построение модели. 39
- •Глава 3. Результаты численного моделирования. Активность одиночного RyR-канала при стационарных условиях 79
- •Введение
- •Глава 1. Обзор литературы
- •1.1 Механизмы сокращения клеток сердечной мышцы
- •1.2 Рианодиновый рецептор – основной элемент управления кальциевой динамикой в клетке
- •1.3 Эксперименты по изучению изолированных RyR-каналов
- •1.4 Модели функционированияRyR-каналов
- •Стохастическая динамика и электронно-конформационные взаимодействия в белках
- •1.7 Модели «общего пула»
- •1.8. Теория локального контроля
- •1.9 Моделирование активности клеток водителей сердечного ритма
- •1.9.1 Современные представления об авторитмической активности пейсмейкеров
- •1.9.3 Модель Мальцева-Лакатты
- •Глава 2. Построение модели.
- •2.1 Электронно-конформационная модель RyR-канала
- •2.1.1 Гамильтониан канала
- •2.1.2. Конформационный потенциал
- •2.1.3 Влияние уровняtrans[Ca] на форму конформационного потенциала RyR-канала
- •2.1.4. Структурные изменения канала в электронно-конформационной модели
- •2.1.5 Динамика конформационной координаты
- •2.1.6 Динамика электронной степени свободы
- •2.1.7 Инактивационое состояние RyR-канала
- •2.1.9 Эффекты туннелирования
- •2.1.10 Проницаемость RyR-канала
- •2.2.1 Электронно-конформационная модель решетки RyR-каналов
- •2.2.1.1 Гамильтониан решетки RyR-каналов
- •2.2.2 Схема динамики RyR-каналов в решетке высвобождающей единицы
- •2.2.3 Сопряжение динамики RyR-каналов с динамикой кальция в отделах высвобождающей единицы
- •2.3 Методы численной реализации модели
- •2.3.1 Метод Эйлера-Марайамы
- •2.3.2 Реализация электронных и туннельных переходов. Метод Монте-Карло
- •2.3.3 Численная схема для эк-модели RyR-канала
- •2.4 Описание программного комплекса
- •2.5 Заключение
- •Глава 3. Результаты численного моделирования. Активность одиночного RyR-канала при стационарных условиях
- •3.1 Анализ временных зависимостей конформационной координатыQ
- •3.2 Медленная конформационная динамика RyR-канала
- •3.2.1 Параметр эффективного трения г. Конформационная динамика RyR-канала
- •3.2.2 Влияние коэффициента упругости каналаK на форму конформационного потенциала
- •3.2.3 Зависимость конформационного потенциала от параметра электронно-конформационного взаимодействияа
- •3.3 Стохастическая динамика RyR-канала. Быстрые переходы
- •3.3.1 Кинетические характеристики динамики RyR-канала
- •3.3.2 Зависимость вероятности электронных переходов отcis[Ca]
- •3.4 Активация одиночного канала
- •3.5 Исследование процесса закрытия RyR-канала
- •3.6 Процесс адаптации RyR-каналов к продолжительной стимуляции
- •3.7 Динамика одиночного RyR-канала при установившемся уровне cis[Ca]
- •3.7.1 Зависимость активности RyR-канала от времени
- •3.7.2 Зависимость активности RyR-канала от уровня cis[Ca]
- •3.8 Заключение
- •4.1 Анализ модели высвобождающей единицы
- •4.1.1 Процессы открытия и закрытия каналов в высвобождающих единицах.
- •4.1.2 Анализ кооперативной динамики RyR-каналов в кластере
- •4.2.1 Высвобождающая единица как самоподдерживающийся кальциевый осциллятор
- •4.2.3 Влияние взаимодействия междуRyR-каналами на стабильность осцилляций системы
- •4.2.3 Эффект случайной остановки автоколебаний
- •4.2.3.1 Форма и устойчивость кластеров открытых каналов
- •4.2.3.2 Характерное время перехода в стационарное состояние
- •4.3 Заключение
- •Заключение
- •Список литературы
- •Основные публикации по теме диссертации
2.2.3 Сопряжение динамики RyR-каналов с динамикой кальция в отделах высвобождающей единицы
Для создания замкнутой модели высвобождающей единицы с учетом стохастической динамики RyR-каналов была установлена связь между параметрами теории высвобождающей единицы и ЭК-моделью.
В модели высвобождающей единицы поток высвобождающегося Са2+ в диадное пространство зависит от числа открытых каналов в кластере.
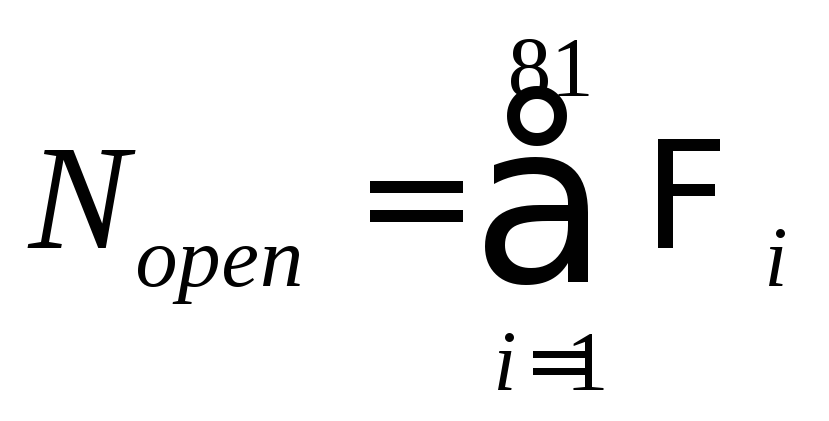 , (2.22)
, (2.22)
где
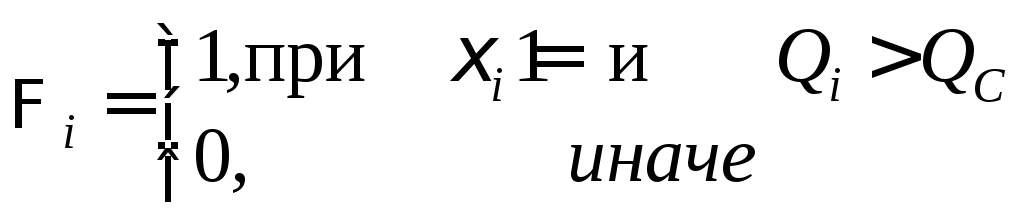 – «открытость» канала, где
– «открытость» канала, где![]() – значение конформационной координаты
точки локального максимума нижней ветвиC
конформационного потенциала (3.3.3) (см.
рис. 2.3).
– значение конформационной координаты
точки локального максимума нижней ветвиC
конформационного потенциала (3.3.3) (см.
рис. 2.3).
Таким образом,
динамика концентрации кальция в отделах
высвобождающей единицы вызывает
изменение параметра
![]() ,
который влияет на динамику состоянийRyR-каналов,
и как следствие, на число открытых
RyR-каналов
Nopen.
Переменная Nopen,
в свою очередь, определяет скорость
высвобождения кальция из люмена СР.
,
который влияет на динамику состоянийRyR-каналов,
и как следствие, на число открытых
RyR-каналов
Nopen.
Переменная Nopen,
в свою очередь, определяет скорость
высвобождения кальция из люмена СР.
На основе вышеизложенных положений получена замкнутая объединенная модель, на базе которой в данной работе проводилось численное моделирование динамики Са2+ в отделах кардиомиоцитов.
2.2.4 Модель Са2+-высвобождающей единицы
Разработка модели Са2+-высвобождающей единицы основана на широко известной модели структуры клетки (рисунок 2.14) [90, 112, 113], состоящей из четырех основных компонентов: диадного пространства, цитозоля, сети СР и просвета ТЦ (люмена) СР. Особенностью данного представления является рассмотрение обобщенной Са2+ высвобождающей единицы.

Основываясь на схеме динамики Са2+ в клетке, введены четыре кальциевых потока между отделами клетки:
1. Поток
заполнения люмена
![]() (от англ.refill
– заполнять), его значение зависит от
параметра скорости заполнения
(от англ.refill
– заполнять), его значение зависит от
параметра скорости заполнения
![]() и разности концентраций Са2+
в сети СР и в люмене и определяется как:
и разности концентраций Са2+
в сети СР и в люмене и определяется как:
![]() .
(2.23)
.
(2.23)
2. Поток
высвобождения
Са2+
из люмена
![]() (от англ.release
– высвобождать), величина которого
зависит от числа открытых каналов в
кластере высвобождающей единицы
(от англ.release
– высвобождать), величина которого
зависит от числа открытых каналов в
кластере высвобождающей единицы
![]() и от величины потока Са2+
через одиночный открытый канал
и от величины потока Са2+
через одиночный открытый канал
![]() :
:
![]() . (2.24)
. (2.24)
Значение потока Са2+ через одиночный канал определяется формулой:
![]() , (2.25)
, (2.25)
где
![]() – параметр скорости высвобождения,
– параметр скорости высвобождения,![]() – концентрация Са2+
в люмене,
– концентрация Са2+
в люмене,
![]() – концентрация Са2+
в диадном пространстве.
– концентрация Са2+
в диадном пространстве.
3. Диффузионный
поток между
диадным пространством и цитозолем
![]() ,
значение которого зависит от градиента
концентраций Са2+
в диадном пространстве и в цитозоли
,
значение которого зависит от градиента
концентраций Са2+
в диадном пространстве и в цитозоли
![]() и определяется как:
и определяется как:
![]() , (2.26)
, (2.26)
где
![]() – параметр скорости диффузии.
– параметр скорости диффузии.
4. Поток
заполнения
сети СР
![]() (от
англ.uptake
– накачка). Процесс накачки СР кальцием
против градиента концентрации требует
энергетических затрат (фосфорилляция
молекул АТФ), значение потока зависит
от концентрации Са2+
в цитозоле и от параметров Са2+-насоса:
(от
англ.uptake
– накачка). Процесс накачки СР кальцием
против градиента концентрации требует
энергетических затрат (фосфорилляция
молекул АТФ), значение потока зависит
от концентрации Са2+
в цитозоле и от параметров Са2+-насоса:
![]() (скорость накачки) и
(скорость накачки) и![]() (чувствительность насоса). Для зависимости
потока от концентрации Са2+
была использована формула, заимствованная
из модели [54]:
(чувствительность насоса). Для зависимости
потока от концентрации Са2+
была использована формула, заимствованная
из модели [54]:
![]() .
(2.27)
.
(2.27)
Кальциевые потоки в упрощенной модели сердечной клетки (рис. 2.14) с учётом квазистационарного взаимодействия с кальциевыми буферами описываются стандартной системой дифференциальных уравнений [91]:
![]()
 (2.28)
(2.28)
В модели учитывается связывание ионов Са2+ с регуляторными глобулярными белками – буферами, которые участвуют в процессе мышечного сокращения. Были учтены следующие Са2+-связывающие буферы, содержащиеся в кардиомиоците: кальсеквестрин, кальмодулин, тропонин.
Параметры
концентраций буферов, учитывающиеся в
модели, взяты из работы [85]: CQtot
= 10-2
М
полная концентрация кальсеквестрина,
CMtot
= 45·10-6
М
полная концентрация кальмодулина, TCtot
= 31·10-6
М - полная концентрация тропонина C.
![]()
константы отношений объемов
константы отношений объемов
![]() и
и![]() отделов клетки (рис. 2.14) (
отделов клетки (рис. 2.14) (![]() = 40,
= 40,![]() = 9.7,
= 9.7,![]() = 0.12,
= 0.12,![]() =
0.022).
=
0.022).![]() = 833·10-6
M,
= 833·10-6
M,
![]() = 2.4·10-6
M,
= 2.4·10-6
M,
![]() = 5·10-6
M
– константы диссоциации соответствующих
буферов. Следует отметить, что все эти
параметры выбраны как типичные для
интегративной модели, а не для модели
одиночной высвобождающей единицы.
= 5·10-6
M
– константы диссоциации соответствующих
буферов. Следует отметить, что все эти
параметры выбраны как типичные для
интегративной модели, а не для модели
одиночной высвобождающей единицы.
Другими словами,
было предположено, что все RyR-каналы
формируют систему идентичных высвобождающих
единиц, функционирующих согласованно.
Параметры ЭК модели (2.5, 2.7, 2.8) при
проведении численных экспериментов
имели следующие значения: a
= 5, K
= 12,
![]() ,
Г = 7. Параметры туннелирования:A
= 1,
,
Г = 7. Параметры туннелирования:A
= 1,
![]() =
0.01 [A2].
=
0.01 [A2].
