
- •Лабораторная работа № 4. Приготовление растворов заданного количественного состава. Определение концентрации растворов титрованием.
- •1. Разделы теоретического курса для повторения.
- •2. Теоретическая часть.
- •7. Моляльность. Моляльность раствора характеризуется количеством растворенного вещества в молях, приходящихся на 1 кг растворителя в данном растворе.
- •В своей рабочей тетради запишите ответы на вопросы и упражнения из раздела 3.
- •3. Вопросы и упражнения.
- •В рабочем журнале оформите раздел 4 и распечатайте его для выполнения в лаборатории(2 стр. На листе).
- •Зависимость плотности раствора от массовой доли растворенного вещества 20◦ , (г/см3)
- •Данные для приготовления раствора заданного количественного состава
- •Результаты эксперимента по приготовлению раствора заданного количественного состава.
- •Количественный состав раствора с заданной массовой долей, выраженный иными способами.
- •Часть 2. Определение концентрации растворов кислот и щелочей титрованием.
- •Результаты титрования раствора щелочи раствором кислоты.
- •Лабораторная работа № 5 Химическая кинетика и химическое равновесие.
- •1. Разделы курса, необходимые для подготовки к лабораторной работе.
- •2. Теоретическая часть. Химическая кинетика.
- •Реагенты→ переходное состояние→ продукты реакции.
- •Химическое равновесие.
- •Смещение химического равновесия.
- •Влияние изменения концентрации на смещение химического равновесия.
- •Влияние изменения давления на смещение химического равновесия.
- •Влияние изменения температуры на смещение химического равновесия.
- •Влияние катализатора на состояние химического равновесия.
- •В своей рабочей тетради запишите ответы на вопросы и упражнения из раздела 3.
- •3. Вопросы и упражнения.
- •В рабочем журнале оформите раздел 4 и распечатайте его для выполнения в лаборатории(2 стр. На листе).
- •Опыт 1. Зависимость скорости реакции от концентрации реагирующих веществ.
- •Зависимость скорости реакции от условной концентрации раствора
- •Опыт 2. Зависимость скорости реакции от температуры.
- •Зависимость скорости реакции от температуры.
- •Опыт 3. Влияние площади поверхности на скорость реакции в гетерогенной системе.
- •Часть 2. Химическое равновесие.
- •Влияние изменения концентрации реагентов и продуктов реакции на смещение химического равновесия.
- •Лабораторная работа № 6. Электролитическая диссоциация.
- •2. Теоретическая часть.
- •Зависимость силы электролита от значения константы его диссоцации.
- •Реакции в растворах электролитов.
- •В своей рабочей тетради запишите ответы на вопросы и упражнения из раздела 3.
- •3. Вопросы и упражнения.
- •4.Экспериментальная часть.
- •Сравнение химической активности электролитов.
- •2. Влияние сильного электролита, содержащего одноименный ион, на диссоциацию слабого электролита.
- •3. Реакции обмена в растворах электролитов.
- •Лабораторная работа № 7 Водородный показатель. Гидролиз солей.
- •1. Разделы теоретического курса для повторения.
- •2. Теоретическая часть.
- •Определение рН среды колориметрическим методом.
- •Изменение окраски индикаторов в зависимости от реакции среды.
- •Определение рН среды потенциометрическим методом.
- •Гидролиз
- •Гидролиз солей.
- •В своей рабочей тетради запишите ответы на вопросы и упражнения из раздела 3.
- •3. Вопросы и упражнения.
- •4. Экспериментальная часть.
- •1. Определение реакции среды колориметрическим методом.
- •Определение реакции среды и величины водородного показателя среды некоторых растворов колориметрическим методом.
- •Б) Определение реакции среды с помощью универсальной индикаторной бумаги.
- •2. Определение рН среды потенциометрическим методом.
- •Результаты определения величины рн среды потенциометрическим методом.
- •Порядок измерения величины рН растворов.
- •3. Влияние разбавления на глубину протекания процесса гидролиза.
- •4. Влияние нагревания на процесс гидролиза.
- •5. Взаимное усиление гидролиза.
- •6. Растворение активного металла в продуктах гидролиза.
- •7. Связь между константой гидролиза Кгидр. И константой диссоциации слабого электролита, образующего гидролизующуюся соль.
Данные для приготовления раствора заданного количественного состава
|
Величина |
Обозначение |
Значение |
Размерность |
|
Плотность раствора заданного количественного состава |
ρраствора теор. |
|
г/см3 |
|
Масса раствора |
mраствора |
|
г |
|
Масса растворенного вещества |
mраств. в-ва |
|
г |
|
Масса растворителя |
mрастворителя |
|
г |
|
Объем растворителя |
Vрастворителя |
|
cм3 |
Растворяемое вещество, найденной массы, взвесьте на весах. Необходимый объем дистиллированной воды отмерьте мерным цилиндром.
Приготовьте раствор в химическом стакане, перемешивая стеклянной палочкой. Термометром измерьте температуру раствора. Если температура отличается от 20°С, то раствор необходимо нагреть или охладить.
Перелейте раствор в цилиндр объемом 25 см3 и осторожно опустите в него ареометр. По шкале ареометра (по нижнему мениску жидкости) определите плотность приготовленного раствора.
Внимание! Необходимо помнить, что во время определения плотности раствора, ареометр не должен касаться стенок цилиндра. После каждого определения ареометр моют, протирают фильтровальной бумагой и осторожно помещают в соответствующее гнездо штатива.
По измеренной плотности эксп., используя, в случае необходимости, метод интерполяции по данным табл. 2 определите значение массовой доли растворенного вещества в приготовленном растворе (ω эксп.).
Сравните найденное значение (ω эксп.) с заданным значением массовой доли (ω теор.) и определите значение относительной ошибки эксперимента (относ.):
относ.
=
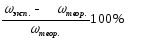
Приведите расчеты и запишите в табл. 4 полученные экспериментальные и расчетные данные.
Таблица 4
Результаты эксперимента по приготовлению раствора заданного количественного состава.
|
Величина и ее обозначение |
Значение |
Размерность |
|
Измеренная плотность приготовленного раствора, ρ эксп. |
|
г/см3 |
|
Массовая доля растворенного вещества в приготовленном растворе, ω эксп |
|
- |
|
Относительная ошибка эксперимента, относ. |
|
- |
Нарисуйте рисунок, изображающий определение плотности раствора ареометром.
Для раствора с заданной массовой долей выразите количественный состав раствора другими способами. Для этого рассчитайте значения массовой, молярной и нормальной концентраций и моляльность этого раствора.
Приведите необходимые расчеты и полученные результаты занесите в таблицу 5:
Таблица 5
Количественный состав раствора с заданной массовой долей, выраженный иными способами.
|
Способы выражения количественного состава растворов |
Обозначение |
Значение |
Размерность |
|
Массовая доля |
ω теор. |
|
|
|
Массовая концентрация |
С масс. |
|
|
|
Молярная концентрация |
С мол. |
|
|
|
Нормальная концентрация |
С норм. |
|
|
|
Моляльность |
С моляльн. |
|
|
