
- •Михаил Бушма Кирилл Бушма
- •ЧастьV. Лекарственные средства, регулирующие обмен веществ
- •24. Гормональные препараты полипептидной структуры и производные тирозина Михаил Бушма
- •25. Препараты стероиднЫх гормонов, их агонисты и антагонисты Михаил Бушма
- •26. Фармакология аутакоидов Михаил Бушма
- •Глюкокортикоиды
- •27. Витаминные препараты. Стимуляторы процессов регенерации тканей. Ферменты Михаил Бушма
- •28. Антиферментные лекарственные средства. Биогенные стимуляторы. Общетонизирующие Михаил Бушма
- •29. Плазмозамещающие растворы. Лекарственные средства, применяемые для парентерального питания Михаил Бушма, Кирилл Бушма
- •ЧастьVi. Противовоспалительные, иммунотропные и противорадиационные лекарственные средства
- •30. Противовоспалительные лекарственные средства Михаил Бушма
- •31. Иммунотропные и противорадиационные лекарственные средства Михаил Бушма
- •ЧастьVii. Противомикробные лекарственные средства
- •33.-Лактамные антибиотики Михаил Бушма, Кирилл Бушма
- •34. Макролиды, тетрациклины, хлорамфеникол, линкоЗамиды, аминогликозиды и дрУгие антибиотики Михаил Бушма, Кирилл Бушма
- •35. Противомикробные химиотерапевтические Лекарственные средства синтетического происхождения Михаил Бушма, Кирилл Бушма
- •36. Противогрибковые, противосифилитические, противотуберкулезные и противолепрозные лекарственные средства Михаил Бушма
- •Противогрибковые лекарственные средства
- •Противосифилитические лекарственные средства
- •ПротивотуберкулЕзные лекарственные средства
- •Противолепрозные лекарственные средства
- •ЧастьViii. Противовирусные, противопротозойные, противоглистные и противоопухолевые лекарственные средства
- •37. Противовирусные лекарственные средства Михаил Бушма
- •38. Противопротозойные лекарственнЫе средства Михаил Бушма
- •Противомалярийные лекарственные средства
- •Противоамебные лекарственные средства
- •Противолямблиозные лекарственные средства
- •Противотрихомонадные лекарственные средства
- •Противобалантидиазные лекарственные средства
- •Противотоксоплазмозные лекарственные средства
- •Противолейшманиозные лекарственные средства
- •39. Противоглистные лекарственные средства Михаил Бушма
- •Противоцестодозные лекарственные средства
- •40. Противоопухолевые лекарственные средства Михаил Бушма
- •ЧастьIx. Фармакотерапия неотложных состояний, наркоманий, токсикоманий и острых отравлений лекарственными средствами
- •41. Фармакотерапия неотложных состояний в клинике внутренних болезней Михаил Бушма, Кирилл Бушма
- •42. Фармакотерапия наркоманий и токсикоманий Михаил Бушма, Кирилл Бушма
- •43. Основные принципы терапии острых отравлений лекарственными средствами Михаил Бушма, Кирилл Бушма
- •ЧастьX.
- •44. Особенности перинатальной и педиатрической фармакологии Михаил Бушма
- •Литература
- •Алфавитный указатель международных непатентованных названий лекарственных средств
- •Содержание
40. Противоопухолевые лекарственные средства Михаил Бушма

«Люди не умирают. Они совершают медленное самоубийство»
Обзор. Примерно у каждого четвертого человека в течение жизни диагностируются опухоли. Каждый 4 раковый больной подвергается только хирургическому лечению и/или местному радиоактивному облучению. 3/4 получают химиотерапию.
Примерно у 10 % больных химиотерапия может вызвать «излечение» или длительную ремиссию. В большинстве случаев она приводит к регрессии заболевания, рецидивам и смерти. Более чем пятилетнее выживание регистрируется ≈ у 40 % раковых больных. 60 % умирает раньше. Среди причин смерти рак занимает второе место.
Принципы химиотерапии рака
Цель лечения– продление жизни. Если основное лечение не достигло результата, проводится паллиативное лечение (например, опиоидные анальгетики), которое позволяет больным поддерживать «нормальное» существование.
Количество опухолевых клеток ↓ после: 1) удаления опухоли, 2) облучения, 3) химиотерапии, 4) комбинации этих воздействий.
Показания для химиотерапии: 1) метастазы (нельзя удалить оперативно), 2) как дополнение к оперативному и радиационному лечению с целью ↓ количества микрометастазов.
Чувствительность опухоли и клеточный цикл. Нормальные и опухолевые клетки проходят одни и те же фазы клеточного цикла.
G0– покой.
G1(≈ 40 % клеточного цикла; сильно варьирует). Клетка готовится к синтезу ДНК. То есть синтезирует необходимые для этого ферменты.
S(39 %). Синтезируется ДНК, происходит ее репликация.
G2(19 %). Завершив синтез ДНК, опухолевая клетка синтезирует другие молекулы, необходимые для деления (↑ объем цитозоля).
М (2 %) – митоз. Опухолевая клетка разделилась на 2 дочерние клетки (рис. 40.1).

Рисунок 40.1. Клеточный цикл
Нормальные и опухолевые ткани могут различаться по числу клеток, находящихся в различных стадиях цикла. Одни цитостатики эффективны только против делящихся клеток. Другие эффективны и против опухолей с низким процентом делящихся клеток.
Скорость роста большинства опухолей первоначально быстрая. ↓ По мере ↑ размера опухоли из-за нарушений кровоснабжения. Это приводит к недостаточности питания и кислорода. Уменьшение опухоли после операции или облучения вызывает возврат клеток к быстрой пролиферации и ↑ чувствительности к цитостатикам.
Действие лечения на нормальные клетки.Цитостатики уничтожают прежде всего быстро делящиеся клетки. При этом также оказывается токсическое действие на нормальные, быс-тро делящиеся клетки: слизистой ЖКТ, волосяных фолликулов, костного мозга.
Скорость уничтожения.Гибель клеток опухоли цитостатиками подчиняется кинетике 1 порядка. Это означает, что уничтожается постоянная часть клеток. Например, диагноз лейкоз обычно ставят тогда, когда присутствует 1х109раковых клеток. Следовательно, если лечение приводит к уничтожению 99,999 % раковых клеток, то 0,001 % от 1х109клеток (или 1х104 клеток) остается. В этот период симптомы исчезают. Наступает ремиссия. Необходимо дополнительное лечение для тотального уничтожения популяции опухолевых клеток (табл. 40.1).
Таблица 40.1. Динамика гибели раковых клеток, вызываемой цитостатиками

В большинстве случаев симптомы рака проявляются, если опухоль достигает массы 1 г (1х109 клеток).
Возможные варианты.
Без лечения. Результат – смерть. Наступает, когда масса опухоли достигает ≈ 1 кг (1х1012 раковых клеток).
Нерегулярное лечение цитостатиками. Результат – продление жизни и повторное появление симптомов между курсами. Смерть.
Раннее и интенсивное лечение. Результат – гибель раковых клеток преобладает над их появлением. Устойчивость к цитостатикам не развивается. [Примечание. Лечение продолжается ≈ в течение 3-х лет после исчезновения симптомов рака].
Раннее удаление опухоли + интенсивное лечение цитостатиками в течение ≈ 1 года. Результат – «излечение» (рис. 40.2).

Рисунок 40.2. Эффекты различных способов лечения у гипотетического больного раком
«Фармакологические убежища». Опухолевые клетки находят «убежища» в тканях, в которые не проникают цитостатики [например, ЦНС, яички]. Поэтому: 1) облучают ЦНС, 2) цитостатик вводят в ликвор. Кроме того, цитостатики не проникают внутрь плотных опухолей.
Устойчивость опухолевых клеток к цитостатикам.Некоторые опухоли изначально устойчивы к цитостатикам. Другие ее приобретают, особенно после длительного лечения низкими дозами цитостатиков. За устойчивость ответственны различные механизмы. Две из них – основные.
Первый механизм множественной устойчивости опухолевых клеток к цитостатикам. В плазматической мембране нормальных тканей (эпителиальные клетки почек, толстого кишечника, надпочечников), а также опухолевых клеток локализуетсяp-гликопротеин. Состоит из 12 доменов. Со стороны цитозоля содержит 2 участка, связывающие цитостатики. [Примечание. Только 1 участок используется для “выброса” цитостатика из клетки]. Расходуется АТФ. Он удаляет и другие лекарственные средства:верапамил,хинидин,циклоспорин. С их помощью можно преодолеть устойчивость опухолевых клеток к цитостатикам (рис. 40.3).

Рисунок 40.3. Устойчивость опухолевых клеток к цитостатикам, обусловленная р-гликопротеином
Второй механизм множественной устойчивости опухолевых клеток к цитостатикам– качественные и количественные изменения топоизомеразыII. Она устраняет повреждения ДНК, вызванные цитостатиками (репорация ДНК).
Устойчивость можно преодолеть кратковременной интенсивной прерывистой терапией комбинацией цитостатиков. Она эффективна против большинства устойчивых опухолей.
Противоопухолевые лекарственные средства
Определение. Это химически неоднородная группа лекарственных средств, способных различными путями блокировать деление опухолевых клеток и предназначенных для химиотерапии опухолей и опухолеподобных заболеваний крови.
Классификация групп(рис. 40.4)

Рисунок 40.4. Группы противоопухолевых лекарственных средств и точки приложения их действия
Цитостатики бывают: 1) специфичные, 2) не специфичные к клеточному циклу.
Специфичные. Блокируют отдельные фазы клеточного цикла. Например, антиметаболиты. Эффективны против быстро растущих опухолей (например, лейкоз).
Не специфичные к клеточному циклу. Подавляют раковые клетки в любой фазе клеточного цикла. Например, алкилирующие. Эффективны против медленно (например, солидные) и быстро (например, меланома) растущих опухолей.
Комбинированная химиотерапия.Необходимые условия: 1) каждый цитостатик комбинации должен быть активным против опухоли, 2) цитостатики должны иметь различные проявления токсичности. Цитостатики с одинаковой токсичностью (например, угнетающие костный мозг) комбинируют только при условии ↓ доз каждого. Комбинация приводит: 1) к суммации или потенцированию цитотоксических эффектов, 2) ↓ токсичности.
Схема лечения прерывистая для: 1) восстановления иммунной системы, 2) ↓ частоты побочных эффектов присоединяющихся тяжелых инфекций.
Побочное действие цитостатиков и пути ↓ его проявлений.Цитостатики обладают узкой широтой терапевтического действия. Быстро делящиеся нормальные ткани чувствительны к повреждению.
Угнетение костного мозга(все цитостатики). Развиваются: 1) лейкопения, 2) тромбоцитопения, 3) анемия.Лечение:1) колониестимулирующие факторы, 2) переливание эритроцитарной и тромбоцитарной массы, 3) ↑ дозы бактерицидных антибиотиков, пока не восстановится лейкопоэз, 4) пересадка костного мозга при безуспешных попытках нормализации его функции. 5) мегалобластическую анемию, вызываемую некоторыми антиметаболитами, лечатлейковорином.
Цитостатики повреждают также: эпителий ЖКТ (понос), зародышевый эпителий в половых железах (бесплодие), волосяные фолликулы (облысение).
Тошноту и тяжелую рвоту устраняют: фенотиазиновыми нейролептиками (пиперазин), препаратами марихуаны (дронабинол), блокаторами D2– (метоклопрамид) и серотониновых (ондансетрон) рецепторов.
Массовая гибель раковых клеток приводит к гиперурикемии и кристаллурии. Назначают ингибитор ксантиноксидазы аллопуринол. На месте инъекции может развиться некроз.
Опухоли, вызванные цитостатиками.Поскольку большинство цитостатиков мутагены, опухоли (например, острый нелимфоцитарный лейкоз) могут появиться спустя 10 и > лет после лечения рака (особенно при назначении алкилирующих лекарственных средств).
Мутагены, тератогены и канцерогены – алкилирующие.
Цитостатики с уникальной токсичностью: кардио- и пневмотоксичность (отдельные антибиотики), нейротоксичность (некоторые препараты растений).
Отдельные алкилирующие лекарственные средства вызывают геморрагический цистит. Его проявления ↓ при ↑ диуреза маннитоломи введением жидкостей в вену.
Ослабление токсичности цитастатиков.Можно достичь ↓ их объема распределения. Например, локальной перфузией при саркоме руки.
Длительность токсичности.Широко варьирует. Например, облысение проходит. Пневмо- и кардиотоксичность необратимы.
Антиметаболиты(рис. 40.5)

Рисунок 40.5. Антиметаболиты
Строение. Напоминают нормальные компоненты клеток.
Механизм действия. Конкурируют с пуриновыми и пиримидиновыми нуклеотидами в синтезе ДНК и РНК. БлокируютS-фазу.
Недостатки.1. Устойчивость опухолевых клеток, 2) разрушение в ЖКТ (цитарабин), 3) не проникают в ЦНС (цитарабин,метотрексат).
Цитарабин
Строение. Цитозинарабинозид.
Механизмы цитотоксического действия.Цитарабинпроникает в клетки с участием переносчика. Фосфолируется до трифосфата. Последний: 1) ингибирует ДНК-полимеразу; 2) включается в нуклеиновые кислоты с образованием дефектных ДНК, РНК и нарушением их функции.
Устойчивость. 1) дефект процессов транспорта; 2) ↓ активности ферментов, катализирующих его фосфорилирование.
Применение. Острый миелолейкоз (в комбинации стиогуанином идаунорубицином).
Фармакокинетика. Не эффективен при приеме через рот, поскольку дезаминируется в слизистой ЖКТ до нецитотоксического урациларабинозида. Распределяется, но не проникает в ЦНС. [Примечание. При опухолях ЦНС вводят субарахноидально]. Фосфорилируется до трифосфата. В печени дезаминируется до урациларабинозида.Цитарабини его метаболит выводятся почками.
Побочное действие. Тошнота, рвота, понос. Тяжелое угнетение костного мозга и функции печени. При субарахноидальном введении – судороги и расстройства психики.
Меркаптопурин
Действие. Проникает в клетки опухоли и превращается в меркаптопурин-рибозофосфат, который оказывает цитотоксическое действие.
Устойчивость. 1. ↓ Образования последнего, 2) ↑ биотрансформации до тиомочевой кислоты.
Применение. Для поддержания ремиссии у онкобольных.
Фармакокинетика.Всасывание в ЖКТ неравномерное. В печени метаболизируется ксантиноксидазой до тиомочевой кислоты. С целью ↓ дозымеркаптопуринаего комбинируют с ингибитором ксантиноксидазыаллопуринолом.Меркаптопурини его метаболиты выводятся почками.
Побочное действие. Тошнота, рвота, понос, угнетение костного мозга.
Метотрексат
Строение. Похож на фолиевую кислоту.
Механизм действия. Антагонист фолата. [Примечание. Метилтетрагидрофолат – источник метильных групп. Последние необходимы делящимся клеткам для биосинтеза метионина, аденина, гуанина, и дезокситимидиловой кислоты.
После всасывания фолиевая кислота пищи или образуемая кишечной флорой превращается в дигидрофолат. Затем он превращается в тетрагидрофолат с участием дигидрофолатредуктазы. Метотрексатингибирует фермент. Обладает исключительно сильным сродством к дигидрофолатредуктазе. Его ингибирующее действие может быть обращено только 100-кратным избытком природного субстрата – дигидрофолата или введениемлейковорина(тетрагидрофолат).
Действие.Метотрексат↓ биосинтез тимидиловой кислоты, метионина, аденина, гуанина. Это приводит к ↓ синтеза ДНК, РНК и гибели клетки.
Устойчивость. Характерна для непролиферирующих клеток.
Механизмы устойчивости. 1. Активация дигидрофолатредуктазы. [Примечание. Дозуметотрексата ↑, но ↑ токсичность]. 2. Модификация дигидрофолатредуктазы. [Примечание. Сродство фермента кметотрексату↓]. 3. ↓ Проникновения в опухолевую клетку.
Применение. 1) опухолевые и 2) неопухолевые заболевания.
Опухолевые заболевания.Острый лимфолейкоз, хориокарцинома, лимфома Баркетта у детей; опухоли молочной железы, головы и шеи. ↑ Дозыметотрексатаиспользуют для лечения остеогенной саркомы. Однако необходимо последующее введениелейковоринадля защиты костного мозга.
Неопухолевые заболевания.Стероидозависимая астма, тяжелый псориаз, ревматоидный артрит, для вызывания аборта.
Фармакокинетика. Быстро всасывается в ЖКТ. Чаще вводят внутримышечно и внутривенно. Поскольку не проходит через ГЭБ, для уничтожения опухолевых клеток в ЦНС вводят субарахноидально.
Метотрексатподвергается гидроксилированию в 7 позиции. 7-OHпроизводное менее растворимо в воде. В ↑ дозах вызывает кристаллурию. Поэтому важно: 1) поддерживатьpHмочи в щелочной области и 2) обильное питье для предотвращения нефротоксичности.Метотрексати 7-OHметаболит выводится с мочой.
Побочное действие. Стоматиты, подавление костного мозга, покраснение, сыпь, облысение, тошнота, рвота и понос. Антидот –лейковорин, который накапливается нормальными клетками быстрее, чем опухолевыми. Дозылейковорина должны быть минимальными, чтобы избежать ослабления противоопухолевого действияметотрексата.
Поражение почек. При применении ↑ доз.
Печень. Цирроз при длительном применении.
Нейротоксичность. При субарахноидальном введении развивается раздражение мозговых оболочек (ригидность мышц шеи, головная боль) и лихорадка. У детей ↓ успеваемость.
Антибиотики
Механизм действия. Связываются с ДНК и нарушают ее функцию. Не специфичны к клеточному циклу, но обладают выраженным действием на быстро делящиеся клетки.
Недостатки. 1. Устойчивость опухолевых клеток и 2) некроз тканей при попадании во внесосудистое пространство.
Классификация(рис. 40.6)

Рисунок 40.6. Противоопухолевые антибиотики
Дактиномицин. Известен биохимикам как актиномицин Д.
Строение.Плоская молекула.
Действие. Внедряется в узкую щель двойной спирали ДНК между смежной парой оснований гуанин-цитозин двух спиралей ДНК. Связывается с дезоксигуаниловой кислотой. Образуется стабильный комплексдактиномицин–ДНК. Он ингибирует ДНК-зависимую РНК-полимеразу и синтез ДНК; разрывает цепь ДНК.
Устойчивость: 1) репарация ДНК, 2) ↑ выбросадактиномицина из клетки.
Применение. 1. Опухоль Вилмса (в комбинации свинкристином + хирургическим удалением опухоли). 2. Хориокарцинома и саркома мягких тканей (в комбинации смето-трексатом).
Фармакокинетика.Дактиминомициннакапливается в печени. Метаболизируется.Дактиминомицини метаболиты выводятся с мочой и желчью.
Побочное действие. Угнетение костного мозга, тошнота, рвота, понос, стоматиты, выпадение волос. При попадании во внесосудистое пространство – некроз тканей.
Взаимодействие.С γ-облучением. Результат – ↑ чувствительности кожи (воспаление) к γ-облучению.
Доксорубицин
Механизм действия.1. Включается в ДНК. ↓ Синтез ДНК и РНК. 2. Связывается с мембранами клеток с повреждением трансмембранного транспорта. 3. ↑ Образование радикалов кислорода. Последние повреждают ДНК (рис. 40.7).

Рисунок 40.7. Повреждение доксорубициномДНК опухолевой клетки
Действие. Максимальное вS-фазе.
Устойчивость.Развивается за счет: 1) ↓ его внутриклеточного накопления, 2) ↑ скорости удаления из клетки транспортным р-гликопротеином, 3) ↓ активности цитохромР450 редуктазы; 4) репарации ДНК.
Применение. Острый лимфолейкоз, рак молочной железы и легкого, болезнь Ходжкина.
Фармакокинетика. Вводят в вену. Связывается с белками плазмы и тканей. Не проникает в ЦНС. Метаболизируется до продуктов, которые так же цитотоксичны. Экскреция – с желчью. У больных с нарушенной функцией печени ↓ дозу. Частично удаляется почками, но у больных с недостаточной функцией почек, дозу не изменяют.
Побочное действие. Обратимое угнетение костного мозга, стоматиты и расстройства ЖКТ. Выпадение волос. При попадании во внесосудистое пространство – некроз тканей. Окрашивают мочу в красный цвет. Кардиотоксичность. [Примечание. В опухоли и сердце ↓ активность супероксиддисмутазы. В сердце ↓ активность и каталазы. Поэтому Н2О2не разрушается. Развивается необратимая дозозависимая кардиотоксичностьдоксорубицина].
Взаимодействие. С γ-облучением грудной клетки. Результат – ↑ риска развития кардиотоксичностидоксорубицина.
Даунорубицин. См.доксорубицин. Кардиотоксичность обратимая и менее тяжелая.
Блеомицин
Строение. Медь-содержащие гликопептиды.
Механизм действия. Образуется комплексблеомицин-Fe++-ДНК. Свободные электроны взаимодействуют с кислородом с образованием супероксидных или гидроксильных радикалов. Они атакуют фосфодиэфирные связи, приводя к разрывам ДНК и хромосомным аберрациям (рис. 40.8).

Рисунок 40.8. Повреждение блеомициномДНК опухолевой клетки
Действие.Блокирует фазуG2 .
Устойчивость. Репарация ДНК.
Применение.1. Опухоли яичек (в комбинации свинбластиномицисплатин). Излечение наступает ≈ в 90 % случаев. 2. Сквамозно-клеточные карциномы и лимфомы.
Фармакокинетика.Вводят под кожу, внутримышечно, внутривенно, в полости. Накапливается в эпителии (кожи, легкого, брюшины, лимфоидных тканей). Не метаболизируется. Выводится с мочой клубочковой фильтрацией. У больных с почечной недостаточностью ↓ дозу.
Побочное действие. Кашель и инфильтрация легких до потенциально смертельного фиброза. Аллергия, лихорадка, поражение слизистых, выпадение волос. Гипертрофия кожи и гиперпигментация ногтей.
Алкилирующие лекарственные средства (рис. 40.9)

Рисунок 40.9. Алкилирующие лекарственные средства
Механизм действия.Связываются с молекулами клеток. Связывание с ДНК приводит к гибели клеток.
Применение. Медленно растущие опухоли (в комбинации с другими цитостатиками).
Побочное действие. Токсичны для покоящихся и, особенно, быстро делящихся клеток.
Недостатки. 1. Устойчивость опухолевых клеток. 2. Нестабильность растворов (поэтому готовят непосредственно перед введением в вену). 3. Некроз тканей при попадании во внесосудистое пространство (мехлоретамин).
Мехлоретамин
Строение.Это азотистый иприт. [Примечание. Разработан в первую мировую войну. Боевое отравляющее вещество кожно-нарывного действия. Вызывает тяжелую лимфоцитопению. Поэтому применяют при лейкозах].
Механизм действия. Транспортируется в клетку. Связывается с азотами гуанинов, расположенных в двух спиралях ДНК. Образовавшийся комплекс:мехлоретамин– 2 молекулы гуанина “выпадает” из ДНК (депуринация). Цепи ДНК разрываются (рис. 40.10).

Рисунок 40.10. Алкилирование мехлоретаминомгуаниновых оснований ДНК раковых клеток, вызывающее их гибель
Реакции алкилирования протекают как в делящихся, так и в покоящихся клетках.
Действие.Мехлоретаминне специфичен к клеточному циклу. Пролиферирующие клетки более чувствительны, особенно вGиSфазах. [Примечание. Быстро делящиеся клетки имеют меньше времени для репарации поврежденного участка ДНК, поэтому они более чувствительны кмехлоретамину].
Устойчивость. Перекрестная устойчивость между алкилирующими лекарственными средствами. Обусловлена: 1) репарацией ДНК, 2) ↓ проникновения цитостатика в ядро клетки.
Применение. Болезнь Ходжкина как часть МОПП-схемы (М –мехлоретамин, О –онковин(винкристин), П –преднизолон, П –прокарбазин).
Фармакокинетика. Очень нестабилен. Растворы готовят непосредственно перед введением. Т1/2– несколько минут.
Побочное действие. Тяжелая рвота центрального генеза. Подавление костного мозга ограничивает широкое применение. Угнетает иммунитет. Могут развиться вирусные инфекции (например, простой герпес). Некроз тканей при попадании во внесосудистое пространство. Мутаген.
Циклофосфамид
Механизм действия. Гидроксилируется цитохромомP450. Образуется фосфорный иприт. Последний образует перекрестные сшивки со спиралями ДНК. Развивается цитотоксичность.
Устойчивость. 1. Репарация ДНК. 2. ↓ Транспорта в клетку.
Применение. Опухолевые и неопухолевые заболевания.
Опухолевые заболевания. Лимфома Баркетта, рак молочной железы и яичников, неходжкинская лимфома (отдельно или в комбинации с другими цитостатиками).
Неопухолевые заболевания. Нефротический синдром, ревматоидный артрит.
Фармакокинетика. Назначают через рот. Пролекарство. Гидроксилируется и транспортируется в ткани-мишени. Превращается в цитотоксический фосфорный иприт. Выводится с желчью и клубочковой фильтрацией.
Побочное действие. Тошнота, рвота, понос, угнетение костного мозга. Геморрагические циститы (раздражение слизистой) могут привести к фиброзу мочевого пузыря. [Примечание. Проявления цистита ↓ обильным питьем или ↑ диурезаманнитолом. Кроме того, в мочевой пузырь вводят ацетилцистеинилимесну. Они связывают токсичный метаболитциклофосфамидаакролеин].
Ломустин
Строение.Производное нитрозомочевины.
Механизм действия. Алкилирует ДНК, что приводит к ↓ ее репликации. ↓ Синтез РНК и белков. [Примечание.Ломустиналкилирует и молекулы покоящихся клеток. Однако цитотоксичен преимущественно по отношению к делящимся клеткам. Покоящиеся имеют больше времени для репарации ДНК].
Фармакокинетика.Ломустинназначают через рот. Липофилен. Проникает в ЦНС. Метаболизируется. Выводится с мочой.
Побочное действие. Метаболиты угнетают костный мозг. Возможна нефротоксичность, головокружение, атаксия.
Взаимодействие. Сфенобарбиталом. Результат – ↓ цитотоксичности в результате ↑ биотрансформации.
Стрептозоцин
Строение. Производное нитрозомочевины.
Действие. Специфически токсичен к-клеткам островков Лангерганса.
Применение. Инсулинома.
Побочное действие. Диабет, нефротоксичность.
Цисплатин
Механизм действия.См.мехлоретамин.Цисплатинсвязывается с белками иSH-группами. Цитотоксическое действие проявляться во всех стадиях клеточного цикла. Наиболее выражено вG1- иS-фазах.
Недостатки. 1. Устойчивость опухолевых клеток (репарация ДНК). 2. Не проникает через ГЭБ.
Применение. Медленно растущие опухоли: метастатическая карцинома яичек (в комбинации свинбластиномиблеомицином), карцинома яичника (в комбинации сциклофосфамидом), карцинома мочевого пузыря и легкого.
Фармакокинетика.Цисплатинвводят внутривенно в солевом растворе. 90% связывается с белками плазмы. Накапливается в печени, почках, кишечнике, яичниках. Выводится с мочой.
Побочное действие. Рвота (через 1 час после введения, до 5 дней). Дозозависимая нефротоксичность (поражаются дистальные извитые канальцы и собирательные трубочки). [Примечание. Нефротоксичность ↓ гидратацией и форсированием диурезаманнитолом]. ↓ В плазме Са++иMg++. Выпадение волос, угнетение костного мозга, ото- и нейротоксичность (парестезии, утрата тактильной чувствительности). Аллергия (покраснение кожи, анафилактический шок).
Взаимодействие.1. С радиоактивным облучением, другими цитостатиками. Результат – ↑ цитотоксичности. 2. С аминогликозидными антибиотиками. Результат – ↑ нефро- и ототоксичности.
Корбоплатин. См.цисплатин. Менее токсичен.
Аспарагиназа
Источник. Бактерии.
Биологическая роль. Дезаминирует аспарагин до аспартата.
Механизм действия. Некоторые опухолевые клетки синтезируют мало аспарагина и нуждаются в его поступлении из крови для поддержания роста и функции.Аспарагиназагидролизует аспарагин крови. Лишает опухолевые клетки аминокислоты, необходимой для синтеза белков (рис.40.11).

Рисунок 40.11. Механизм действия аспарагиназы
Недостатки.1. Устойчивость опухолевых клеток. [Примечание. Опухолевые клетки синтезируют аспарагин. Не нуждаются в его поступлении из крови]. 2. Разрушение в ЖКТ.
Применение. Острый лимфолейкоз у детей (в комбинации с винкристиномипреднизолоном).
Фармакокинетика. Разрушается в ЖКТ. Поэтому вводят в вену или мышцу.
Побочное действие. Аллергия. [Примечание.Аспарагиназа– чужеродный белок, поэтому аллергенна]. ↓ Факторов свертывания крови. Нарушения функции печени, панкреатиты. Судороги и кома.
Препараты растений (рис.40.12)

Рисунок 40.12. Препараты растений, применяемые в онкологии
Лекарственные средства, повреждающие митотическое веретено. Митотическое веретено – часть цитоскелета. Содержит микротрубочки, необходимые для разделения ДНК в две дочерние клетки.
Винкристин
Происхождение.Алкалоид барвинка.
Механизм действия.Связывается с тубулином митотического веретена. Происходит его деполимеризация. Тубулин не сокращается. Хромосомы не разделяются в 2 дочерние клетки. Митоз останавливается в метафазе. Анафаза не наступает. Клетка погибает в фазе М (рис.40.13).

Рисунок 40.13. Механизм противоопухолевого действия винкристина
Недостатки.1. Устойчивость опухолевых клеток. 2. Флебиты и целлюлиты (при попадании во внесосудистое пространство).
Устойчивость.Винкристинудаляется р-гликопротеином, который отсутствует у чувствительных к нему опухолевых клеток.
Применение. Опухоль Вилмса. Саркома мягких тканей Эвинга у детей (в комбинации с другими цитостатиками). Болезнь Ходжкина. [Примечание. Входит в МОПП-схему (см.мехлоретамин)].
Фармакокинетика. Накапливается в печени. Выводится с калом. У больных с нарушенной функцией печени или с внепеченочным холестазом ↓ дозу.
Побочное действие.Внутривенное введение приводит к массивной гибели раковых клеток. Это сопровождается высвобождением и деградацией пуринов с образованием мочевой кислоты и последующей гиперурикемией. Ее устраняют введением ингибитора ксантиноксидазыаллопуринола. Тошнота, рвота, понос. Угнетение косного мозга. Периферическая нейропатия (парестезии, снижение рефлексов, «падающая стопа» и атаксия).
Винбластин. См.винкристин.
Применение.Метастатическая карцинома яичек (сблеомициномицисплатин).
Паклитаксел
Источник. Древесина тиса.
Механизм действия. Обратимо связывается с тубулином. Вызывает гиперстабилизацию полимеризированных микротрубочек. Они не функционируют. Анафаза не поступает. Клетка погибает в фазе М (рис.40.14).

Рисунок 40.14. Механизм действия паклитаксела
Устойчивость. 1. Удаление из клетки р-гликопротеином. 2. Мутация веретена.
Применение. Рак яичника и метастатический рак молочной железы. Мелкоклеточный рак легкого, сквамозно-клеточная карцинома головы и шеи.
Фармакокинетика.Паклитакселвводят в вену 3–4 часа. Плохо проникает в ЦНС. Метаболиты выводятся с желчью. При нарушении функции печени ↓ дозу.
Побочное действие. 1. Сверхчувствительность (затрудненное дыхание, крапивница, гипотония). Поэтому предварительно назначаютдексаметазон,дифенгидрамин, Н2-блокаторы. 2. Нейтропения. Это дозолимитированная токсичностьпаклитаксела. Лечение –филграстим. 3. Периферическая нейропатия, проходящая асимптомная брадикардия, облысение, понос.
Ингибиторы топоизомеразы ДНК
Этопозид
Происхождение. Полусинтетическое производное подофиллотоксина, выделенного из корня мандрагоры.
Механизм действия.Нарушает четвертичную структуру топоизомеразы ДНК.
Действие. Тормозит клеточный цикл и пролиферацию клеток.
Применение.Моно- или комбинированная терапия при мелкоклеточном раке легкого, опухоли яичек, болезни Ходжкина, неходжинской лимфоме, остром нелимфоцитарном лейкозе.
Побочное действие.Лейко- и тромбоцитопения, анемия, тошнота, рвота, понос, ↑ температуры, облысение.
Противопоказания. Тромбоцито- и нейтропения, нарушения функции печени и почек, беременность, кормление грудью.
Гормоны, агонисты и антагонисты
Гормоны. Контролируют пролиферацию молочных желез, простаты и других тканей, содержащих их рецепторы.
В онкологии применяют: 1) агонисты и антагонисты глюкокортикоидов, 2) агонисты гонадорелина, 3) агонисты и антагонисты андрогенов, 4) эстрогены, агонисты и антагонисты, 5) агонисты прогестинов.
Агонисты и антагонисты глюкокортикоидов (рис. 40.15)

Рисунок 40.15. Агонисты и антагонисты глюкокортикоидов, применяемые в онкологии
Агонисты глюкокортикоидов
Преднизолон
История. У больных с Кушингоидным синдромом, вызванным длительным лечениемпреднизолоном, регистрировалась лимфоцитопения и ↓ массы лимфоидной ткани. Этот эффект стали использовать при лимфомах.
Механизм действия.Преднизолонсвязывается с внутриклеточным рецептором. Комплекс проникает в ядро. Связывается с ДНК. Синтезируются специфические ферменты (рис. 40.16).
Механизм лимфоцитопенического действия.Не известен. Может запускать апоптоз. Действует даже на покоящиеся клетки.
Недостатки. Устойчивость, обусловленная: 1) отсутствием рецептора, 2) ↓ сродствапреднизолонак рецептору.
Применение. Для вызывания ремиссии у больных с острым лейкозом. Астма, артрит.
Побочное действие. Кушингоидный синдром, иммунодепрессия, катаракта, остеопороз, пептическая язва желудка, ↑ АД, диабет.

Рисунок 40.16. Механизм действия преднизолона
Антагонисты глюкокортикоидов
Аминоглютетимид
Механизм действия. ↓ Синтез прегненолона в надпочечниках и эстрогенов в яичниках.
Применение. Метастатический рак молочной железы (лекарственное средство второй линии).
Фармакокинетика.Аминоглютетимидназначают через рот. Метаболизируется цитохромамиP450 до неактивных метаболитов. Ускоряет собственный метаболизм.
Побочное действие. Преходящая депрессия. Пятнисто-папулезная эритема.
Взаимодействие. Сдексаметазоном,теофиллином,дигоксином. Результат – ускорение их метаболизма.
Агонисты гонадорелина (рис. 40.17)

Рисунок 40.17. Агонисты гонадорелина, применяемые в онкологии
Действие. Кратковременное повышение, затем (через 3 недели непрерывного введения) снижение секреции фолликулостимулирующего и лютеинизирующего гормонов. Это приводит к снижению содержания половых гормонов в крови, вплоть до их полного исчезновения на период введения агонистов гонадорелина.
Применение.
Бусерелин. Гормонзависимый рак простаты, миома матки.
Гозерелин. Гормонзависимый рак простаты и молочной железы, фибромиома матки.
Лейпрорелин. Гормонзависимый рак простаты, фибромиома матки.
Трипторелин. Гормонзависимый рак простаты, миома матки, прогрессирующая карцинома яичников.
Агонисты и антагонисты андрогенов (рис. 40.18).

Рисунок. 40.18. Противоопухолевые агонисты и антагонисты андрогенов
Агонисты
Дростанолон
Строение и действие. См.тестостерон.
Применение. Метастатический рак молочной железы (у женщин с сохраненным менструальным циклом и с климаксом менее 5 лет).
Взаимодействия.С локальным γ-облучением опухолей или удалением яичников. Результат – ↑ противоопухолевого действия.
Побочное действие. Гиперкальциемия, гепатит, вирилизация.
Антагонисты андрогенов
Флутамид
Строение. Синтетический нестероидный антиандроген.
Действие.Флутамид блокирует ингибирующий эффект тестостерона на секрецию гонадотропина, вызывая ↑ в плазме лютеинизирующего гормона.
Применение. Рак простаты (в комбинации сгозерелином).
Фармакокинетика. Метаболизируется до активного гидроксипроизводного, который блокирует рецепторы андрогенов.
Побочное действие. Гинекомастия, расстройства ЖКТ.
Эстрогены, агонисты и антагонисты (рис. 40.19)

Рисунок 40.19. Эстрогены, агонисты и антагонисты, применяемые в онкологии
Эстрогены
Эстрон
Механизм действия. Конкурирует с андрогенами за рецептор. Блокирует эффекты андрогенов в андроген-зависимых опухолях простаты. ↓ Деление раковых клеток в простате.
Применение. Рак простаты, метастатическая карцинома молочной железы у женщин в период более 5-ти лет от начала климакса.
Побочное действие. Тромбоэмболия, инфаркт миокарда, кровоизлияние в головной мозг, гиперкальциемия, нарушения менструального цикла. Гинекомастия и импотенция.
Агонисты эстрогенов
Диэтилстильбестрол. См.эстрон.
Фосфэстрол
Строение. Фосфорный эфирдиэтилстильбестрола.
Применение. Рак простаты.
Фармакокинетика. Проникает в простату. Превращается вдиэтилстильбестрол.
Побочное действие. Тошнота, зуд кожи, боли в метастатических узлах, ↓ свертываемости крови, гинекомастия.
Антагонисты эстрогенов
Летрозол
Механизм действия. В период климакса в коре надпочечников и других тканях из андрогенов под действием ароматазы образуются эстрогены.Летрозол ингибирует ароматазу и блокирует биосинтез эстрогенов.
Действие. Торможение развития эстрогензависимых опухолей.
Применение. Рак молочной железы в период климакса.
Тамоксифен
Строение.Напоминаетдиэтилстильбестрол.
Механизм действия. Связывается с рецептором эстрогенов. Комплекс не активный. Синтез РНК не происходит (рис. 40.20).

Рисунок 40.20. Механизм действия тамоксифена
Действие. В результате блокирования рецепторов эстрогенов, ↓ ростстимулирующее действиетамоксифенана раковые клетки. Действие не связано с фазой клеточного цикла. Эстрогены конкурируют стамоксифен, поэтомутамоксифен не эффективен у женщин с низким уровнем эстрогенов (климакс).
Устойчивость.Обусловлена ↓: 1) сродства к рецептору, 2) количества рецепторов.
Применение. Эстрогензависимые опухоли молочной железы и матки у женщин до климакса.
Фармакокинетика. Назначают через рот. Частично метаболизируется в печени.Тамоксифени метаболиты выводятся с желчью.
Побочное действие. Напоминает климакс (приливы крови, покраснение кожи, тошнота, рвота, маточные кровотечения). Может усиливать боли, если опухоль метастазирует в кости.
Агонист прогестинов (рис. 40.21)

Рисунок 40.21. Агонист прогестинов, применяемый в онкологии
Медроксипрогестерон
Действие.См. гестагены и антиэстрогены.
Применение. Гормончувствительные злокачественные опухоли молочной железы и эндометрия у женщин в период климакса.
Цитокины
Активированные антигеном лимфоциты и моноциты выделяют белки (цитокины). Они ↑ иммунный ответ.
Классификация (рис. 40.22)
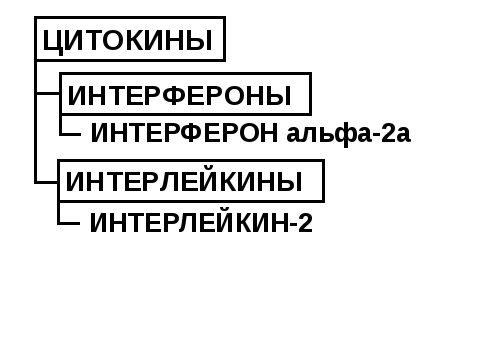
Рисунок 40.22. Противоопухолевые цитокины
Интерфероны.См. «Противовирусные лекарственные средства».
Интерферон альфа-2а
Естественный источник. Лейкоциты.
Действие. Активация макрофагов, Т-лимфоцитов, клеток-киллеров.
Применение.Хронический миелолейкоз, саркома Капоши.
Побочное действие. Лихорадка; головная, суставная, мышечная боли. Диспепсия, ↓ кроветворения, нефрит. Нарушения функций ЦНС и щитовидной железы.
Интерлейкины
Интерлейкин-2 (ронколейкин)
Естественный источник. Активированные Т-лимфоциты.
Биологическая роль.Фактор роста Т- и В-лимфоцитов. Активирует Т-лимфоциты и киллеры. ↑ Секрецию γ-интерферона.
Получение.Рекомбинантный метод (продуцируется дрожжеподобными грибками).
Применение.Метастатическая карцинома почки, меланома, саркома Капоши.
Побочное действие. Цитокиновый шок (при быстром внутривенном введении), отек легких, ↓ кроветворения, аллергия, нефротоксичность, нарушения ЦНС.
Противораковые антитела(рис. 40.23)

Рисунок 40.23. Моноклональные антитела, применяемые в онкологии
Трастузумаб
Получение.Методы генной инженерии.
Механизм действия.Блокада HER 2-рецепторов раковых клеток молочной железы.
Применение.Метастатический рак молочной железы с гиперэкспрессией HER 2-рецепторов.
Побочное действие. Лихорадка, тошнота, рвота, сыпь, головная боль, отеки, ↓ АД, бронхоспазм, кашель, лимфо- и лейкопения.
Ритуксимаб
Получение.Методы генной инженерии.
Механизм действия.Блокада CD 20 антигена мембран В-клеток неходжкинских лимфом.
Применение.Неходжкинская лимфома.
Побочное действие. См.трастузумаб+ кардиомиопатия.
Бевацизумаб
Механизм действия. Ингибирующий фактор роста эндотелия.
Действие. Подавляет прорастание сосудов в опухоль. ↓ Ее оксигенация и питание. Тормозится рост.
Применение. Колоректальный рак.
Побочное действие. Нарушение целостности стенки толстой кишки, кровотечение, замедление заживления ран. Нефротоксичность, тромбофлебиты.
Ингибиторы тирозинкиназ(рис. 40.24)

Рисунок 40.24. Ингибиторы тирозинкиназ, применяемые в онкологии
Тирозинкиназы – составная часть рецепторов факторов роста. При их ингибировании факторы роста не стимулируют пролиферацию клеток.
Иматиниб
Механизм действия. Ингибирует тирозинкиназу рецепторов: 1) тромбоцитарного фактора роста, 2) фактора стволовых клеток, 3) ВСR/ABL.
Применение.Хронический миелолейкоз, гастроинтестинальные стромальные опухоли.
Фармакокинетика.Всасывается в ЖКТ.
Побочное действие.Тошнота, рвота, отеки, нейтропения, кожная сыпь.
Гефитиниб
Механизм действия. Ингибирует тирозинкиназу рецепторов эпидермального фактора роста.
Применение. Немелкоклеточный рак легкого, рак головы и шеи.
Эрлотиниб
Применение.Немелкоклеточный рак легкого.
Сунитинаб
Механизм действия. Ингибирует тирозинкиназу рецепторов факторов роста.
Применение. Стромальные опухоли ЖКТ, светлоклеточный рак почки.
Синтетические цитостатики разных групп(рис. 40.25)

Рисунок 40.25. Синтетические цитостатики разных групп
Амсакрин
Механизм действия. Встраивается между парами оснований ДНК. С его участием образуется комплекс топоизомераза-ДНК. Спирали ДНК разрываются.
Применение.Острый миелолейкоз, лимфомы и карциномы яичников, устойчивые к другим цитостатикам.
Фармакокинетика. Метаболизируется. Т½ 8–9 часов. Кумулирует при нарушениях функции печени.
Побочное действие. Угнетение костного мозга, остановка сердца во время введения.
Гидроксимочевина
Механизм действия. Ингибирует нуклеотидредуктазу. ↓ Содержание дезоксинуклеозидтрифосфатов. ↓ Синтез ДНК.
Действие.Блокирует S-фазу клеточного цикла.
Применение. Резервный цитостатик при меланоме, хроническом миелолейкозе.
Фармакокинетика. Назначают внутрь.
Побочное действие. Угнетение костного мозга. Мегало-бластическая анемия, устойчивая кцианокобаламинуифолиевой кислоте. Тошнота, рвота, понос (при назначении ↑ доз).
Митоксантрон
Механизм действия. 1. ↓ Синтез нуклеиновых кислот. 2. Связывается с ДНК, вызывая ее разрыв.
Применение. Резистентные формы острого миелолейкоза, неходжскинская лимфома, рак молочной железы.
Фармакокинетика. Т½ 32 часа. Выводится с калом.
Побочное действие. Лейкопения, тошнота, рвота, стоматиты, аритмии.
Митотан
Происхождение.Предшественник инсектицида ДДТ (дуст).
Действие. Атрофия надпочечников. Регрессия карциномы надпочечников и ↓ чрезмерной секреции стероидов.
Применение. Карцинома коры надпочечников.
Побочное действие. Сыпь, дерматиты, анорексия, тошнота, понос, сонливость, депрессия.
Изотретиноин
Строение.13-Цис-ретиноевая кислота.
Механизм действия.Утрата раковыми клетками способности к пролиферации.
Применение. Профилактика рецидивов чешуйчато-клеточной карциномы головы и шеи (цитостатик второй линии).
Побочное действие. Поражения кожи, слизистых, скелета, печени. Тератоген.
Клеточно-трансфузионная терапия рака(рис. 40.26)
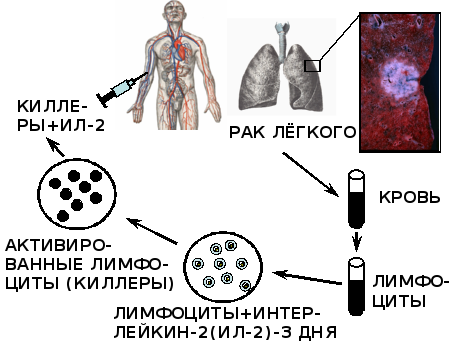
Рисунок 40.26. Клеточно-трансфузионная терапия рака
РЕЗЮМЕ (табл. 40.1)
Таблица 40.1. Применение цитостатиков
|
Цитостатики |
Применение |
|
1 |
2 |
|
Антиметаболиты | |
|
Цитарабин |
Острый миелолейкоз |
|
Меркаптопурин |
Для поддержания ремиссии у онкобольных |
|
Метотрексат |
Острый лимфолейкоз. Остеогенная саркома, хориокарцинома, лимфома Баркетта у детей. Рак молочной железы, головы и шеи |
|
Антибиотики | |
|
Дактиномицин |
Опухоль Вилмса, хориокарцинома и саркома мягких тканей |
|
Доксорубицин, даунорубицин |
Острый лимфолейкоз, болезнь Ходжкина Рак молочной железы и легкого |
|
Блеомицин |
Опухоли яичек. Сквамозно-клеточные карциномы и лимфомы |
|
1 |
2 |
|
Алкилирующие | |
|
Мехлоретамин |
Болезнь Ходжкина |
|
Циклофосфамид |
Лимфомы (Баркетта, неходжкинская). Рак молочной железы и яичников |
|
Ломустин |
Опухоли ЦНС, легких, ЖКТ, почек. Лимфогранулематоз, лимфома, лимфосаркома, меланома. Миеломная болезнь |
|
Стрептозоцин |
Инсулинома |
|
Цесплатин, карбоплатин |
Метастатическая карцинома яичек и яичников. Рак мочевого пузыря и легкого |
|
Ферменты | |
|
Аспарагиназа |
Острый лимфолейкоз у детей |
|
Препараты растений (повреждающие митатическое веретено) | |
|
Винкристин |
Опухоль Вилмса у детей. Саркома мягких тканей Эвинга. Болезнь Ходжкина |
|
Винбластин |
Метастатическая карцинома яичек |
|
Паклитаксел |
Рак яичника, молочной железы и легкого. Сквамозно-клеточная карцинома головы и шеи |
|
Препараты растений (ингибиторы топоизомеразы ДНК) | |
|
Этопозид |
Рак легкого и яичек. Болезнь Ходжкина |
|
Агонисты глюкокортикоидов | |
|
Преднизолон |
Острый лейкоз (для вызывания ремиссии) |
|
Антагонисты глюкокортикоидов | |
|
Аминоглютетимид |
Рак молочной железы (препарат второй линии) |
|
Агонисты гонадорелина | |
|
Бусерелин, гозерелин, лейпрорелин, трипторелин |
Рак простаты |
|
Агонисты андрогенов | |
|
Дростанолон |
Рак молочной железы (до климакса или с климаксом < 5 лет) |
|
Антагонисты андрогенов | |
|
Флутамид |
Метастатический рак простаты |
|
Эстрогены | |
|
Эстрон |
Рак молочной железы (с климаксом < 5 лет) и простаты |
|
Агонисты эстрогенов | |
|
Диэтилстильбестрол |
Рак молочной железы (с климаксом < 5 лет) и простаты |
|
1 |
2 |
|
Фосфэстрол |
Рак простаты |
|
Антагонисты эстрогенов | |
|
Летрозол, тамоксифен |
Эстрогензависимые опухоли молочной железы и матки |
|
Агонисты прогестинов | |
|
Медроксипрогестерон |
Прогестеронзависимые опухоли молочной железы и матки в период климакса |
|
Интерфероны | |
|
Интерферон альфа-2а |
Хронический миелолейкоз, саркома Капоши |
|
Интерлейкины | |
|
Интерлейкин-2 |
Метастатическая карцинома почки, меланома, саркома Капоши |
|
Антитела | |
|
Трастузумаб |
Метастатический рак молочной железы |
|
Ритуксимаб |
Неходжскинская лимфома |
|
Бевацизумаб |
Колоректальный рак |
|
Ингибиторы тирозинкиназ | |
|
Имитиниб |
Хронический миелолейкоз |
|
Гефитинаб, эрлотиниб |
Рак легкого |
|
Сунитинаб |
Опухоли ЖКТ, почек |
|
Синтетические | |
|
Амсакрин |
Острый миелолейкоз, лимфома, карцинома яичников |
|
Гидроксимочевина |
Хронический миелолейкоз, меланома |
|
Митоксантрон |
Острый миелолейкоз, неходжскинская лимфома, рак молочной железы |
|
Митотан |
Рак коры надпочечников |
|
Изотретиноин |
Чешуйчато-клеточная карцинома головы и шеи (для профилактики рецидивов) |
