
- •6.0929 „ Промислова біотехнологія ”
- •6.0929 „ Промислова біотехнологія ”
- •Розділ 1. Якісний аналіз
- •Якісний аналіз неорганічних катіонів
- •Лабораторна робота №1 Якісні реакції катіонів і-іі груп.
- •Контрольні питання.
- •Якісний аналіз неорганічних аніонів
- •Реакції аніонів I аналітичної групи Реакції сульфат-іонів sо42-
- •Реакції карбонат-іонів со32-
- •Реакції фосфат-іонів ро43-
- •Реакції аніонів II аналітичної групи
- •Реакції хлорид-аніонів Сl-
- •Реакції бромід-іонів Вr-
- •Реакції йодид-іонів і-
- •Реакції аніонів III аналітичної групи
- •Реакції нітрат-аніонів no3-
- •Лабораторна робота №2 Якісні реакції катіонів ііі групи. Якісні реакції аніонів
- •Контрольні питання.
- •Лабораторна робота №3 Контрольний аналіз суміші катіонів і аніонів (невідома сіль)
- •Аналіз речовини або суміші речовин невідомого складу
- •Розділ 2. Титриметричні методи аналізу
- •Кислотно-основне титрування (метод нейтралцзації)
- •Лабораторна робота № 4 Приготування розчину соляної кислоти. Визначення концентрації соляної кислоти за титрованим розчином NаОн.
- •Контрольні питання.
- •Лабораторна робота № 5 Визначення концентрації соляної кислоти за натрій тетраборатом.
- •Контрольні питання.
- •Лабораторна робота № 6 Приготування робочого розчину натрію гідроксиду з наважки та визначення його концентрації за оксалатовою кислотою. Визначення масової частки лимонної (винної) кислоти.
- •Контрольні питання.
- •Перманганатометрія
- •Лабораторна робота № 7 Приготування та стандартизація робочого розчину kMnO4
- •Контрольні питання.
- •Йодометрія
- •Лабораторна робота № 8 Приготування титрованого розчину йоду за точною наважкою хімічно чистого препарату.
- •Лабораторна робота № 9 Приготування титрованого розчину натрію тіосульфату та визначення його точної концентрації за розчином калію біхромату.
- •Контрольні питання.
- •Лабораторна робота № 10 Йодометричне визначення міді
- •Контрольні питання.
- •Комплексонометрія
- •Лабораторна робота № 11 Приготування титрованого розчину комплексону ііі
- •Контрольні питання.
- •Лабораторна робота № 12 Трилонометричне визначення цинку
- •Контрольні питання.
- •Лабораторна робота № 13 Комплексонометричне визначення загальної жорсткості води
- •Контрольні питання.
- •Розділ 3. Фізико-хімічні методи аналізу Потенціометричний метод
- •Лабораторна робота № 14 Визначення заліза в солі Мора
- •Результати титрування заліза р-ном к2Сr2o7 концентрацією 0,1 m
- •Контрольні питання.
- •Лабораторна робота № 15 Потенціометричне титрування хлорид - та йодид - іонів
- •Контрольні питання.
- •Вольтамперометричний метод аналізу
- •1. Визначення концентрації металів за рівняння м Ільковича
- •2. Визначення концентрації методом стандартних розчинів
- •3. Визначення концентрації речовини за методом калібрувального графіка
- •4. Визначення концентрацій речовин методом добавок
- •Лабораторна робота № 16 Визначення концентрації гідрохінона
- •Контрольні питання.
- •Амперметричне титрування
- •Лабораторна робота № 17 Визначення заліза ванадатом амонію
- •Контрольні питання.
- •Фотометричний метод аналізу
- •Прилади, які використовуються для фотометрії
- •Лабораторна робота № 19 Визначення заліза (III) із сульфосаліциловою кислотою диференційним методом
- •Контрольні питання.
- •Розділ 4. Використання фізико-хімічних методів в аналізі біооб’єктів Лабораторна робота № 20 Кількісне визначення вмісту білків за нінгідриновим методом
- •Контрольні питання.
- •Хроматографічні методи
- •Список літератури
1. Визначення концентрації металів за рівняння м Ільковича
Зв’язок дифузійного струму з концентрацією іону й іншими величинами виражається рівнянням Ільковича, що лежить в основі даного методу:
![]()
де n – число електронів прийнятих або відданих в процесі електродної реакції; С — концентрація визначуваної речовини, моль/л; D — коефіцієнт дифузії (см∙с-1); m - маса краплі, яка витікає з капіляра в 1 с, мг; τ — час утворення краплі, с.
Найважче
визначати D, m2/3·t1/6
– характеристика капіляра, завжди в
роботах вказується. D1/2·m2/3·t1/6
знаходять
за допомогою стандартних розчинів. При
постійних умовах D1/2·m2/3·t1/6
=const=k
![]()
2. Визначення концентрації методом стандартних розчинів
При аналізі деяких добре вивчених систем, для яких застосовують рівняння
іграндиф=К∙Сх
цілком
надійно, можна використовувати метод
стандартних розчинів. У цьому методі в
строго однакових умовах знімають
полярограми аналізованого розчину та
одного стандартного розчину того ж
елемента з точно відомою концентрацією.
Вимірюють значения
![]() ,
(або h мм) i розраховують невідому
концентрацію. Якщо:
,
(або h мм) i розраховують невідому
концентрацію. Якщо:
hCT=K·CCT, hx=K·CX,
то
![]() .
.
3. Визначення концентрації речовини за методом калібрувального графіка
При
великій кількості однотипних визначень
концентрації електровідновної речовини
дуже зручно користуватися методом
калi6pyвальної кривої. Знаючи приблизно
інтервали концентрацій, у яких може
коливатися вміст визначуваного ioнa,
готують ряд еталонних (стандартних)
розчинів з концентраціями того ж
елемента, які відрізняються одна від
одної. Знімають їx полярограми i наносять
на графік по oci ординат висоту хвиль
стандартних розчинів, а по oci абсцис
відповідні концентрації. Знявши
полярограму i визначивши
![]() -
досліджуваного розчину невідомо
концентрації (або висоту хвилі h), за
калібрувальною кривою графічно знаходять
концентрацію досліджуваного розчину
(рис.8)
-
досліджуваного розчину невідомо
концентрації (або висоту хвилі h), за
калібрувальною кривою графічно знаходять
концентрацію досліджуваного розчину
(рис.8)

а) б)
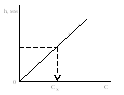
Рис. 8 Визначення концентрації Рb2+ за методом калібрувальної кривої а) — полярограми розчину свинцю (II): I - 1·10-3 н; 2 - 8·10-4 н; 3 - 6·10-4 н; 4 - 4·10-4 н; 5 - 2·10-4 н;
б) — крива залежності величини граничного струму від концентрації
4. Визначення концентрацій речовин методом добавок
Метод добавок полягає в тiм, що спочатку знімають полярограму розчину з досліджуваними іонами, потім доливають з мікробюретки розчин тих же іонів з точно відомою концентрацією, більшої приблизно в 10 або 100 разів, чим концентрація іонів у аналізованому розчині.
Оскільки концентрація стандартного розчину набагато більша концентрації аналізованого, то додаються невеликі об'єми 0,2—1 мл i зміна загального об'єму розчину при розрахунку не враховується. Знімають полярограму розчину з добавкою, а тоді просто вимірюють значення граничного дифузійного струму.
У випадку аліквотування аналізованого розчину часто поступають таким чином: беруть дві мipнi колби, однакового об'єму в які вносять однаковий об'єм аналізованого розчину i тільки в одну з них - добавку стандарту. Доводять фоновим електролітом до позначки, знімають дві полярограми, вимірюють значения висоти полярографічних хвиль hx i hx+cт, мм. Виведення загально1 формули для розрахунків засновано на рівностях:
ix=KCx
або
hx=KCx
іх+ст=К(Сх+Сст) або hx+ст=K(Cx+Cст),
де К — в умовах виконання експерименту стала величина.
Метод добавок простий у виконанні i дозволяє одержати найбільш точні результати, тому що в розчин зі стандартом вводиться аналізований розчин з усіма супутніми компонентами.
