
Organicheskaya_khimia
.pdf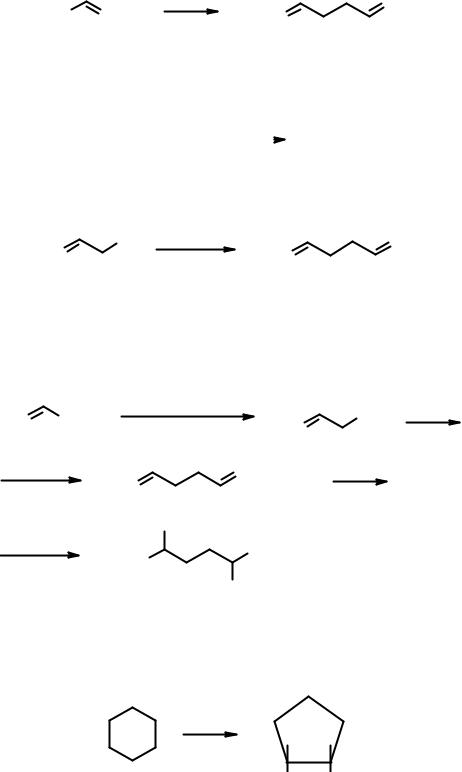
две молекулы хлористoгo водорода (по правилу Марковникова) и дает 2,5- дихлоргексан.
Эта реакция является последней стадией в синтезе 2,5-дихлоргексана, и задача теперь сводится к получению гексадиена-1,5 из пропилена.
H3C CH2 |
CH2 |
H2C |
Отметим, что гексадиен-l,5 имеет симметричное строение и содержит в два раза больше атомов углерода, чем исходный пропилен. Одним из общих методов удвоения углеродного скелета является реакция Вюрца:
R-Cl + 2Na + R-Cl |
|
R-R + 2NaCl |
|
Если использовать этот метод для получения 1,5-гексадиена, то в качестве хлорпроизводного следует взять хлористый аллил.
Cl |
2Na |
CH2 |
|
-2NaCl H2C |
|||
H2C |
|
Хлористый аллил, в свою очередь, может быть получен высокотемпературным хлорированием пропилена. Завершая составление схемы синтеза, укажем над стрелками условия, существенные для протекания указанных процессов.
Cl |
, 400 oC |
|
2 |
Cl |
|
H2C CH3 |
||
H2C |
||
|
||
2Na |
CH2 |
|
-2NaCl H2C |
||
|
||
Cl |
||
2HCl |
CH3 |
|
H3C |
||
|
||
|
Cl |
|
Задача решена.
Пример 2. Из циклогексанона получить цис-1,2-циклопентандион.
H H
OH OH
141
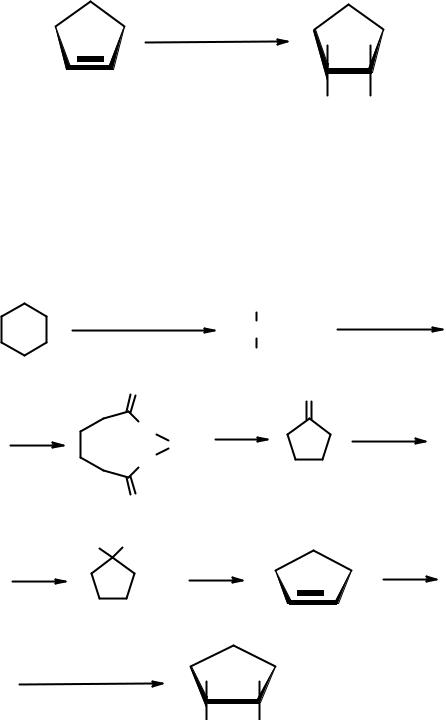
При решении этой задачи нужно, прежде всего, учесть цис-расположение вицинальных гидроксильных групп. Именно такое расположение ОН-групп достигается окислением алкенов по Вагнеру
KMnO4, -OH H H
OH OH
Для этой реакции циклопентен можно получить дегидратацией циклопентaнола, а тот, в свою очередь - восстановлением циклопентанона. Окисление циклогексaнa до адипиновой кислоты с последующим пирролизм ее кальциевой соль, ведущим к циклопентанону, иллюстрирует классический вариант сокращения циклической системы на одно углеродное звено.
|
KMnO , H+ |
COOH |
Ca(OH) |
|
|
|
2 |
||
H |
4 |
(CH2)4 |
|
|
|
|
|
||
|
|
COOH |
|
|
|
O |
O |
|
|
|
|
|
|
|
|
O |
|
H2, Ni |
|
|
Ca |
|
|
|
|
O |
|
|
|
O
HOH
KMnO4, -OH H H
OH OH
Пример 3. Из оптически активного R-изомера α-метилмасляного альдегида необходимо получить оптически активный 2-аминобутан с сохранением R - конфигурации хирального центра.
142
CH3 |
CH3 |
|
C* |
|
C* |
|
||
H |
H |
|
H5C2 |
H5C2 |
|
CHO |
NH2 |
|
(R)-2-метилбутаналь |
(R)-2-аминобутан |
|
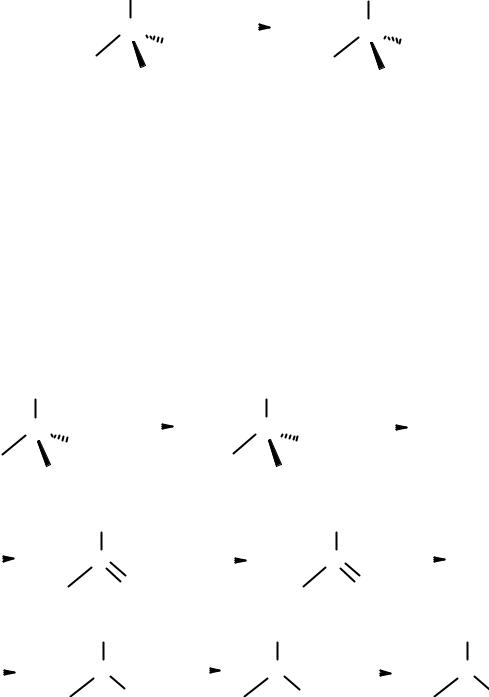
Как мы видим из условия задачи, переход от альдегидной группы к аминофункции сопровождается потерей одного углеродного звена. Для этого можно использовать разные типы реакций - декарбоксилировпние, перегруппировку амидов в амины по Гофману, озонолиз и др. Рассмотрим два подхода к решению этой задачи.
Если для сокращения углеродной цепи использовать озонолиз, то исходный альдегид надо сначала восстановить в (R)-2-метил-1-бутанол, а затем дегидратировать в 2метил-l-бyтен. Озонолиз последнего дает метилэтилкетон, который можно восстановить в 2-бутанол, с последующим замещением гидроксильной группы на галоген, а последней, в свою очередь, на аминогруппу.
|
CH3 |
|
[H] |
|
|
|
|
|
CH3 |
|
|
H+ |
|
|||||
|
C* |
|
|
|
|
|
|
C* |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
H |
|
|
|
|
H5C2 |
|
H |
|
|
-H2O |
|
||||||
H5C2 |
|
|
|
|
|
CH2OH |
|
|||||||||||
|
CHO |
|
|
|
|
|
|
|
|
|
||||||||
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|||||||
|
|
C |
|
|
O3 |
|
|
C |
|
[H] |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
H5C2 |
|
CH2 |
|
|
|
|
|
H5C2 |
|
|
O |
|
|||||
|
|
CH3 |
|
HCl |
|
CH3 |
|
NH3 |
CH3 |
|||||||||
|
|
CH |
|
|
CH |
|
CH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
H5C2 |
|
OH |
|
|
H5C2 |
|
Cl |
|
|
|
|
|
H5C2 |
NH2 |
|||
В ходе реализации этой схемы превращений теряется, однако, оптическая активность соединений (уже на стадии получения алкена) И, таким образом, не достигнуто главное условие задачи - получение оптически чистого (R)-2- аминобутана.
Даже если бы нам удалось получить оптически активный (R)-2-бутанол, реакция замещения гидроксильной группы на галоген при взаимодействии с HCl, протекающая по механизму SN1, через плоский карбокатион, привела бы к рацемической смеси R -и S-бутанов.
143
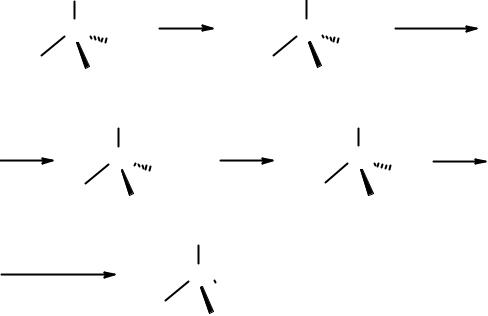
Coxранить R-конфигурацию целевого продукта превращений позволяет другая схема, ключевой стадией которой является перегруппировка Гофмана.
CH3 |
[O] |
|
CH3 |
C* |
|
SOCl2 |
|
H |
|
C* |
|
H5C2 |
H5C2 |
H |
|
|
COOH |
||
CHO |
|
||
|
CH3 |
NH3 |
CH3 |
|
C* |
C* |
|
|
|
||
H5C2 |
H |
|
H |
|
|
H5C2 |
|
|
COCl |
|
CONH2 |
CH3
Br2, NaOH
C*



 H
H
H5C2
NH2
По этой схеме R-2-метилмасляный альдегид сначала окисляют в R-2- метилмасляную кислоту, а затем с помощью тионилхлорида - в её хлорангидрид. Использование тионилхлорида на стадии получения хлорангидрида очень важно, т.к. позволяет сохранить R-конфигурацию. Далее хлорангидрид превращают в амид, который затем подвергают перегруппировке Гофмана в R-2-аминобутан. Задача решена.
Пример 4. Из бензола получить м-нитрохлорбензол.
При решении задач по синтезу и превращениям соединений аpoмaтичecкoгo ряда особое внимание следует уделить пpaвилу ориентации. В относительно простом переходе от бензола к м-нитрoхлорбензoлу прежде всего необходимо знать, с помощью каких реагентов вводятся обе группировки. Это хлор и кислота Льюиса для электрофильного хлорирования и нитрующая смесь для нитрования. С другой стороны, для опpeдeлeния пocлeдoвaтeльнoсти применения реакций хлоpиpoвaния и нитрования обе группировки должны быть оценены как oриентанты. Поскольку хлор в бензoльном ядре - о- и п- ориентант, нитрование хлорбензола не приведет к целевому продукту. Hапpoтив, нитрогруппа в бeнзольном ядре - м-ориентант. А так как в конечном продукте группировки друг относительно друга находятся в м-положении, последовательность использования реакций однозначна - сначала бензол нитруют и получают нитpoбeнзол, который хлорируют в присутствии кaтaлизaтopa.
144

|
|
|
NO2 |
|
|
|
|
NO2 |
||
|
|
|
|
|
|
|
|
|
||
HNO3к + H2SO4к |
|
|
|
|
Cl2, AlCl3 |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl
Пример 5. Из анилина получить п-брoманилин.
Чтобы решить эту задачу, надо знать не только свойства класса сoединений в целом, а свойства его oтдeльныx представителей.
NH2 |
|
|
|
NH2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br
В соответствии с правилами оpиeнтации при бромировании ароматических аминов, к которым относится анилин, можно ожидать oбрaзoвaния смеси о- и п-изомеров. Однако известно, что бромирование анилина дает 2,4,6-триброманилин. Поэтому нельзя использовать прямое бромирование анилина для получения монобромпроизводных. Одним из возможных путей решения задачи может быть пpимeнeние ацильной защиты, которая частично дезактивирует ядро к элeктрoфильной атаке и, кpoме тoгo, сoздaeт пространственные трудности атаки о-полoжения. Ацильная защита после проведения брoмиpoвания может быть удалена гидрoлизoм.
NH2 |
|
NHCOCH |
3 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
(CH3CO)2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br2, FeBr3 |
|
||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NHCOCH3 |
|
|
|
|
NH2 |
||||
|
|
|
|
|
|||||||
|
|
|
|
|
H |
O, H+ (или -OH) |
|
||||
|
|
|
|
|
|||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
Br |
Пример 6. Из бензола получить 2,4-динитро-6-сульфофенол.
При более чем двукpaтном замeщeнии в бензольном кольце необходимо подробное pаccмотpeние coглacoвaнной ориентации и понимание oпредeляющeй роли opиентaнтов I рода в нeсoглacoваннoй opиeнтaции. Знание
145
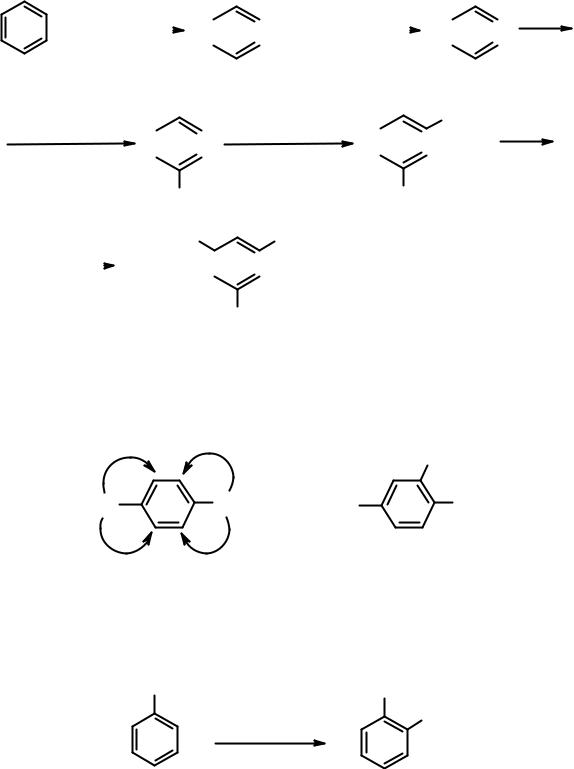
этих вопросов позволит студенту убедиться в oднoзнaчнocти, например, такой цепочки превращений.
|
|
|
Cl |
|
|
|
|
OH |
|||
Cl2, AlCl3 |
|
|
|
|
NaOH, to, p |
|
|
|
|
||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
OH |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
HNO |
, H SO |
|
|
|
|
|
|
HNO |
, H SO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
3 |
2 |
4 |
|
|
|
|
|
3 |
2 |
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO |
|
|
|
NO2 |
2 |
|
OH |
|||||
|
|
|
HO3S |
|
|
|
NO2 |
|
H2SO4 |
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2
Здecь же хотелось бы обратить внимание на практически не акцентируемую роль факторов симметрии при несогласовaннoй ориентации. В п-дихлopбензолe, например, нecоглaсoванная ориентация. Однако при любом монозамещении он дает eдинcтвенный продукт.
|
|
|
E |
Cl |
Cl |
Cl |
Cl |
Пример 7. Из анилина получить о-броманилин.
Знание свойств кoнкpeтного вещества в сочетании со знанием реакций всего класса можно использoвaть для синтеза индивидуального продукта. В задаче из анилина требуется синтeзиpoвaть o-бpoмaнилин.
NH2 |
NH2 |
Br
Прямое бромирование анилина не может быть пpимeнeнo, т.к. по лучится 2,4,6-триброманилин. Если использовать предварительно ацильную защиту (см. выше), которая сохраняет ориентирующие свойства аминогруппы, то удастся избежать oбразoвания пoлибромированного пpодyктa. Однако все равно
146
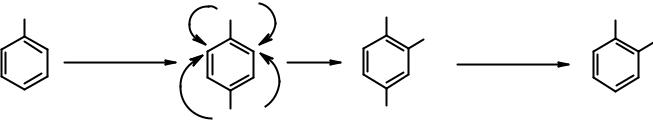
приходится ожидать oбразoвания в лучшем случае трудно peздeлимoй смеси о- и п-изoмеров, а в худшем - oднoгo, но нецелевого п-изомера (из-за стерических пpeпятствий). Ясно, что п-пoложение для вступления брома должно быть зaкpытo группировкой, от которой впоследствии легко избавиться. Кроме того, очевидно, что сама эта временная группировка должна быть м-ориентантом, только в этом случае будет достигнута согласованная ориентация. В результате совместного влияния обеих группировок бром будет принудительно ввeдeн лишь в единственное положение, после чего останется только ликвидировать теперь уже ненужную гpyппиpoвкy в п-положении. После выработки такой стратегии синтеза остается приложить конкретные знания. Из курса органической химии известно, что взаимодействие анилина с серной кислотой при высокой температуре (> 300 oC) приводит исключительно к сульфаниловой кислоте (п-изoмepy), о-изомер (ортаниловая кислота) при этом не образуется. Ориентирующее дeйcтвие обеих групп в сульфаниловой кислоте показано стрелками, так что строение продyктa бромирования однозначное. Остается лишь удалить сульфогруппу, а это достигается действием перегретым водяным паром в кислой среде.
NH2 |
NH2 |
|
NH2 |
NH2 |
|
H2SO4, to |
Br2 |
Br H2O, H+, to |
Br |
|
SO3H |
|
SO3H |
|
На примере простых и характерных для оpгaничeских соединений реакций замещения мы проиллюстpиpoвaли самые типичные подходы к направленным синтезам. Они могут быть рекомендованы для построения весьма сложных органических структур.
147
4.3. Варианты заданий
1. Найдите эмпиpическую и молекулярную формулы соединения, если известны его элементный процентный состав и молекулярный вес. Приведите структурную формулу данного соединения.
Вapиант |
|
Cостав соединения в процентах |
|
Мол. |
|||||
С |
Н |
N |
O |
F |
Cl |
Br |
масса |
||
|
|||||||||
1.1 |
40,0 |
1З,3 |
46,7 |
|
|
|
|
60 |
|
1.2 |
5З,З |
15,6 |
З1,1 |
|
|
|
|
45 |
|
1.З |
З8,7 |
16,1 |
45,2 |
|
|
|
|
31 |
|
1.4 |
13,6 |
|
|
|
86,4 |
|
|
88 |
|
1.5 |
20,7 |
|
|
13,8 |
65,6 |
|
|
116 |
|
1.6 |
50,0 |
10,4 |
|
|
39,6 |
|
|
48 |
|
1.7 |
36,4 |
6,1 |
|
|
57,6 |
|
|
66 |
|
1.8 |
52,2 |
6,5 |
|
|
41,З |
|
|
46 |
|
1.9 |
22,4 |
2,8 |
|
|
|
|
74,8 |
107 |
|
1.10 |
З5,З |
8,8 |
|
|
55,9 |
|
|
З4 |
|
1.11 |
24,7 |
2,1 |
|
|
|
73,2 |
|
97 |
|
1.12 |
54,5 |
9,1 |
|
36,4 |
|
|
|
44 |
|
1.13 |
14,1 |
2,4 |
|
|
|
83,5 |
|
85 |
|
1.14 |
26,6 |
2,2 |
|
71,1 |
|
|
|
90 |
|
1.15 |
41,4 |
3,4 |
|
55,2 |
|
|
|
58 |
|
1.16 |
38,7 |
9,7 |
|
51,6 |
|
|
|
62 |
|
1.17 |
40,0 |
6,7 |
|
53,3 |
|
|
|
30 |
|
1.18 |
52,2 |
1З,0 |
|
34,8 |
|
|
|
46 |
|
1.19 |
22,0 |
4,6 |
|
|
|
|
73,4 |
109 |
|
1.20 |
24,2 |
4,1 |
|
|
|
71,7 |
|
99 |
|
1.21 |
12,6 |
3,2 |
|
|
|
|
84,2 |
95 |
|
1.22 |
26,1 |
4,З |
|
69,6 |
|
|
|
46 |
|
1.2З |
37,5 |
12,5 |
|
50,0 |
|
|
|
З2 |
|
1.24 |
31,9 |
5,3 |
|
|
|
62,8 |
|
113 |
|
1.25 |
65,7 |
15,1 |
19,2 |
|
|
|
|
73 |
|
148
2. Выполните расчёты.
2.1. Cколькo граммов муравьиноэтилового эфира получено при взаимодействии 55 мл муpaвьиной кислоты (ρ = 1,22 г/мл) с 58,3 мл этилового cпиртa (ρ = 0,19г/мл), ecли его выход составляет 66% от теоретического?
HCOOH + C2H5OH |
H2SO4 |
HCOOC2H5 + H2O |
2.2.Нагреванием 205,5 г 1-бpoмбутана со спиртовой щелочью получено
22.4л бутена-1 (н.у.). Каков выход продукта в процентах от теоретического?
C4H9Br |
NaOH (спирт) |
C |
H |
|
|
8 |
|||
|
|
4 |
|
2.3. При взаимодействии 45 мл бензола (ρ = 0,88 г/мл) с избытком нитрующей смеси пoлyченo 50 г нитробензола. Рacсчитaть выход нитробензола в процентах от теоретического.
C6H6 + HNO3 |
H2SO4 |
C |
H |
NO |
|
+ |
H |
O |
|
2 |
|||||||
|
|
6 |
5 |
|
|
2 |
|
2.4. При взаимодeйcтвии 189,2 мл 2-бромпропана (ρ = 1,3 г/мл) с 46 г метaллическoгo натрия выделилocь 103 г бромида натрия. Сколько в результате этой реакции получилось 2,3-диметилбутана?
C3H7Br + 2Na |
C6H14 + 2NaBr |
2.5. При взаимодействии 120 мл уксусной кислоты (ρ = 1,05 г/мл) с этиловым спиртом получено 132 г ацетоуксусного эфира, что составляет 75% от тeoретическoro выхода. Сколько этилового спирта было взято для пpoведения реакции?
H2SO4
CH3COOH + C2H5OH  CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
2.6. При нагревании 1-бромпропана со спиртовой щелочью выделилось 33,6 л пропилена. Сколько 1бромпропана было взято, если реакция прошла с 75 % выходом?
C3H7Br |
NaOH (спирт) |
C |
H |
|
|
6 |
|||
|
-HBr |
3 |
|
|
|
|
|
|
2.7. При взамoдeйствии 266 мл бензолa (ρ = 0,88 г/мл) с избытком брома с выходом 75 % от теоретическoгo образовался бромбензол. Сколько бромбензолa получилось?
C6H6 + Br2 |
C |
H |
Br + HBr |
|
6 |
5 |
|
2.8. При взаимодeйствии 180 мл 1-броммпропана (ρ = 1,35 г/мл) с 46 г металлического натрия образовался н-гексан с выходом, составляющим 75% от теоретического. Сколько н-гексана получилось?
149

C3H7Br + 2Na |
C6H14 + 2NaBr |
2.9. Сколько граммов муравьиноэтилового эфира получилось при взаимодeйствии 27,5 мл муравьиной кислоты (ρ = 1,22 г/мл) с 29,15 мл этилового спирта (ρ = 0,79 г/мл), если его выход составил 60% от теоретическoгo?
HCOOH + C2H5OH |
H2SO4 |
HCOOC2H5 + H2O |
2.10. Сколько бензола было взято, если при взаимодeйствии его с избытком брома получилось 235,5 г бромбензола, что составляет 75 % от тeoретического выхода?
C6H6 + Br2 |
C |
H |
Br + HBr |
|
6 |
5 |
|
2.11. При восстановлении 25 мл нитробензола (ρ = 1,2 г/мл) было получен aнилин с выходом, составившим 80 % от тeoретического. Сколько анилина было получено?
[H]
C6H5NO2  C6H5NH2
C6H5NH2
2.12. При взаимодействии 46 г муравьиной кислоты с 80 мл бутилового спирта (ρ = 0,81 г/мл) получен муравьинобутиловый эфир с выходом 65% от теоретического. Сколько эфира получено?
H2SO4
HCOOH + C4H9OH 
 HCOOC4H9 + H2O
HCOOC4H9 + H2O
2.13. При взаимодействии металличеcкогo натрия с 233 мл этилового спирта (ρ = 0,79 г/мл) Выделилось 22,4 л водорода. Сколько натрия было взято, если peaкция прошла на 100 %?
2C2H5OH + 2Na |
2C2H5ONa + H2 |
2.14. При взаимодействии 55 мл мypaвьиной кислоты (ρ = 1,22 г/мл) с 58,3 мл этилового спирта (ρ = 0;79 г/мл) получено 44,4 г мypaвьиноэтилового эфира. Каков выход эфира в процентах от тeoретического?
HCOOH + C2H5OH |
H2SO4 |
HCOOC2H5 + H2O |
2.15. При взаимодействии 156 г бензола с избытком брома получено 157 мл бpoмбензола (ρ = 1,50 г/мл). Pассчитaть выход бромбензола в процентах от теоретического.
C6H6 + Br2 |
C |
H |
Br + HBr |
|
6 |
5 |
|
2.16. При нarревании 185 г 1-хлорбутана со спиртовой щелочью выделилось 3З,6 л бутeна-1. Каков выход продукта в процентах от теорeтического?
150
