
- •Таврійський державний агротехнологічний університет
- •Змістовий модуль I. Неорганічна хімія
- •Тема 5. Гідроген. Хімія лужних металів. Хімія лужно - земельних елементів.
- •Змістовий модуль іі. Фізична та колоїдна хімія
- •Тема 14. Дисперсні системи та їх класифікація.
- •Тема 15. Мікрогетерогенні системи.
- •Тема 16. Напівколоїди та розчини високомолекулярних сполук.
- •Розподіл балів, що присвоюються студентам
- •Техніка безпеки та правила роботи в хімічній лабораторії Вимоги безпеки перед початком роботи
- •Вимоги безпеки під час роботи
- •Вимоги безпеки після закінчення роботи
- •Вимоги безпеки в аварійних ситуаціях
- •Розділ і. Неорганічна хімія Лабораторна робота №1. Класи неорганічних сполук
- •Вимоги до знань та умінь
- •Теоретична частина
- •Оксиди.
- •Кислоти.
- •Основи.
- •Амфоліти.
- •Паспорт роботи
- •Експериментальна частина Техніка безпеки.
- •Контрольні питання
- •Теоретична частина
- •Паспорт роботи
- •Результати оформлення роботи
- •Контрольні питання
- •Теоретична частина
- •Паспорт роботи
- •Результати оформлення роботи
- •Контрольні питання
- •ТермоХімія. Мета роботи – навчитися експериментально визначати ентальпію хімічних реакцій і робити розрахунки, використовуючи термохімічні рівняння.
- •Фактори, що визначають напрямок хімічних реакцій.
- •Паспорт роботи.
- •Експериментальна частина
- •Хід роботи.
- •Результати. Оформлення роботи.
- •Контрольні питання.
- •Рекомендована література
- •Лабораторна робота №5. Кінетика та швидкість хімічних реакцій
- •Вимоги до знань та умінь
- •Теоретична частина
- •Хімічна рівновага
- •Паспорт роботи
- •Експеріментальна частина
- •Контрольні питання
- •Рекомендована література
- •Лабораторна робота №6. Періодична система та періодичний закон д.І. Менделєєва
- •Вимоги до знань та умінь
- •Теоретична частина
- •Періодична система і будова атома.
- •Контрольні питання
- •Лабораторна робота №7. Властивості гідрогену та його сполук
- •Теоретична частина
- •Проста речовина
- •Практична частина Одержання та властивості Гідрогену. Окисно-відновні властивості Гідрогену.
- •Контрольні питання
- •Лабораторна робота №8. Властивості лужних металів.
- •Теоретична частина
- •Практична частина Властивості лужних металів та їх сполук.
- •Контрольні питання
- •Лабораторна робота №9. Властивості лужноземельних металів.
- •Теоретична частина
- •Практична частина Властивості лужноземельних металів та їх сполук
- •Контрольні питання
- •Елементи іv – а групи
- •Властивості Алюмінію, Карбону, Силіцію, Стануму, Плюмбуму та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 8 Властивості Нітрогену, фосфору та їх сполук.
- •Контрольні питання
- •Галогени
- •Практична частина Властивості р-елементів та її сполук.
- •Контрольні питання
- •Лабораторна робота №13. Загальна характеристика d-елементів
- •Теоретична частина
- •Практична частина
- •Контрольні питання
- •Лабораторна робота №14. Тема: комплексні сполуки
- •Експериментальна робота Комплексні сполуки та їх властивості.
- •Контрольні питання
- •Контрольні питання:
- •Задачі:
- •Лабораторна робота № 16. Розчини неелектролітів
- •Способи вираження складу розчину
- •Тиск насиченого пару розведених розчинів
- •Температура замерзання розбавлених розчинів
- •Температура кипіння розведених розчинів
- •Осмотичний тиск
- •Контрольні питання:
- •Задачі:
- •Лабораторна робота № 17. Розчини електролітів
- •Роль розчинника в процесі дисоціації
- •Стан сильних електролітів у розчинах. Коефіцієнт активності
- •Дисоціація слабких електролітів
- •Рівновага в насичених розчинах електролітів
- •Реакція обміну в розчинах електролітів. Іонні рівняння
- •Контрольні питання:
- •Задачі:
- •Лабораторна робота № 18. Розчини електролітів
- •Гідроліз солей
- •Контрольні питання:
- •Задачі:
- •Лабораторна робота № 19. Поверхневі явища та адсорбційні рівноваги
- •Контрольні питання:
- •Задачі:
- •Лабораторна робота № 20. Дисперсні систем та їх класифікація
- •Методи визначення молекулярної маси високомолекулярних сполук.
- •Середня молекулярна маса
- •Контрольні питання:
- •Список літератури
Дисоціація слабких електролітів
Слабкі електроліти, на відміну від сильних, дисоціюють на іони зворотно, між молекулами та іонами встановлюється рівновага, стан якої характеризується константою дисоціації (константа рівноваги). Наприклад, для оцтової кислоти:
СН3СООН ⇄ Н+ + СН3СОО-
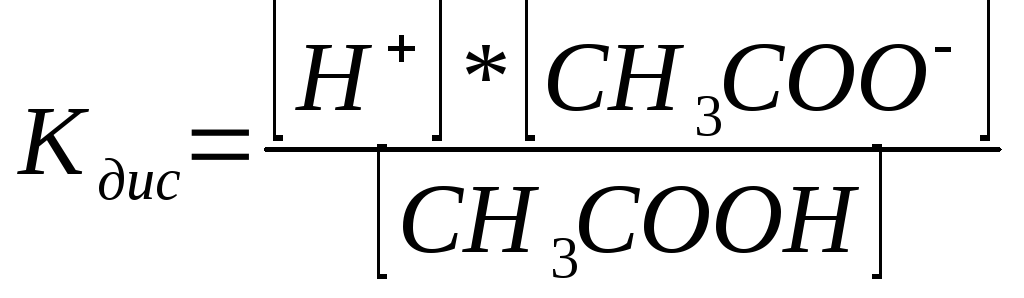 (8)
(8)
Значення
константи дисоціації можна зв'язати з
величиною ступеня
дисоціації а,
який відповідає відношенню концентрації
дисоційованих
молекул до вихідної (аналітичної)
концентрації
![]() .
Концентрацію кислоти, що розпалась на
іони, можна
виразити співвідношенням: [Н+
] = [СН3СОО-]
= α*С . Рівноважна
концентрація недисоційованих молекул
дорівнює С
- α*С.
Підставивши ці значення у вираз для
константи рівноваги
(8), дістанемо рівняння, яке називається
законом
розбавлення:
.
Концентрацію кислоти, що розпалась на
іони, можна
виразити співвідношенням: [Н+
] = [СН3СОО-]
= α*С . Рівноважна
концентрація недисоційованих молекул
дорівнює С
- α*С.
Підставивши ці значення у вираз для
константи рівноваги
(8), дістанемо рівняння, яке називається
законом
розбавлення:
![]() (9)
(9)
Під час розбавлення концентрація оцтової кислоти в розчині зменшується. Відповідно до принципу Ле Шательє рівновага в системі зсувається так, щоб послабити зменшення кількості розчинених частинок. Збільшенню числа частинок у розчині сприяє процес дисоціації (1 молекула СН3СООН —> 2 іони), і α зростає. Але це збільшення відбувається так, що константа дисоціації залишається сталою, оскільки вона не залежить від концентрації.
Рівновага процесу дисоціації зміщується й тоді, коли в розчин вводити надлишок одного з іонів, що утворюються в результаті дисоціації (такі іони називають однойменними). Так, якщо до розчину оцтової кислоти додати розчинної у воді солі цієї кислоти, наприклад СН3СООNа, остання повністю дисоціює на іони:
СН3СОONа = СН3СОO- + Na+,
підвищуючи концентрацію ацетат-іонів СН3СОО- у розчині. Згідно з принципом ле Шательє рівновага дисоціації оцтової кислоти зміститься так, щоб послабити зростання концентрації цих іонів у розчині, тобто в бік утворення вихідної речовини - оцтової кислоти. Ступінь дисоціації кислоти при цьому зменшиться. Отже, збільшення [СН3СОО-] призводить до зміни концентрацій усіх частинок у розчині: зменшення [Н+], збільшення [СН3СООН], але так, щоб значення константи дисоціації залишалося незмінним.
Таким чином, за сталої температури константа дисоціації слабкого електроліту є сталою величиною і може використовуватись для характеристики сили такого електроліту, а ступінь дисоціації - для характеристики стану рівноваги в системі.
Зміна температури впливає як на значення констант дисоціації так і ступенів дисоціації слабких електролітів, але її вплив найчастіше є не дуже значним.
Слабкі електроліти, з однієї молекули яких внаслідок дисоціації утворюється більш ніж два іони, дисоціюють ступінчасто, і кожному ступеню відповідає своє значення константи дисоціації, наприклад:
H2S
⇄
H+
+HS-
![]()
HS-
⇄
H+
S2-
![]()
Перший ступінь дисоціації є значно більшим від наступних, тобто К1>К2. Спрощено це можна пояснити тим, що катіон Н+ на другій стадії долає сильніше притягання двозарядного аніона S2-, ніж однозарядного НS- на першій стадії. Оскільки ступені дисоціації окремих стадій процесу суттєво різняться між собою, їх не об'єднують в загальне рівняння:
Н2S ⇄ 2Н+ + S2-
Проте іноді для розрахунків використовують загальну константу дисоціації, яка дорівнює добуткові констант окремих стадій:
Кдис=
К1*К2=
![]() *
*![]() =
=
![]()
Ступінчасто дисоціюють також кислі та основні солі. Так, кисла сіль - гідрокарбонат натрію подібно до середніх солей повністю дисоціює на катіон металу та аніон кислотного залишку:
NаНСО3 = Na+ + НСО3-,
наступна ж стадія дисоціації залишку слабкої кислоти іде зворотно і в тій мірі, в якій дисоціює карбонатна кислота за другим ступенем:
НСО3- = Н+ + СО32-
Аналогічно відбувається дисоціація основних солей.
