
Материаловедение
.pdf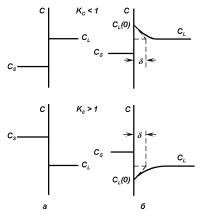
5.2. Коэффициент разделения примесей |
201 |
Рис. 5.6. Схематическое изображение распределения примесей на границе раздела твердой и жидкой фаз при различных условиях кристаллизации: а — в равновесных условиях; б — в неравновесных условиях.
AIIВVI, AIVBVI. В этом случае на первый план выходят не методы очистки соединения, а методы, позволяющие приблизить состав кристалла к стехиометрическому (например, отжиг при фиксированном парциальном давлении более летучего компонента, см. гл. 4). Синтез разлагающихся соединений проводят либо в запаянных кварцевых ампулах при контролируемом давлении паров летучего компонента в рабочем объеме, либо под слоем жидкого флюса (например, особо чистый обезвоженный борный ангидрид). Синтез соединений, имеющих большое давление паров летучего компонента над расплавом, осуществляется в камерах высокого давления.
5.2.2. Эффективный коэффициент разделения примесей
До сих пор мы рассматривали равновесные коэффициенты разделения, рассчитываемые из фазовых диаграмм или получаемые методом, основанным на измерении концентрации свободных носителей в легированных полупроводниках. И в том, и в другом методах коэффициент разделения определялся в условиях, близких к равновесным. Эти условия, как правило, выполняются при достаточно малых скоростях кристаллизации расплава. В этом случае концентрация примеси CL, растворенной в расплаве, одинакова во всем его объеме (рис. 5.6,а), а ее концентрация в закристаллизовавшейся части CS = K0CL.
202Глава 5. Получение чистых полупроводниковых материалов
Вреальных условиях фронт кристаллизации движется со скоростью большей, чем скорость диффузии примесей в расплаве. Пусть для определенности K0 < 1. Тогда по мере роста кристалла со скоростью V за счет того, что твердая фаза содержит меньше примеси, чем исходный расплав, из которого она образуется, концентрация примеси в расплаве у границы раздела возрастает. Накопление избытка примеси, выделяющейся у движущегося фронта кристаллизации, приводит к образованию перед ним диффузионного слоя δ, из которого примесь путем диффузии переходит в объем расплава (рис. 5.6,б). Если же равновесный коэффициент разделения примеси K0 > 1, то вблизи поверхности роста ощущается недостаток примеси. В стационарном режиме роста кристалла должен существовать поток примесного компонента от границы роста в глубь расплава, если К0 < 1, или к ней, если К0 > 1. В этих условиях содержание примеси в закристаллизовавшейся части кристалла CS определяется концентрацией примеси в расплаве у фронта кристаллизации CL(0). Так как CL(0), как правило, неизвестна, то в этих неравновесных условиях связь между концентрациями примеси в твердой CS и жидкой CL фазах определяется с помощью эффективного коэффициента разделения K:
K = CS/CL, |
(5.5) |
где CL — средняя концентрация примеси в расплаве.
Найдем связь между эффективным K и равновесным K0 коэффициентами разделения примеси. Для этого необходимо найти зависимость, описывающую распределение концентрации примеси в расплаве перед движущемся фронтом кристаллизации. Математически распределение примеси в системе кристалл–расплав описывается дифференциальным уравнением массообмена в движущейся среде:
/ τ = |
w |
grad C + D |
|
2C, |
(5.6) |
dC d |
− · |
|
|
|
где w — скорость движения расплава, D — коэффициент диффузии, τ —
время. Без ущерба для общности решение поставленной задачи можно
получить, решив это уравнение для одного направления, перпендикулярного границе раздела кристалл–расплав. Пусть начало координат совпадает с границей раздела кристалл–расплав, а положительное направление соответствует движению в глубь расплава. В этом случае уравнение примет вид:
dC/dτ = −wxdC(x)/dx + Dd2C(x)/dx2. |
(5.7) |
Пусть D = const в диффузионном слое, а режим роста кристалла установившийся, то есть dC/dτ = 0. Тогда уравнение (5.7) примет вид:
Dd2C/dx2 − wxdC/dx = 0. |
(5.8) |

5.2. Коэффициент разделения примесей |
203 |
Пусть в пределах слоя δ скорость движения расплава wx равна скорости роста кристалла V, то есть wx = −V; концентрация примеси в твердой фазе равна CS, а в глубине жидкой фазы (при x > δ) CL — средней концентрации примеси в расплаве; CL(0) — концентрация примеси в расплаве на границе раздела фаз при x = 0. Граничные условия определяют из равенства потоков примеси, подводимого к границе раздела фаз за счет оттеснения ее из твердой фазы и отводимого от нее вследствие диффузии. Таким образом,
V[CL(0) − CS] + DdC/dx = 0 |
при x = 0, |
(5.9) |
C = CL |
при x = δ. |
|
Решение уравнения (5.8) с граничными условиями (5.9) при x = 0
имеет вид: |
|
|
D |
|
|
CL − CS |
|
||||
CL(0) |
− CS |
= exp |
Vδ |
. |
(5.10) |
|
|
|
|||
Вводя равновесный K0 = CS/CL(0) и эффективный K = CS/CL коэффициенты разделения и обозначая Vδ/D = ∆, получим уравнение, связывающее их между собой:
|
K0 |
|
K(V) = |
K0 + (1 − K0) exp(−∆). |
(5.11) |
Как видно, значение K зависит от скорости выращивания кристалла V, а также от значения δ и коэффициента диффузии примеси в расплаве D. Величина D для большинства систем полупроводник–примесь (в расплаве) лежит в диапазоне 10−5–10−4 см2/с, а значение δ может меняться от 1 до 10−3 см в зависимости от условий выращивания; V обычно выбирают ≈1–3 мм/ч.
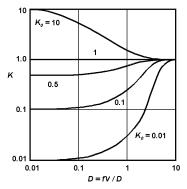
∆ — безразмерная величина, называемая приведенной скоростью кристаллизации. На рис. 5.7 представлен график зависимости K от ∆ для разных K0. Видно, что увеличение приведенной скорости кристаллизации ∆ смещает K в сторону 1 независимо от значения равновесного коэффициента разделения K0. И, наоборот, уменьшение ∆ приближает
K к K0.
Ясно, что для повышения эффективности процесса очистки необходимо предельно приблизить значение K к K0, что может быть достигнуто уменьшением скорости кристаллизации. Того же эффекта можно достичь, проводя очистку кристаллизацией в условиях интенсивного перемешивания жидкой фазы. В этом случае отвод примеси от фронта кристаллизации (при K0 < 1) в основном осуществляется не за счет диффузии в жидкой фазе, а за счет конвекции, что существенно уменьшает
204 Глава 5. Получение чистых полупроводниковых материалов
Рис. 5.7. Зависимости эффективного коэффициента разделения примесей K от приведенной скорости роста ∆ = Vδ/D [37].
содержание примеси у фронта кристаллизации по сравнению с ее содержанием, получаемым без перемешивания, и уменьшает K, приближая его к K0.
5.3.Методы и принципиальные возможности очистки кристаллизацией
Рассмотрим сущность основных методов очистки кристаллизацией. Для того, чтобы обеспечить получение материала с предельной степенью чистоты кристаллизационными методами необходимо, чтобы кристаллизация начиналась в заданном месте и происходила в определенном направлении, то есть необходимо создать четкую границу между твердой и жидкой фазами и обеспечить ее медленное и равномерное движение вдоль очищаемого слитка. Эти условия достигаются заданием градиента температуры, обеспечивающего направленный отвод тепла и направленное продвижение фронта кристаллизации. При этом, в зависимости от значений K, примесь будет или «захватываться» твердой фазой (K > 1), освобождая от нее расплав, или оттесняться от границы раздела в расплав (K < 1). В первом случае части слитка, затвердевающие позже, будут чище предыдущих; во втором случае наиболее чистой оказывается начальная часть слитка. При рассмотрении процессов очистки кристаллов, выращиваемых из расплава, все многообразие методов выращивания кристаллов направленной кристаллизацией можно свести к двум идеализированным схемам: нормальной направленной кристаллизации и зонной плавке. В частности, первой схемой описывается процесс очистки кристаллов, выращиваемых широко используемым в промыш-
5.3. Методы кристаллизационной очистки |
205 |
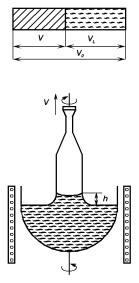
Рис. 5.8. Схема выращивания кристалла методом нормальной направленной кристаллизации.
Рис. 5.9. Схема выращивания кристалла методом вытягивания из расплава.
ленной практике методом вытягивания кристаллов из расплава.
Вметоде нормальной направленной кристаллизации вещество расплавляют в тигле заданной формы, который затем медленно охлаждают с одного конца, осуществляя отсюда направленную кристаллизацию (рис. 5.8).
Вметоде вытягивания кристаллов из расплава в расплав опускают затравку в виде небольшого монокристалла, которую затем непрерывно перемещают вверх. Затравка увлекает за собой жидкий столбик, который, попадая в зону более низкой температуры, непрерывно кристаллизуется. Схема этого метода показана на рис. 5.9 (более подробно см. гл. 6).
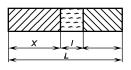
При зонной плавке в слитке вещества расплавляют только небольшую зону, которую перемещают вдоль образца. По мере ее направленного продвижения впереди зоны происходит плавление вещества, а позади — его кристаллизация (рис. 5.10).
Степень чистоты вещества и распределение примеси вдоль кристалла
вкаждой из идеализированных схем различаются и являются характеристиками схемы. В настоящее время зонная плавка стала одним из наиболее распространенных кристаллизационных методов, применяемых для глубокой очистки многих материалов.
Используя основные законы фазовых превращений в многокомпонент-
206 Глава 5. Получение чистых полупроводниковых материалов
Рис. 5.10. Схема выращивания кристалла методом зонной плавки.
ных системах, выведем аналитические выражения для распределения концентрации остаточной примеси в твердой фазе в методах нормальной направленной кристаллизации и зонной плавки. Рассмотрим наиболее распространенный случай — бинарную систему (полупроводник — примесь) при небольшой концентрации примеси. Достаточно четкое и надежное математическое описание распределения примеси при направленной кристаллизации бинарной системы может быть получено только в некотором приближении.
Пусть:
1. Процессами диффузионного перераспределения компонентов в твердой фазе можно пренебречь, то есть коэффициент диффузии компонентов в твердой фазе
DS = 0. |
(5.12) |
2. Перераспределение компонентов и соответственно выравнивание состава в жидкой фазе происходит мгновенно, то есть коэффициент диффузии в жидкой фазе
DL = ∞. |
(5.13) |
Это условие обычно называют условием полного перемешивания жидкой фазы.
3. Значение эффективного коэффициента разделения постоянно, то есть
K = const. |
(5.14) |
Это допущение справедливо в области малых концентраций примеси, когда K не зависит от концентрации примеси. Кроме того, так как K зависит и от скорости роста кристалла (уравнение (5.11)), то условие K = const также подразумевает постоянство скорости роста кристалла на протяжении всего процесса:
V = const. |
(5.15) |
4. При плавлении и затвердевании объем кристаллизуемого материала не изменяется, то есть плотности жидкой и твердой фаз равны:
ρL = ρS = ρ. |
(5.16) |

5.3. Методы кристаллизационной очистки |
207 |
5. В системе нет летучих и диссоциирующих компонентов. Рассмотрим в рамках сделанных предположений распределение при-
меси в кристалле, выращиваемом разными методами.
5.3.1.Распределение примесей при нормальной направленной кристаллизации
Этой схемой описывается распределение примесей в кристаллах, выращенных методом нормальной направленной кристаллизации и методом вытягивания из расплава.
Пусть в некоторый момент времени объем расплава составляет VL (рис. 5.8), а CL и CS — концентрации примесного компонента в расплаве и кристалле соответственно. Для определенности пусть K < 1. Так как слиток вначале расплавлен весь, то его состав вследствие перемешивания усредняется и равен исходной концентрации примеси в жидкой фазе C0. Пусть при понижении температуры закристаллизовался объем расплава, равный dVL. Тогда количество примесного компонента, перешедшего из расплава в кристалл, составит CSdVL. В жидкой фазе при этом останется избыточное по отношению к начальному количество примесного компонента (CL − CS)dVL. Оно приведет к изменению концентрации примеси в расплаве:
( |
) = |
− |
CL(VL) − CS(VL) |
dVL |
. |
(5.17) |
|
VL |
|||||||
dCL VL |
|
|
|
Опуская аргумент у функций CS и CL и учитывая, что K = CS/CL, получаем
dCL |
= |
− |
CL − KCL |
dVL |
= |
− |
(1 − K)CL |
dVL |
. |
(5.18) |
|
VL |
VL |
||||||||||
|
|
|
|
Знак минус перед дробью означает, что при уменьшении объема расплава концентрация примесного элемента в нем увеличивается. Интегрирование проводится при начальных условиях:
CS|VL=V0 = KCL|VL=V0 = KC0, |
(5.19) |
где V0 — общий объем материала.
Разделим в выражении (5.18) переменные и проинтегрируем его:
VL |
1 |
CS /K |
|
|
||
|
dVL |
dCL |
|
|
||
0 |
|
|
0(K 1) |
|
|
|
− |
VL |
= 1−K |
CL |
, |
(5.20) |
|
V |
|
|
|
C |
|
|
CS = KC0(VL/V0) − .
208 Глава 5. Получение чистых полупроводниковых материалов
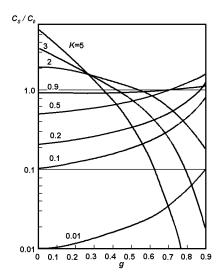
Рис. 5.11. Распределение относительной концентрации примеси с различными значениями K по длине кристаллов, выращенных нормальной направленной кристаллизацией (L — длина слитка) [37].
Переходя теперь от доли расплава VL/V0, остающейся жидкой в момент кристаллизации слоя состава CS(VL), к доле вещества g, закристаллизовавшейся к этому моменту,
g = 1 −VL/V0, |
(5.21) |
получим |
|
CS(g)/C0 = K(1 − g)(K−1). |
(5.22) |
Эта зависимость для различных K представлена на рис. 5.11. Видно, что специфика очистки с помощью метода нормальной направленной кристаллизации заключается в перемещении примеси в тот или другой конец слитка. Максимальная степень очистки имеет место в начале (K < 1) или конце (K > 1) слитка. Заметим, что при K < 1 CS(g)/C0 по мере приближения g к 1 неограниченно возрастает, то есть как бы ни была мала концентрация примеси в расплаве C0 в начале, концентрация ее в конечных частях кристалла согласно (5.22) должна быть безгранично большой, что противоречит физическому смыслу. Это противоречие является следствием нарушения допущения, что K = const, в конечных частях кристалла и поэтому выражение (5.22) не справедливо для этих частей кристалла.
Недостаток этого метода — его принципиальная однократность. Чтобы очистить материал более чем в K раз, необходимо удалить загрязнен-
5.3. Методы кристаллизационной очистки |
209 |
ную часть слитка и только тогда повторить цикл снова. Но любые манипуляции с материалом являются источниками его поверхностного загрязнения. Для повышения эффективности очистки необходимо проведение многократной направленной кристаллизации без какого-либо взаимодействия материала с внешней средой. Эта цель достигается с помощью метода зонной плавки.
5.3.2. Распределение примесей при зонной плавке
При зонной плавке в начале слитка из очищаемого материала с помощью специального нагревателя (например, катушки высокочастотного нагрева) создается узкая расплавленная зона, которая затем движется вдоль слитка. Схема расположения зоны в произвольной части слитка показана на рис. 5.10. Расплавленная зона заключена между двумя твердыми частями кристалла: уже затвердевшей и еще не расплавленной. Проходя по слитку, она «вбирает» в себя примесь (при K < 1), перенося ее к концу. Принципиальным отличием зонной плавки от нормальной направленной кристаллизации является то, что доведенная до конца слитка зона может быть «перекинута» в его начало, где при повторном ее проходе она контактирует с уже предварительно очищенными участками, извлекая из них оставшиеся примеси и продолжая таким образом очистку материала.
Пусть при количественном рассмотрении распределения примеси в твердой фазе в случае зонной плавки остаются в силе все допущения, в которых получена формула (5.22), и пусть длина зоны l в течение всего времени проведения процесса остается постоянной: l = const.
Следует отметить, что поскольку при зонной плавке весь образец сразу не плавят, то его состав не усредняется. Поэтому распределение примеси в кристалле после зонной плавки в отличие от нормальной направленной кристаллизации должно зависеть от вида исходного распределения примеси в заготовке.
Рассмотрим распределение примеси в кристалле после первого прохода зоны через слиток с длиной L, постоянной площадью сечения S и первоначальным равномерным распределением примеси C0 по нему. Пусть зона находится на расстоянии x от начала слитка (рис. 5.10). Положение зоны будем определять по границе ее затвердевания. Концентрация примеси в расплавленной зоне — CL(x). Рассмотрим баланс примеси в зоне в процессе ее движения.
Если зона сдвинется на расстояние dx, то из расплава у фронта кристаллизации в кристалл перейдет количество примеси, равное
dML = KCL(x)S dx. |
(5.23) |
210 Глава 5. Получение чистых полупроводниковых материалов
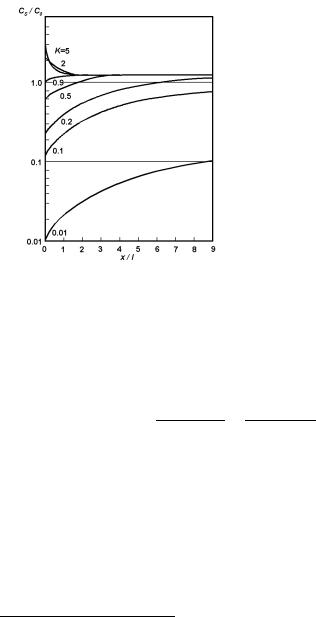
Рис. 5.12. Распределение относительной концентрации примеси с различными значениями K по длине кристаллов, выращенных зонной плавкой, после первого прохода зоны [37].
У другого края зоны, где произошло расплавление слоя исходного слитка, в зону поступит количество примеси, равное
dML = C0S dx. |
(5.24) |
Тогда изменение концентрации примеси в расплавленной зоне при ее перемещении на dx будет
( |
) = |
dML |
− dML |
= |
C0 − KCL(x) |
. |
(5.25) |
|||
|
||||||||||
dCL |
x |
lS |
|
|
l |
dx |
|
|||
|
|
|
|
|
|
|
||||
Концентрация примеси в начальном положении зоны |
|
|
||||||||
|
CL(0) = l 0 |
l |
|
|
|
(5.26) |
||||
|
C0(x) dx = C0. |
|
||||||||
|
|
|
|
1 |
|
|
|
|
|
|
Интегрирование выражения (5.25) с учетом начальных условий (5.26) дает:
CS(x) = C0[1 − (1 − K) exp(−Kx/l)]. |
(5.27) |
Эта зависимость в приведенных координатах для различных K представлена на рис. 5.12 (в приведенных координатах2 вид кривой относительной концентрации CS(x)/C0 не зависит от длины зоны). Как видно
2В приведенных координатах расстояние от начала образца измеряется в единицах длины расплавленной зоны x/l.
