
- •Раздел 1 общеприкладная медицинская микробиология микробиология как наука
- •История развития микробиологии
- •Систематика и номенклатура микроорганизмов
- •Микроскопические методы исследования микроскопы и способы микроскопии
- •Методы приготовления мазков–препаратов из материала (культур) и способы их окрашивания
- •Морфология и ультраструктура прокариот эубактерии
- •Патогенные спирохеты
- •Актиномицеты
- •Риккетсии
- •Микоплазмы
- •Физиология микроорганизмов
- •Выделение чистых культур бактерий
- •Выделение и изучение культуральных свойств бактерий–аэробов
- •Особенности выделения и изучения культуральных свойств бактерий–анаэробов
- •Действие физических, химических и биологических факторов на микроорганизмы
- •Бактериофаги (фаги)
- •Стерилизация
- •Инфекция
- •Механизмы неспецифической резистентности
- •Антигены как индукторы приобретенного антимикробного иммунитета
- •Органы иммунитета и иммунокомпетентные клетки
- •Антитела (иммуноглобулины)
- •Процесс антителообразования
- •Аллергия (гиперчувствительность)
- •Патогенез и характер проявления анафилаксии и инфекционной аллергии
- •Иммунопрофилактика и иммунотерапия вакцины
- •Иммунные сыворотки (гамма–глобулины)
- •Серологические реакции иммунитета
- •Реакция агглютинации
- •Реакция преципитации
- •Реакция связывания комплемента
- •Реакция иммунофлюоресценции
- •Реакция торможения гемагглютинации
- •Раздел 2 инфекционная микробиология возбудители бактериальных инфекций пиогенные кокки
- •Общая характеристика патогенных энтеробактерий и вызываемых ими кишечных инфекций
- •Эшерихии
- •Возбудители брюшного тифа и паратифов а и в
- •Возбудители сальмонеллезов
- •Возбудители дизентерии
- •Холерный вибрион
- •Коринебактерии дифтерии
- •Возбудители туберкулеза и микобактериозов
- •Возбудитель сифилиса
- •Возбудители вирусных инфекций общая характеристика вирусов
- •Вирусы гриппа
- •Вирусы парагриппа
- •Аденовирусы
- •Вирусы гепатита
- •Спид и спид–ассоциированные инфекции
- •Возбудители протозойных болезней плазмодии малярии
- •Токсоплазмы
- •Трихомонады
- •Лямблии
- •Приложение устройство, оснащение и правила работы в микробиологических лабораториях
Механизмы неспецифической резистентности
Антиинфекционная резистентность организмов вырабатывалась в процессе длительной эволюции и является свойством всей популяции вида однотипно реагировать на внедрение микроорганизмов, используя для их подавления естественно–физиологические факторы антиинфекционной защиты широкого спектра действия.
Тканевые факторы. Среди тканевых факторов антиинфекционной защиты главную роль играют ареактивность клеток, кожа, слизистые оболочки, лимфатические узлы как иммунологические барьеры, фагоциты и нормальные киллеры.
Видовая ареактивность клеток к патогенным микробам и токсинам обусловлена генотипом, который детерминирует образование на поверхности клеток соответствующих рецепторов. При их отсутствии адсорбция и проникновение инфекционного агента или яда в клетку будут невозможны. Генотипическая ареактивность может быть связана также с дефицитом необходимых для микроба веществ или, например, избирательной специфичностью действия микробных ферментов. Клеточная ареактивность является очень стабильным видовым признаком, но может изменяться под действием различных факторов окружающей среды. Так, Л. Пастер показал наличие ареактивности кур к сибиреязвенной инфекции, но при погружении их лапок в ледяную воду и резком охлаждении организма зараженные птицы заболевают. В другом классическом опыте И. И. Мечникова была отмечена природная нечувствительность лягушек, черепах, ящериц к столбнячному токсину. Развитие столбняка у пойкилотермных животных достигалось помещением их в термостат и повышением температуры тела.
Кожные покровы и слизистые оболочки обеспечивают невосприимчивость как механические барьеры и вследствие выделения антимикробных веществ широкого диапазона действия (ферментов, кислот, специфических ингибиторов).
Мощным естественным барьером являются лимфатические узлы. Проникшие в них патогенные бактерии вызывают воспалительный процесс, сопровождающийся освобождением из тканей биологически активных веществ, под влиянием которых происходит активация лейкоцитов, скапливающихся вокруг патогенных микробов и препятствующих их распространению в кровоток, подлежащие ткани и внутренние органы. Наряду с этим в очаге воспаления активируется фагоцитарная реакция.
Рис. 26
Незавершённый фагоцитоз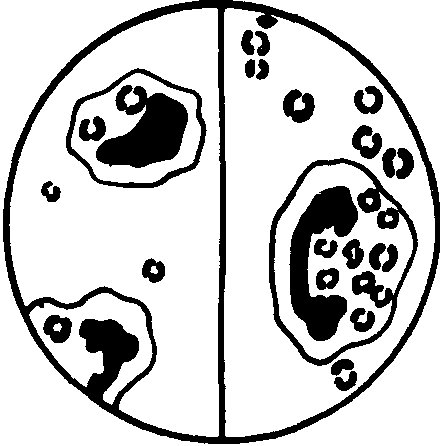
Фагоцитарная реакция осуществляется поэтапно. При завершенном фагоцитозе, заканчивающемся разрушением микроба, различают четыре стадии: 1) приближение фагоцита к микробу (положительный хемотаксис); 2) прилипание фагоцита к микробу; 3) впячивание наружной мембраны фагоцита с последующим образованием фагосомы и ее слияние с лизосомой; 4) инактивация и ферментативное расщепление микроба в фаголизосоме, проявляющиеся набуханием, фрагментацией и лизисом с полной деградацией до аминокислот и низкомолекулярных соединений. Некоторые виды микроорганизмов, особенно вирусы, проявляют большую устойчивость к лизосомным ферментам или даже размножаются внутри фагоцитов (рис. 26). Такой незавершенный вид фагоцитоза чаще наблюдается в нейтрофилах и заканчивается их гибелью или выталкиванием микробов.
В разрушении микробов, проникших в клетки, активное участие принимают нормальные киллеры (англ. killer – убийца). Это большие лимфоциты с относительно рыхлым почковидным крупным ядром и обильной цитоплазмой, в которой содержится большое количество цитотоксических веществ. На их внешней мембране имеются специфические рецепторы, благодаря которым нормальные киллеры узнают инфицированные вирусом или опухолеродные клетки. Связываясь с ними, нормальные киллеры активируются и выбрасывают содержимое своих гранул, которое разрушает их.
Гуморальные факторы. Гуморальные факторы иммунитета, обеспечивающие неспецифическую резистентность организма, очень многочисленны. Большинство из них обладает антимикробной активностью. Концентрация их в крови и лимфе здоровых людей небольшая, но при инфицировании может резко возрастать. Обладают широким спектром действия. Природа гуморальных факторов многообразна, но, как правило, они являются полипептидами. Механизм антимикробного действия многосторонний. Вырабатываются разнообразными клетками, главным образом Т–лимфоцитами и макрофагами.
Среди гуморальных факторов антиинфекционной защиты основное значение придают комплементу, пропердину, лизоциму, нормальным антителам, интерферонам I типа.
Комплемент. Структурно сформированного комплемента (лат. сотр1етеп1ит – дополнение) как гуморального фактора иммунитета в организме здоровых людей и животных нет. В их крови циркулируют различные фракции комплемента, обозначаемые символами С1, С2, СЗ...С9, В и др. Находясь в дискретном (разобщенном) состоянии, они являются инертными белками – предшественниками комплемента. Сборка (активация) фракций комплемента в единое целое происходит при внедрении в организм болезнетворных микробов. Сформировавшись, комплемент способен лизировать клетки (бактерии, эритроциты) или чаще просто элиминировать генетически чужеродную метку, повышая бактерицидную активность сыворотки крови. О содержании в ней комплемента судят по его гемолитической активности в отношении эритроцитов барана, обработанных сывороткой кролика, содержащей антитела гемолизины. Титр комплемента выражают в минимальном количестве сыворотки, которое в нормальных условиях лизирует 100 % или 50 % оптимально сенсибилизированных гемолизинами эритроцитов.
Содержание комплемента в сыворотках сильно колеблется в зависимости от вида и возраста животных, сезона и даже времени суток. Наиболее постоянный и высокий его титр регистрируется у морских свинок, поэтому именно их сыворотка используется как комплемент для постановки реакции связывания комплемента. У здоровых людей уровень комплемента варьирует незначительно, но у больных может резко повышаться или снижаться.
Система комплемента очень лабильна. Его инактивация происходит в течение 2–4 дней даже при надежном хранении сывороток (5°С). Быстро разрушается комплемент при УФ–облучении, действии солнечного света, протеаз, слабых растворов кислот и щелочей. Исчезает комплементарная активность сывороток после их прогревания при температуре 56 °С в течение 29–30 мин.
Пропердин. Защитный белок, состоящий из пяти компонентов. Три из них специфические, а два остальных являются фракциями комплемента. Совместно действуя с комплементом, этот защитный белок тоже разрушает бактерии, усиливает фагоцитарную реакцию и воспалительный процесс.
Лизоцим. Фермент с молекулярной массой около 15 000, нарушающий синтез оболочек бактерий. При частичной утрате оболочек бактерии превращаются в сферопласты, при полной – в протопласты. Те и другие быстро погибают или же лизируются. Основным источником лизоцима в крови являются макрофаги.
Нормальные антитела. В сыворотке крови новорожденных могут содержаться антитела к различным видам микроорганизмов. По структуре они ничем не отличаются от иммунных, т. е. приобретенных в процессе инфекции.. Идентичны с ними и по механизму взаимодействия с микробами, т. е. реагируют по закону строгой специфичности. Нормальные антитела экспрессируются на поверхностных мембранах незрелых В–лимфоцитов в виде рецепторов. Будучи цитофильными, в крови новорожденных они обнаруживаются в очень низких титрах, как правило, в цельной сыворотке.
Интерфероны (ИНФ) I типа. Это низкомолекулярные белки, содержащие небольшое количество углеводов (англ. interfere – препятствую размножению). Различают две серологические группы ИНФ I типа – и . –ИНФ – это семейство 20 полипептидов с молекулярной массой около 18 кД; –ИНФ – гликопротеин с молекулярной массой 20 кД. Отличаясь по структуре, они обладают одинаковым механизмом действия. В норме –ИНФ продуцируется мононуклеарными фагоцитами, а –ИНФ –фибробластами. Под воздействием инфекционного начала секретируются многими клетками и в месте входных ворот инфекции концентрация ИНФ I типа в считанные часы многократно возрастает. Его защитное действие в отношении вирусов сводится к ингибированию репликации РНК или ДНК. Связавшийся со здоровыми клетками ИНФ I типа защищает их от проникновения вирусов.
Факторы саморегуляции. В основе антиинфекционного иммунитета лежит также способность организма к саморегуляции. Эта форма иммунитета прежде всего проявляется обычным повышением температуры тела, губительно сказывающимся на жизнедеятельности многих бактерий и особенно вирусов в результате непосредственного влияния или изменения окислительно–восстановительного потенциала и рН пораженных тканей. Большое значение в обеспечении естественного иммунитета имеет выведение микробов и токсинов с мокротой, испражнениями, мочой и другими секретами и экскретами при усилении выделительных функций различных органов и систем. Эти и другие, еще не учтенные факторы и механизмы общефизиологического характера находятся под регулирующим влиянием нейрогуморальных и гормональных функций организма.
