
- •1. Характеристика предмета коллоидной химии
- •1.1 Признаки объектов коллоидной химии
- •1.2 Количественные характеристики дисперсных систем
- •1.3 Энергетическая и геометрические характеристики поверхности
- •1.4 Классификация дисперсных систем
- •1.5 Методы получения коллоидных систем
- •1.6. Правило фаз Гиббса для дисперсных систем
- •2. Поверхностное натяжение
- •2.1 Термодинамические параметры поверхностного слоя
- •2.2 Экспериментальные методы определения поверхностного натяжения.
- •2.3 Внутренняя полная поверхностная энергия.
- •2.4 Температурная зависимость σ и полной внутренней поверхностной энергии.
- •2.5 Механизм процессов самопроизвольного уменьшения σ. Принцип Гиббса-Кюри.
- •2.6 Внутреннее давление. Уравнение Лапласа
- •2.7 Влияние дисперсности на реакционную способность
- •2.8 Влияние дисперсности на растворимость вещества
- •2.9 Влияние дисперсности на равновесие химической реакции.
- •2.10 Влияние дисперсности на температуру фазовых переходов.
- •2.11 Уравнение капиллярной конденсации
- •3. Термодинамика образования новой фазы.
- •3.1 Кинетика образования новой фазы в системе “ж – т”.
- •3.2 Управление степенью дисперсности.
- •4. Двойной электрический слой. Механизм его образования.
- •4.1 Строение дэс
- •4.2 Примеры д.Э.С. И строение мицеллы
- •4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
- •5. Адсорбция. Зависимость от параметров системы
- •5.1 Типы адсорбции
- •5.2 Ионный обмен
- •5.3 Фундаментальные адсорбционные уравнения Гиббса
- •5.4 Адсорбция на границе ж-г
- •5.5 Уравнение Шишковского
- •5.6 Изотерма адсорбции Ленгмюра
- •5.7 Многокомпонентная адсорбция из газовой фазы.
- •5.8 Учет неэквивалентности адсорбционных центров
- •5.9. Капиллярные явления. Формула Жюрена
- •5.10 Адсорбция на пористых телах.
- •5.11 Адсорбция на микропористых телах.
- •5.12 Селективная адсорбция из растворов
- •6. Электрокинетические явления
- •6.1 Электроосмос
- •6.2 Электрофорез
- •7. Адгезия. Механизм процессов адгезии
- •7.1 Смачивание. Краевой угол
- •7.2 Связь работы адгезии с краевым углом
- •7.3 Эффект Марагони.
- •7.4 Правило Антонова
- •8. Флотация
- •9. Рассеяние света ультромикрогетерогенными частицами
- •10. Устойчивость дисперсных систем.
- •10.1 Седиментационная устойчивость дисперсных систем
- •10.2 Седиментационный анализ.
- •I метод.
- •10.3 Механические методы седиментации
- •10.4 Агрегативная устойчивость дисперсных систем
- •10.5 Кинетика коагуляции.
- •10.6 Коагуляция золей электролитами
- •10.7 Условие термодинамической устойчивости дисперсных систем
- •11. Эмульсии. Их стабилизация и разрушение.
- •12. Пены, стабилизация и разрушение.
- •13. Аэрозоли. Устойчивость и разрушение.
- •14. Суспензии. Обеспечение их устойчивости.
- •15. Гели
- •16. Экспериментальные методы изучения поверхностей.
4.1 Строение дэс
Представление о строение ДЭС за сто лет истории претерпели изменения
Квинки сделал предположения об его образовании. Гельмгольц и Перрен представляли его строение по аналогии со строением плоского конденсатора. Предполагалось, что на границе прикасающихся фаз заряды располагаются в виде двух рядов разноимённых ионов. Толщина слоя считалась близкой к размерам молекул или сольватированных ионов на этом расстоянии φ уменьшалась до 0. Поверхностный заряд определяется в соответствии с теорией плоского конденсатора.
Гюи (Франц)
Однако , такое строение возможно без учёта теплового движения ионов.
Независимо друг от друга Гюи и Чепмен предположили строение ДЭС с учётом теплового движения. По их мнению все противоионы будут рядом с потенцио определяющим ионами только при 279 К. При более высоких температурах из-за кинетической энергии ионов они располагаются не упорядочено, образуя размытую диффузную структуру Отто Штерн (нем). – нобелевская премия.
Современная теория строения ДЭС предложена Штерном. Она объединяет обе предыдущие теории: слой противоионов состоит из двух частей: в близи поверхности есть адсорбционный слой Гельмгольца, Толщиной δ не более диаметра гидратированных ионов; далее находится диффузный слой Гюи, толщиной λ с потенциалом φδ , зависящих от свойств и состава системы. Т.к. противоионы в диффузной части распределены неравномерно, φ его изменяется не линейно
qДЭС = qδ + qλ , где qδ и qλ – заряды на межфазной поверхности и границе слоя Гельмгольца. В свою очередь: qδ= qэлектростатич.вз.+ qковалент.св. из-за наличия различных адсорбционных центров.
Гуи и Чепмен предположили, что в диффузной части ионы в результате теплового движения распределяются в соответствии с законом Больцмана. В результате было в ведено уравнение, определяющее связь ДЭС с расстояние от поверхности (уравнение Гуи-Чепмена).
При φд.э.с.<<25мВ
φх=φδе-х/λ, при х=λ, φх=φδ/е,
т.е. за толщину дифференциальной части д.э.с. берется расстояние на котором φ уменьшается в «е» раз (2,718 раз).
Каково же это
расстояние? Так симметрично одновалентного
элемента при его концентрациях 10-1,
10-3,
10-5
моль/л, λ=1,10,100 нм, т.е.
![]() ,
т.е. много больше диаметра ионов.
На
λ оказывают влияние состав раствора,
Т, ε (они его повышают), z
(понижает).
,
т.е. много больше диаметра ионов.
На
λ оказывают влияние состав раствора,
Т, ε (они его повышают), z
(понижает).
Полная электрическая
емкость д.э.с. выражается как суммарная
емкость двух последовательно соединенных
конденсаторов
![]() ,
,
В разбавленных растворах сδ>>cλ, отсюда ссλ, т.к. δ<<λ.
4.2 Примеры д.Э.С. И строение мицеллы
Система AgJ – вода (избыток AgNO3)
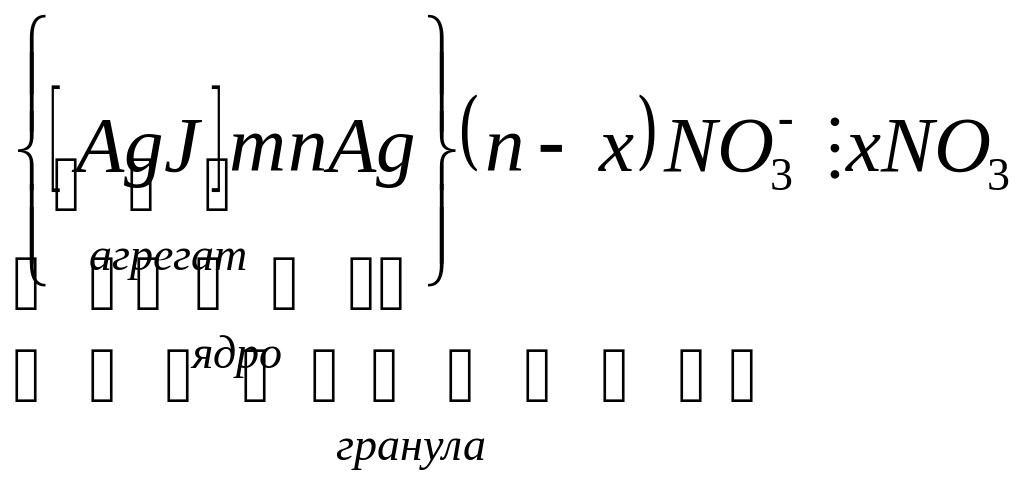 -
-![]() мицелла
мицелла
систем AgJ-вода (избыток KJ)
![]()
Для амфотерных веществ заряд поверхности может изменяться в зависимости от pH среды. В этом случае потенциалопределяющими ионами могут быть либо OH-, либо H+.
4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
Образование д.э.с. происходит самопроизвольно в результате стремления системы уменьшить энергию поверхностного слоя. Избыточная поверхностная энергия при образовании д.э.с. превращается в электрическую. Из объединенного уравнения I и II начал т.д. имеем:
![]() ,
при
T, p, ni
– const
,
при
T, p, ni
– const
Полный дифференциал энергии Гиббса
![]()
вычитая из него первое уравнение имеем
![]() или
или
![]() - 1 уравнение Липмана.
- 1 уравнение Липмана.
Оно определяет связи между q, φ, σ д.э.с.
Если знаки qs и φ совпадают, то с увеличением φ σ уменьшается
![]()
Если знаки qs и φ различны, то с увеличением φ σ увеличивается.
При малом значении qs σ слабо зависит от φ.
В реальных системах,
стремящихся к равновесию, знаки qs
и φ
совпадают, а значит уменьшение σ
сопровождается увеличением φ. Емкость
конденсатора
![]() .
Считая д.э.с. конденсатором и подставив
в это уравнение значение q
из 1 уравнения Липмана
.
Считая д.э.с. конденсатором и подставив
в это уравнение значение q
из 1 уравнения Липмана
![]() - 2 уравнение
Липмана.
- 2 уравнение
Липмана.
Оно позволяет определить с, зная зависимость σ от φ.
4.4 Уравнение электрокапиллярной кривой.
Название связано
с прибором капиллярным электрометром,
используемым Липманом для экспериментов
по выводу этого уравнения. Емкость
![]() подставив в 1 уравнение Липмана д.э.с.
подставив в 1 уравнение Липмана д.э.с.
![]() ;
; ![]() ;
; ![]() .
Проинтегрируем по σ от σ до σmax
и по φ от φ до φ0
(точка нулевого заряда) получим:
.
Проинтегрируем по σ от σ до σmax
и по φ от φ до φ0
(точка нулевого заряда) получим:
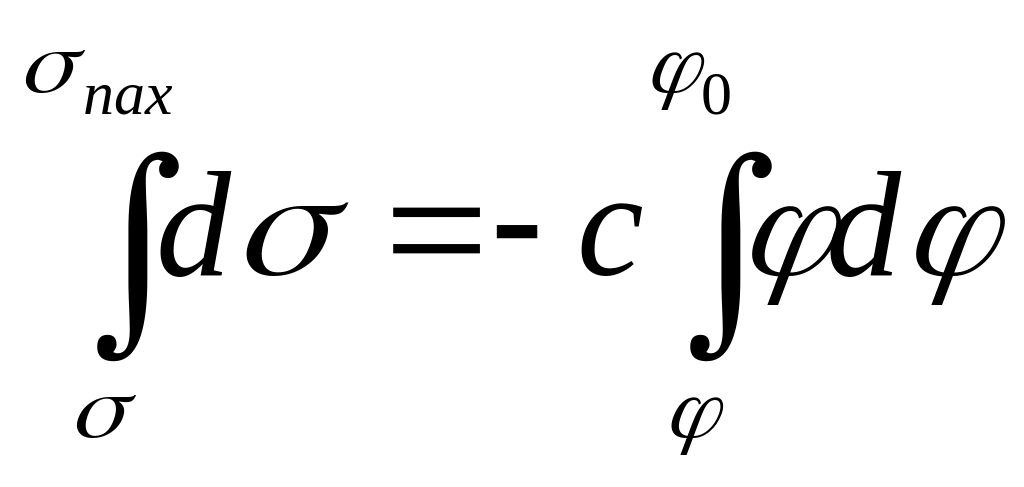
![]()
Если принять φ=0
в точке «0» заряда
![]() - уравнение капиллярной кривой. Оно
характеризует изменение σ от φ при
с=const.
- уравнение капиллярной кривой. Оно
характеризует изменение σ от φ при
с=const.
Симметричность ветвей параболы говорит о равном сродстве катионов и анионов к поверхности, если они выступают в качестве противоионов.
Обычно ветви
несимметричны. Вершина кривой отмечает
точки «О» заряда в этой точке:
![]() ,
т.е. σ не зависит от φ, но φ может быть
≠0, его тогда называют потенциалом
«нулевого заряда».
,
т.е. σ не зависит от φ, но φ может быть
≠0, его тогда называют потенциалом
«нулевого заряда».
Для оксидов и гидроксидов, у которых в воде потенциал определяющими ионами являются OH- и H+. Точка «О» заряда соответствует определенному значению pH (здесь величины зарядов обоих знаков равны, их алгебраическая сумма равна нулю). pHи.э.т. зависит от кислотно-основных свойств вещества.
![]() .
.
Чем больше кислотность вещества, тем меньше pHи.э.т.
