
- •1. Характеристика предмета коллоидной химии
- •1.1 Признаки объектов коллоидной химии
- •1.2 Количественные характеристики дисперсных систем
- •1.3 Энергетическая и геометрические характеристики поверхности
- •1.4 Классификация дисперсных систем
- •1.5 Методы получения коллоидных систем
- •1.6. Правило фаз Гиббса для дисперсных систем
- •2. Поверхностное натяжение
- •2.1 Термодинамические параметры поверхностного слоя
- •2.2 Экспериментальные методы определения поверхностного натяжения.
- •2.3 Внутренняя полная поверхностная энергия.
- •2.4 Температурная зависимость σ и полной внутренней поверхностной энергии.
- •2.5 Механизм процессов самопроизвольного уменьшения σ. Принцип Гиббса-Кюри.
- •2.6 Внутреннее давление. Уравнение Лапласа
- •2.7 Влияние дисперсности на реакционную способность
- •2.8 Влияние дисперсности на растворимость вещества
- •2.9 Влияние дисперсности на равновесие химической реакции.
- •2.10 Влияние дисперсности на температуру фазовых переходов.
- •2.11 Уравнение капиллярной конденсации
- •3. Термодинамика образования новой фазы.
- •3.1 Кинетика образования новой фазы в системе “ж – т”.
- •3.2 Управление степенью дисперсности.
- •4. Двойной электрический слой. Механизм его образования.
- •4.1 Строение дэс
- •4.2 Примеры д.Э.С. И строение мицеллы
- •4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
- •5. Адсорбция. Зависимость от параметров системы
- •5.1 Типы адсорбции
- •5.2 Ионный обмен
- •5.3 Фундаментальные адсорбционные уравнения Гиббса
- •5.4 Адсорбция на границе ж-г
- •5.5 Уравнение Шишковского
- •5.6 Изотерма адсорбции Ленгмюра
- •5.7 Многокомпонентная адсорбция из газовой фазы.
- •5.8 Учет неэквивалентности адсорбционных центров
- •5.9. Капиллярные явления. Формула Жюрена
- •5.10 Адсорбция на пористых телах.
- •5.11 Адсорбция на микропористых телах.
- •5.12 Селективная адсорбция из растворов
- •6. Электрокинетические явления
- •6.1 Электроосмос
- •6.2 Электрофорез
- •7. Адгезия. Механизм процессов адгезии
- •7.1 Смачивание. Краевой угол
- •7.2 Связь работы адгезии с краевым углом
- •7.3 Эффект Марагони.
- •7.4 Правило Антонова
- •8. Флотация
- •9. Рассеяние света ультромикрогетерогенными частицами
- •10. Устойчивость дисперсных систем.
- •10.1 Седиментационная устойчивость дисперсных систем
- •10.2 Седиментационный анализ.
- •I метод.
- •10.3 Механические методы седиментации
- •10.4 Агрегативная устойчивость дисперсных систем
- •10.5 Кинетика коагуляции.
- •10.6 Коагуляция золей электролитами
- •10.7 Условие термодинамической устойчивости дисперсных систем
- •11. Эмульсии. Их стабилизация и разрушение.
- •12. Пены, стабилизация и разрушение.
- •13. Аэрозоли. Устойчивость и разрушение.
- •14. Суспензии. Обеспечение их устойчивости.
- •15. Гели
- •16. Экспериментальные методы изучения поверхностей.
10.2 Седиментационный анализ.
(исследование дисперсных систем в гравитационном или центобежном поле).
Цель – определение гранулометрического состава дисперсной фазы, распределение частиц по размерам, а также определение Sуд., преобладающего размера.
Методы, которые в основе:
- измерение скорости осаждения
- измерение распределения частиц по высоте
1 – метод для r 10-4 – 10-7 м
2 – метод для r < 10-7м с использованием центробежного поля (для крупных молекул)
I метод.
![]() или
или ![]()
Если
Частицы имеют сферическую форму
Движутся ламинарно с U – const
Не взаимодействуют между собой
Химически инертны к среде
Не агрегатируют между собой, то
Выполняется закон
Стокса
![]() и
и
![]()
Анализ проводится для c ≤ 1 масс %. r называют эквивал. на весах Одена (торзионных) или весах Фигурновского.
Последовательность анлиза:
1. Построение
кривой седиментации
![]()
2. Построение
кривой интегральной
![]()
3. Построение
дифференциальной кривой или кривой
распределения
![]()
а). монодисперсная
система
![]() (скорость накопления)
(скорость накопления)
![]()
б). бидисперсная система
участок ОА – осажденные фракции 1 и 2,
участок АА1 – осажденная фракция 2
Обработку кривых седиментации часто проводят методом касательной. Касательная, проведенная к седиментационной кривой в точке τ1 и τ2 отсекает на оси ординат массы от осадков соответственно, фракции 1 и 2 m1 и m2.
r
будет определяться как
![]() ;
;
![]()
в). Полидисперсная система. В этом случае всю кривую разбивают на псевдомонодисперсные участки, соответствующие времени осаждения τ1 , τ2 ,…τn
1.
τ1~ m1, τ2-τ1~ m2, τ3-τ2~ m3; …..
rmax – касательная из «0», rmin – касательная соответствует переходу кривой в прямую.
2.Интегральная кривая
![]() ;
;
![]()
3.Дифференциальная кривая
10.3 Механические методы седиментации
Кон. Сведберг (Ноб. прем.) в начале XIX в.
![]() ;
;
![]() ;
;
![]()
h – расстояние от центра вращения.
Уравнение Сведберга связывает rчастиц с расстоянием х1 и х2 на которые они смещаются за τ1 и τ2 ; х1 и х2 – расстояние от оси вращения до фронта частиц
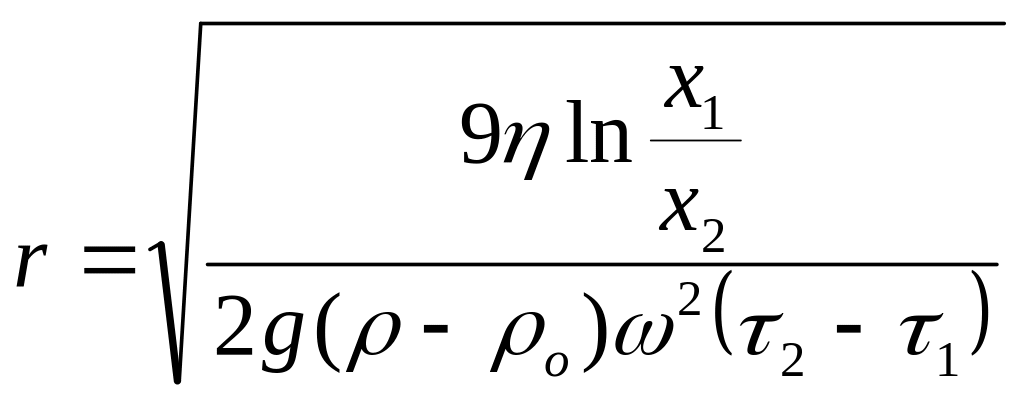
Уравнение Сведберга-Николаса
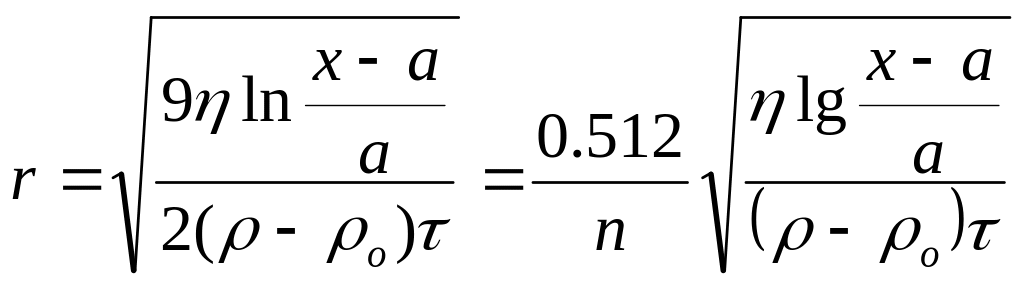
а – расстояние от оси вращения до мениска золя
х – расстояние от мениска золя до фронта
Уравнение Сведберга-Ринде
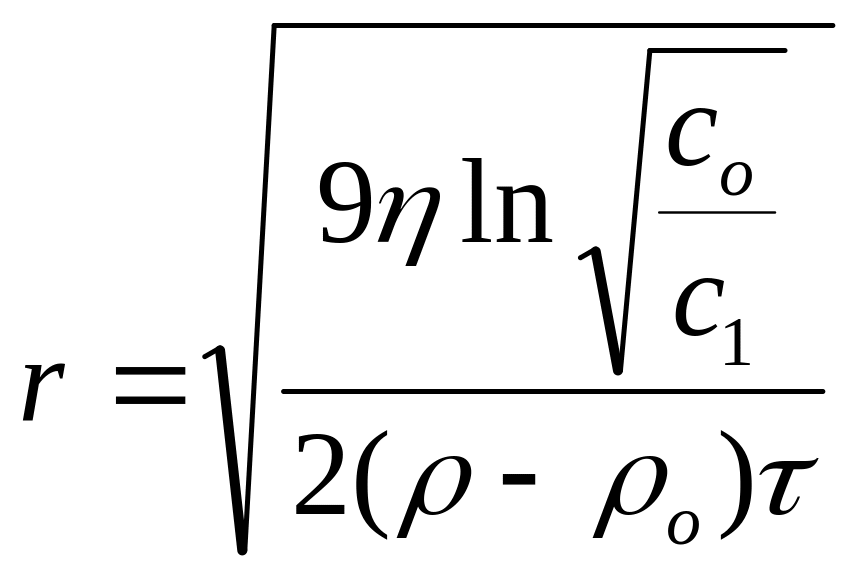 ;
со,
с1
– концентрация золя в % ко времени τо
и τ1
;
со,
с1
– концентрация золя в % ко времени τо
и τ1
10.4 Агрегативная устойчивость дисперсных систем
В большинстве д.с. самопроизвольно идут процессы укрупнения частиц д. фазы из-за стремления уменьшить избыточную поверхностную энергию. Укрупнение частиц может идти двумя путями:
1.изотермическая перегонка – перенос вещества от мелких частиц к более крупным (↓G). Движущая сила – разность μчастиц различного размера
2.коагуляция – слипание, слияние частиц д. фазы.
Коагуляция в узком смысле – это слипание частиц, а в широком смысле – потеря агрегативной устойчивости. Для характеристики слипания частиц часто используют термин «коалесценция».
Коагуляция ведет к седиментационной неустойчивости или увеличивает скорость ее протекания.
В концентрированных растворах коагуляция может приводить к образованию объемных структур в системе. Коагуляция включает несколько последовательных стадий:
- образование флоккул (агрегатов частиц), разделенных прослойками среды – флокуляция. Обратный процесс называется пептизация (из флоккул → частицы)
- разрушение прослоек, слияние частиц или образование жестких конденсационных структур.
Все эти процессы идут с ↓G. Коагуляция зависит от термодинамических и кинетических факторов.
А. – Термодинамические факторы устойчивости:
1)электростатический – заключается в ↓σ, вследствие образования на межфазной поверхности ДЭС.
2)адсорбционно-сольватный – заключается в ↓σ, вследствие адсорбции (уравнение Гиббса) и адгезии (Дюпре).
3)энтропийный – заключается в стремлении системы к равномерному распределению частиц. Действует в системах с броуновским движением.
Б. – Кинетические факторы устойчивости – способствуют уменьшению скорости коагуляции.
1)структурно-механический – заключается в необходимости приложения энергии и времени для разрушения пленки среды из-за ее определенной упругости и прочности.
2)гидродинамический – заключается в уменьшении скорости коагуляции за счет увеличения η и ∆ρ.
В. – Смешанные факторы устойчивости – заключаются в возникновении синергетического эффекта, т.е. одновременного влияния нескольких выше указанных факторов и их усилении (↓σ изменяет механические свойства пленки среды).
Для каждого фактора устойчивости при необходимости может быть предложен специфический метод его нейтрализации
- введение электролитов уменьшает электростатический фактор
- введение ПАВ изменяет механическую прочность прослоек
В основе т.д. агрегативной устойчивости лежит представление о расклинивающем давлении, введенным Б. Деряминым в 1935. Оно возникает при сильном ↓dпленки , при взаимодействии сближающихся поверхностных слоев частиц. Поверхностные слои начинают перекрываться. Расклинивающее давление – суммарный параметр, учитывающий силы притяжения (Ван-дер-Вальса) и силы отталкивания – имеют различную природу.
Уменьшение dпленки приводит к исчезновению в ней молекул среды с min энергией, т.к. находящиеся в ней частицы увеличивают свою избыточную энергию в связи с потерей соседей или сольватных оболочек. В результате молекулы в прослойке стремятся втянуть в нее другие молекулы из объема, возникает как бы расклинивающее давление. Его физический смысл – это давление, которое нужно приложить к пленке, чтобы сохранить равновесную толщину.
Современная теория
устойчивости дисперсных систем носит
название ДЛФО (Дерябина-Ландау-Фервея-Обербека).
В ее основе общая энергия взаимодействия
частиц, определяется как алгебраическая
сумма энергий молекулярного притяжения
и электростатического отталкивания
![]()
Давление отталкивания определяется только электростатическими силами. Однако, к настоящему времени общей теории агрегативной устойчивости и коагуляции пока не создано.
