
- •1. Характеристика предмета коллоидной химии
- •1.1 Признаки объектов коллоидной химии
- •1.2 Количественные характеристики дисперсных систем
- •1.3 Энергетическая и геометрические характеристики поверхности
- •1.4 Классификация дисперсных систем
- •1.5 Методы получения коллоидных систем
- •1.6. Правило фаз Гиббса для дисперсных систем
- •2. Поверхностное натяжение
- •2.1 Термодинамические параметры поверхностного слоя
- •2.2 Экспериментальные методы определения поверхностного натяжения.
- •2.3 Внутренняя полная поверхностная энергия.
- •2.4 Температурная зависимость σ и полной внутренней поверхностной энергии.
- •2.5 Механизм процессов самопроизвольного уменьшения σ. Принцип Гиббса-Кюри.
- •2.6 Внутреннее давление. Уравнение Лапласа
- •2.7 Влияние дисперсности на реакционную способность
- •2.8 Влияние дисперсности на растворимость вещества
- •2.9 Влияние дисперсности на равновесие химической реакции.
- •2.10 Влияние дисперсности на температуру фазовых переходов.
- •2.11 Уравнение капиллярной конденсации
- •3. Термодинамика образования новой фазы.
- •3.1 Кинетика образования новой фазы в системе “ж – т”.
- •3.2 Управление степенью дисперсности.
- •4. Двойной электрический слой. Механизм его образования.
- •4.1 Строение дэс
- •4.2 Примеры д.Э.С. И строение мицеллы
- •4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
- •5. Адсорбция. Зависимость от параметров системы
- •5.1 Типы адсорбции
- •5.2 Ионный обмен
- •5.3 Фундаментальные адсорбционные уравнения Гиббса
- •5.4 Адсорбция на границе ж-г
- •5.5 Уравнение Шишковского
- •5.6 Изотерма адсорбции Ленгмюра
- •5.7 Многокомпонентная адсорбция из газовой фазы.
- •5.8 Учет неэквивалентности адсорбционных центров
- •5.9. Капиллярные явления. Формула Жюрена
- •5.10 Адсорбция на пористых телах.
- •5.11 Адсорбция на микропористых телах.
- •5.12 Селективная адсорбция из растворов
- •6. Электрокинетические явления
- •6.1 Электроосмос
- •6.2 Электрофорез
- •7. Адгезия. Механизм процессов адгезии
- •7.1 Смачивание. Краевой угол
- •7.2 Связь работы адгезии с краевым углом
- •7.3 Эффект Марагони.
- •7.4 Правило Антонова
- •8. Флотация
- •9. Рассеяние света ультромикрогетерогенными частицами
- •10. Устойчивость дисперсных систем.
- •10.1 Седиментационная устойчивость дисперсных систем
- •10.2 Седиментационный анализ.
- •I метод.
- •10.3 Механические методы седиментации
- •10.4 Агрегативная устойчивость дисперсных систем
- •10.5 Кинетика коагуляции.
- •10.6 Коагуляция золей электролитами
- •10.7 Условие термодинамической устойчивости дисперсных систем
- •11. Эмульсии. Их стабилизация и разрушение.
- •12. Пены, стабилизация и разрушение.
- •13. Аэрозоли. Устойчивость и разрушение.
- •14. Суспензии. Обеспечение их устойчивости.
- •15. Гели
- •16. Экспериментальные методы изучения поверхностей.
14. Суспензии. Обеспечение их устойчивости.
Suspensio – подвешивание. Дисперсионные системы с твердой дисперсной фазой и жидкой дисперсионной средой. Обладают большой склонностью к седиментации. Для получения агрегативно и седиментационно устойчивых суспензий необходимо:
1. обеспечить
диспергирование до требуемой степени
дисперсности. Какао, чтобы не оседало,
10 мин должно иметь
![]() .
Шоколад имеет
.
Шоколад имеет
![]() (это затвердевшая суспензия) – среда
какао-масло, фазы все другие.
(это затвердевшая суспензия) – среда
какао-масло, фазы все другие.
2. подбор дисперсной среды, смачивающей частицы дисперсной фазы (сажа – вода – неустойчивая, сажа – бензол – устойчивая)
3. подбор и введение в систему веществ стабилизаторов (ПАВ, образующих на частицах дисперсной фазы защитную пленку, препятствующую процессу коагуляции) – желатин, крахмал, сапонины, альбумины и т.д.
15. Гели
Гелями называются структуры, образованные коллоидными частицами или молекулами полимеров в форме простейших сеток, ячейки которых обычно заполнены раствором.
Занимают промежуточное положение между растворами и твердыми полимерами (мясо, клеточные оболочки, адсорбенты).
Гели бывают хрупкими, образованными коллоидными частицами SiO2, TiO2, SuO2, и эластичными (желатин,каучук, полимеры). Хрупкие гели имеют жесткий каркас и не изменяют свой объем при высушивании, поэтому называются ненабухающими. Образуются при коагуляции золей с последующим уплотнением их структуры. До уплотнения структуры возможен обратный переход геля в золь. Взаимообратимый переход золя в гель называется тиксотропией. Обратный переход геля в золь происходит при нагреве или механическом воздействии.
Эластичные гели называются студнями. Благодаря гибкости молекулярных цепей в пространственной сетке они легко изменяют свой объем при поглощении или отдаче растворителя. Объем студня может возрастать в десятки раз. Процесс поглощения растворителя называется набуханием. Оно может быть неограниченным и тогда гель переходит в золь (набухание каучука в бензине).
Эластичные гели или студни образуются при, как правило, за счет снижения растворимости дисперсной фазы в растворителе (снижение температуры). Если процесс их застудневания предшествует достижению равновесия между дисперсной фазой и дисперсной средой, либо за счет старения, то происходит расслоение студня на более плотный осадок и слой жидкости. Процесс самопроизвольного расслоения геля называется синерезисом. Имеет практическое значение: жидкость делится на свободную и связанную (входит в сольватную оболочку). У младенцев она 70%, у пожилых людей <40% – дряблость кожи, морщины.
16. Экспериментальные методы изучения поверхностей.
Чтобы понять суть процессов, происходящих на поверхности, необходимо знать количество адсорбционных молекул, химический состав поверхности, порядок расположения компонентов, их энергетическую однородность и т.д. Обычные методы химического и рентгеноструктурного анализа для этого непригодны.
Наиболее простой способ определения числа молекул, адсорбированных на твердой поверхности, состоит в прямом измерении. Так при адсорбции газа определяют:
∆р газовой фазы до и после адсорбции на порошкообразном материале.
сверхточным взвешиванием (гравиметрия) для растворов:
химический анализ раствора
фотометрия при адсорбции окрашенных соединений.
О чень
эффективен метод температурно-программируемой
десорбции (ТПД) образец с адсорбируемым
веществом нагревают со строго определенной
скоростью и одновременно
масс-спектрометрическим анализом
определяют количество десорбирующихся
молекул, их энергетическую однородность.
чень
эффективен метод температурно-программируемой
десорбции (ТПД) образец с адсорбируемым
веществом нагревают со строго определенной
скоростью и одновременно
масс-спектрометрическим анализом
определяют количество десорбирующихся
молекул, их энергетическую однородность.
Спектр десорбции Н2, адсорбированного на W.
Качественный анализ химического состава могут дать методы ЯМР и ЭПР, однако для первого вещество должно быть магниточувствительным, а для второго в веществе должны быть неспаренные электроны (радикалы).
Наиболее эффективными современными методами исследования поверхности по химическому составу являются:
ультрафиолетовая фотоэлектронная спектроскопия (УФЭС)
рентгеновская фотоэлектронная спектроскопия (РФЭС).
Суть их в том, что твердое тело облучают ультрафиолетовым или мягким рентгеновским излучением в результате из атомов выбиваются электроны с внешних либо внутренних оболочек.
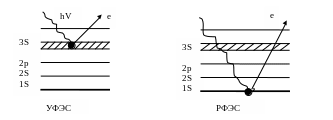 Энергия
падающих квантов (hν),
кинетическая энергия испущенного
электрона (Ек)
Энергия
падающих квантов (hν),
кинетическая энергия испущенного
электрона (Ек)
и энергия связи электрона (Ев) связаны соотношением
Ек= hν – Ев
Ек определяют с помощью анализаторов, поэтому используя монохроматическое излучение hν можно найти Ев, величина которой однозначно связана с видом химического элемента.
Такая техника получила название «ЭСХА»
т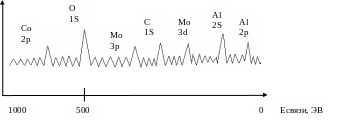 ипичный
спектр РФЭ – спектр поверхности СоМоО4
на подложке Al2O3
ипичный
спектр РФЭ – спектр поверхности СоМоО4
на подложке Al2O3
В зависимости от характера химической связи и окружения пики могут смещаться – «химический сдвиг», что дает дополнительную информацию о упорядоченности элементов и их химических связях.
Очень информативна оже-электроннная спектроскопия (ОЭС). Принцип ее лежит в выбивании электронов с внутренних оболочек и последующего перехода в это состояние электронов с более высоких орбит, в ходе которого избыточная энергия сообщается другим электронам, получившим название «оже». Их появление не зависит от частоты излучения.
С
Пик «настоящих» вторичных е
Пики оже
N(E)
Ep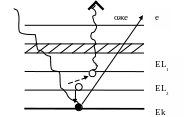
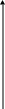

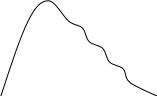

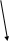

«Химический сдвиг» спектра меди в разных спектрах по данным оже.
Поверхностную структуру, ее периодичность эффективнее всего исследовать, используя явление дифракции электронов, в частности медленных (ДМЕ).
Р ентгеновские
лучи проникают глубоко. С их помощью
исследуют трехмерную структуру твердого
тела. В то же время высокой чувствительностью
к поверхностной упорядоченности
обладают медленные электроны. Электроны
могут упруго рассеяться и неупруго.
Упруго рассеивающиеся электроны дают
дифракционную картину, которая
регистрируется флуоресцентным экраном,
на котором можно судить о кристаллической
упорядоченности поверхности. Метод
известен еще с 1927 года.
ентгеновские
лучи проникают глубоко. С их помощью
исследуют трехмерную структуру твердого
тела. В то же время высокой чувствительностью
к поверхностной упорядоченности
обладают медленные электроны. Электроны
могут упруго рассеяться и неупруго.
Упруго рассеивающиеся электроны дают
дифракционную картину, которая
регистрируется флуоресцентным экраном,
на котором можно судить о кристаллической
упорядоченности поверхности. Метод
известен еще с 1927 года.
Автоионная микроскопия (АИМ) – изобретена Мюллером в 1951 году позволяет наблюдать атомы на поверхности.
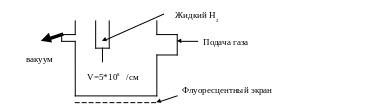
На острие образца V=5*108в/см плотность поля. Вся система заполнена «проявительным газом» (Не, Ne). Газ вблизи острия ионизируется. Ионы ускоряются и попадают на флуоресцентный экран. Изоэлектрические поверхности вблизи острия отражают особенности структуры поверхности. Разрешающая способность составляет 2Å.
Колебательные спектры адсорбирующих веществ.
Э то
эффективный метод изучения их структуры.
Спектроскопия характеристических
потерь энергии электронами (СХПЭЭ)
1967. метод основан на непосредственном
определении колебательных энергетических
уровней по кинетической энергии
медленных электронов после их неупругого
рассеивания на поверхности. Колебательная
энергия молекул 0,1-1 ЭВ. Метод дает
разрешение 10 МЭВ.
то
эффективный метод изучения их структуры.
Спектроскопия характеристических
потерь энергии электронами (СХПЭЭ)
1967. метод основан на непосредственном
определении колебательных энергетических
уровней по кинетической энергии
медленных электронов после их неупругого
рассеивания на поверхности. Колебательная
энергия молекул 0,1-1 ЭВ. Метод дает
разрешение 10 МЭВ.
