
- •1. Характеристика предмета коллоидной химии
- •1.1 Признаки объектов коллоидной химии
- •1.2 Количественные характеристики дисперсных систем
- •1.3 Энергетическая и геометрические характеристики поверхности
- •1.4 Классификация дисперсных систем
- •1.5 Методы получения коллоидных систем
- •1.6. Правило фаз Гиббса для дисперсных систем
- •2. Поверхностное натяжение
- •2.1 Термодинамические параметры поверхностного слоя
- •2.2 Экспериментальные методы определения поверхностного натяжения.
- •2.3 Внутренняя полная поверхностная энергия.
- •2.4 Температурная зависимость σ и полной внутренней поверхностной энергии.
- •2.5 Механизм процессов самопроизвольного уменьшения σ. Принцип Гиббса-Кюри.
- •2.6 Внутреннее давление. Уравнение Лапласа
- •2.7 Влияние дисперсности на реакционную способность
- •2.8 Влияние дисперсности на растворимость вещества
- •2.9 Влияние дисперсности на равновесие химической реакции.
- •2.10 Влияние дисперсности на температуру фазовых переходов.
- •2.11 Уравнение капиллярной конденсации
- •3. Термодинамика образования новой фазы.
- •3.1 Кинетика образования новой фазы в системе “ж – т”.
- •3.2 Управление степенью дисперсности.
- •4. Двойной электрический слой. Механизм его образования.
- •4.1 Строение дэс
- •4.2 Примеры д.Э.С. И строение мицеллы
- •4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
- •5. Адсорбция. Зависимость от параметров системы
- •5.1 Типы адсорбции
- •5.2 Ионный обмен
- •5.3 Фундаментальные адсорбционные уравнения Гиббса
- •5.4 Адсорбция на границе ж-г
- •5.5 Уравнение Шишковского
- •5.6 Изотерма адсорбции Ленгмюра
- •5.7 Многокомпонентная адсорбция из газовой фазы.
- •5.8 Учет неэквивалентности адсорбционных центров
- •5.9. Капиллярные явления. Формула Жюрена
- •5.10 Адсорбция на пористых телах.
- •5.11 Адсорбция на микропористых телах.
- •5.12 Селективная адсорбция из растворов
- •6. Электрокинетические явления
- •6.1 Электроосмос
- •6.2 Электрофорез
- •7. Адгезия. Механизм процессов адгезии
- •7.1 Смачивание. Краевой угол
- •7.2 Связь работы адгезии с краевым углом
- •7.3 Эффект Марагони.
- •7.4 Правило Антонова
- •8. Флотация
- •9. Рассеяние света ультромикрогетерогенными частицами
- •10. Устойчивость дисперсных систем.
- •10.1 Седиментационная устойчивость дисперсных систем
- •10.2 Седиментационный анализ.
- •I метод.
- •10.3 Механические методы седиментации
- •10.4 Агрегативная устойчивость дисперсных систем
- •10.5 Кинетика коагуляции.
- •10.6 Коагуляция золей электролитами
- •10.7 Условие термодинамической устойчивости дисперсных систем
- •11. Эмульсии. Их стабилизация и разрушение.
- •12. Пены, стабилизация и разрушение.
- •13. Аэрозоли. Устойчивость и разрушение.
- •14. Суспензии. Обеспечение их устойчивости.
- •15. Гели
- •16. Экспериментальные методы изучения поверхностей.
6.1 Электроосмос
Линейная скорость:
![]() - уравнение Гельмгольца-Смоулховского.
- уравнение Гельмгольца-Смоулховского.
![]()
![]() - электроосмотическая
подвижность [м2/сВ]
- электроосмотическая
подвижность [м2/сВ]
![]() через объемную
скорость можно выразить как
через объемную
скорость можно выразить как
![]() ,
где S
– поперечное сечение в капилляре.
,
где S
– поперечное сечение в капилляре.
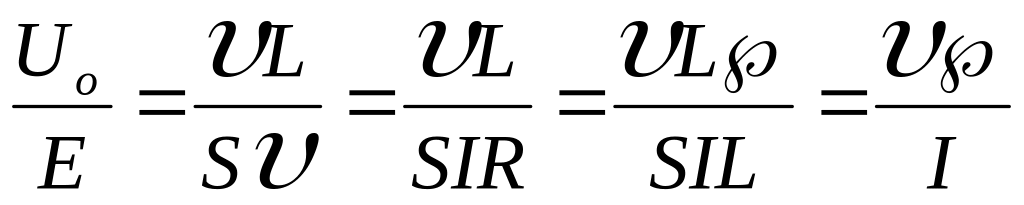
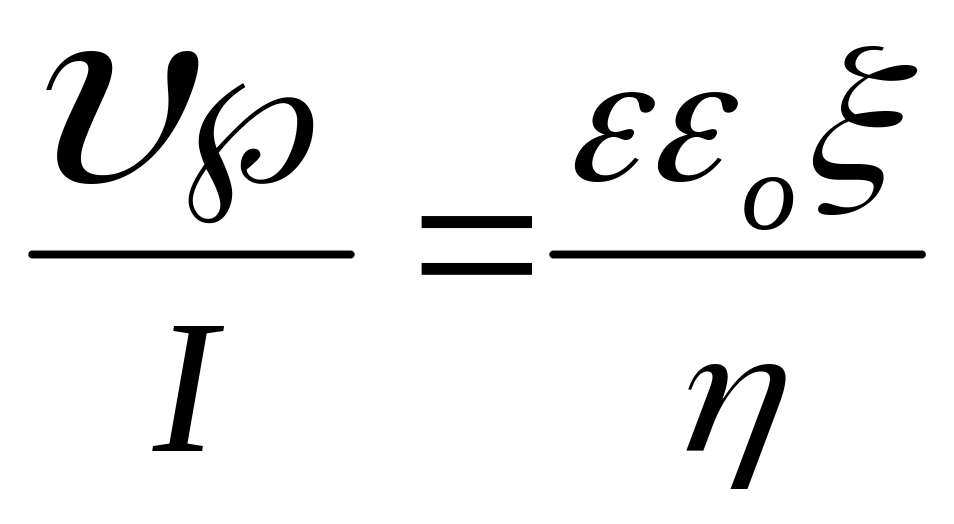 ;
;  ;
;
![]() ;
; ![]()
L – расстояние между электродами
- Δφ
I – сила тока, R – сопротивление
![]() - удельная объемная
электропроводность
- удельная объемная
электропроводность
![]() - поверхностная
проводимость
- поверхностная
проводимость
![]() - коэф. эффективности
диафрагмы
- коэф. эффективности
диафрагмы
это приращение проводимости в растворе за счет ДЭС, если диаметры капилляров велики - можно пренебречь.
6.2 Электрофорез
Подвижность:
![]()
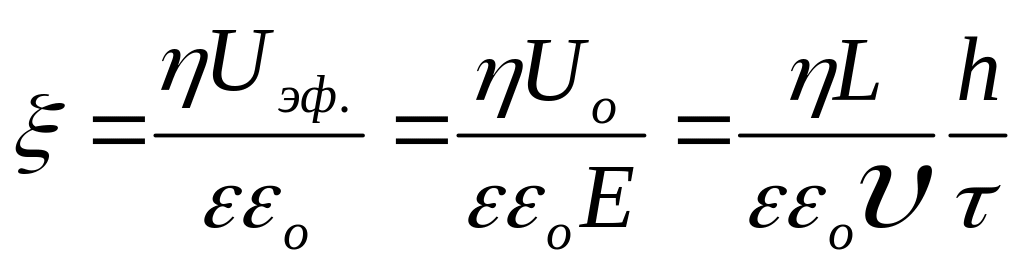 ;
;
В разбавленных
растворах при 20 ºС:
![]() ;
;
![]() ;
;
с – концентрация суспензии;
S – поверхность электродов.
Уравнение Гельмгольца-Смоулховского для ξ – потенциала через потенциал течения имеет вид:
![]()
![]() -
число частиц в единице объема;
-
число частиц в единице объема;
Е – напряжение поля, возникающее при седиментации.
![]() заменится
на
заменится
на
![]() .
.
Потенциал течения и потенциалседиментации могут являться причиной взрывов и пожаров при перекачке топлива, технологических растворов, осаждении суспензий и эмульсий в связи с возникновением высоких .
Практическое использование:
электроосмос – осушка различных объектов (стен зданий, сыпучих материалов, при строительстве плотин, дамб), электроды – полые трубы с отверстиями → откачка, фильтрация – трудно фильтруемых сред
электрофорез – в авто и электронной промышленности нанесение покрытий равномерно на детали сложной формы.
1й электрод – деталь, 2й электрод – емкость с суспензией. Анодофарез и катодофарез – деталь.
Медицина – фракционирование полимеров.
7. Адгезия. Механизм процессов адгезии
В гетерогенных системах различают взаимодействие внутри фаз и между фазами.
Взаимодействие атомов и молекул внутри фазы называют когезией. Она определяет существование веществ в конденсированном состоянии.
Взаимодействие между приведенными в контакт поверхностями конденсирующих фаз называют адгезией (прилипание).
Различают адгезию между фазами Т – Т – мах. адг. нед.
м.б. мах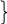
Ж – Ж
Это явление очень распространено в природе и технике. Оно определяет силу межфазного взаимодействия, и исходя из этого качество некоторых материалов или эффективность процессов:
Склеивание
Крашение
Пайка, сварка
Печатание
Получение бетона, резины, композитов.
Процессы эти наиболее изучены для систем, где одна из фаз – жидкая.
Различают адгезив – вещество наносится. Субстрат – тело, на которое наносится.
Ранее – σ – работа образования ед. поверхности , т.е. характеризует силу когезионного взаимодействия т.к. при разрыве тела образуются 2 ед. поверхности, т.е.
![]() .
.
Энергию когезии количественно характеризует Екрист.реш, Епорообраз., Ткип. и т.д.
Адгезия – результат стремления системы к уменьшению поверхностной энергии. Это самопроизвольный процесс.
Работа адгезии
![]() - работа, затраченная на разрыв адгезионных
связей ед. поверхности.
- работа, затраченная на разрыв адгезионных
связей ед. поверхности.
Определим взаимосвязь и σ.
![]()
![]()
![]()
![]() ,
т.к. при совмещении 2х поверхностей
энергия Гиббса уменьшается на величину,
равную
,
т.к. при совмещении 2х поверхностей
энергия Гиббса уменьшается на величину,
равную
![]() .
.
![]() - уравнение Дюпре
– отражает закон сохранения энергии
при адгезии.
- уравнение Дюпре
– отражает закон сохранения энергии
при адгезии.
Чем >
![]() и <
и <
![]() тем >
и наоборот.
тем >
и наоборот.
При растворении
вещества
![]()
![]()
При растворении
вещества
![]() полусуммы работ когезии обоих веществ.
полусуммы работ когезии обоих веществ.
От
следует отличать адгезионную прочность
![]() - работу, затраченную на разрушение
адгезионного соединения.
- работу, затраченную на разрушение
адгезионного соединения.
![]() ,
где
,
где
![]() может быть значительно больше
может быть значительно больше
Процесс образования адгезионной связи делят на 2 стадии:
Транспортную (перемещение и определенное ориентированных молекул адгезива на поверхности субстрата) способствует увеличению Т, Р, перевод вещества в «ж»
Непосредственное взаимодействие (Ван-дер-Вальсовы силыхимическое взаимодействие)
Различают следующие механизмы адгезии:
механическую (поры, трещины)
адсорбционный (Ван-дер-Вальса, водородные связи)
электрический (ДЭС)
диффузионный(взаимная диффузия)
химическое взаимодействие
Как правило, действует смешанный механизм. Т.к. теоретическая оценка адгезии затруднена и определяют экспериментально, путем разрушения соединения.
