
- •1. Характеристика предмета коллоидной химии
- •1.1 Признаки объектов коллоидной химии
- •1.2 Количественные характеристики дисперсных систем
- •1.3 Энергетическая и геометрические характеристики поверхности
- •1.4 Классификация дисперсных систем
- •1.5 Методы получения коллоидных систем
- •1.6. Правило фаз Гиббса для дисперсных систем
- •2. Поверхностное натяжение
- •2.1 Термодинамические параметры поверхностного слоя
- •2.2 Экспериментальные методы определения поверхностного натяжения.
- •2.3 Внутренняя полная поверхностная энергия.
- •2.4 Температурная зависимость σ и полной внутренней поверхностной энергии.
- •2.5 Механизм процессов самопроизвольного уменьшения σ. Принцип Гиббса-Кюри.
- •2.6 Внутреннее давление. Уравнение Лапласа
- •2.7 Влияние дисперсности на реакционную способность
- •2.8 Влияние дисперсности на растворимость вещества
- •2.9 Влияние дисперсности на равновесие химической реакции.
- •2.10 Влияние дисперсности на температуру фазовых переходов.
- •2.11 Уравнение капиллярной конденсации
- •3. Термодинамика образования новой фазы.
- •3.1 Кинетика образования новой фазы в системе “ж – т”.
- •3.2 Управление степенью дисперсности.
- •4. Двойной электрический слой. Механизм его образования.
- •4.1 Строение дэс
- •4.2 Примеры д.Э.С. И строение мицеллы
- •4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
- •5. Адсорбция. Зависимость от параметров системы
- •5.1 Типы адсорбции
- •5.2 Ионный обмен
- •5.3 Фундаментальные адсорбционные уравнения Гиббса
- •5.4 Адсорбция на границе ж-г
- •5.5 Уравнение Шишковского
- •5.6 Изотерма адсорбции Ленгмюра
- •5.7 Многокомпонентная адсорбция из газовой фазы.
- •5.8 Учет неэквивалентности адсорбционных центров
- •5.9. Капиллярные явления. Формула Жюрена
- •5.10 Адсорбция на пористых телах.
- •5.11 Адсорбция на микропористых телах.
- •5.12 Селективная адсорбция из растворов
- •6. Электрокинетические явления
- •6.1 Электроосмос
- •6.2 Электрофорез
- •7. Адгезия. Механизм процессов адгезии
- •7.1 Смачивание. Краевой угол
- •7.2 Связь работы адгезии с краевым углом
- •7.3 Эффект Марагони.
- •7.4 Правило Антонова
- •8. Флотация
- •9. Рассеяние света ультромикрогетерогенными частицами
- •10. Устойчивость дисперсных систем.
- •10.1 Седиментационная устойчивость дисперсных систем
- •10.2 Седиментационный анализ.
- •I метод.
- •10.3 Механические методы седиментации
- •10.4 Агрегативная устойчивость дисперсных систем
- •10.5 Кинетика коагуляции.
- •10.6 Коагуляция золей электролитами
- •10.7 Условие термодинамической устойчивости дисперсных систем
- •11. Эмульсии. Их стабилизация и разрушение.
- •12. Пены, стабилизация и разрушение.
- •13. Аэрозоли. Устойчивость и разрушение.
- •14. Суспензии. Обеспечение их устойчивости.
- •15. Гели
- •16. Экспериментальные методы изучения поверхностей.
1.2 Количественные характеристики дисперсных систем
Для характеристики дисперсных систем используют три основных величины: 1.Поперечный размер частиц (ø, ребро куба) – d; [d]=см, м 2.Дисперсность (Д) – величина, обратная поперечному размеру частиц: Д=1/d; [Д]=см-1, м-1
Физический смысл – число частиц, расположенных на длине 1см или 1м 3.Физический смысл (Sуд) – это межфазная поверхность (S1.2), приходящаяся на единицу объема (V) или единицу массы (m)
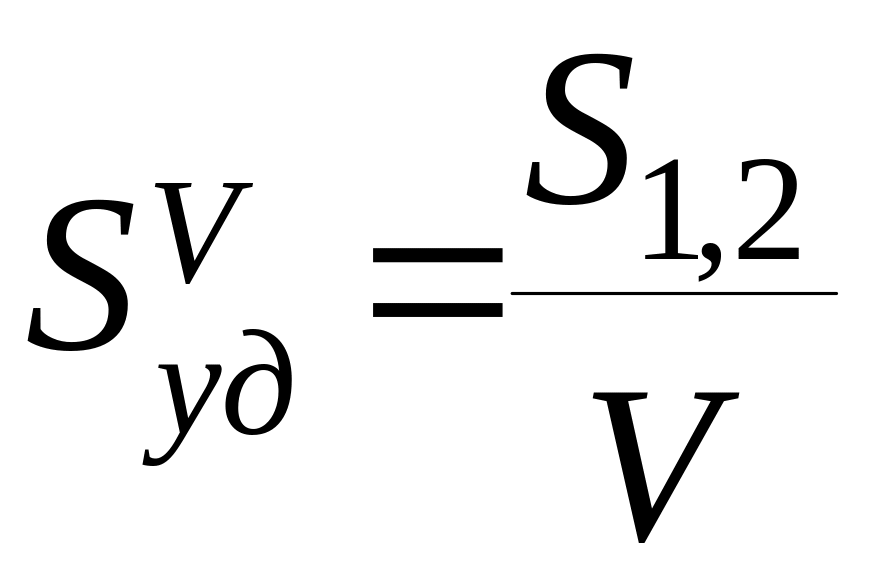 ; [SVуд]=см2/см3=см-1(м-1)
; [SVуд]=см2/см3=см-1(м-1)
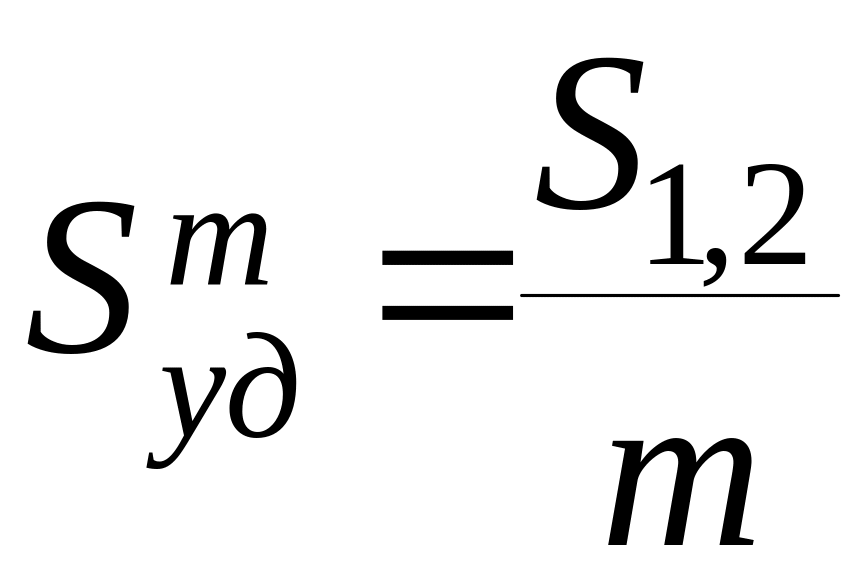
 ;[Smуд]=см2/г,
м2/кг
для
кубических частиц
;[Smуд]=см2/г,
м2/кг
для
кубических частиц
 для
волокон
для
волокон
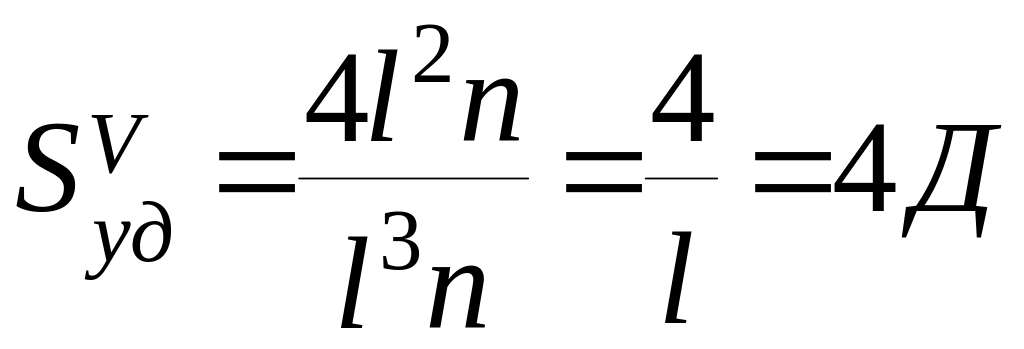 для
пленок
для
пленок
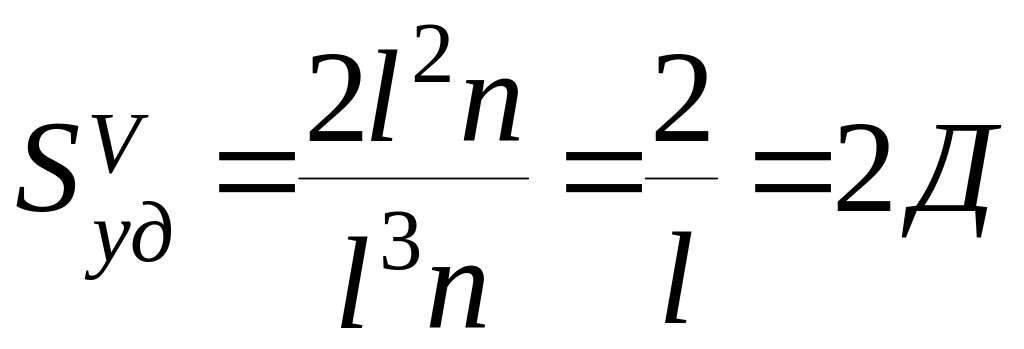 для
сферы
для
сферы
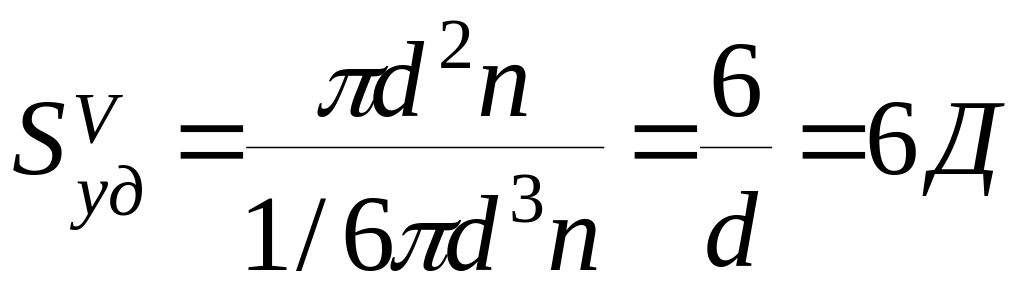 В
общем виде
В
общем виде
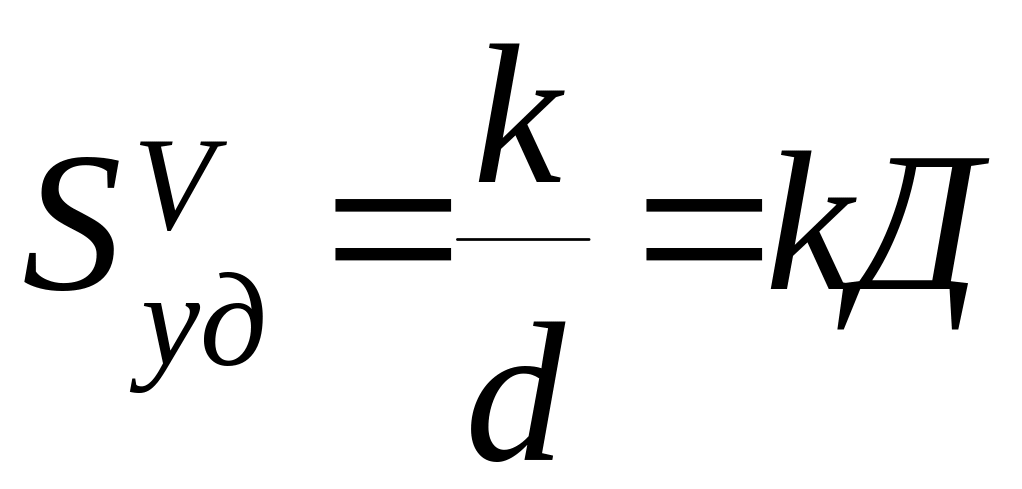 ,
где k
– коэффициент формы
,
где k
– коэффициент формы
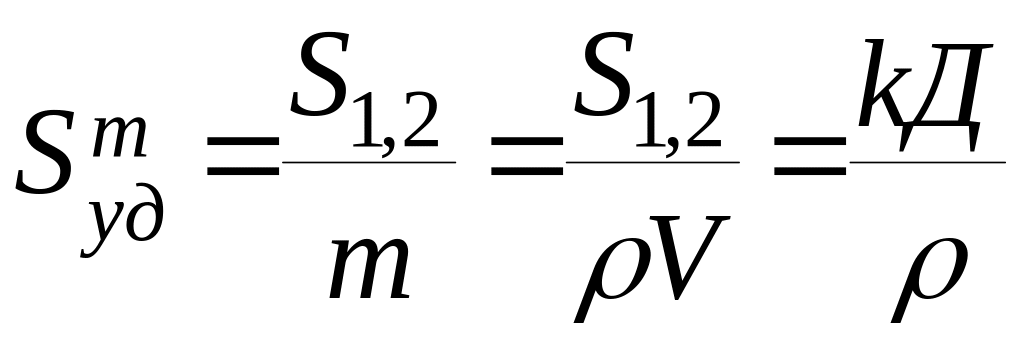
Рис.1 Зависимость удельной поверхности от поперечного размера частиц (d) и от дисперсности (Д)
В зависимости от размера частиц системы могут быть моно- и полидисперсные. Реальные системы - полидисперсные.
1.3 Энергетическая и геометрические характеристики поверхности
Любая поверхность обладает избыточной энергией, которая характеризуется ∆G. Величина ∆G, относящаяся к единице поверхности, называется поверхностным натяжением.
Поверхностный слой жидкости постоянно обновляется. Толщина его зависит от межмолекулярного взаимодействия и составляет несколько молекул. Плотность его колеблется от dж до dп. Время пребывания молекул в поверхностном слое ~ 107с. Внутренняя граница поверхностного слоя определяется по изменению ее структуры.
Благодаря высокой подвижности молекул, находящихся в поверхностном слое, ее поверхность сплошная и энергетически однородная (эквипотенциальная). Силы межмолекулярного взаимодействия в твердом теле значительно выше. Значит и время больше τ=1032c. Малая подвижность атомов в поверхностном слое обеспечивает неизменность формы твердого тела во времени. Поверхность его неоднородна (шероховата) и практически не бывает эквипотенциальна. В системах т-ж межфазная поверхность определяет профиль твердого тела.
Важной характеристикой поверхности является ее кривизна(H) – это ½ производной площади по объему. H=1/2dS/dV.
Для сферических частиц S=4πr2; V=(4/3)πr3
dS=8πrdr; dV=4πr2dr
H=(1/2)8πrdr/4πr2dr=1/r Если центр окружности описывает поверхность внутри тела, то H – положительна, если вне, то H – отрицательна.
1.4 Классификация дисперсных систем
1.По степени дисперсности
Грубодисперсные d ≥ 10-5м (10 мкм) – пыли, пески.
Микрогетерогенные 10-5 – 10-7м – эмульсии, суспензии, пены.
Коллоидно-дисперсные в жидкой среде (золи) 10-7 – 10-9 (истинно коллоидные) – гидрозоли, органозоли, аэрозоли
Молекулярно или ионодисперсные (истинные растворы) < 10-9м
Частицы золей невидимы в оптический микроскоп, водные системы прозрачны, фильтруются через обычные фильтры.
Самую большую Sуд имеют коллоидные растворы, в истинных растворах межфазные поверхности отсутствуют. Коллоидные системы реальные как правило полидисперсны.
2.По степени взаимодействия между частицами дисперсной фазы
Свободнодисперсные – частицы не связаны, это системы, обладающие текучестью, как обычные жидкости и растворы (коллоидные растворы, взвеси, суспензии)
Связнодисперсные – это структурированные системы, имеющие пространственную сетку, каркас и приобретающие свойства полутвердых тел (гели, пористые тела, аморфные осадки) при dпор < 2нм – микропористые 2 – 200нм – переходные > 200нм – микропористые
3. По взаимодействию между дисперсной фазой и дисперсионной средой (для жидкой среды)
Системы с интенсивным взаимодействием фазы и среды с образованием, например в жидкостях, на поверхности дисперсной фазы сольватных слоев называются лиофильными (гидрофильными). При слабом взаимодействии дисперсной фазы и дисперсионной среды системы называются лиофобными (гидрофобными). 4. По топографическому признаку (учитывается различие в форме частиц)
Корпускулярные (частицы малы во всех измерениях)
Фибриллярные (волокнистые – частицы малы по двум измерениям)
Ламинарные (пленочные – малой является только толщина)
Если минимальные размеры частиц в этих системах близки, то и удельные поверхности их близки
5. По агрегатному состоянию
И дисперсная фаза и дисперсионная среда могут быть в трех агрегатных состояниях (твердое, жидкое, газообразное). Комбинируя попарно эти агрегатные состояния можно получить 9 различных состояний.
Дисперсионная среда |
Дисперсная фаза |
Условн. обознач. |
Примеры |
газ |
1.газ |
г1/г2 |
смеси некоторых газов при высоких давлениях |
2.жидкость |
ж/г |
туманы, облака, аэрозоли |
|
3.твердое |
т/г |
дымы, пыль, аэрозоли |
|
жидкость |
1.газ |
г/ж |
пены (пивная, противопожарная, пастила) |
2.жидкость |
ж1/ж2 |
эмульсии (молоко, нефть, кремы, латекс, майонез) |
|
3.твердое |
т/ж |
суспензии, взвеси, пасты, илы, шоколад, какао |
|
твердое |
1.газ |
г/т |
гели, пемза, древесный уголь, пенопласт, пенобетон, силикагель |
2.жидкость |
ж/т |
почвы, грунты, жемчуг |
|
3.твердое |
т1/т2 |
металлические сплавы, бетоны, минералы, рубиновые стекла, аметисты, эмали, композиционные материалы |
Отдельно, вне классификации стоят растворы высокомолекулярных соединений. Имея большие размеры молекул они являются объектами изучения коллоидной химии. Занимая положение между истинными растворами и коллоидными, оно не являются гетерогенными системами (нет одного признака). В то же время изучение свойств высокомолекулярных соединений представляет исключительный интерес в биологии и медицине, т.к. к ним относят растворы белков, полисахаридов, нуклеотидов.
