
- •1. Характеристика предмета коллоидной химии
- •1.1 Признаки объектов коллоидной химии
- •1.2 Количественные характеристики дисперсных систем
- •1.3 Энергетическая и геометрические характеристики поверхности
- •1.4 Классификация дисперсных систем
- •1.5 Методы получения коллоидных систем
- •1.6. Правило фаз Гиббса для дисперсных систем
- •2. Поверхностное натяжение
- •2.1 Термодинамические параметры поверхностного слоя
- •2.2 Экспериментальные методы определения поверхностного натяжения.
- •2.3 Внутренняя полная поверхностная энергия.
- •2.4 Температурная зависимость σ и полной внутренней поверхностной энергии.
- •2.5 Механизм процессов самопроизвольного уменьшения σ. Принцип Гиббса-Кюри.
- •2.6 Внутреннее давление. Уравнение Лапласа
- •2.7 Влияние дисперсности на реакционную способность
- •2.8 Влияние дисперсности на растворимость вещества
- •2.9 Влияние дисперсности на равновесие химической реакции.
- •2.10 Влияние дисперсности на температуру фазовых переходов.
- •2.11 Уравнение капиллярной конденсации
- •3. Термодинамика образования новой фазы.
- •3.1 Кинетика образования новой фазы в системе “ж – т”.
- •3.2 Управление степенью дисперсности.
- •4. Двойной электрический слой. Механизм его образования.
- •4.1 Строение дэс
- •4.2 Примеры д.Э.С. И строение мицеллы
- •4.3 Термодинамика образования д.Э.С. Уравнение Габриэль-Липмана
- •5. Адсорбция. Зависимость от параметров системы
- •5.1 Типы адсорбции
- •5.2 Ионный обмен
- •5.3 Фундаментальные адсорбционные уравнения Гиббса
- •5.4 Адсорбция на границе ж-г
- •5.5 Уравнение Шишковского
- •5.6 Изотерма адсорбции Ленгмюра
- •5.7 Многокомпонентная адсорбция из газовой фазы.
- •5.8 Учет неэквивалентности адсорбционных центров
- •5.9. Капиллярные явления. Формула Жюрена
- •5.10 Адсорбция на пористых телах.
- •5.11 Адсорбция на микропористых телах.
- •5.12 Селективная адсорбция из растворов
- •6. Электрокинетические явления
- •6.1 Электроосмос
- •6.2 Электрофорез
- •7. Адгезия. Механизм процессов адгезии
- •7.1 Смачивание. Краевой угол
- •7.2 Связь работы адгезии с краевым углом
- •7.3 Эффект Марагони.
- •7.4 Правило Антонова
- •8. Флотация
- •9. Рассеяние света ультромикрогетерогенными частицами
- •10. Устойчивость дисперсных систем.
- •10.1 Седиментационная устойчивость дисперсных систем
- •10.2 Седиментационный анализ.
- •I метод.
- •10.3 Механические методы седиментации
- •10.4 Агрегативная устойчивость дисперсных систем
- •10.5 Кинетика коагуляции.
- •10.6 Коагуляция золей электролитами
- •10.7 Условие термодинамической устойчивости дисперсных систем
- •11. Эмульсии. Их стабилизация и разрушение.
- •12. Пены, стабилизация и разрушение.
- •13. Аэрозоли. Устойчивость и разрушение.
- •14. Суспензии. Обеспечение их устойчивости.
- •15. Гели
- •16. Экспериментальные методы изучения поверхностей.
2. Поверхностное натяжение
Почему по водной поверхности бегают пауки?
Почему металлическая игла удерживается на водной поверхности?
Почему англичане еще в XVII – XVIII вв. выливали в бушующее море тюлений или китовый жир?
Как норвежские рыбаки определяли место косяка сельди?
Еще раз посмотрим на энергетическое положение атома внутри тела и на его поверхности.
А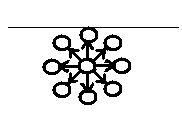 .(внутри)
.(внутри)
F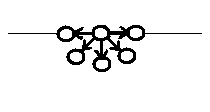 рез=0
рез=0
Б.(на поверхности)
Fрез≠0
и направлена внутрь тела
Втягивая поверхностные атомы внутрь, тело как бы стремится уменьшить свою поверхность. На поверхности возникает напряжение, вызванное наличием избыточной энергии из-за нескомпенсированности энергии поверхностных атомов.
1. Избыточная
поверхностная энергия приходящаяся
на единицу площади поверхности получила
название поверхностного натяжения
(σ)
![]()
Физическая природа σ в нескомпенсированности поля межмолекулярных сил на межфазных поверхностях.
2. Его можно также трактовать как силу, действующую тангенциально поверхности (вдоль нее) и препятствующую увеличению поверхности. Опыт Дюпре с мыльной пеной.
3. σ – можно также рассматривать как работу, затраченную на разрыв межатомных или межмолекулярных связей, т.е. это работа образования единицы поверхности. На σ влияют T, q, добавки ПАВ. [σ]=Дж/м2; Нм/м2=Н/м. В СГС: дин/см; 1 Н/м=1000 дин/см
Чем сильнее межмолекулярные связи в веществе, тем больше σ на его межфазной поверхности.
Отсюда: H2O → σ=0,0721 Дж/м2
Здесь атомы
связаны сильнее
 C2H5OH
→ 0,0221
C2H5OH
→ 0,0221
Говорят о удельной
поверхностной энергии
Fe → 4,0
W → 6,8
Алмаз → 11,4 – макс. знач.
2.1 Термодинамические параметры поверхностного слоя
Все поверхностные явления, вызванные наличием избыточной энергии удобно классифицировать, используя объединенное уравнение I и II начала термодинамики. Его дифференциальная форма:
![]()
G – энергия Гиббса
S – энтропия
Т – температура
V – объем
P – давление
σ – поверхностное натяжение
s – площадь поверхности
μi – химический потенциал i-го компонента
ni – число молей i-го компонента
φ – электрический потенциал
q – количество электричества (заряд)
Уравнение выражает приращение энергии Гиббса через алгебраическую сумму приращений других видов энергии, присущих явления на межфазной поверхности.
Поверхностная энергия σds может превращаться:
1. в энергию Гиббса (соответствует изменению реакционной способности)
2. в теплоту (соотв. пр. адгезии и смачивания)
3. в механическую энергию (явление капиллярности)
4. в химическую энергию (явление адсорбции)
5. в электрическую энергию (электрические и электрокинетические явления)
При
T, p, ni, q – const ![]() , т.е.
, т.е.
σ – есть частная производная от энергии Гиббса на площади межфазной поверхности при T. p, ni, q - const . Если объединенное уравнение записать относительно других термодинамических потенциалов (υ, F, Hэнтальма), то при постоянстве других параметров системы получим:
![]() ;
;
![]() ;
;
![]()
Таким образом: σ – есть частная производная от любого т.д. потенциала по площади межфазной поверхности при постоянстве соответствующих параметров системы.
Т.к. легче всего осуществить const p и T, то σ чаще всего выражают через производную от G.
