
- •Кількісний аналіз
- •Інструкція до навчальної практики №1
- •Контроль знань
- •Лабораторна робота
- •Хід виконання роботи:
- •Інструкція до навчальної практики №2
- •Контроль знань
- •Лабораторна робота
- •Хід виконання роботи:
- •Маса 1 дм3води (г) при різних температурах (°с)
- •Інструкція до навчальної практики №3
- •Контроль знань
- •Лабораторна робота
- •Хід виконання роботи:
- •Титриметричний аналіз.
- •Алгоритм характеристики методу об’ємного аналізу
- •1.Приготування вихідного розчину – Na2в4o7 • 10h2o
- •2.Стандартизація робочого розчину hCl (за вихідним розчином Na2в4o7 • 10h2o)
- •Інструкція до навчальної практики №5
- •Лабораторна робота
- •2.Аналіз досліджуваної речовини:
- •Контрольні завдання
- •Інструкція до навчальної практики №6
- •Лабораторна робота
- •1.Приготування вихідного розчину – NаСl
- •2.Аналіз досліджуваної речовини: (Спосіб титрування прямий)
- •Контрольні завдання
- •Інструкція до навчальної практики №8
- •Лабораторна робота
- •Стандартизація робочого розчину nh4scn(за титрованим робочим розчином AgNo3)
- •2.Аналіз досліджуваної речовини:( Спосіб титрування зворотній)
- •Контрольні завдання
- •Інструкція до навчальної практики №9
- •Приготування вихідного розчину – MgSo4 ·7h2o
- •Приготування робочого розчину – Трилону б
- •Стандартизація робочого розчину –Трилону б (за вихідним розчином MgSo4 · 7h2o)
- •Інструкція до навчальної практики №10
- •Хід роботи
- •Аналіз досліджуваної речовини:( Спосіб титрування прямий)
- •Контрольні завдання
- •2. Стандартизація робочого розчину kMnO4
- •Контрольні завдання
- •Інструкція до навчальної практики №14 -15
- •Лабораторна робота
- •1.Приготування вихідного розчину – k2Cr2o7
- •2.Стандартизація робочого розчину Na2s2o3 за вихідним розчином k2Cr2o7
- •3.Аналіз досліджуваної речовини: (Спосіб титрування прямий)
- •Контрольні завдання
- •Інструкція до навчальної практики №16
- •10.Результати оформити за схемою:
- •Інструкція до навчальної практики №17
- •Підготувати іономір до роботи згідно інструкції користувача приладом
- •Потенціометрія
- •Хід виконання
- •Інструкція до навчальної практики №18
- •Інструкція до навчальної практики №19
Титриметричний аналіз.
П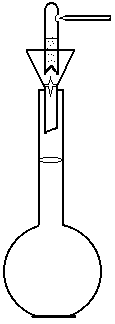 риготування
первинно - стандартного) розчину
риготування
первинно - стандартного) розчину
Із фіксаналу. У вимірювальну колбу вставляють лійку, в яку поміщають спеціальний скляний бойок промитий дистильованою водою (якщо у фіксаналі не розчин, а суха речовина, то лійка і бойок повинні бути сухими). Ампулу протирають спиртом, щоб змити напис і обмивають дистильованою водою. Потім її вставляють у лійку так, щоб вона своїм ввігнутим дном торкалася бойка, потім піднімають її і не сильно вдаряють по кінцю бойка. При цьому вміст фіксаналу потрапляє через лійку у колбу (див.мал.). Збоку або зверху в ампулі є заглиблення, в якому пробивають отвір скляною паличкою з загостреним кінцем. Через цей отвір промивають дистильованою водою внутрішні стінки ампули. Промивати потрібно декілька разів малими порціями. Після цього споліскують зовнішні стінки ампули і ампулу викидають. Споліскують лійку і бойок ззовні і всередині. Обмивають верхню частину шийки вимірювальної колби.
Проводячи промивання слідкують за тим, щоб об’єм води в мірній колбі не перевищив 2/3 об’єму колби. Обережно коловими рухами перемішують розчин. Якщо фіксанал містив суху речовину перемішують до повного її розчинення. Потім розчин в колбі доводять водою до мітки. Щільно закривають колбу і перемішують розчин, перевертаючи її 12-15разів.
За точно взятою наважкою.
Розраховують наважку речовини за формулою: q прак. = CN * Vк * M екв / 1000
Речовину зважують на аптечних або техно-хімічних терезах.
На цих же терезах зважують годинникове скло або бюкс.
Речовину у бюксі або на годинниковому склі зважують на аналітичних терезах.
Висипають зважену речовину у вимірювальну колбу.
Зважують порожній бюкс або годинникове скло на аналітичних терезах.
Речовину розчиняють у воді, що займає 1/3 об’єму вимірювальної колби.
Розчин у колбі доводять водою до мітки. Щільно закривають колбу корком і перемішують,
перевертаючи колбу на 1800 12 -15 разів.
Розраховують концентрацію і титр одержаного розчину за формулами:
CN= q прак. * 1000 / Vк * M екв; T = CN * M екв / 1000
Приготування вторинно- стандартного розчину (лугу)
Розчин NаОН або КОН не можна приготувати точно заданої концентрації за точно взятою наважкою, так як тверда основа завжди містить воду та карбонати, звідси виходить, що кількість NаОН не буде відповідати взятій наважці.
Луги не можна розчинити у товстостінних бутлях, так як при розчиненні відбувається сильне розігрівання: бутель може лопнути.
Зважену на технохімічних терезах кількість лугу поміщають у велику фарфорову чашку чи склянку. В цей посуд наливають таку кількість води, щоб розчин мав концентрацію 35-40%. Перемішують розчин скляною паличкою, доки увесь луг не розчиниться. Потім розчин залишають стояти до охолодження і випадання осаду. Осад - це домішки (в основному карбонати), які не розчиняються у концентрованих розчинах лугів. Луг обережно зливають в інший посуд куди доливають потрібну кількість води.
Розчин лугу не завжди вдається приготувати заданої концентрації, тому, приготувавши розчин, потрібно визначити за допомогою ареометра його густину та по таблиці знайти відсотковий вміст лугу.
Приготування вторинно- стандартного розчину (кислоти)
Найчастіше в лабораторії застосовують хлоридну, сульфатну, оцтову та нітратну кислоти. Технічні кислоти містять багато домішок, тому для аналітичних робіт застосовують тільки чисті кислоти.
Потрібну кількість кислоти не відважують а відмірюють мірним циліндром.
При приготуванні розчинів кислот потрібно дотримуватися наступних правил:
1. Розчини не можна готувати в товстостінних бутлях тому, що при розведенні кислот, особливо сульфатної, відбувається сильне нагрівання. Розчини кислот готують у колбах.
2. У колбу наливається розрахована кількість води, а потім тоненьким струмочком, поступово, при перемішуванні приливають потрібну кількість кислоти. Кислоту та воду відмірюють вимірювальними циліндрами.
3. Після охолодження розчину, його переливають у бутель і наклеюють етикетку (паперову етикетку парафінують); можна зробити етикетку особливою фарбою на бутлях.
4. Якщо концентрована кислота, з якої беруть готувати розбавлений розчин, зберігається тривалий час, необхідно перевірити її концентрацію. Для цього вимірюють її густину ареометром і по таблиці знаходять точний вміст кислоти в розчині.
Стандартизація розчину (встановлення точної концентрації речовини у розчині титруванням)
метод піпеткування.
1. Точний об’єм досліджуваного розчину( або наважку речовини взяту на аналітичних терезах) помістити у вимірювальну колбу.
2. Розчин у колбі довести водою до мітки, перемішати.
3. Взяти для аналізу точний об’єм приготовленого розчину у колбу для титрування..
4. Протитрувати не менше 3 разів, розрахувати середній об’єм титранту.
5. Провести обчислення за формулами:
СN (дослідж.) = СN (титранту) * V (титранту ) / V(дослідж.)
q (дослідж.) = СN (дослідж.) * Vк * Mекв / 1000
W% = q * 100 % / а контр.
метод окремих наважок
1.Контрольний розчин ( або наважку речовини взяту на аналітичних терезах попередньо розчинити у воді) помістити у колбу Ерленмейєра.
2.Протитрувати його робочим розчином.
3.Провести розрахунки за формулами:
q (дослідж.) = СN (титранту ) * V (титранту) * Mекв (досліджуваного) / 1000
W% = q (дослідж.) * 100 % / а контр
