- •Міністерство освіти і науки, молоді та спорту України
- •Навчальний посібник до вивчення курсу «Основи проектування хімічних виробництв»
- •Оглавление
- •Глава 1 основные этапы и организация проектирования
- •Глава 2 состав исходных данных и основные стадии
- •Глава 3 системы автоматизированного проектирования 78
- •Глава 4 введение в проектирование 90
- •Глава 5 выбор и разработка технологической схемы
- •Глава 6 выбор технологического оборудования
- •Глава 7 уравнения материального баланса технологи-
- •Глава 8 технологический расчет основной и
- •Глава 9 тепловой расчет основного оборудования 141
- •Глава 10 гидравлические расчеты 166
- •Глава 11 механический расчет 175
- •Глава 12 конструкционные материалы в химическом
- •Глава 13 оформление отдельных элементов химической
- •Глава 14 трубопроводы и трубопроводная арматура 224
- •Глава 15 вспомогательное оборудование химических
- •Введение
- •Глава 1 основные этапы и организация проектирования химических производств
- •1.1. Перспективный план и технико-экономическое обоснование
- •1.2. Задание на проектирование
- •1.3. Выбор района размещения предприятия и площадки строительства
- •1.3. «Роза ветров» района размещения предприятия и площадки строительства
- •1.4. Основные принципы проектирования зданий и сооружений химической промышленности
- •1.5. Разработка проектной документации по охране окружающей среды
- •1.5.1. Экологическое прогнозирование
- •1.5.2. Разработка прогноза загрязнения воздуха
- •1.5.3. Прогнозирование состояния поверхностных и подземных вод
- •1.5.4. Прогноз воздействия объекта при возможных авариях
- •1.6. Технологический процесс как основа промышленного проектирования
- •1.7. Генеральный план химических предприятий
- •1.8. Типы промышленных зданий
- •1.8.1 Основные элементы конструкции производственных зданий и их назначение
- •1.8.2 Одноэтажные промышленные здания
- •1.8.3. Многоэтажные здания
- •1.8.4. Вспомогательные здания и помещения химических предприятий
- •1.8.5. Склады промышленных предприятий
- •1.9. Инженерные сооружения
- •1.10. Специальные вопросы проектирования химических предприятий
- •Глава 2 состав исходных данных и основные стадии
- •2.2 Виды конструкторских документов
- •2.3. Содержание разделов исходных данных для проектирования промышленного химического производства
- •Раздел 1. Общие сведения и технология
- •Раздел 2. Характеристика выполненных научно-исследовательских и опытных работ, положенных в основу исходных данных для проектирования
- •Раздел 3. Технико-экономическое обоснование рекомендуемого метода производства. Перспективы производства и потребления
- •Раздел 4. Патентный формуляр
- •Раздел 5. Техническая характеристика исходного сырья, вспомогательных материалов, основных и конечных продуктов. Целевое назначение и области применения основных продуктов
- •Раздел 6. Физико-химические корстанты и свойства исходных,
- •Раздел 7. Химизм, физико-химические основы и принципиальная
- •Раздел 8. Рабочие и технологические параметры производства
- •Раздел 9. Материальный баланс производства
- •Раздел 10. Технологическая характеристика побочных продуктов и
- •Раздел 11. Математическое описание технологических процессов и
- •Раздел 12. Данные для расчета, конструирования и выбора основного промышленного технологического оборудования и защиты строительных конструкций
- •Раздел 13. Рекомендации для проектирования автоматизации
- •Раздел 14. Аналитический контроль производства
- •Раздел 15. Методы и технологические параметры очистки химически и механически загрязненных сточных вод, обезвреживания газовых выбросов и ликвидации вредных отходов
- •Раздел 16. Мероприятия по технике безопасности, промсанитарии и противопожарной профилактике
- •Раздел 17. Указатель отчетов и рекомендуемой литературы по
- •2.4 Проектирование в системе подготовки
- •2.4.1 Курсовое проектирование
- •2.4.2. Дипломное проектирование
- •Глава 3 системы автоматизированного проектирования
- •3.1. История развития сапр
- •3.2. Основные принципы создания сапр
- •3.3 Применение эвм для автоматизации процесса пректирования
- •3.4. Автоматическое изготовление чертежей
- •3.5 Основные преимущества автоматизации проектирования.
- •3.6. Основные требования к сапр
- •3.7. Связь сапр с производством, расширение области применения
- •Глава 4 введение в проектирование
- •4.1. Проектно-сметная документация
- •4.2. Технико-экономическое обоснование проекта
- •4.2.1. Исходные положения
- •4.2.2. Обоснование способа производства химической продукции
- •4.2.3. Экономика строительства предприятия и производства продукции
- •Глава 5 выбор и разработка технологической схемы производства
- •5.1. Общие положения
- •5.2. Последовательность разработки технологической схемы
- •5.3. Принципиальная технологическая схема
- •5.4. Размещение технологического оборудования
- •Глава 6 выбор технологического оборудования химических производств
- •6.1. Основные типы химических реакторов
- •6.2. Химические факторы, влияющие на выбор реактора
- •6.2.1. Реакции расщепления
- •6.2.2 Реакции полимеризации
- •6.2.3. Параллельные реакции
- •6.2.4. Комбинация реактора смешения с реактором вытеснения
- •6.3. Эскизная конструктивная разработка основной химической аппаратуры
- •6.3.1. Общие положения
- •6.3.2. Реакторы
- •6.4. Оптимизация процессов химической технологии
- •Глава 7 уравнения материального баланса технологического процесса
- •7.1. Стехиометрические расчеты
- •7.2. Общее уравнение баланса массы
- •7.3. Практический материальный баланс
- •7.4. Физико-химические основы технологического процесса
- •Глава8 технологический расчет основной и вспомогательной аппаратуры
- •8.1. Общие положения
- •8.2. Расчет объемов реакторов
- •8.2.1. Основные положения химической кинетики
- •8.2.2. Расчет идеальных реакторов
- •8.3. Определение объемов аппарата
- •Глава 9 тепловой расчет основного оборудования
- •9.1. Общее уравнение баланса энергии
- •9.2. Практический тепловой баланс
- •9.3. Теплообмен в реакторах
- •9.4. Расчет энтальпий и теплоемкостей
- •9.5. Расчет реактора периодического действия
- •9.6. Степень термодинамического совершенства технологических процессов
- •Глава 10 гидравлические расчеты
- •10.1. Расчет диаметра трубопровода
- •10.2. Расчет гидравлических сопротивлений в трубопроводе
- •10.3. Гидравлическое сопротивление кожухотрубчатых теплообменников
- •10.4. Подбор насосов
- •Глава 11 механический расчет
- •11.1. Расчет сварных химических аппаратов
- •11.1.1. Основные расчетные параметры
- •11.1.2. Расчет на механическую прочность
- •11.1.3 Требования к конструированию.
- •11.1.4 Расчет цилиндрических обечаек.
- •11.1.6. Подбор стандартных элементов
- •11.2. Расчет толстостенных аппаратов
- •Глава 12 конструкционные материалы в химическом машиностроении
- •12.1. Виды конструкционных материалов
- •12.2. Коррозия металлов и сплавов
- •12.2.1. Виды коррозии
- •12.2.2. Виды коррозионных разрушений
- •12.2.3. Способы борьбы с коррозией
- •12.3. Влияние материала на конструкцию аппарата и способ его изготовления
- •12.3.1. Конструкционные особенности аппаратов из высоколегированных сталей
- •12.3.2. Конструктивные особенности эмалированных аппаратов
- •12.3.3. Конструктивные особенности аппаратов из цветных металлов
- •12.3.4. Конструктивные особенности аппаратов из пластмасс
- •Глава 13 оформление отдельных элементов химической аппаратуры
- •13.1. Оформление поверхности теплообмена
- •13.2. Перемешивающие устройства
- •13.3. Уплотнения вращающихся деталей
- •Глава 14 трубопроводы и трубопроводная арматура
- •Глава 15 вспомогательное оборудование химических заводов
- •15.1. Виды вспомогательного оборудования
- •15.2. Транспортные средства
- •15.2.1. Классификация транспортных средств для твердых материалов
- •15.2.2. Машины для транспортировки жидкостей и газов
- •Список рекомендованой литературы
- •1Вимоги до оформлення розрахунково-пояснювальної записки та графічної частини
- •1.1 Загальні вимоги
- •1.2 Вимоги до тексту
- •1.2.10. Оформлення ілюстрацій і додатків.
- •1.3 Оформлення графічної частини
- •2 Склад розрахунково-пояснювальної записки
- •3 Стандартизація і метрологія
- •4 Матеріалоємність і ресурсозбереження
- •5 Будівельна частина
- •5.1 Вибір майданчика для будівництва
- •5.2 Пов’язування технологічної лінії з об’ємно-планувальним рішенням промислової будови
- •5.3 Вибір конструктивного рішення будівлі
- •5.4 Допоміжні будівлі і приміщення
7.3. Практический материальный баланс
Практический материальный баланс учитывает составы исходного сырья и готовой продукции, избыток одного из компонентов сырья, степень превращения реагентов, потери сырья и готового продукта и т.д.
Исходными данными для составления такого баланса являются:
- технологическая схема, отражающая вид и последовательность стадий производства;
- годовая производительность по данному продукту или данному спектру продуктов;
- производственная рецептура загрузки компонентов на каждой технологической стадии;
- потери сырья и готового продукта на каждой технологической стадии производства.
В зависимости от характера требований материальный баланс периодичес
ких процессов может составляться в трех вариантах: во-первых, исходя из суточной производительности вещества; во-вторых, на единицу массы готового продукта (чаще всего на 1 т); в-третьих, на количество готового продукта, полученного за один цикл работы. В этом случае наиболее целесообразен суточный материальный баланс.
Для непрерывных процессов материальный баланс составляется с учетом выработки в единицу времени (т/год, т/сут, т/ч, кг/ч, кг/мин, кг/с и т.д.).
В любом случае баланс делится на две основные части - общий материальный баланс и пооперационный (постадийный) материальный баланс.
При общем балансе материальные расчеты связаны с определением расхо
дов всех видов сырья. В большинстве случаев такие расчеты завершаются определением расходных коэффициентов всех компонентов процесса на единицу массы готового продукта (например, на 1 т) и сравнением их с расходными коэффициентами аналогичного существующего производства. Первым этапом будет определение рабочего времени в цехе. Его величина зависит от характера производства. Для периодических процессов
Д = 365 - (Р + В),
где Д - количество рабочих дней в году; Р - количество дней в году, отведенных на все виды ремонта; В - количество праздничных и выходных дней в году.
Для непрерывных процессов
Д = 365 - Р.
В этом случае величина Р включает в себя и время на все виды ремонтов, и время периодических остановок на чистку оборудования, замену катализатора и т. п.
Далее необходимо определить производительность по готовому продукту. Вначале рассчитывается производительность без учета потерь
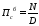
где
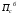 - суточная производительность по готовому
продукту без учета потерь, т/сут; N -
годовой выход готового продукта, т.
- суточная производительность по готовому
продукту без учета потерь, т/сут; N -
годовой выход готового продукта, т.
Производительность с учетом потерь продукта по стадиям
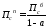
где а - общая доля потерь продукта на всех стадиях процесса.
Общая величина потерь по всем стадиям
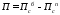
Определяя доли потерь по стадиям как аi можем найти их количество из соотно-
шения
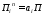
При этом
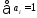
Далее определяется расход каждого вида сырья с учетом потерь, исходя из рецептуры загрузки компонентов реакционной смеси. При этом предварительно рассчитывается рецептура в процентах на содержание каждого компонента, полагая за 100% всю реакционную смесь. Потери реакционной смеси на каждой стадии в равной степени относятся к каждому из компонентов, если нет отгона одного из продуктов, выделения его в осадок и др.
К полученным расходам сырьевых компонентов добавляются их возмож-
ные потери до получения реакционной смеси при транспортировке, загрузке и т.д. Окончательно производят расчет расходных коэффициентов сырьевых ком-
понентов на тонну готового продукта. Результаты расчета расходных коэффициентов оформляются в виде таблицы (см. таблицу 7.1)
Таблица 7.1. Пример представления расходных коэффициентов
|
№ п/п |
Наименование сырья |
Расход, т/сут (т/год) |
Расходные коэффициенты, т/т готового продукта |
|
1 |
Компонент А |
А1 (А1 Д) |
А1/ |
|
2 |
Компонент В |
В1 (В1 Д) |
В1/ |
Кроме расходных коэффициентов сырья рассчитываются аналогичные величины, характеризующие расход воды, пара, топлива, электроэнергии и т.д. Естественно, чем меньше расходные коэффициенты, тем экономичнее технологический процесс.
Особое значение имеют расходные коэффициенты по сырью, так как для большин-
ства химических производств львиная доля себестоимости продуктов приходится на эту статью.
Постадийный материальный баланс составляется в виде таблиц на каждой стадии, исходя из результатов расчета общего материального баланса.
Пример 7.4. Составить материальный баланс реактора каталитического окисления метанола в формальдегид. Производительность реактора по формальдегиду 10 000 т/год. Степень превращения метанола в формальдегид - 0,7; общая степень превращения метанола (с учетом побочных реакций) - 0,8.
Содержание метанола в спирто-воздушной смеси - 40% по объему. Мольные соотношения побочных продуктов на выходе из реактора
НСООН : СО2: СО : СН4 = 1,8 : 1,6 : 0,1 : 0,3.
Аппарат работает 341 день в году с учетом времени ППР (планово-предупреди-
тельных ремонтов) и простоев.
Решение: Формальдегид получается в результате окисления паров метанола кислородом воздуха при температуре 550 - 600 °С на серебряном катализаторе, где протекают следующие реакции:
|
СН3ОН + 1/2О2 = СН2О + Н2О, |
(1) |
|
СН3ОН = СН2О + Н2, |
(2) |
|
СН3ОН = СО + 2Н2, |
(3) |
|
СН3ОН + Н2 = СН4 + Н2О, |
(4) |
|
СН3ОН + О2 = НСООН + Н2О, |
(5) |
|
СН3ОН + 1,5О2 = СО2 + 2Н2О. |
(6) |
Возможная реакция Н2 + 1/2О2 = Н2О стехиометрически зависима, так как она в сумме с реакцией (2) дает реакцию (1), поэтому ее нужно из балансовых расчетов исключить.
На реакцию подается лишь около 80% воздуха от мольного соотношения метанол : кислород = 2 : 1 и процесс проводится с неполным сгоранием водорода, образую-
щегося по реакции (3).
Отходящие газы содержат 20 - 21% формальдегида, 36 - 38% азота и примеси в ви-
де СО, СО2, СН4, СН3ОН, НСООН и др. Вся эта смесь после охлаждения в котле-утилизаторе и холодильнике до 60 °С подается в поглотительную башню, оро-
шаемую водой. Полученный раствор формалина содержит 10 - 12% метанола, который в данном случае является желательной примесью, так как препятствует по-
лимеризации формальдегида. Молекулярные массы: формалина - 30; метанола - 32; кислорода - 16.
Производительность реактора по формальдегиду
10 000∙1000/341/24 = 1222 кг/ч или 1222/30 = 40,73 кмоль/ч.
Так как по реакциям (1) и (2) на образование 1 моля формальдегида расходуется 1 моль метанола, то, при 70% степени превращения метанола в формальдегид, имеем расход метанола:
40,7/0,7 = 58,143 кмоль/ч или 58,143 ∙32= 1860,6 кг/ч.
Определим объемные расходы исходных веществ при нормальных условиях.
Метанол - 58,143 ∙22,4= 1302,4 м3/ч.
Спирто-воздушная смесь - 1302,4/0,4 = 3256 м3/ч.
Воздух - 3256 – 1302,4 = 1953,6 м3/ч, в нем:
кислорода – 1953,6 ∙0,21 = 410,26 м3/ч или 410,26 ∙32/22,4 = 586 кг/ч;
азота – 1953,6 ∙0,79 = 1543 м3/ч или 1543 ∙28/22,4 = 1929 кг/ч.
Определим расход метанола, пошедшего на образование побочных продуктов по реакциям (3) - (6). При общей степени превращения метанола 80% имеем расход метанола по побочным реакциям
58,143 ∙(0,8 - 0,7) = 5,81 кмоль/ч.
Не прореагировало метанола
58,143∙ 0,2 = 11,63 кмоль/ч или 11,63∙32 = 372 кг/ч.
Сумма долей побочных продуктов 1,8+ 1,6 + 0,1 + 0,3 = 3,8.
Тогда расходы побочных продуктов в отходящих газах будут равны:
Уксусная кислота
(НСООН) - 5,8∙1,8/3,8 = 2,75 кмоль/ч или 2,75∙46 = 126,5 кг/ч.
Диоксид углерода (СО2) - 5,8∙1,6/3,8 = 2,45 кмоль/ч или 2,45∙44 = 108,0 кг/ч.
Оксид углерода (СО) - 5,8∙0,1/3,8 = 0,158 кмоль/ч или 0,158∙28 = 4,3 кг/ч.
Метан (СН4) - 5,8∙0,3/3,8 = 0,459 кмоль/ч или 0,459∙16 = 7,3 кг/ч.
Для определения расходов водяного пара и водорода составим баланс по кислороду и водороду.
В реактор поступает кислорода:
с воздухом - 586 кг/ч;
в составе метанола – 1860,6∙16/32 = 930 кг/ч.
Всего: 586 + 930 = 1516 кг/ч.
Расходуется кислорода:
на образование формальдегида -1220∙16/30 = 650 кг/ч;
на образование НСООН - 126,5∙32/46 = 88 кг/ч;
на образование СО2 - 108∙32/44 = 78,6 кг/ч;
на образование СО - 4,3∙16/28 = 2,45 кг/ч;
в составе не прореагировавшего метанола - 372 16/32 = 186 кг/ч.
Всего: 1005 кг/ч.
Остальное количество кислорода, равное 1516 -1005 = 509 кг/ч, пошло на образование воды по реакциям (1), (4), (5) и (6). В результате расход воды равен - 509∙18/16 = 572 кг/ч.
В реактор поступает водорода - 1860∙4/32 = 233 кг/ч.
Водород расходуется:
на образование СН2О - 1220∙22/30 = 81,5 кг/ч;
на образование НСООН - 126,5 2/46 = 5,5 кг/ч;
на образование СН4 - 7,3∙4/16 = 1,82 кг/ч;
на образование Н2О - 572 2/18 = 63,6 кг/ч;
в составе не прореагировавшего газа - 372∙4/32 = 46,5 кг/ч.
Всего: 198,9 кг/ч.
Количество водорода в свободном состоянии: 233 - 198,9 = 34,1 кг/ч.
Результаты расчета сведены в табл. 7.2 материального баланса.
Таблица 7.2. Материальный баланс процесса получения формальдегида
|
Приход |
Расход | |||||
|
Статьи |
кг/ч |
% |
Статьи |
кг/ч |
% | |
|
|
(по массе) |
|
(по массе) | |||
|
Спирто-воз- |
|
|
Формальдегид |
1220,0 |
27,89 | |
|
душная смесь. |
|
|
Метанол |
372,0 |
8,58 | |
|
метанол |
1860 |
42,6 |
Водяной пар |
572,0 |
13,12 | |
|
кислород |
586 |
13,4 |
НСООН |
126,5 |
2,90 | |
|
азот |
1920 |
44,0 |
СО2 |
108,0 |
2,47 | |
|
|
|
|
СО |
4,3 |
0,09 | |
|
|
|
|
Метан |
7,3 |
0.16 | |
|
|
|
|
Водород |
34,1 |
0,78 | |
|
|
|
|
Азот |
1920,0 |
43.97 | |
|
|
|
|
Ошибки |
|
| |
|
|
|
|
округления |
1,8 |
0,04 | |
|
Итого |
4366 |
100,0 |
Итого |
4466,0 |
100,00 | |