- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Характер соединений оксидов ме
II группы главной подгруппы
Оксидов
|
|
BeO |
MgO |
CaO |
SrO |
BaO |
Ra | ||||
|
Агрегатное состояние |
Белые тугоплавкие вещества | |||||||||
|
Характер |
Амфотерный |
Основные свойства увеличиваются | ||||||||
|
Химические свойства |
+ |
——— |
медленно |
| ||||||
|
|
| |||||||||
|
+ |
| |||||||||
|
+ |
| |||||||||
|
|
| |||||||||
Гидроксидов
|
|
|
|
|
|
|
| |||||
|
Агрегатное состояние |
Белые тугоплавкие вещества | ||||||||||
|
Характер |
Амфотерный |
Основные свойства увеличиваются | |||||||||
|
Химические свойства |
+ |
очень плохо |
слабо |
хорошо растворяются | |||||||
|
+ |
| ||||||||||
|
|
слабо |
| |||||||||
|
3 | |||||||||||
Жесткость воды
|
|
Обусловлена наличием в ней ионов Сa2+, Mg2+ |
|
|
Временная
Карбонатная
|
|
Постоянная
Некарбонатная
CaCl2, CaSO4, MgCl2, MgSO4 |
|
|
"Смягчение воды" |
|

|
|
Удаление ионов Сa2+, Mg2+ из воды |
| |
|
|
|
| |
|
| ||
|
| |||
|
| |||
|
|
Добавлением соды
| ||
|
| |||
Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
|
Символ химического элемента |
Содержание в земной коре, % |
Основные соединения |
Валентные
|
R ат. |
R иона |
Восстановительные свойства |
Степень окисления |
|
B |
3 |
|
2s22p1 |
увеличивается ← |
увеличиваются → |
увеличиваются ← |
↑ +3 ↓ |
|
Al |
8,8 |
|
3s23p1 | ||||
|
Ga |
1,5 |
редкие,
рассеянные элементы, являются примесями природных соединений Zn, Pb, Fe |
4s24p1 | ||||
|
In |
1 |
5s25p1 | |||||
|
Tl |
3 |
6s26p1 |
+1,
+3 |
Сравнительная характеристика физических свойств простых веществ
|
Формула простого вещества |
Агрегатное состояние |
Цвет |
Свойства |
Твердость |
Т пл.,°С |
Т кип.,°С |
Химическая активность |
Образование химических связей | ||||
|
В неметалл |
аллотропия |
|
черный, темно-серый, коричневый |
Плохо проводит эл. ток, но при to проводимость увеличивается резко |
увеличиваются → |
увеличивается |
← |
2075 |
увеличивается → |
3700 |
инертен |
ковалентные |
|
Аl переходный |
твердый |
серебристо-белые |
тепло-, электропроводны, легкоплавкие, легкие, пластичные |
← |
660 |
|
амфотерен | |||||
|
мягкие |
увеличиваются металлические свойства ← | |||||||||||
|
2247 | ||||||||||||
|
Ga металл |
29,8 | |||||||||||
|
2070 | ||||||||||||
|
156,4 | ||||||||||||
|
In металл | ||||||||||||
|
304,0 |
1487 | |||||||||||
|
Tl металл | ||||||||||||
|
|
B |
Al |
Ga |
In |
Tl | ||
|
ОКСИДЫ |
получение |
4B
+ 3 |
4Al
+ 3 белый |
4Э
+ 3 белый |
4Tl
+ 3 черный
| ||
|
+ |
|
| |||||
|
кислотный |
амфотерный |
амфотерный, но преобладают кислотные свойства |
амфотерный, но преобладают основные свойства |
| |||
|
+ |
|
——— | |||||
|
+ |
——— |
| |||||
|
ГИДРОКСИДЫ |
формулы |
кислотный |
амфотерный |
амфотерный, но преобладают кислотные свойства |
амфотерный, но преобладают основные свойства |
TlOH — желтый основные | |
|
+ |
4
бура |
гидроксоалюминат калия |
|
очень конц.
|
——— | ||
|
+ |
——— |
| |||||
|
|
TlOH
+ HCl → TlCl +
| ||||||














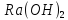



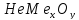

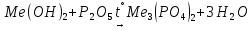
















 —бура
—бура
 —боксит
—боксит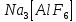 —криолит
—криолит —корунд
—корунд












 —черный
—черный







 —б/цв
кристаллы
—б/цв
кристаллы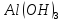 —белый
—белый —белый
—белый —белый
—белый —коричневый
—коричневый