
- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Химические свойства воды ()
|
С простыми веществами |
+
щелочные → 2Na + 2
щелочно-
→ Ca + 2 земельные Ме
+
другие Ме → 2Fe + 3 |
|
+
Hal2→
| |
|
Со сложными веществами |
основной
+
оксиды кислотный
|
|
гидролиз
+ соль
образование
кристалло- б/цв. голубой гидратов | |
|
+
гидрид активного Ме
| |
|
+
органические вещества
этилен этиловый спирт |
Очистка воды
От растворенных солей:

временная жесткость
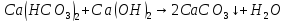 осаждение
осаждение
постоянная жесткость солей

От взвесей — добавление

 —клейкий
осадок захватывает взвеси
—клейкий
осадок захватывает взвеси
От крупных частиц
От жидкостей, не смешивающихся с водой
От жидкостей, хорошо растворимых в воде, имеющих разные t° кипения
Растворы
Гомогенные системы переменного состава, состоящие из двух и более
компонентов
Раствор = Растворитель = Вещество, расворенное в нем
Растворимость веществ
Это свойство веществ распространяться в растворителе
|
Вещества по растворимости в воде | ||
|
растворимые |
мало растворимые |
нерастворимые |
|
Твердые вещества | ||
|
сахар, медный купорос |
гипс, сульфат свинца |
стекло, кремнезем, золото |
|
Жидкие вещества | ||
|
спирт, ацетон |
диэтиловый спирт |
керосин, растительное масло |
|
Газообразные вещества | ||
|
хлороводород, аммиак |
метан, азот, кислород |
инертные газы |

















|
1 |
|
2 |
|
3 |
Растворение твердых веществ в жидкости
Растворитель
Твердое вещество
Ионы или молекулы
(отрываются с поверхности)
Количество растворенного вещества
|
|
|
|
|
|
|
|
|
| ||
|
ненасыщенный раствор |
насыщенный раствор — максимально возможное количество растворенного вещества при данной t° |
пересыщенный раствор — неустойчивый при данной t° |

|
|
|
|
|
| |
|
избыток |
твердое вещество |
растворение
кристаллизация
|
вещество в растворе |
над твердым веществом | |
|
|
|
|
|
| |
|
Концентрация насыщенного раствора — мера растворимости вещества Коэффициент растворимости (растворимость) вещества выражается максимальным числом граммов вещества, которое можно растворить в 100 г растворителя при данной t°
| |||||
Концентрации растворов
|
|
|
|
|
V — объем раствора = 1 литр |

 → 2NaOH +
→ 2NaOH +

 →
→
 +
+











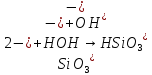


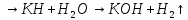





 —
35,9 г NaCl
—
35,9 г NaCl


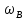 —массовая доля
растворенного вещества
—массовая доля
растворенного вещества —масса растворенного
вещества
—масса растворенного
вещества —масса раствора
—масса раствора —доля от единицы
—доля от единицы

 —молярная
концентрация (молярность)
—молярная
концентрация (молярность) —число молей
вещества
—число молей
вещества