
- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Аллотропия серы (s)
 —сера
ромбическая
—сера
ромбическая
 —сера
моноклинная
—сера
моноклинная
лимонно-желтая
tплавления=112,8
 =2,07
г/см3
=2,07
г/см3
темно-желтая
tплавления=119,3
 =1,96
г/см3
=1,96
г/см3
|
Кристаллы разной формы из S8 |
охлаждение
Пластическая Sx
Плохо
растворяется в

Хорошо растворяется в CS2
В парх: S8, S6, S4, S2, S
Соединения серы (s)
|
+6 |
+4 |
–2 |
|
Бесцветная жидкость, затвердевает
при t<17 |
S Бесцветный газ с резким запахом |
Бесцветный газ с запахом тухлых яиц, ядовит, поражает нервную систему |
|
2S |
(конц.) |
|
|
S |
S |
|
|
S изб.
S изб. кислоты) |
S изб.
S изб. кислоты) |
2 недост. 2 изб.
|
|
S | ||
|
+2 +4 o +4 2CO
+ S S | ||
|
S | ||
|
S S |
Кислоты серы (s)
|
+6 |
+4 |
–2 |
|
серная |
сернистая |
сероводородная |
|
тяжелая, бесцветная, маслянистая жидкость, гигроскопична, нелетуча, не имеет запаха,. не проводит электрический ток |
существует только в растворе, непрочное соединение |
неустойчивая, на свету мутнеет, так как 2
|
|
S В растворе: (сильная кислота)
|
S 40V
: 1V при
t=20 В растворе: (средней силы кислота)
|
1V
кислота
—
В растворе: (слабая кислота)
|
|
Общие химические свойства кислот +Me
(до ( основной основание | ||
|
6 конц. обугливание 4 конц. |
Качественная
реакция на
|
Качественная
реакция на
|
|
"вскипание" |
Почти все осадки (сульфиды) — цветные | |
|
Качественная
реакция на
| ||
|
белый | ||
Производство
Сырье:
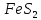 —
железный колчедан или пирит
—
железный колчедан или пирит
S — самородная
 —сероводород
— отходы цветной металлургии и коксования
—сероводород
— отходы цветной металлургии и коксования
 и
др. — сульфиды цветных металлов
и
др. — сульфиды цветных металлов
I
стадия производства Получение S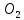

4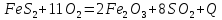
тв.
 ,
насыщение воздуха
,
насыщение воздуха
 ,
"кипящий слой"
,
"кипящий слой"Печь для обжига колчедана, циклон, электрофильтры, сушильная башня

II
стадия производства S
2S +
+
газ газ
cat —
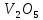 ,
,
Теплообменник, контактный аппарат (теплообмен, противоток)

III
стадия производства Гидратация S
S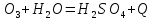
Поглотительная
башня (противоток, увеличение поверхности
соприкосновения реагирующих веществ)
Научные принципы
Непрерывность
Создание оптимальных условий
Применение катализатора
Утилизация теплоты химических реакций
Теплообмен
Противоток
Измельчение, увеличение поверхности соприкосновения реагирующих веществ
Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
|
Символ химического элемента |
Принадлежность к классу |
Содержание в земной коре, % |
Основные соединения |
Валентные
|
R ат. |
Электро-отрицатель-ность |
Образование хим. связей |
Степень окисления | ||||||||||
|
F |
неметаллы |
2,7 |
фосориты,
|
2s22p5 |
увеличивается |
← |
увеличиваются неметаллические свойства, электроотрицательность |
→ |
ковалентная, ионная (с Ме) |
–1 | ||||||||
|
Cl |
4,5 |
|
3s23p5 |
↑ –1 0 +3 +5 +7 ↓ | ||||||||||||||
|
Br |
1,6 |
NaBr,
KBr,
бромиды |
4s24p5 | |||||||||||||||
|
J |
3 |
NaJ, KJ — иодиды |
5s25p5 | |||||||||||||||
|
At |
радиоактивный |
——— |
6s26p5 | |||||||||||||||
|
|
| |||||||||||||||||

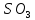



 +
+





 — кислотный
оксид
— кислотный
оксид —
кислотный оксид
—
кислотный оксид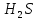 —восстановитель
—восстановитель соли
соли
 (серной
(серной соли
соли
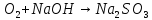 (сернистой
(сернистой
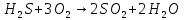

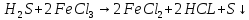
 — окислитель
— окислитель

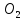 — восстановитель
— восстановитель






 —гидросульфат
ион
—гидросульфат
ион —сульфат
ион
—сульфат
ион

 —гидросульфит
—гидросульфит —сульфит
ион
—сульфит
ион : 2,5V
: 2,5V
 приt=20
приt=20

 —гидросульфид
ион
—гидросульфид
ион —сульфид
ион
—сульфид
ион )),
)),
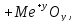
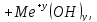 +соль
+соль




 запах
запах ярко-желтый
ярко-желтый черный
черный



 —
плавиковый шпат, апатиты
—
плавиковый шпат, апатиты
 —сильвинит
—сильвинит —карналит
—карналит
 —
—
