
- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Железо (Fe) — представитель химических элементов побочных подгрупп
|
Содержание в земной коре, % |
Основные природные соединения |
№ химического элемента |
Z ядра |
Электронная формула |
Схема распределения
|
Степень окисления |
|
5,10 |
(магнитный железняк)
(красный железняк)
(бурый железняк) FeC (шпатовый железняк) Самородное Fe
|
26 |
+26 |
1s22s22p63s23p63d64s2 |
|
+6 +4 +3 харак- +2 терные 0 |
Железо (Fe) — простое вещество
|
Цвет |
Связь |
Кристал. решетка |
Свойства |
г/см3 |
Тпл., |
Ткип., | ||||
|
серебристо-белый |
металлическая |
электро-, теплопроводно, мягкое, пластичное, обладает магнитными свойствами |
7,87 |
1539 |
2770 | |||||
Химические свойтсва () — восстановитель
|
Взаимодействие с простыми веществами |
+ |
O
←
о
+3 +2
+2 3Fe
+ 2
O
←
| |
|
+не Ме |
+ |
o o +3 – 2Fe
+ 3 | |
|
+S |
o o +2 –2 Fe
+ S
| ||
|
+ |
o o +3 –3 Fe
+
| ||
|
+C |
o o Fe
+ C
| ||
|
|
и др. | ||
|
Взаимодействие со сложными веществами |
+ |
3Fe
+ 4 пар o +3 4Fe
+ 6 | |
|
+ разб. |
o +2 4Fe
+ 10HN | ||
|
+ не оч. конц. |
o +3 Fe
+ 4HN o +3 2Fe
+ 6 | ||
|
+соль |
| ||
Соединения железа в степени окисления
|
+2 |
+3 | |||||
|
Оксиды |
формула |
|
черно-фиолетового | |||
|
получение |
( |
2 | ||||
|
характер |
основной |
амфотерный, но основные свойства выражены сильнее | ||||
|
+ |
——————— |
——————— | ||||
|
+ |
|
| ||||
|
+ |
——————— |
феррит | ||||
|
Гидроксиды |
формула |
Fe
|
на воздухе
белый → зеленый → |
| ||
|
получение |
| |||||
|
|
| |||||
|
+ |
|
| ||||
|
+ |
|
| ||||
|
+ |
————— |
| ||||
Продолжение
|
Соли |
цвет |
бесцветный |
желтый | ||
|
+ |
хорошо гидрализуются по катиону | ||||
|
|
| ||||
|
окислительно-восстановительные процессы |
Восстановительные свойства | ||||
|
+2 +7 10
FeS +3 +2
|
+3 0 2 +3
| ||||
|
Окислительные свойства | |||||
|
——————— |
2Fe | ||||
|
+соль |
Fe
|
2Fe
| |||
|
+Ме более акт. |
|
| |||
|
+ |
FeS
+ 2 |
| |||
|
|
2 желтая кровяная соль |
+ → |
2 | ||
|
качественная реакция |
FeS
|
Fe
| |||
|
темно-синий (берлинская лазурь) | |||||
|
|
|
тиоцинат кроваво-красный раствор | |||


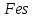 —пирит
—пирит
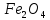 —магнезит
—магнезит —гематит
—гематит —гетит
—гетит —
сидерит
—
сидерит ,
,

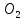
 О
О




 —хлоридFe
—хлоридFe —сульфидFe
—сульфидFe

 —нитридFe
—нитридFe —карбидFe
—карбидFe

 —
ржавчина
—
ржавчина
 ,
где
,
где
 —
HCl,
—
HCl,


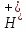





 —черный
—черный
 от
красного до
от
красного до 

 (
( )
)



 +
6
+
6





 бурый
бурый →4
→4















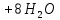





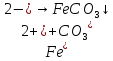





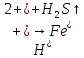



 + 2KCl
красная
кровяная соль
+ 2KCl
красная
кровяная соль +
+


 K
K



 K
K
