
- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Производство чугуна
|
№ |
Сырье |
Химические реакции, лежащие в основе производства |
Продукты процесса |
Применение образующихся продуктов |
|
1 |
Подготовка сырья: измельчение, агломерация, офлюсовывание |
в регенератор |
А. доменный газ |
|
|
2
а |
Шихта
флюсы |
CaO
+ Si 3CaO
+
|
Б. шлаки |
Строительное дело, сельское хозяйство |
|
б |
обогащенная руда (концентрат)
примеси |
3Fe
+ C =
MnO + C = Mn + CO
|
В. чугун Fe
Si, Mn, P, S |
Переработка в сталь |
Продолжение
|
в
3
4 |
кокс
воздух,
↑ обогащенный кислородом t°=1000° природный ↑ газ |
|
|
|
|
Научные принципы организации производства
| ||||
Производство стали
СЫРЬЕ



|
СаО |
железная руда |
железный лом |
передельный чугун |
Способы получения стали
|
Способ |
Кислородно-конвертерный |
Мартеновский |
В электропечах |
|
Источник тепла |
Экзотермические реакции окисления примесей |
Газообразное или жидкое топливо (мазут) |
Электродуга
(без
|
|
Местонахождение источника тепла |
В шихте |
Над шихтой |
Между электродом и шихтой |
|
t° |
~1600°С |
~2000°С |
~2500°С |
|
Время плавки |
30–40 минут |
6–8 часов |
|
|
Выход за одну плавку |
~300 тонн |
~900 тонн |
~350 тонн |
|
Недостатки |
Периодичность |
Низкое качество стали |
Большая электрозатрата |
|
Достоинства |
|
Можно регулировать подачу топлива ↓ Можно регулировать t° ↓ Разные сорта стали |
Высококачественные легирующие стали |
Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
2Fe +
 FeO — основной
окислитель примесей
FeO — основной
окислитель примесейОкисление примесей
Si
+ 2FeO → Si
Mn + FeO → MnO + Fe + Q
2P
+ 5FeO →

C + FeO → CO + Fe – Q
Удаление примесей
Si
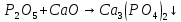 или
или
 —используют
как фосфорное удобрение
—используют
как фосфорное удобрение
FeS + CaO → CaS↓ + FeO
MnO
+ Si
Удаление избытка FeO, регулирование содержания Mn, Si, C. Добавление раскислителей (ферромарганец, ферросилиций, алюминий).
Mn
+ FeO

↓
в шлак
Условия производства
Применять воздух, обогащенный
 ,
или полностью заменить его на
,
или полностью заменить его на .
.Увеличение поверхности реагирующих веществ.
Увеличить температуру процесса для уменьшения расхода топлива и увеличения скорости всех реакций.








 ,
,

























 восстано-
восстано-
 вители
вители )
)