- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Химическая связь
|
Виды химической связи |
Ионная |
Металлическая |
Ковалентная |
Водородная | |||||
|
Полярная |
Неполярная |
Донорно-акцепторная |
| ||||||
|
Природа соединяющихся частиц |
Активные
металлы и активные неметаллы
|
Атомы металлов |
Атомы
разных неметаллов
|
Атомы с равной электроотрица-тельностью
|
Атомы неметаллов А□
+ В□ донор акцептор А□В |
Молекулы или части одной молекулы | |||
|
Механизм образования связей |
Передача электронов более электроотрица-тельному атому А□
+ В□ взаимодействие ионов |
Обобществление электронов и свободное перемещение их в поле ядер атомов металла
+
+ +
+
+ +
|
Общие электронные пары принадлежат двум атомам |
Притяжение сильно поляризованного атома водорода одной молекулы к неподеленным электронам электроотрица-тельного элемента (O, N, F) другой молекулы | |||||
|
Общие электроны до соединения принадлежали разным атомам |
Общие электроны до соединения принадлежали одному из атомов | ||||||||
|
А□
+ В□
Общая электронная пара смещена к элементу с большей электроотрица-тельностью |
А□
+ В□ А□В |
| |||||||
|
Примеры |
NaCl, CuSO4 |
|
HCl, H2O |
O2,
|
H
|
H→
| |||
Типы кристаллических решеток
|
Химическая связь
|
|
?
?
физические
свойства
?
?
|
|
ионная связь |
t°
высокая +
– → + –
–
+
+ Н2О
→ +
– ионная
кристаллическая решетка гидратная оболочка | |
|
ковалентная связь |
+
Н2О
→ + – NH3
HCl молекулярная низкая кристаллическая решетка t° кипения, t° плавления ±
±
+
Н2О
→ J2,
N2,
O2 ±
±
| |
|
высокая
° кипения, t°
плавления A
A
высокая твердость
A
A
алмаз гранит , Н2О, Q соединения атомная кристаллическая решетка Si, B | ||
|
металлическая связь |
Me+
Me+
пластичность электро- и
теплопроводность
Q
Me+
Me+
металлическая кристаллическая решетка |


 или мало активных металлов
или мало активных металлов



 А–В
А–В








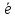












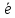







 □
□ А→В
А→В




 А–В
А–В

 ,
,