
Meditsina_neotlozhnykh_sostoyany_3
.pdf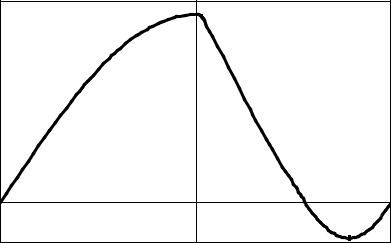
80 |
Медицина неотложных состояний. Избранные клинические лекции. Том 3 |
|
|
есть регулируемый по объему) или когда истечет заданное время вдоха (тайм-циклический респиратор, то есть регулируемый по частоте дыханий), вдувание прекращается и начинается пассивный выдох (под действием эластических сил, возникающих в грудной клетке), при этом давление в дыхательных путях снижается постепенно до 0. Таким образом, давление в дыхательных путях изменяется от 0 до определенных положительных величин (при неповрежденных легких это давление составляет 15–20 мм вод.ст. и зависит от растяжимости легких и каркаса грудной клетки), отсюда и название режима — перемежающееся положительное давление.
Исторический интерес представляет режим ИВЛ с активным выдохом, ныне практически не применяемый. Этот режим мы рассмотрим и из-за его исторического аспекта, а также для иллюстрации еще одного механизма вентиляционной ОДН. Кривая давления при этом режиме ИВЛ выглядит так, как показано на рис. 3.
В конце выдоха респиратор создает отрицательное давление (разрежение), что призвано удалить больше воздуха из легких и увеличить тем самым альвеолярную вентиляцию. Такой метод применялся при выраженном отеке мозга, особенно при нейрохирургических операциях, когда отечный мозг создает трудности для работы нейрохирурга. Как отмечалось выше, увеличение альвеолярной вентиляции ведет к гипокапнии, а она, в свою очередь, к вазоконстрикции в головном мозге,
Вдох |
Выдох |
|
|
р |
|
|
t |
0 |
|
Рисунок 3. Изменение давления в дыхательных путях |
|
|
при использовании активного выдоха |
Острая дыхательная недостаточность |
81 |
|
|
что и снижает степень отека. Однако такой режим можно применять лишь кратковременно и только у пациентов с неповрежденными легкими, а лучше не применять вовсе.
Для понимания последствий применения активного выдоха нужно вспомнить, что в легких существует определенное транспульмональное давление (как и в любом органе имеется свое трансорганное давление), которое действует, в частности, и на стенки бронхиол.
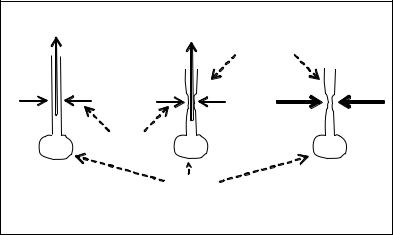
При создании респиратором разрежения в конце выдоха давление в бронхиоле становится ниже транспульмонального (ТПД), и только стенка бронхиолы здорового легкого в состоянии противостоять возникшей разнице между ТПД и атмосферным давлением, предупреждая спадение бронхиолы (рис. 4А). При ряде повреждений легких искусственный активный выдох может привести к схлопыванию бронхиолы под действием возросшей разницы между ТПД и атмосферным давлением, в результате чего остаточный объем воздуха в альвеоле увеличится, а альвеолярная вентиляция уменьшится (рис. 4Б). Такое явление носит название «экспираторное закрытие дыхательных путей» (ЭЗДП). Длительное проведение ИВЛ в режиме активного выдоха у больных с различными повреждениями легких (как острыми, так и хроническими) приведет к повышению воздушности альвеол, то есть к эмфиземе,
иухудшит альвеолярную вентиляцию. Механизму ЭЗДП способствует
иповышенная скорость выдоха.
Активный выдох |
Активный выдох |
|
ТПД |
|
Альвеола |
А. Здоровые легкие |
Б. ЭЗДП при |
|
активном выдохе |
Бронхиола
Форсированный выдох
В. ЭЗДП при бронхиальной астме
Рисунок 4. Механизмы экспираторного закрытия дыхательных путей
82 |
Медицина неотложных состояний. Избранные клинические лекции. Том 3 |
|
|
ЭЗДП может развиться и у больных с бронхиальной астмой, при которой, как известно, затруднен выдох. Больной вынужден форсировать выдох, что приводит к росту ТПД, то есть опять-таки растет разница между ТПД и атмосферным давлением (рис. 4В). Именно ЭЗДП является основной причиной эмфиземы легких у пациентов с бронхиальной астмой.
Как и всякое воздействие ИТ, ИВЛ должна проводиться под интенсивным наблюдением. Прежде всего должен контролироваться газовый состав крови. Уже давно оставлена «мода» проводить ИВЛ в режиме так называемой умеренной гипервентиляции, когда РCO2 поддерживается чуть ниже нормы. В настоящее время ИВЛ проводят исключительно в режиме нормовентиляции, поддерживая РaCO2 на нормальном уровне (35–45 мм рт.ст.), поскольку, как отмечено выше, гипокапния приводит к вазоконстрикции в головном мозге и, следовательно, к его ишемии и гипоксии. При изолированных нарушениях вентиляции адекватная ИВЛ атмосферным воздухом обеспечивает достаточный уровень РO2. В других случаях требуются дополнительные методы, о которых речь пойдет ниже.
Принципы ИТ диффузионной ОДН
Поскольку основным механизмом диффузионной ОДН является затруднение проникновения кислорода из альвеолы в кровь через измененную альвеолокапиллярную мембрану, естественно предположить, что основные усилия должны быть направлены на нормализацию свойств этой мембраны. Однако, к сожалению, как это сплошь и рядом бывает в практике ИТ, на это может потребоваться слишком много времени, в течение которого больной может успеть погибнуть несколько раз. Следовательно, пока мы восстанавливаем свойства альвеолокапиллярной мембраны, необходимо обеспечить достаточную скорость диффузии кислорода из альвеолы в кровь.
Как показано выше, скорость диффузии зависит от градиента концентраций (давлений) газов по обе стороны от мембраны, свойств мембраны и диффузионной способности газов. На последнюю влиять невозможно (поскольку диффузионная способность определяется физико-химическими свойствами диффундирующих веществ), изменение свойств мембраны занимает слишком много времени, и только первый из перечисленных факторов (градиент концентраций (давлений) газов по обе стороны от мембраны) является легко управляемым. Кроме того, нельзя забывать, что диффузия CO2 практически не страдает в силу его высокой диффузионной способности.
Острая дыхательная недостаточность |
83 |
|
|
Простейшим способом повышения градиента концентрации (давления) кислорода по обе стороны мембраны является ингаляция чистого кислорода под атмосферным давлением. Как было показано в табл. 1, РO2 в альвеоле тогда составит 650 мм рт.ст., а РvO2 равно ≈40 мм рт.ст. В этом случае градиент давлений кислорода составит около 590 мм рт.ст., тогда как в обычных условиях он равен ≈ 60 мм рт.ст. (практически в 10 раз меньше!). К сожалению, по изложенным выше причинам длительно ингалировать чистый кислород крайне опасно, и в клинических условиях максимальное FiO2 не должно превышать 0,4. При этом РO2 в альвеоле составит 760 ×0,4 = 304 мм рт.ст., а градиент концентраций — около 260 мм рт.ст. При тяжелых нарушениях диффузии этого градиента может оказаться недостаточно.
В этом случае прибегают к механическому способу повышения давления кислорода в альвеоле, используя специальный режим спонтанного дыхания, называемый «положительное давление в конце выдоха»
(ПДКВ). Суть метода заключается в том, что кривая давления в дыхательных путях при спонтанном дыхании (рис. 1) поднимается на определенную величину, равную ПДКВ (эта величина колеблется обычно от 5 до 15 см вод.ст.). Кривая давления в дыхательных путях при режиме ПДКВ показана на рис. 5, из которого видно, что этот режим обеспечивает постоянный «подпор» давления воздуха и, следовательно, кислорода, поэтому градиент давлений кислорода по обе стороны мембраны увеличивается. Режим ПДКВ препятствует ЭЗДП, так как, с одной стороны, дополнительное давление препятствует спадению бронхиолы под действием ТПД, а с другой — замедляется скорость выдоха, что также препятствует спадению бронхиолы. Кстати, мы порой неосознанно сами себе создаем этот режим после тяжелой физической работы или эпизода эмоционального напряжения, выдыхая через сомкнутые губы (когда «отдуваемся», при этом получается звук вроде «Уфффф!»).
Существует много методик создания режима ПДКВ, но наиболее простая и точная заключается в следующем (рис. 6).
Больной вдыхает воздух из атмосферы, а выдыхает в шланг, погруженный на определенную глубину в ведро с водой. Давление воды на уровне, до которого опущен шланг, можно посчитать по известной формуле сgh, а если это давление выразить в сантиметрах водного столба, то достаточно измерить глубину погружения шланга. Для обеспечения величины ПДКВ в 5–15 см вод.ст. шланг нужно погрузить на глубину 5–15 см.

84 |
Медицина неотложных состояний. Избранные клинические лекции. Том 3 |
|
|
Не все больные, особенно находящиеся в сознании, легко принимают режим ПДКВ, поэтому иногда требуется умелое применение суггестивных методов. Нередко с помощью убеждения удается примирить больного с этим режимом, и тогда пациент может даже не захотеть отменять его. Если же суггестивный метод оказывается безуспешным, приходится проводить седацию. Когда на фоне ПДКВ нарастает РO2, нормализуется РCO2 (ликвидация гипоксемии купирует обусловленную ею ненужную гипервентиляцию — механизм регуляции по РO2), можно считать применение ПДКВ эффективным.
|
Вдох |
Выдох |
|
р |
|
О |
|
ПДКВ |
2 |
|
|
см Н |
|
|
|
|
|
5–15 |
0 |
|
|
t |
|
|
|
|
|
|
СВЛ |
Рисунок 5. Изменения давления воздуха в дыхательных путях при ПДКВ |
||
От больного
ПДКВ
(5–15 см Н2О)
Вода
Рисунок 6. Техника режима ПДКВ
Острая дыхательная недостаточность |
85 |
|
|
К сожалению, ПДКВ не всегда приносит желаемый результат. Обычно это связано с крайне тяжелыми нарушениями диффузии. В этом случае достигаемого повышения внутриальвеолярного давления воздуха недостаточно. Повышать ПДКВ более 15 см вод.ст. не рекомендуется, так как это может вызвать нарушения гемодинамики вследствие сопротивления насосной работе сердца и снижения венозного возврата. В таких ситуациях дополнительного повышения давления приходится достигать, сочетая режим ПДКВ с вдуванием воздуха в легкие, то есть с ИВЛ. То же самое приходится делать и при сочетании нарушений диффузии с нарушением вентиляции.
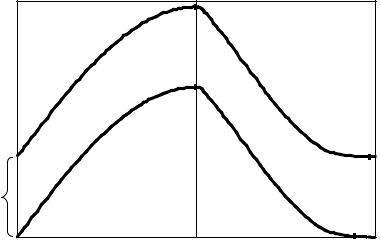
Сочетание обычной ИВЛ (в режиме ППД) с режимом ПДКВ дает новый режим ИВЛ — непрерывно положительное давление (НПД). При этом режиме кривая давления режима ППД повышается на определенную величину, равную ПДКВ (рис. 7), а давление в дыхательных путях все время (непрерывно) положительное.
|
|
Принципы ИТ нарушений |
|
вентиляционно-перфузионных соотношений |
|
Принципы ИТ шунтирования справа налево (венозного примешивания) |
||
Напомним, что патологическое шунтирование справа налево обу- |
||
словлено нарушениями вентиляции в некоторых участках легких, |
||
нередко носящими мозаичный характер. Поскольку объем воздуха, |
||
|
Вдох |
Выдох |
|
р |
|
|
|
НПД |
|
|
ППД |
О |
|
|
2 |
|
|
5–15 см Н |
0 |
t |
|
Рисунок 7. Давление в дыхательных путях при режиме НПД |
|
86 |
Медицина неотложных состояний. Избранные клинические лекции. Том 3 |
|
|
соприкасающегося в легких с кровью, значительно снижен, оксигенотерапия оказывается неэффективной. Сохраняющаяся гипоксемия часто сопровождается гипокапнией вследствие гипервентиляции, неспособной повысить РO2. В то же время эта гипервентиляция значительно увеличивает кислородную цену дыхания, то есть большая часть добываемого кислорода уходит на обеспечение его добывания (то есть на работу дыхательных мышц).
В таких случаях неоценимое значение приобретает респираторная терапия, призванная восстановить проходимость дыхательных путей вплоть до терминальных бронхиол, о которой речь пойдет ниже. Невозможно обойтись и без ИВЛ, которая сама по себе может улучшить проходимость многих участков ТБД, но главное — она снимает с пациента необходимость совершать работу по добыче кислорода, который может быть использован для выполнения более важных задач.
Принципы ИТ увеличения функционального мертвого пространства
Данное нарушение ВПС наблюдается при нарушениях легочного кровотока, которые тоже часто носят мозаичный характер. Трудно представить себе какой-либо шок в декомпенсированной стадии, при котором бы не было увеличения функционального мертвого пространства. К этой же ситуации приведет и тромбоэмболия ветвей (мелких или крупных) легочной артерии. Отсюда ясно, что главная задача при лечении такого состояния — нормализация легочного кровотока, которую можно решить, выведя больного из шока, восстановив проходимость ветвей легочной артерии и т.п. Естественно, все эти мероприятия чаще всего должны проводиться на фоне ИВЛ, которая в данном случае снижает потребность организма в кислороде (дыхательные мышцы не работают).
Принципы ведения больного на ИВЛ
ИВЛ резко ограничивает возможности больного во многих отношениях. Двигательная активность больного близка к нулевой, удаление мокроты практически невозможно (так как невозможен полноценный кашель из-за препятствия смыканию голосовой щели и нарушена работа естественного механизма дренирования мокроты), если больной в сознании, он испытывает выраженный дискомфорт в связи с нахождением в дыхательных путях и полости рта инородных тел (эндотрахеальная трубка, желудочный, а иногда еще и гастроинтестинальный зонд, тампонада полости рта и ротоглотки). Правда, дискомфорт можно уменьшить, введя трубку и зонд через нос; трахеостомия так-
Острая дыхательная недостаточность |
87 |
|
|
же его уменьшает, принося при этом, к сожалению, другие проблемы (уменьшение анатомического мертвого пространства, снятие барьеров между трахеей и окружающей атмосферой и многие другие). Все это делает ведение больного на ИВЛ чрезвычайно сложной и ответственной задачей.
Таким образом, основные принципы ведения больного на ИВЛ связаны с ограничением его двигательной активности и нарушением дренирования мокроты. Естественно, сохраняют свое значение и общие принципы ведения больного, находящегося в критическом состоянии.
Во время ИВЛ необходимо периодически изменять положение больного в постели (примерно каждые 2 часа): на спине — на одном боку — на другом боку — на спине. Такое несложное мероприятие предотвращает или хотя бы тормозит развитие пролежней, улучшает кровообращение в легких и способствует лучшему удалению мокроты.
При проведении ИВЛ жизненно необходим также комплекс мероприятий, носящий название респираторной терапии, которая призвана нормализовать дренирование мокроты.
Все методы респираторной терапии можно разделить на 4 группы.
1.Методы улучшения реологических свойств мокроты.
1.1.Аэрозольная терапия увлажнителями и детергентами.
1.2.Интратрахеальная инстилляция тех же средств.
2.Методы улучшения активности слизистой дыхательных путей.
2.1.Кондиционирование (увлажнение, согревание и обеззаражива-
ние) вдыхаемых газов.
2.2.Аэрозольная терапия противовоспалительными средствами, увлажнителями и сурфактантами.
2.3.Инфузионная гидратация.
3. Методы стабилизации стенки дыхательных путей.
3.1. Применение бронхолитиков аэрозольным, внутривенным или энтеральным путем.
3.2. Применение режима ПДКВ.
4. Методы, способствующие удалению мокроты.
4.1.Постуральный дренаж.
4.2.Вибрационный, перкуссионный и вакуумный массаж.
4.3.Увеличение внутрилегочного давления, повышающее коллатеральную вентиляцию (через межальвеолярные поры Кона).
4.4.Стимуляция и имитация кашля.
4.5.Бронхиальный лаваж.
4.6.Отсасывание мокроты.
88 |
Медицина неотложных состояний. Избранные клинические лекции. Том 3 |
|
|
Кондиционирование вдыхаемых газов требуется всегда, когда дыхание осуществляется через эндотрахеальную трубку или трахеостому, поскольку при дыхании через естественные дыхательные пути воздух получает около 75 % воды и тепла. Без кондиционирования слизистая дыхательных путей высыхает, нарушаются ее защитные свойства и мукоцилиарный механизм дренирования мокроты. Кроме того, надо учитывать, что газы, поступающие из баллонов (прежде всего кислород), слишком сухие.
Для увлажнения вдыхаемых газов используются увлажнители всевозможных конструкций и аэрозольные ингаляторы для ингаляции воды и других препаратов, улучшающих мукокинез, оказывающих бронхолитический, антибактериальный, противовоспалительный, местноанестезирующий и поверхностно-активный эффекты.
Интратрахеальная инстилляция чаще всего используется для стимуляции кашля. Для ее осуществления производят катетеризацию трахеи по методике Seldinger через lig. conicum. Катетер вводят на глубину 5–6 см так, чтобы его конец располагался чуть выше бифуркации трахеи. Через него вводят одномоментно 3–5 мл раствора тех веществ, которые перечислены выше.
Инфузионная терапия при ОДН призвана восстановить гидратацию тканей (так как при ОДН гипогидратация наблюдается довольно часто), что приведет к улучшению реологических свойств мокроты.
Постуральный дренаж — придание больному определенного положения в постели с целью добиться пассивного истечения мокроты из определенных участков легких. Положение больного зависит от того, из каких сегментов требуется удалить мокроту.
Постуральный дренаж полезно дополнять лечебной перкуссией грудной клетки, которая выполняется путем поколачивания чашеобразно сложенными ладонями с частотой 40–60 раз в минуту в течение минуты, затем следует минутный перерыв.
Вибрационный массаж выполняют встряхивающими движениями кистей, приложенных к грудной клетке.
Вакуумный массаж производят с помощью крупной медицинской банки, которая должна иметь диаметр около 6 см и объем до 200 мл. После стандартной процедуры постановки банки на стенку грудной клетки банку в течение 10–15 минут перемещают по грудной клетке, постепенно массируя всю ее поверхность. Такое мероприятие улучшает проходимость мелких дыхательных путей и в 1,5 раза увеличивает количество отходящей мокроты.
Острая дыхательная недостаточность |
89 |
|
|
Бронхопульмональный лаваж (промывание) может потребоваться при аспирации желудочного содержимого, бронхоастматическом статусе и некоторых других состояниях. Выполняется с помощью фибробронхоскопа.
Отсасывание мокроты может быть самостоятельной процедурой и обязательной завершающей предыдущие методы составной частью респираторной терапии. Для отсасывания мокроты используют стерильные резиновые или пластиковые катетеры (желательно одноразовые) со сглаженными краями. Перед отсасыванием проводят оксигенотерапию (во время отсасывания может развиться гипоксия) и инстилляцию в трахею муколитиков, а также местных анестетиков (для предупреждения рефлекторных вагусных реакций). Каждое отсасывание должно длиться не более 15 с. Процедура требует большой аккуратности и осторожности, чтобы не вызвать повреждения слизистой с последующим ее инфицированием.
Фибробронхоскопия под местной анестезией получает все большее распространение, так как позволяет целенаправленно санировать дыхательные пути под контролем зрения.
Типы дыхательных аппаратов
Все респираторы можно классифицировать по двум признакам: по виду потребляемой энергии и по принципу переключения со вдоха на выдох.
Респираторы могут потреблять электрическую энергию и энергию сжатого газа, как правило кислорода (пневматические респираторы).
Электрические респираторы имеют то преимущество, что они потребляют только такое количество кислорода, которое необходимо дать больному (в среднем 3–7 л/мин), а энергию для своей работы они получают из электрического источника. Кроме того, электрические респираторы могут работать при минимальном давлении кислорода и даже при полном его отсутствии (тогда ИВЛ проводится атмосферным воздухом, чего нередко бывает достаточно). Недостатком такого типа респираторов является невозможность их работы при аварийном отключении электроэнергии.
Работа пневматических респираторов не зависит от капризов электроснабжения, что, безусловно, является их преимуществом. Однако такие респираторы потребляют большое количество кислорода, так как он не только идет в дыхательные пути больного, но и обеспечивает энергией работу респиратора (за 2–3 часа работы обычно расходуется
