
304- Органическая химия_Черных В.П. и др_Х., 2007 -776с
.pdf
СераОрГанИЧеСКИе СОеДИненИя
531
образующийся сульфонамид-анион проявляет нуклеофильные свойства. При хлорировании натрия бензолсульфонамида получают бензолсульфон-
дихлорамид (дихлорамин б), который является сильным окислителем и используется для дезинфекции и дегазации ядовитых веществ.
дезинфицирующие свойства проявляют также и другие хлорамины.
среди аренсульфонамидов выделяют многочисленную группу лекарственных препаратов антибактериального действия — сульфаниламиды. структурным фрагментом сульфаниламидов является сульфаниловая кислота (см. с. 310).
наличие в молекуле сульфаниловой кислоты кислотного (группа —SO3H) и основного (группа —NH2) центров обусловливает ее существование в виде внутренней соли (биполярного иона)
сульфаниловая кислота является довольно сильной кислотой (ркa = 3,22), реагируя с основаниями, легко образует соли:
из-за биполярной структуры сульфаниловая кислота не образует солей с мине-
ральными кислотами, то есть, несмотря на наличие аминогруппы, она не обладает основными свойствами.
родоначальником сульфаниламидных препаратов является амид сульфаниловой кислоты, применяемый в медицинской практике под названием «Сульфанил-
амид» или «Стрептоцид»:



Глава 29
534
сложные эфиры п-бромбензолсульфоновой кислоты общей формулы п-BrC6H4SO2OR называют брозилаты, п-толуолсульфоновой кислоты — тозилаты ( п-CH3C6H4SO2OR), трифторметансульфоновой кислоты — трифлаты (CF3SO2OR). Приведенные сульфонаты проявляют сильнейшие алкилирующие свойства, так как в реакциях SN образуют стабильные уходящие группы (анионы соответствующих сульфоновых кислот).
нуклеофильное замещение сульфогруппы (SN). сульфогруппа имеет тетраэд-
рическое строение и практически не вступает в сопряжение с -электронами ароматической системы. следует также учитывать, что сульфирование является обратимым процессом. Поэтому при действии сильных нуклеофильных реагентов возможно замещение сульфогруппы другими функциональными группами. Протека-
нию реакций нуклеофильного замещения сульфогруппы способствуют также дефицит электронной плотности на атоме углерода ароматического кольца.
Гидролиз аренсульфоновых кислот (десульфирование). реакцию используют для удаления из ароматического кольца сульфогруппы.
Реакция щелочного плавления. сульфогруппа может быть удалена из ароматического кольца при действии различных нуклеофилов. Щелочное плавление солей сульфоновых кислот проводят с твердыми щелочами при температуре 300—350 °с. с помощью реакции щелочного плавления получают не только фенолы (см. с. 366, 377), но и другие классы органических соединений:
основным недостатком способа являются жесткие условия реакции и выделение значительного количества отходов (экологический аспект).
Электрофильное замещение (SE) по ароматическому ядру. сульфогруппа
—SO3H, являясь сильным электроноакцептором, дезактивирует ароматическое ядро в реакциях SE и ориентирует замещение в м-положение.

Глава 29
53
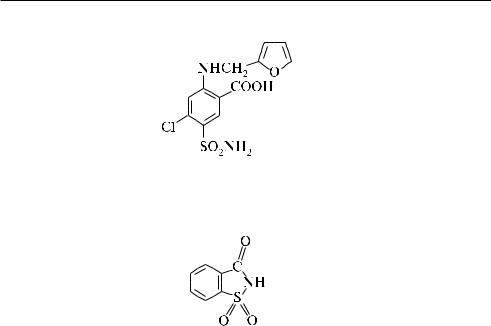
в медицинской практике используется под названием «Фуросемид».
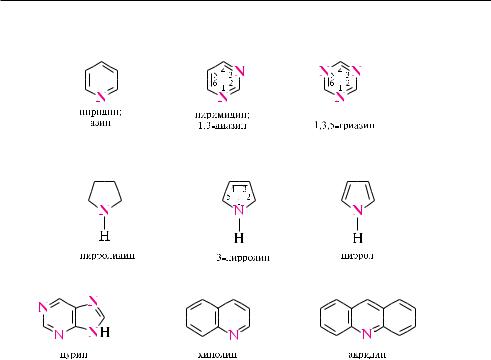
Имид о-сульфобензойной кислоты (сахарин). бесцветное кристаллическое вещество. труднорастворимое в воде (1 : 250), спирте (1 : 40), (т. пл. 224—226 °с). дигидрат натриевой соли сахарина называют кристаллозой. слаще сахара в 500— 600 раз. выводится с мочой в неизменном виде.
Применяют в качестве подсластителя диетических пищевых продуктов.

Глава 30
538
количество гетероатомов (моно-, диили три- и так далее гетероатомные циклы):
степень насыщенности цикла (насыщенные, ненасыщенные и ароматические гетероциклы):
в особую группу выделены конденсированные системы:
30.2. нОМенКлаТура
для гетероциклических соединений применяют тривиальные и систематиче-
ские названия. Тривиальные названия приняты номенклатурой IUPAC и в большинстве случаев являются более предпочтительными.
При построении систематических названий гетероциклов номенклатурными правилами IUPAC учитывается природа и количество гетероатомов, а также размер цикла и степень его насыщенности. При этом природа гетероатома отражается в префиксе, размер цикла — в корне, а степень насыщенности — в суффиксе названия. для обозначения гетероатомов используют префиксы окса- (O), тиа- (S), аза- (N) и др. размер цикла обозначается корнями -ир- (трех-), -ет- (четырех-), -ол- (пяти-), -ин- (шести-), -еп- (семичленный), а степень насыщенности — суф-
фиксами -идин (насыщенный цикл с атомом азота), -ан (насыщенный цикл без атома азота), -ин (ненасыщенный цикл). в названии гетероциклов с максимально возможным количеством двойных связей в цикле суффикс не указывается. для частично гидрированных соединений используют приставки дигидро-, тетрагидро- с указанием номеров атомов, к которым присоединен водород. если атом водорода присоединен только к одному атому цикла, то в названии указывается номер гидрированного атома и символ н. в шести- и семичленных азотсодержащих гетероциклах полная насыщенность цикла обозначается приставкой пергид- ро-. количество гетероатомов одного вида указывают в названии множительными приставками ди-, три-, тетра- и т. д. если гетероцикл содержит несколько разных гетероатомов, то называют их в определенной последовательности: окса-,
тиа-, аза- и др.

Глава 30
540
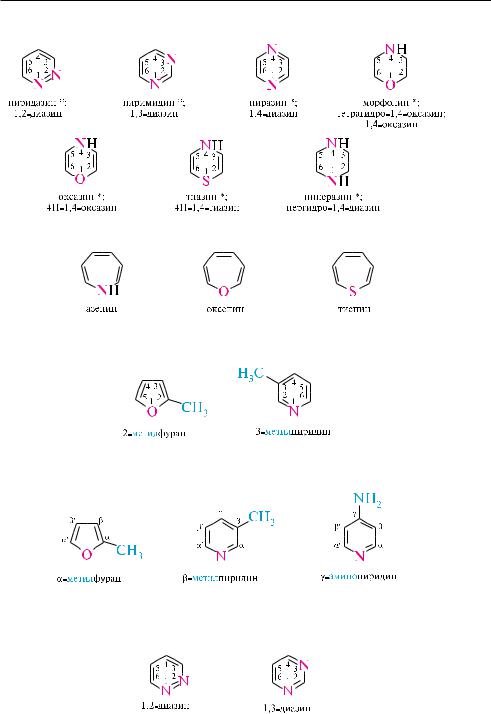
шестичленные гетероциклические соединения с двумя гетероатомами:
семичленные гетероциклические соединения с одним гетероатомом:
нумерацию атомов в гетероцикле обычно начинают с гетероатома и проводят
втом направлении, чтобы заместители получили возможно меньшие номера.
впяти- и шестичленных гетероциклах с одним гетероатомом атомы углерода иногда обозначают греческими буквами .
вгетероциклах с несколькими равноценными гетероатомами нумерацию проводят таким образом, чтобы гетероатомы получили наименьшие из возможных номеров:
если в гетероцикле имеется несколько разных гетероатомов, то нумерацию начинают с того, который в ряду O, S, NH, N расположен левее; проводят в таком направлении, чтобы остальные гетероатомы получили возможно меньшие номера:
