
304- Органическая химия_Черных В.П. и др_Х., 2007 -776с
.pdf
ГеТерОЦИКлИЧеСКИе СОеДИненИя
541
для некоторых гетероциклов существует особый порядок нумерации. большую группу составляют гетероциклические соединения с двумя и более
конденсированными циклами. системы могут состоять из одного гетероциклического и одного или нескольких бензольных колец, а также из нескольких гетероциклических ядер. обычно для таких гетероциклов применяют тривиальные названия:
индол
систематические названия конденсированных гетероциклических систем образуют, используя в качестве родоначальных структур тривиальные названия гетероциклов.
При построении названий конденсированных систем, состоящих из одного гетероциклического и одного или двух бензольных ядер, к названию гетероцикла присоединяют префикс бенз- (бензо-) или дибенз- (дибензо-) с указанием буквами a, b , c , d и так далее связи гетероцикла, по которой происходит конденсация. обозначение связей начинают от гетероатома:
если конденсированная система состоит из двух гетероциклов, за основу на-
звания принимают название цикла, большего по размеру; при одинаковом размере — цикла с большим числом гетероатомов, и, наконец, если по первым двум критериям циклы равнозначны, то азотсодержащий цикл имеет предпочтение перед кислородсодержащим, а последний — перед серосодержащим. При помощи букв указывают связь основного цикла, которая является общей для обоих циклов, а при помощи цифр — общую связь второго цикла с основным:
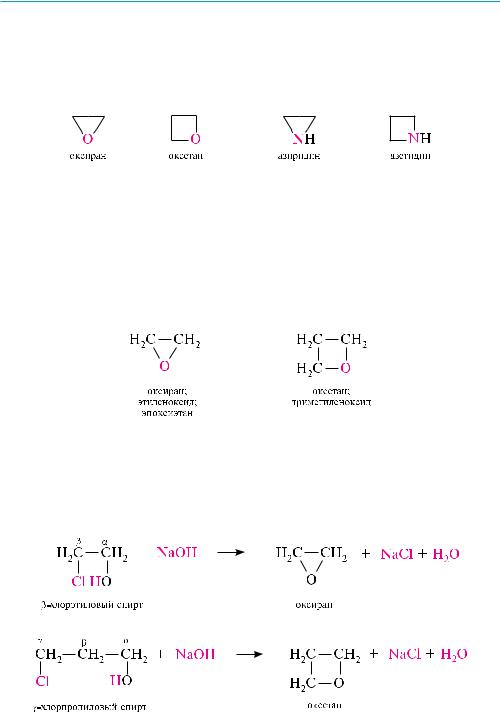

Трех- И ЧеТЫрехЧленнЫе ГеТерОЦИКлИЧеСКИе СОеДИненИя
543
в промышленности оксиран получают в основном окислением этилена кислородом воздуха при температуре 300—400 °с над серебряным катализатором.
31.1.2. ФИЗИЧеСКИе СВОЙСТВа
Оксиран — бесцветный газ с эфирным запахом (т. кип. 10,7 °с), хорошо растворяется в воде и органических растворителях.
Оксетан — жидкость (т. кип. 47,8 °с), хорошо растворяется в воде, этиловом спирте и диэтиловом эфире.
31.1.3. хИмИЧеСКИе СВОЙСТВа
в химическом отношении оксиран и оксетан являются весьма реакционноспособными соединениями. Это связано с угловым и торсионным напряжением циклов (подобно циклопропану и циклобутану), а также наличием полярных связей с—о. При действии электрофильных и нуклеофильных реагентов происходит разрыв кислород-углеродной связи и присоединение молекулы реагента по месту разрыва цикла. особенно легко эти реакции проходят в условиях кислотного катализа.
так, в присутствии серной или фосфорной кислот оксиран легко присоединяет воду и спирты:
Механизм приведенных реакций включает образование оксониевого соединения (продукт взаимодействия оксирана с кислотой), которое гораздо легче подвергается атаке нуклеофильным реагентом, чем сам оксиран ( '+ > +):


Трех- И ЧеТЫрехЧленнЫе ГеТерОЦИКлИЧеСКИе СОеДИненИя
545
Полиэтиленгликоль, в зависимости от молекулярной массы, имеет различное агрегатное состояние. Полимер с молекулярной массой 400 представляет собой жидкость, хорошо растворимую во многих органических растворителях. Применяется в фармации в качестве растворителя лекарственных веществ, основы для мазей и суппозиториев, а также как связывающее вещество в производстве таблеток.
оксетан по химическим свойствам сходен с оксираном и вступает в характерные реакции присоединения с раскрытием цикла. однако меньшая степень напряжения в четырехчленном цикле способствует тому, что эти реакции протекают гораздо медленнее.
Многие реакции оксетана приводят к образованию 1,3-дизамещенных пропана:
31.1.4. ВажнеЙШИе ПрОИЗВОДнЫе ОКСИрана И ОКСеТана
Эпихлоргидрин (3-хлор-1,2-эпоксипропан). бесцветная жидкость с запахом хлороформа (т. кип. 116,1 °с),
 хорошо растворимая в органических растворителях. используют эпихлоргидрин в производстве эпоксидных смол, для получения
хорошо растворимая в органических растворителях. используют эпихлоргидрин в производстве эпоксидных смол, для получения
глицерина и как растворитель эфиров целлюлозы.
β-Пропиолактон (лактон -гидроксипропионовой кислоты). бесцветная жидкость с резким запахом (т. кип. 155 °с), растворяется в органических растворителях, быстро гидролизуется до -гидрок-
сипропионовой кислоты.
-Пропиолактон легко взаимодействует со спиртами и аминами с раскрытием цикла:

Глава 31
54
-Пропиолактон применяется в медицине для стерилизации крови, вакцин и других биологических препаратов.
31.2. аЗиридин и аЗеТидин
31.2.1. СПОСОБЫ ПОлУЧенИя
общим способом получения азиридина и азетидина является циклизация гало-
генаминов в присутствии щелочи.
азиридин получают циклизацией -галогенэтиламинов:
для получения азетидина используют -галогенпропиламины.
в промышленности азиридин получают взаимодействием 1,2-дихлорэтана с аммиаком в присутствии кальция оксида сао.
31.2.2. ФИЗИЧеСКИе СВОЙСТВа
Азиридин — бесцветная жидкость (т. кип. 55 °с), хорошо растворяется в воде и органических растворителях.


Глава 31
548
31.2.4. ВажнеЙШИе ПрОИЗВОДнЫе аЗИрИДИна И аЗеТИДИна
среди производных азиридина обнаружены вещества, обладающие выраженной противоопухолевой активностью, на основе которых создан ряд противоопухолевых лекарственных препаратов (тиофосфамид, бензотэф, фторбензотэф и др.). все они содержат, как правило, остатки фосфорной и тиофосфорной кислот.
из производных азетидина важное значение имеет внутримолекулярный амид -аминопропионовой кислоты — 2-азетидинон ( -лактам). синтезируют путем термической циклизации -ами- нопропионовой кислоты. При действии водных растворов кислот и щелочей, аммиака и аминов -лактамное кольцо раскрывается.
2-азетидинон входит в состав антибиотиков группы пенициллина (см.
с. 588).

глава 32
ПЯТи- и ШесТиЧленные геТерОциКлиЧесКие сОединениЯ с ОдниМ и двуМЯ геТерОаТОМаМи
из большого числа пяти- и шестичленных гетероциклических соединений
содним и двумя гетероатомами в данном разделе рассматриваются гетероциклы
сгетероатомами O, N и S, обладающие ароматическими свойствами. такие вещества по своей устойчивости и химическим свойствам во многом напоминают бензол и поэтому получили название «гетероциклические ароматические», или
«гетероароматические соединения».
важнейшими представителями данной группы соединений являются:
пятичленные гетероциклы
шестичленные гетероциклы
конденсированные гетероциклические системы
32.1. арОМаТиЧнОсТЬ геТерОциКлОв
как известно, признаком ароматичности соединения является наличие плоской циклической системы, имеющей замкнутую цепь сопряжения, содержащую (4n + 2) -электронов.
ароматичность пятичленных гетероциклов с двумя -связями обусловлена тем, что в сопряжение с -электронами двойных связей вступает неподеленная пара электронов гетероатома N, O или S.
Глава 32
550
в результате образуется замкнутая сопряженная система, в которой число |
|
обобщенных электронов соответствует правилу хюккеля (4n + 2). |
|
|
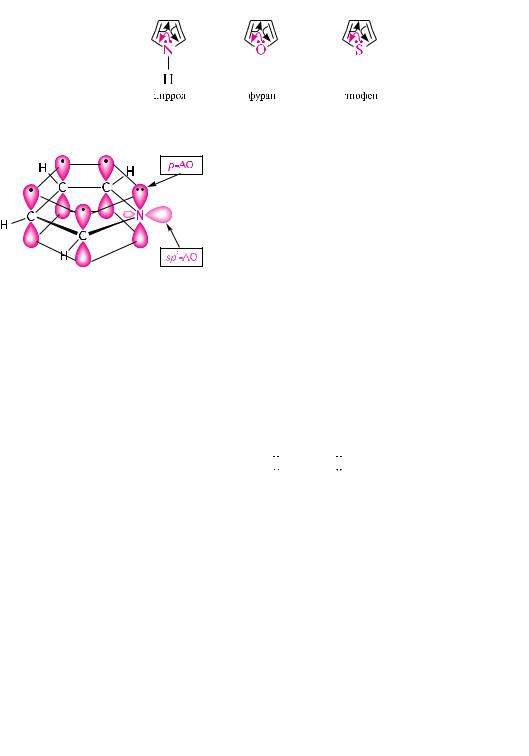
в молекуле пиррола (рис. 32.1) |
|
атомы углерода и атом азота нахо- |
|
дятся в состоянии sp2-гибридизации. |
|
за счет sp2-гибридных орбиталей каж- |
|
дый атом, входящий в состав цикла, |
|
образует три s-связи, расположенные |
|
в плоскости кольца. При этом у ато- |
|
мов углерода и атома азота остается |
рис. 32.1. Электронное строение молекулы пиррола |
по одной негибридизованной p-ор- |
битали, которые расположены парал- |
|
лельно друг другу в плоскости, перпендикулярной плоскости кольца. каждая из |
|
p-ао атомов углерода имеет один электрон, а на p-орбитали атома азота нахо- |
|
дится неподеленная пара электронов. При перекрывании p-орбиталей образуется |
|
единое шестиэлектронное облако, охватывающее все атомы цикла. |
|
атом азота в sp2-гибридизации, имеющий электронную конфигурацию, в которой |
||
неподеленная пара электронов занимает негибридизованную p-атомную орбиталь, |
||
называется пиррольным. |
|
|
аналогично образуется сопряженная система и в других пятичленных гете- |
||
роциклах с двумя -связями, в частности, в молекулах фурана и тиофена. как |
||
и атом азота в пирроле, гетероатомы (—O— и —S—) вносят в ароматический |
||
секстет неподеленную пару p-электронов. По аналогии с пирролом: |
||
гетероатом, вносящий в π-электронную систему два электрона, занимающих |
||
p-атомную oрбиталь, и образующий с другими атомами только σ-связи, принято |
||
называть гетероатомом пиррольного типа. |
||
в ряду шестичленных гетероциклов ароматические свойства харак- |
||
терны для структур, представляющих собой гетероциклические аналоги |
||
бензола. так, в молекуле пиридина (pиc. 32.2) все атомы углерода и атом |
||
азота находятся в состоянии sp2-гибридизации. замкнутая шести- -элек- |
||
|
тронная система образована пятью p-орбита- |
|
|
лями атомов углерода (по одной от каждого) |
|
|
и p-орбиталью атома азота. то есть в молекуле |
|
|
пиридина, как и в молекуле бензола, каждый |
|
|
атом цикла вносит в ароматический секстет по |
|
|
одному p-электрону. |
|
|
неподеленная пара электронов атома азота |
|
|
в молекуле пиридина, в отличие от молеку- |
|
|
лы пиррола, занимает sp2-гибридную орбиталь |
|
рис. 32.2. Электронное строение |
и не принимает участия в образовании арома- |
|
тического секстета. |
||
молекулы пиридина |
||
