
- •Таб.1. 23. Этиология внебольничных пневмоний у детей
- •ЖЕЛЕЗОДЕФИЦИТНЫЕ СОСТОЯНИЯ У ДЕТЕЙ
- •Рис. 1.29. Схема патогенеза наследственного сфероцитоза
- •Электролиты ммоль/кг/сут
- •Краткая информация о тромбоцитах, дифференцировке мегакариоцитарного ростка
- •Дифференциальный диагноз ИТП проводят с острым лейкозом, апластическими анемиями, наследственными тромбоцитопатиями, симптоматическими тромбоцитопеническими пурпурами.
- •Задачи лечения: нормализация уровня тромбоцитов в крови, купирование проявлений ИТП.
- •Спленэктомия показана при ИТП не поддающейся коррекции базисными препаратами, при угрожающих жизни кровотечениях, хронизации процесса, но не ранее чем через 1 год с момента дебюта заболевания.
- •Прогноз при ИТП для жизни благоприятный. Летальность не превышает 2-3%.
- •Глава I. Введение в неонатологию
- •Глава II. Организация медицинского обслуживания новорожденных в родильном доме
- •Первичный туалет новорожденного
- •Уход за новорожденными детьми
- •Профилактические прививки
- •ОРГАНИЗАЦИЯ МЕДИЦИНСКОГО ОБСЛУЖИВАНИЯ НОВОРОЖДННЫХ ДЕТЕЙ НА ВТОРОМ ЭТАПЕ ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ
- •Глава III. Адаптация, пограничные состояния
- •НЕОНАТАЛЬНАЯ АДАПТАЦИЯ И ПЕРЕХОДНЫЕ (ПОГРАНИЧНЫЕ) СОСТОЯНИЯ
- •Глава IV. Задержка внутриутробного развития
- •Тактика ведения новорожденных после завершения первичных реанимационных мероприятий
- •ЦЕРЕБРАЛЬНАЯ ИШЕМИЯ
- •Классификация гипоксических поражений ЦНС представлена в таблице 2.13.
- •Лечение восстановительного периода
- •Глава VI. Родовая травма. Интранатальные повреждения нервной системы
- •Перелом ключицы считается одним из наиболее частых повреждений костей. Данный вид перелома развивается во время родов при прохождении плечевого пояса при головном предлежании и при отведении рук при тазовом предлежании плода.
- •Диагноз инфратенториального субдурального кровоизлияния подтверждается результатам УЗИ, МРТ и компьютерной томографии.
- •ИНТРА- И ПЕРИВЕНТРИКУЛЯРНЫЕ КРОВОИЗЛИЯНИЯ НЕТРАВМАТИЧЕСКОГО ГЕНЕЗА
- •Глава VII. Недоношенные дети
- •Причины рождения недоношенных детей:
- •Энтеральное питание
- •Возможные варианты питания ребенка в зависимости от гестационного возраста и наличия заболеваний:
- •ОСОБЕННОСТИ ТЕЧЕНИЯ НЕКОТОРЫХ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ У НЕДОНОШЕННЫХ
- •Глава VIII. Гемолитическая болезнь новорожденных
- •Глава IX. Инфекционные заболевания новорожденных
- •Термин «внутриутробная инфекция» при использовании в клинической практике в качестве диагноза должен быть конкретизирован не только по этиологии, но и по периоду инфицирования, особенностям поражения тех или иных внутренних органов.
- •Цитомегаловирусная инфекция (ЦМВИ) является одной из вариантов ВУИ и встречается у 0,2% новорожденных детей (предполагаемая частота 2 : 1000). В разных странах удельный вес серопозитивного населения к ЦМВ составляет от 20 до 95%.
- •Врожденный листериоз (ВЛ) относят к более редким вариантам ВУИ. Около 10% всей акушерской патологии связывают с ВЛ, 30% взрослого населения являются носителями данной инфекции.
- •Глава IX. Неинфекционные заболевания системы дыхания
- •СИНДРОМ АСПИРАЦИИ МЕКОНИЯ (САМ)
- •САМ – дыхательное расстройство, обусловленное попаданием мекония вместе с околоплодными водами в дыхательные пути ребенка до родов или в момент рождения.
- •Глава X. Болезни кожи и пупочной ранки
- •ВЕЗИКУЛОПУСТУЛЕЗ (стафилококковый перипорит) - часто встречающееся заболевание новорожденных, характеризующееся воспалительными изменениями в области устьев эккринных потовых желез.
- •ПУЗЫРЧАТКА НОВОРОЖДЕННЫХ (пемфигус) (ПН)- острое контагиозное заболевание, характеризующееся быстрым образованием и распространением на коже вялых тонкостенных пузырей (фликтен) различного диаметра на неизмененном фоне.
- •ЭКСФОЛИАТИВНЫЙ ДЕРМАТИТ РИТТЕРА - рядом авторов рассматривается как злокачественная разновидность пиококкового пемфигоида.
- •ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ ПУПОЧНОЙ РАНКИ, ПУПОВИННОГО ОСТАТКА И ПУПОЧНЫХ СОСУДОВ
- •Омфалит - воспалительный процесс дна пупочной ранки, пупочных сосудов, кожи и подкожной клетчатки в области пупка.
- •Глава XI. Геморрагическая болезнь новорожденного
- •Энергия, ккал/сутки
Методическое
пособие по
педиатрии
1
ББК УДК 616-053.2: 616\18-005
Методическое пособие подготовлено: Быковым В.О., Водовозовой Э.В., Душко С.А., Губаревой Г.Н., Кузнецовой И.Г., Кулаковой Е.В., Леденевой Л.Н., Мироновой Э.В., Поповой Т.А. Стременковой И.В, Щетининым Е.В,
Методическое пособие написано в соответствии с требованиями «Программы для студентов по «Педиатрии» педиатрических факультетов. В пособии содержатся современные данные об этиологии, патогенезе, клинике, принципах диагностики и лечения важнейших заболеваний и детей младшего и старшего возраста, а также у новорожденных детей.
Методическое пособие рассчитано на студентов педиатрического факультета, интернов, клинических ординаторов.
Рецензент:
Ставропольская государственная медицинская академия, 2010
2
ПРЕДИСЛОВИЕ
Внастоящее время для обучения студентов педиатрических факультетов вопросам педиатрии широко используются учебники Н.П. Шабалова «Детские болезни» и «Неонатология». Отдавая должное качеству изложения материала, охвату всех разделов педиатрии, наличию современной информации по этиологии, патогенезу и лечению заболеваний в тоже время необходимо указать и некоторые недостатки указанных учебников, связанных в первую очередь с не всегда обоснованным обилием предлагаемой для освоения информации.
Многолетний опыт преподавания студентам педиатрического факультета «детских болезней» свидетельствует о том, что не все разделы существующих учебников по «Педиатрии» и «Неонатологии» одинаково доступны для восприятия студентами.
Указанные проблемы настоятельно требуют создания методических пособий для студентов, которые бы не подменяя собой, существующие учебники облегчали бы освоение обучающимися сложных разделов педиатрии.
Разработанное сотрудниками Ставропольской медицинской академии методическое пособие по педиатрии включает в себя материал, соответствующий требованиям «Программы для студентов по «Педиатрии» педиатрических факультетов.
Впервой части пособия представлены заболевания детей младшего
истаршего возраста, освещенные с современных позиций и требований консенсусов, национальных программ, руководств и методических указаний, выпущенных в последние годы. Вторая часть методического пособия посвящена вопросам неонатологии.
Авторы надеется, что данное пособие будет полезным при обучении студентов педиатрии.
3
ЧАСТЬ I. БОЛЕЗНИ ДЕТЕЙ МЛАДШЕГО И СТАРШЕГО ВОЗРАСТА
Глава I. Аномалии конституции
ДИАТЕЗЫ (аномалии конституции) являются наиболее спорной проблемой в педиатрии. В последние годы преобладает точка зрения, согласно которой диатезы - это своеобразная «дань традиции». Более того, данное понятие сохранилось только в отечественной педиатрии. За рубежом, в МКБ-10 шифры для данной патологии не предусмотрены.
В настоящее время в понятие конституция вкладывается следующий смысл – это совокупность гено- и фенотипических свойств и особенностей (морфологических, биохимических и функциональных) организма, определяющих возможность его защитноприспособительных реакций, направленных на сохранение гомеостаза, т.е. здоровья. В то же время, здоровье всегда индивидуально и обусловлено, в том числе, и метаболическими особенностями детского организма. Особенности обмена веществ могут быть относительно одинаковыми у разных людей, что позволяет классифицировать их, различать их виды. Это и есть диатезы – или аномалии конституции, т.е. генетически детерминированные особенности обмена веществ (метаболическая индивидуальность), определяющие своеобразие адаптивных реакций организма и предрасполагающие к развитию определенных заболеваний.
Известно, что факторы риска формирования многих заболеваний заключаются не только в воздействии окружающей среды, но подчас, в большей мере, в конституциональных особенностях организма. Полагают, что большинство хронических заболеваний имеет в своей основе конституцию больных. В этом смысле диатезы рассматривают как предболезни.
Выделение того или иного вида диатеза помогает в разработке рекомендаций по первичной профилактике, возможных в будущем, заболеваний. Т.О. диатез – это предрасположенность, предболезнь, преднедостаточность тех или иных метаболических механизмов. Определить предрасположенность и степень риска возникновения заболевания значительно сложнее, чем поставить диагноз уже развившегося заболевания, даже в случаях его минимальных проявлений.
Предрасположенность (диатез) к заболеваниям определяется особенностями структуры и функции одной или нескольких систем орга-
4
низма: иммунной, ЦНС, нервно-гуморальной и т. д. Амплитуда колебания «нормального» функционирования организма очень индивидуальна. Крайние показатели нормы и компенсированные дефекты метаболизма и составляют сущность предрасположенности (диатеза). В тех случаях, когда организм не может обеспечить адаптацию к меняющимся условиям внешней среды, предрасположенность реализуется заболеванием.
В настоящее время выделяют около 20 диатезов, объединенных в группы:
I. Иммунопатологические: атопический, аутоиммунный, лимфатический, инфекционно-аллергический.
II. Дисметаболические: мочекислый, оксалатный, диабетический, геморрагический, адипозодиатез.
III. Органотопические: нефротический, интестинальный, гипертонический, кардиоишемический, атеросклеротический.
IV.Нейротопические: психо-астенический, вегето-дистонический. В самые последние годы описан энергетический диатез. Педиатры чаще всего сталкиваются с четырьмя диатезами: аллер-
гическим (атопический), экссудативно-катаральным, лимфатикогипопластическим, нервно-артритическим.
Экссудативно-катаральный и аллергический диатезы имеют во многом сходную клиническую картину (оба могут реализоваться как атопический дерматит) и этиологические моменты, но различаются по патогенезу.
Профилактику заболеваний, к которым предрасположены некоторые дети можно вести исходя из: 1) выделения групп риска по развитию тех или иных заболеваний, или 2) отнесения таких детей к тому или иному диатезу. В настоящее время все большее распространение получает выделение групп риска (группа здоровья IIА и IIБ) по развитию хронической патологии. Т.О. в настоящее время диатезы являются основанием для отнесения этой категории детей к той или иной группе риска.
Профилактика заболеваний, к которым предрасположены дети с диатезами, должна начинаться до рождения ребенка. Еще до беременности необходимо позаботиться о лечении хронической генитальной и экстрагенитальной патологии у будущей матери. Беременная женщина должна соблюдать рациональную диету. Важное значение играет устранение с первого месяца беременности профессиональных вредностей, избыточного пребывания на солнце, прекращение активного и пассивного курения, неблагоприятного воздействия различный излучений, медикаментов. Следует иметь в виду, что пролонгированное
5

естественное вскармливание является важным фактором при предупреждении многих заболеваний. Вопросы питания детей с диатезами являются ключевыми для предотвращения развития таких заболеваний как атопический дерматит, бронхиальная астма, пищевая аллергия. Важное место питание занимает и в предотвращении развитий обменных заболеваний.
Существенным моментом предупреждения развития заболеваний является контроль за состоянием окружающей среды. Хорошо известно, что частые инфекционные заболевания, аллергические болезни напрямую связаны с неблагополучием в состоянии окружающей среды.
Повышение адаптации организма к неблагоприятным факторам окружающей среды, инфекциям особенно важно для детей с такими диатезами, как лимфатико-гипопластический и экссудативно - катаральный. Укрепление иммунологической реактивности организма таких детей путем закаливания, организации рационального образа жизни, применения адаптагенов, иммуномодуляторов поможет уменьшить частоту инфекционных заболеваний и патологических состояний к которым были предрасположены дети с диатезами.
Вопросы к экзамену. Понятие о конституции человека, конституцио-
нальных типах, диатезах. Современные направления профилактики развития заболеваний, связанных с диатезами.
ЭКССУДАТИВНО-КАТАРАЛЬНЫЙ (псевдоаллергический)
ДИАТЕЗ (ЭКД) – своеобразное состояние организма, сопровождающееся наклонностью кожи и слизистых к возникновению инфильтра- тивно-десквамотозных процессов, лимфоидной гиперплазией, лабильностью водно-солевого обмена, особенностями обмена гистамина, белка и углеводов.
Эпидемиология. ЭКД встречается у 40-60% детей первого года жизни.
Этиология и патогенез. В основе ЭКД лежит наследственная предрасположенность к особенностям обмена веществ, водноэлектролитного баланса. Формированию указанных особенностей способствуют: патология беременности, заболевания матери, патология ЦНС у ребенка. В результате формируется своеобразие функций вегетативной нервной системы (ваготония с повышением уровня ацетилхолина), мастоцитарной системы (повышенная либерация медиаторов воспаления), регуляции внутриклеточных функций кальция, своеобра-
6
зие структуры соединительной ткани и сосудистой стенки. Морфофункциональная незрелость ЖКТ приводит к неполному расщеплению пищи, нарушениям всасывания, гиперпродукции IgE.
При ЭКД имеют место многочисленные особенности обменов, которые проявляются: тенденциями к гипопротеинемии, гипергликемии, гиперлипидемии, дисфункции надпочечников (дискортицизм), формированию нестабильности клеточных мембран, снижению барьерной функции кишечника, снижению активности ферментов кишечника, анаэробному типом обмена веществ, неполноценности соединительной ткани, нарушению обмена трансферрина, лабильности водноэлектролитного обмена.
Патогенез ЭКД в некоторых аспектах похож на механизмы развития атопического дерматита, однако при ЭКД отсутствует иммунологическая стадия, а есть лишь патохимическая и патофизиологическая. Характерны гистаминазные и либераторные нарушения (избыточный синтез гистамина, недостаточная активность гистаминазы), а так же нарушения в обмене циклических нуклеотидов (нарушения синтеза ц- АМФ и ц-ГМФ).
7
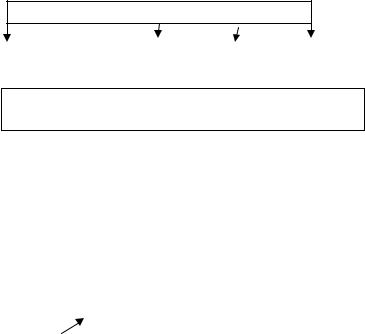
Факторы, способствующие формированию ЭКД
Незрелость |
|
Наследственная |
|
Патология бе- |
|
Патология |
ЖКТ |
|
предрасположенность |
|
ременной |
|
НС у ребенка |
|
|
|
|
|
|
|
Формирование у ребенка особенностей обмена веществ, вводно-
электролитного баланса, иммунологической реактивности
Снижение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Формиро- |
|
Нару- |
|||
|
|
Форми- |
|
|
Тенден- |
|
Пастоз- |
|
|||||||||||||||
барьерной |
|
|
|
|
ция к |
|
|
|
вание |
|
шения |
||||||||||||
функции |
|
|
рование |
|
|
|
ность, |
|
|
|
|
веге- |
|||||||||||
|
|
неста- |
|
|
гипо- |
|
рых- |
|
|
|
дисфунк- |
|
|||||||||||
кишечни- |
|
|
|
|
протеи- |
|
|
|
|
ции над- |
|
татив- |
|||||||||||
ка |
|
|
бильно- |
|
|
|
лость, |
|
|
|
|
ной |
|||||||||||
|
|
|
|
немии, |
|
|
|
|
почечни- |
|
|||||||||||||
|
|
|
|
сти кле- |
|
|
|
избы- |
|
|
|
|
НС |
||||||||||
|
|
|
|
|
|
гиперг- |
|
|
|
|
ков |
|
|||||||||||
|
|
|
|
точных |
|
|
|
точная |
|
|
|
|
(веге- |
||||||||||
|
|
|
|
|
|
лике- |
|
|
|
|
|
|
|||||||||||
|
|
|
|
мембран |
|
|
мии, |
|
масса |
|
|
|
|
|
тоди- |
||||||||
|
|
|
|
|
|
|
|
|
|
|
гипер- |
|
тела |
|
|
|
|
|
сто- |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ния) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
липи- |
|
|
|
|
|
|
|
|
|
|||
Низкая ак- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
тивность |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
гистаминазы |
|
|
|
Высвобождение |
|
|
|
Избыток секреции, уси- |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
ленный выброс гистамина |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
гистамина |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Дозо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
Развитие кожных и других проявлений экссуда- |
|
|
||||||||||||||||
|
зависи- |
|
|
|
|||||||||||||||||||
|
си- |
|
|
|
|
|
|
|
тивно-катарального диатеза |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 1.1. Схема патогенеза ЭКД
Исследования при ЭКД не требуются.
Анамнез, клиника. Начальные появления ЭКД обнаруживаются уже в первые месяцы жизни. Дети с ЭКД имеют избыточную массу тела. Кожа отличается бледно-розовой окраской. При прикладывании к коже кисти руки на ней остаются отпечатки ладоней, свидетельствующие о выраженной лабильности сосудистых реакций. Характерны пастозность (не отеки!) и снижение тургора мягких тканей. Часто возникают опрелости, которые носят упорный характер даже при хорошем уходе за ребенком. Отмечается неравномерная прибавка в массе тела. Периодически возникает поллакиурия и/или склонность к олигурии.
Наиболее частыми кожными проявлениями при ЭКД являются:
8

1)пастозность кожи щек, которая сопровождается легким шелуше-
нием;
2)гнейс, молочный струп;
3)преходящая эритема кожи щек, ягодиц.
Основной особенностью кожных проявлений считается их обратимость при применении элиминационных мероприятий, гипоаллергенной диеты. К 3-4 годам проявления ЭКД проходят. Несвоевременное и неадекватное проведение у ребенка с ЭКД лечебно-профилактических мероприятий приводит к трансформации ЭКД в атопический дерматит.
Диагноз ЭКД устанавливают при наличии характерных клинических проявлений. Лабораторные исследования бывают необходимы для проведения дифференциального диагноза.
Дифференциальный диагноз ЭКД проводят в первую очередь с атопическим дерматитом (табл. 1.1).
Табл. 1.1. Дифференциальный диагноз экссудативно -
катарального диатеза и атопического дерматита
Признак |
Экссудативно - |
Атопический дер- |
|
катаральный |
матит |
|
диатез |
|
Атопия в анамнезе или |
Редко (10-15%) |
Характерно |
наследственная пред- |
|
|
расположенность |
|
|
Зуд кожных покровов |
Не характерно |
Характерно |
Реакция немедленного |
Не характерна |
Характерно |
типа при кожном тести- |
|
|
ровании с аллергенами |
|
|
Высокий уровень IgЕ в |
Не характерен |
Характерен |
сыворотке крови |
|
|
Дозозависимость (ко- |
Характерно |
Не характерно |
личество съеденной |
|
|
пищи) |
|
|
Кожные проявления |
Гнейс, молочный |
Стойкая гиперемия |
|
струп, опрелости, |
или преходящая эри- |
|
сухость кожи. |
тема, папуло- |
|
Кожный синдром |
везикулезные высы- |
|
нестойкий, ло- |
пания на эритематоз- |
|
кальный |
ном фоне с экссуда- |
|
|
цией или инфильтра- |
9

цией, лихинификации
* лихинификация – утолщение и усиление кожного рисунка
Лечение, задачи лечения: предупреждение развития атопического дерматита и других аллергических заболеваний.
Схема лечения: Обязательное лечение: уход, диета, воспитание.
Вспомогательное лечение: антигистаминные препараты, ферменты, витамины, препараты кальция, кетотифен, местное лечение.
Показания для госпитализации. Дети с ЭКД наблюдаются амбула-
торно.
Диета: гипоаллергенная с исключением облигатных аллергенов. Питание детей с ЭКД должно проводиться с учетом следующих
положений:
а) необходимо обеспечить детям с ЭКД длительное грудное вскармливание (хотя бы до 4-6 месяцев).
б) детей со слабой чувствительностью к белкам коровьего молока можно кормить кисломолочными смесями (НаН кисломолочный, Бифилин, ацидофильная смесь Малютка и др.);
в) если при исключении из рациона белков коровьего молока сохраняются проявления ЭКД необходимо исключить реакции на глютен (белок злаков). В этом случае следует назначить продукты, не содержащие глютен (каши НаН, Хумана, Хайнц);
г) первый прикорм вводят с 5-6 месяцев в виде гипоаллергенных каш промышленного производства. Наименее аллергогенными являются: кукурузная и гречневая каши;
д) второй прикорм – овощного пюре (кабачки, патиссоны, капуста, картофель). Объем картофеля не должен превышать в составе овощного пюре 20%. Вначале дают прикорм одного вида овощей, затем его состав постепенно расширяют каждые 3-4 дня;
е) мясное пюре начинают вводить в 6-7 месяцев: постная говядина и свинина, конина, белое мясо индейки;
ж) третий прикорм – в 7-8 месяцев – второе овощное или овощекрупяные блюда (кабачки, тыква, гречка);
з) требования к обработке продуктов: картофель вымачивают 12-14 часов, крупы – 1-2 часа, мясо дважды проваривают;
и) исключают: яйца, копчености, печень, рыбу, икру, морепродукты, сыры острые и плавленые, грибы, орехи, кофе, шоколад, газированные напитки, мед.
Медикаментозное лечение. В лечении ЭКД используют антигистаминные препараты: I поколения (супрастин, диазолин, фенкарол, тавегил по 2 мг/кг массы тела в сутки в 3 приёма в течение 10-14 дней); II
10

поколения (зиртек с 6 месяцев 5-10 капель 1 раз в сутки натощак в т е- чение от 14 дней до 6 месяцев) ксизал; эриус, кестин, телфаст с 4-х летнего возраста по 1 таблетке 1 раз в день утром.
Антилибераторы, мембраностабилизаторы показаны при упорном течении ЭКД (кетотифен 0,05 мг/кг массы тела в сутки в 2 приёма во время еды); циннаризин – по 12,5 мг 3 раза в день, длительно в течение нескольких месяцев.
Местное лечение включает ванны с ромашкой, отрубями, чередой. Показаны индифферентные мази без гормонов (например, нафтолановая).
Детям с ЭКД необходимо ограничить необоснованное применение медикаментозных средств. Показан индивидуальный подход к проведению профилактических прививок.
Прогноз. При соблюдении требований к питанию, уходу, окружающей среде, проведении адекватных лечебных мероприятий прогноз благоприятный.
Вопросы к экзамену. Экссудативно-катаральный диатез: этиология,
патогенез, проявления, лечебно-профилактические мероприятия, прогноз.
ЛИМФОТИКО-ГИПОПЛАСТИЧЕСКИЙ ДИАТЕЗ (ЛГД)
ЛГД – врожденная генерализованная иммунопатия с нарушением одновременно клеточного и гуморального иммунитета и дисфункцией эндокринной системы. При ЛГД о тмечается: гиперплазия ретикулярной стромы вилочковой железы и лимфатических узлов, и гипоплазия хромаффинной ткани, ретикулоэпителиального аппарата, аорты, сердца, гладкой мускулатуры, половых желез, а главное – гипофункция надпочечников. Из всех диатезов ЛГД наименее востребованный практическим здравоохранением. С практических позиций большее практическое значение имеет синдром увеличенной вилочковой железы (СУВЖ).
Предрасполагающие факторы. По данным Л.В. Володиной к группе риска рождения ребенка с ЛГД относятся женщины, имеющие следующие заболевания:
1)эндокринные – ожирение, сахарный диабет;
2)аллергические – бронхиальная астма, поллиноз, аллергодерматоз, рецидивирующая крапивница, отек Квинке, инсектная и медикаментозная аллергия, фотодерматоз;
3)гнойно-септические – абсцессы, гнойный аппендицит, гнойный отит, фурункулез, рецидивирующий блефарит, длительное заживление ран.
11
Эпидемиология. Частота ЛГД изучена недостаточно. Увеличение вилочковой железы II–III степени чаще встречается у детей первого года, а I степени - у детей старше года.
Этиология. Причины развития ЛГД мультифакториальные. Чаще всего они обусловлены неблагоприятными воздействиями на плод в периоде эмбрио- и фетогенеза (неблагоприятные воздействие факторов внешней среды, заболевания матери, неблагоприятное течение беременности и родов), что приводит к нарушениям формирования органов иммунной и эндокринной систем. Матери детей с СУВЖ имеют хронические очаги инфекции, аллергические заболевания, эндокринную патологию, отягощенный акушерский анамнез, неблагоприятное течение беременности (гестоз 2-й половины), патологию в родах.
В некоторых случаях СУВЖ может быть генетически детерминированным, а также может развиваться при интранатальном поражении плода и в периоде постнатального онтогенеза.
Патогенез. Неблагоприятные факторы, воздействующие на плод во время беременности, приводят к формированию нарушений в функционировании гормональной системы. В результате развивается дисфункция гипофиза, щитовидной железы, гипоталамуса (по принципам прямой и обратной связи).
У детей с ЛГД выявляется снижение уровня кортизола в крови. Низкому уровню кортизола соответствует низкий уровень АКТГ, что свидетельствует о нарушении регуляции коры надпочечников гипота- ламо-гипофизарной системой.
Система иммунитета у детей раннего возраста с ЛГД функционирует с большим напряжением, что создает предпосылки для ее быстрого истощения.
Иммунная недостаточность при ЛГД характеризуется избыточной пролиферацией и задержкой созревания Т-лимфоцитов в тимусе. У детей с ЛГД как в острый период интеркурентных заболеваний, так и в период реконвалесценции отмечается высокий лимфоцитоз и более низкие показатели IgG, а в период выздоровления и IgA. Также снижено содержание лизоцима, комплемента в сыворотке крови, фагоцитарная активность нейтрофилов.
Нарушения в иммунной системе являются одним из факторов формирования повышенной частоты инфекционных заболеваний у ребенка.
Исследования. Общий анализ крови и мочи, рентгенография органов грудной клетки, УЗИ вилочковой железы, иммунограмма.
12
Анамнез, клиника. У большинства детей с ЛГД отмечаются округлые формы тела, легкая пастозность тканей, относительно крупные черты лица, гипертелоризм, запавшая переносица, короткая шея, широкая грудная клетка, широкие плечи, широкие ладони и стопы, относительно короткие и широкие пальцы, светлая окраска волос и глаз, слабо развитая мускулатура и сниженная физическая активность. Особенностями роста и развития детей с ЛГД являются асинхронизм развития и созревания, наиболее выраженный на 1-м году жизни.
Характерна бледность кожных покровов с мраморным рисунком, повышенная гидрофильность тканей. У многих детей с ЛГД выявляют генерализованную гиперплазию лимфатических узлов и скоплений лимфоидных тканей, гипертрофию миндалин и аденоидов, возникающую при инфекционных заболеваниях, вакцинации, и сохраняющуюся длительно после выздоровления.
Ребенок с ЛГД отличается спокойствием, замедленной реакцией на болевые раздражители, снижением возбудимости ЦНС. С возрастом – отсутствуют претензии на лидерство. Отмечается склонность к рецидивирующим (затяжным) или хроническим воспалительным заболеваниям (частые ОРИ, аденоидиты, синуситы, хронические тонзиллиты, длительные субфебрилитеты).
У детей раннего возраста с ЛГД отмечается высокая частота атопического дерматита. Со стороны ЦНС чаще встречаются такие синдромы как гипертензионно-гидроцефальный, судорожный, мышечной гипотонии, вегетативно-висцеральных дисфункций. Нередко возникает нарушение терморегуляции вслед за перенесенным инфекционновоспалительным заболеванием в виде длительного (от 2 нед. до 2-3 мес.) субфебрилитета.
Эти дети угрожаемы по развитию аутоиммунных состояний, лимфом, лейкозов, бронхиальной астмы, сахарного диабета. Отмечается высокий риск синдрома внезапной смерти, имеется предрасположенность к туберкулезу. Возможны анафилактоидные реакции на вакцины, некоторые лекарственные средства.
Диагноз ЛГД устанавливается на основании особенностей клиники: 1) внешний вид: избыточная полнота, пастозность тканей (не отеки!), бледность кожных покровов, снижение тургора тканей, некоторая гиподинамия и эмоциональная вялость, диспропорции телосложения (короткая шея и туловище, относительно длинные конечности);
2)лимфопролиферативный синдром: лимфополиаденопатия, ги-
перплазия небных и глоточных миндалин, разрастание аденоидов, тимомегалия;
3)склонность к надпочечниковой недостаточности;
13
4)сердечно-сосудистый синдром: приглушенность тонов, функ-
циональный систолический шум на сосудах шеи, тенденция к тахикардии, тенденция к снижению АД;
5)аллергические (неатопические) симптомы: артралгии;
6)синдром сдавления жизненно важных органов у детей с тимо-
мегалией: осиплость голоса, низкий тембр, «петушиный крик» при плаче, запрокидывание головы во время сна, шумное дыхание, жесткое дыхание (тимическая астма);
7)гипопластический синдром (редко): гипоплазия половых орга-
нов, сердца, аорты, щитовидной и паращитовидных желез, хромаффинной ткани надпочечников.
Диагноз СУВЖ основывается на выявлении при рентгенологическом (ультразвуковом) исследовании увеличенной вилочковой железы.
Лабораторные исследования В анализах крови отмечается повышение общего количества лим-
фоцитов; Иммунограмма: снижение уровня Т-лимфоцитов и более высокое
содержание В-лимфоцитов. Выявляется более низкий уровень Т- лимфоцитов-супрессоров, что приводит к повышению иммунорегуляторного индекса (CD4/CD8). Функциональная активность В- лимфоцитов ниже показателей у здоровых детей. Уровень IgG часто снижается, содержание IgE - повышается.
Дифференциальный диагноз
Табл. 1.2. Основные направления дифференциальной диагно-
стики при ЛГД
Признак |
Исключаемая патология |
Увеличение вилочко- |
ВПС, врожденные и приобретенные карди- |
вой железы |
ты, ложная кардиомегалия, кардиомиопатии |
Снижение уровня |
Железодефицитная анемия |
ферритина в крови |
|
Повышенная частота |
Первичные и вторичные иммунодефицитные |
инфекционных забо- |
состояния, запаздывание созревания иммун- |
леваний |
ной системы, «часто болеющие дети» |
Лимфополиаденопатия |
Лимфогранулематоз, лимфомы, лейкозы, |
|
туберкулез, болезнь кошечьих царапин, ток- |
|
соплазмоз, инфекционный мононуклеоз, ин- |
|
фекции при иммунодефицитах, гистиоцитоз |
|
Х, саркоидоз, ОРВИ, болезни накопления |
|
14 |
Лечение, задачи лечения: предупреждение неблагоприятных реакций организма на стрессы, инфекции, оперативные вмешательства; уменьшение частоты инфекционных заболеваний.
Схема лечения. Обязательное лечение: диета, режим, адаптогены, витамины.
Вспомогательное лечение: иммуномодуляторы, бактериальные лизаты, глюкокортикоиды.
Показания для госпитализации: необходимость проведения углубленного обследования.
Диета. Борьба за грудное вскармливание. В случае его отсутствия - использование адаптированных кисломолочных или гипоаллергенных смесей («NAN ГА» и «Nutrilon ГА»). Постепенно и осторожно вводятся овощи и фрукты, нежирные сорта мяса, рыбы.
Режим. Необходим оптимальный двигательный режим, пребывание на свежем воздухе, массаж. Исключение сильных раздражителей (оральный путь введения медикаментов, применение щадящих процедур и т.д.)
Медикаментозное лечение. Иммуномодуляторы (Тактивин - от 6 месяцев до 14 лет препарат назначают подкожно из расчета 2–3 мкг на 1 кг массы тела в течение 7-10 дней; тимоген – интраназально детям до 1 года по 10 мкг, 1-3 лет – по 10-20 мкг, 4-6 лет по 20-30 мкг, 7-14 лет 50 мкг в течение 3 -10 дней;). Повторные курсы Тактивина до 4 раз в год. Терапию Тактивином проводят под контролем иммунограммы.
Витамины: А курсом 30 дней; В1 курсом 15-30 дней; В5 курсом 10-
15 дней; В15 –, курсом 2-3 месяца; С – курсом 15-30 дней; В15 - курсом 2-3 месяца.
Профилактика ОРИ также включает: ограничение контактов с больными детьми, курсы виферона (мазь) 2 раза в день в нос в течение 10 дней каждого месяца 3 месяца; имунорикс - детям старше 3 лет: по 400 мг (1 флакон) один раз в сутки вне приема пищи в течение 20 дней и более., аскорбиновая кислота и витамины группы В; эхинацею – детям 1-6 лет по 5-10 капель, 6-12 лет по 10-15 капель, старше 21 лет по 20 капель 3 раза в сутки, продолжительностью не менее 8 недель.
Показано применение бактериальных лизатов местного (ИРС-19, имудон) и системного действия (бронхомунал, рибомунил и др.).
При проведении плановых оперативных вмешательств у детей с СУВЖ рекомендуют применение малых доз (25 мг) гидрокортизона непосредственно перед оперативным вмешательством.
15
Фитотерапия. Назначают травы и растения, обладающие десенсибилизирующим эффектом: ромашка, тысячелистник, черника, черемша, почки и соцветия березы.
С целью стимуляции функций коры надпочечников используют настой листьев черной смородины, корень солодки.
Рекомендуются адаптогены: пантокрин - внутрь по 10-15 капель или 1/4-1/2 таблетки 2-3 раза в день, запивая водой, за 20-30 мин до еды или через 3 ч после еды. Курс лечения составляет 3-4 недели, заманиха, левзея, настойка женьшеня по 1 капле на год жизни 3 раза в день 10 дней и др.
При тимомегалии: фитотерапия (ромашка, тысячелистник, почки и соцветия березы, черемша, черника, облепиховое масло). При выраженной тимомегалии - короткие курсы глюкокортикоидов.
Вакцинопрофилактика у детей с СУВЖ имеет свои особенности. Для детей с увеличенной вилочковой железой I–II степени остаются те же показания и противопоказания, что и для здоровых детей. Однако, учитывая высокую частоту перинатальной энцефалопатии, в т.ч. ги- пертензионно-гидроцефального синдрома, у этого контингента детей показано назначение диакарба по схеме. Вакцинацию следует проводить на фоне гипоаллергенной диеты и гипосенсибилизирующей терапии за 3 дня до и 3 дня после прививки.
Дети с СУВЖ III степени требуют наблюдения и временного медицинского отвода от профилактических прививок сроком на 3–6 месяцев. Этим детям рекомендуется повторное обследование для уточнения размеров вилочковой железы. При уменьшении размеров вилочковой железы в период клинического благополучия показана вакцинация на фоне гипоаллергенной диеты и гипосенсибилизирующей терапии. Вакцинация у детей с СУВЖ разной степени требует рациональной тактики подготовки и проведения с учетом индивидуальных особенностей ребенка. У детей с СУВЖ III степени рекомендуют курс иммунокорригирующей терапии Тактивином. После курса Тактивина реакцию Манту можно делать не ранее, чем через 2 месяца, так как возможен ложноположительный результат.
После проведения иммунокорригирующей терапии вакцинация показана не ранее чем через 1-2 месяца после ее окончания.
Дети с ЛГД и СУВЖ требуют диспансерного наблюдения иммунолога и эндокринолога.
Прогноз при ЛГД определяется особенностями клинических проявления диатеза, степенью иммунологических нарушений, эффективностью лечебно-профилактических мероприятий. Обычно при ЛДГ прогноз благоприятный.
16

Вопросы к экзамену. Лимфатический диатез: этиология, патогенез,
проявления, лечебно-профилактические мероприятия, прогноз.
НЕРВНО-АРТРИТИЧЕСКИЙ ДИАТЕЗ (НАД) (урекимический или мочекислый диатез) - наследственно обусловленный, энзимодефицитный синдром с нарушением пуринового обмена и повышением синтеза мочевой кислоты. Характерна неустойчивость углеводного и липидного обмена, кетоацидоз, нарушение ацетилирования.
Эпидемиология. НАД встречается у 2-5% детей.
Этиология НАД связана с наследственно обусловленным дефектом пуринов, нарушениями питания у матерей во время беременности (избыток мяса), и у детей раннего возраста. В наследственном анамнезе выявляется повышение возбудимости ЦНС и нарушение активности энзимов, обеспечивающих метаболизм пуриновых и пиримидиновых оснований и ацетилирующей способности печени: артриты, моче- и желчекаменная болезнь, подагра, СВД, мигрень и др.
Патогенез. Гиперурикемия повышает возбудимость ЦНС, усиливает чувствительность стенки сосудов к действию катехоламинов, оказывает диабетогенное действие, способствует камнеобразованию (см.
рис. 1.2.).
Исследования. Общий анализ крови и мочи, определение уровня мочевой кислоты в крови, исследование показателей КОС.
Анамнез клиника. НАД наиболее ярко проявляется в детей в возрасте 6-7 лет. В анамнезе: плохая прибавка в массе тела, неустойчивый стул, снижение аппетита. Часто отмечается белый быстрый дермографизм, тахикардия, субфебрилитет, симпатикотония.
Дети с НАД предрасположены к развитию гипотрофии, рвоте, психоневрозам, инфекционно-метаболическому артриту, дисметаболическим нефропатиям, интерстициальному нефриту, сахарному диабету.
Нервно-психический синдром: повышенная возбудимость, хорееподобные гиперкинезы, тики, ночные страхи, эмоциональная лабильность, ускоренное развитие психики и речи (дети – вундеркинды);
Мутация гена, |
|
Повышенный распад |
|
Повышенное посту- |
регулирующего |
|
пуринов при гемоли- |
|
пление пуринов в |
ферменты обме- |
|
тических заболева- |
|
организм с продук- |
на |
|
ниях |
|
тами питания |
|
|
|
|
|
 17
17

|
|
Гиперурикемия |
|
ЦНС |
|
||
|
|
|
|
|
|
|
|
|
|
|
Система |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Суставы |
|
|
|
|
|
Угле- |
|
||||||
Нев- |
|
мочевы- |
|
|
|
|
|
Белко- |
|
|
водный |
|
|||||
|
деления |
|
|
|
|
|
|
|
|
||||||||
расте- |
|
|
|
Арт- |
|
|
вый |
|
|
обмен |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
ниче- |
|
|
|
|
|
|
ралгии |
|
|
обмен |
|
|
|
|
|
|
|
ский |
|
|
Сти- |
|
|
|
|
|
|
|
|
|
|
|
|||
син- |
|
|
муля- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Бронхос- |
|
|||||
дром |
|
|
ция |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Салурия, |
|
|
|
|
|
пазмы, |
|
||||||
|
|
|
|
мозго- |
|
|
|
Ацетоне- |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
мигрени, |
|
|||||
|
|
|
|
|
|
нефро- |
|
|
|
||||||||
|
|
|
|
вой |
|
|
|
мическая |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
колики, |
|
|||||||
|
|
|
|
дея- |
|
|
литиаз |
|
рвота |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
запоры, |
|
|||||||
|
|
|
|
тель- |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
кожные |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
ности |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
проявле- |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ния |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Рис. 1.2. Схема патогенеза НАД
Дисметаболический синдром: извращение аппетита, анорексия, медленная прибавка массы тела, «беспричинные» повышения температуры, транзиторные аритмии, приглушенность тонов сердца, симптомы ацетонемических кризов (внезапная, частая, циклическая рвота с развитием обезвоживания, повышением температуры, появлением запаха ацетона), болевые симптомы (боли в животе, дизурические проявления, боли в мышцах разгибателях, мигрени, невралгии, артралгии, реже артриты).
Спастический синдром: склонность к повышению артериального давления, бронхоспазмы, головные боли, запоры, кардиалгии.
Диагноз. НАД диагностируют по наличию нарушений обмена веществ в анамнезе, выявлению клинических проявлений диатеза.
Лабораторные данные. Маркерами НАД являются: уратурия и высокий уровень мочевой кислоты в крови.
В общем анализе крови встречается эозинофилия.
При исследовании КОС выявляют ацидоз.
Дифференциальный диагноз
Табл. 1.3. Дифференциальный диагноз нервно-артритического диатеза (основные направления)
Признак |
Исключаемая патология |
Гиперкинезы |
Ревматизм, интоксикации, хорея подражания, ги- |
|
18 |
|
перкинетическая форма ДЦП, хорея Гентингтона, |
|
болезнь Вильсона-Коновалова, опухоль мозга, син- |
|
дром Леша-Нихана, пароксизмальный хореоатетоз |
Тики |
Экзогенные перегрузки в школе, миоклонии, син- |
|
дром Жиль де Ла Туретта, синдром китайского |
|
болванчика |
Эмоциональная |
Вегетативная дисфункция, соматические заболева- |
лабильность |
ния, минимальная мозговая дисфункция, интокси- |
|
кации, прием наркотиков, и т.д. |
Боли в животе |
Глистная инвазия, пиелонефрит, гастрит, гепатит, |
|
панкреатит, и т.д. |
Дизурические |
Цистит, инфекция мочевых путей, дисметаболиче- |
проявления |
ская нефропатия, пиелонефрит |
Мигрень |
Повышение внутричерепного давления, повышение |
|
АД, эпилепсия, нейроинфекции, опухоли мозга, го- |
|
ловная боль при соматических и инфекционных за- |
|
болеваниях |
Анорексия |
Нарушения питания, острые и хронические заболе- |
|
вания органов пищеварения, ЖДА, наследственные |
|
дегенеративные поражения мозга, обменные заболе- |
|
вания, хронические интоксикации, сердечные не- |
|
достаточность, ХПН, острые и хронические инфек- |
|
ционные заболевания |
Рвота с разви- |
Острые кишечные инфекции, острая надпочечнико- |
тием обезво- |
вая недостаточность, сахарный диабет, инвагинация |
живания |
кишечника, пиелонефрит, язвенная болезнь, холеци- |
|
стит |
Лечение, задачи лечения: нормализация обмена мочевой кислоты, предупреждение негативного влияния мочевой кислоты на внутренние органы.
Схема лечения: Обязательное лечение: диета, режим.
Вспомогательное лечение: витаминотерапия, седативная терапия, нормализация обмена мочевой кислоты.
Показания для госпитализации: ацетонемическая рвота, необходимость углубленного обследования.
Диета: а) ограничение в рационе: телятины, птицы, субпродуктов (печень, сердце, мозги, почки, легкие), колбасных изделий, грибов (белые, шампиньоны), рыбных бульонов, студня, щавеля, шпината, ревеня, петрушки, спаржи, цветной капусты, полированного риса, ов-
19

сяной крупы, соусов, бобов, рыбы, кофе, какао, крепкого чая, пряностей, специй;
-обильное щелочное питье, особенно во вторую половину дня (с 1 месяца 1 чайная ложка теплого дегазированного боржоми на кг массы на сутки);
-клюква, лимоны;
-витамин В6 в утренние часы;
-цитратная смесь;
б) в период ацетонических кризов рекомендуют: яблочные, арбузные, картофельные и другие разгрузочные дни;
в) рекомендуют в диете: молоко, молочные продукты, овощи (кроме запрещенных), фрукты и ягоды, мучные и крупяные изделия, варенье, мед, сахар, сливочное и растительное масла.
Режим охранительный: достаточный отдых, ограничение чрезмерных психо-эмоциональных нагрузок, гимнастика, водные процедуры.
Седативная терапия (травы: валериана, хвощ, мята, пустырник, при необходимости - медикаментозная терапия).
Транквилизаторы (при отсутствии эффекта от фитотерапии) - сибазон, диазепам, седуксен – максимальная суточная доза для детей 10 мг 2-3 раза в день курсом по 10-14 дней.
При выраженной гиперурикемии у детей старше 10 лет показаны: этамид – детям школьного возраста по 1/2-1 таблетке 4 раза в сутки, курс лечения 10-12 дней, спустя 5-7 дней курс повторяют, лечение проводят под контролем лабораторных исследований мочи; бутадион
– детям до 6 месяцев не назначают, 6-12 месяцев разовая доза 0,01 г, 1-
3лет 0,02 г, 3-4 лет 0,03г., 5-6 лет 0,04 г, 7-9 лет 0,05-0,06 г., 10-14 лет
0,08-0,1 г 3 раза в день во время еды, курс лечения 15 -30 дней; аллапуринол –10-20 мг/кг в сутки, принимают внутрь 3 раза в день после еды, запивая большим количеством воды, в течение 2-4 недель; оротовая кислота – внутрь за 1 час до или через 4 часа после еды по 0,25-0,3 г 2-
3раза в день, колхицин – для профилактики 1 мг вечером, курс 3 месяца, применяется у детей старше 12 лет.
Прогноз при НАД определяется выраженностью проявлений диатеза, степенью нарушений обмена мочевой кислоты, реакцией ребенка на проведение лечебно-профилактических мероприятий.
Вопросы к экзамену. Нервно-артритический (мочекислый) диатез: этиология, патогенез, проявления, лечебно-профилактические мероприятия, прогноз.
20
Глава II. Аллергические заболевания
АТОПИЧЕСКИЙ ДЕРМАТИТ (атопическая экзема, синдром атопической экземы/дерматита) (АД) – хроническое воспалительное заболевание кожи, сопровождающееся зудом, которое начинается в раннем детском возрасте, может продолжаться или рецидивировать в зрелом возрасте и приводит к физической и эмоциональной дезадаптации ребенка и членов его семьи.
АД развивается у лиц с наследственной предрасположенностью и часто сочетается с другими аллергическими заболеваниями.
Эпидемиология. Частота АД возросла за последние 3 десятилетия и составляет в развитых странах 10-15% у детей в возрасте до 5 лет и 15-20% у школьников.
Этиология АД многофакторна и полиэтиологична по своей природе. АД развивается у 81% детей, если больны оба родителя, и у 56% если болен один из родителей.
Аллергены, значение которых в развитии АД научно доказано: Пищевые: молоко, яйцо, орехи, соя, пшеница, ракообразные, рыба. Пыльцевые: пыльца, плесневые грибы (споры), пылевые клещи, перхоть животных, тараканы.
Бактериальные: бактерии, staphylococcus aureus, стрептококки. Грибковые: pitorosporum ovale, trichophyton.
Неаллергенные триггеры АД: климат; высокие значения температуры и влажности; химические раздражающие вещества (средства для стирки, мыла, химические вещества для уборки помещений, лосьоны с отдушкой); пища, оказывающая раздражающий эффект (острая, кислая); эмоциональный стресс; хронические заболевания; инфекция; нарушение сна; психосоциальные стрессоры.
Патогенез
При контакте организма с аллергеном образуются IgE антитела, которые фиксируются на тучных клетках в различных органах (период сенсибилизации). При повторном попадании аллергена в организм происходит активация Т-лимфоцитов, которые вырабатывают интерлейкины (IL4, IL5, IL13), цитокины. IL4 является ведущим фактором в переключении синтеза В клетками не обычных иммуноглобулинов, а IgE. В результате реакции антиген + антитело выделяются биологически активные вещества (медиаторы аллергии).
Главным медиатором аллергии является гистамин. Гистамин оказывает свое действие через стимуляцию гистаминовых рецепторов (Н1, Н2, Н3, Н4). В результате развиваются клинические проявления аллер-
21

гии: зуд, сыпи, гиперемия, формирование волдырей. Описываемые изменения относят к ранней аллергической реакции.
Через 4-6 часов после воздействия аллергена развивается поздняя аллергическая реакция. В развитии этого компонента аллергии принимают участие базофилы, эозинофилы, Т-лимфоциты, а так же вещества, выделяемые этими клетками. В результате формируется хроническое аллергическое воспаление.
Воздействие аллергена на организм
Активация Th2 клона CD4 + Т-лимфоцитов
Выработка IL4, IL5, IL13
Гиперпродукция IgE
Образование комплекса IgE + аллерген при
его повторном поступлении
Выделение биологи- |
|
Стресс, дисфункция |
|
Инфекция: sta- |
чески активных ве- |
|
центральной и веге- |
|
phylococcus au- |
ществ: гистамин, |
|
тативной НС. По- |
|
reus, Pityrospo- |
серотонин, брадики- |
|
вышение нейропеп- |
|
rum |
нин, лейкотриены и |
|
тидов, продукция |
|
|
др. |
|
цитокинов |
|
|
|
|
|
|
|
Аллергическое воспаление кожи 

Зуд, расчесы
Атопический дерматит
Рис. 1.3. Схема патогенеза АД
22
Рабочая классификация АД
Возрастные периоды болезни:
-I возрастной период - младенческий (до 2-х лет);
-II возрастной период - детский (от 2-х лет до 13 лет);
-III возрастной период - подростковый и взрослый (от 13 лет и старше).
Стадии болезни:
-стадия обострения (фаза выраженных клинических проявлений, фаза умеренных клинических проявлений);
-стадия ремиссии (неполная и полная ремиссия).
Эпидемиология процесса: ограниченно-локализованный; распространенный; диффузный.
Степень тяжести процесса: легкое течение; средней тяжести; тяжелое течение
Исследования. Общий анализ крови и мочи, копрограмма, УЗИ паренхиматозных органов, кожные пробы, кал на яйца глист, определе-
ние общего IgE. По показаниям: анализ мочи по Нечипоренко, коагулограмма, определение АлАТ, АсАТ, глюкоза крови, при частых обострениях показано иммунологическое исследование и определение специфических IgE; ЭХОЭГ, ЭЭГ, УЗИ, рентгенография придаточных пазух и грудной клетки, постановка кожных проб (не ранее 3 лет при удовле-
творительном состоянии кожи).
Специалисты: аллерголог (установление диагноза, проведение аллергообследования, подбор и коррекция терапии, обучение пациента), дерматолог (диагноз, дифдиагноз, подбор и коррекция местной терапии, обучение), диетолог (индивидуальное питание), гастроэнтеролог (диагностика и лечение гастропатологии), ЛОР (выявление и санация очагов инфекции), психоневролог (коррекция поведенческих нарушений), медицинский психолог (обучение технике релаксации, снятие стресса, модификация поведения).
Исследования амбулаторно, приказ МЗ РФ №268: общий анализ крови, консультация аллерголога. По показаниям: исследование кала на глисты и простейшие, определение общего и специфических IgE, тромбоциты крови, глюкоза крови, посев кала на флору, копрограмма, кожные пробы.
Анамнез, клиника. Клиническая картина АД зависит от возраста ребенка. У детей первого года жизни выделяют два типа течения заболевания.
Себорейный тип характеризуется наличием чешуек на волосистой части головы, которые появляются уже в первые недели жизни, либо
23
протекает как дерматит в области кожных складок. В дальнейшем возможна трансформация в эритродермию.
Нумулярный тип возникает в возрасте 2-6 месяцев и характеризуется появлением пятнистых элементов с корочками; характерная локализация – щеки, ягодицы и/или конечности. Также часто трансформируется в эритродермию.
Дошкольный возраст: у 50% детей, страдающих детской экземой, кожные проявления нивелируются к 2 годам жизни. У оставшейся половины характерная локализация процесса – кожные складки.
Школьный возраст: характерная локализация – кожные складки. Отдельная форма АД в этом возрасте – ювенильный ладонноподошвенный дерматоз, при котором кожный патологический процесс локализуется на ладонях и стопах. Для этой формы АД характерна сезонность: обострение симптомов в холодное время года и ремиссия в летние месяцы. При наличии дерматита стоп необходимо помнить, что дерматофитии у детей наблюдают очень редко. АД с локализацией в области ягодиц и внутренней поверхности бедер обычно появляется в возрасте 4-6 лет и сохраняется в подростковом возрасте.
Фазы атопического дерматита:
Острая фаза (зуд, эритематозные папулы и везикулы, на фоне кожной эритемы, часто сопровождающиеся значительными экскориациями и эрозиями, выделением серозного экссудата).
Подострая фаза (кожная эритема, экскориации, шелушение), в том числе - на фоне уплотнения (лихенификации) кожи.
Хроническая фаза (утолщенные бляшки, лихенификация, фиброзные папулы).
Диагноз. Диагностические критерии АД делят на основные и дополнительные.
Основные критерии: зуд, экзема (острая, подострая, хроническая): с типичными морфологическими элементами и локализацией, характерной для определенного возраста (лицо, шея и разгибательные поверхности у детей 1 года жизни и старшего возраста; сгибательные поверхности, пах и подмышечные области – для всех возрастных групп); с хроническим или рецидивирующим течением.
Дополнительные критерии: наличие дерматита (или дерматит в анамнезе) в области сгибательных поверхностей конечностей (локтевые и подколенные сгибы, передняя поверхность лодыжек); наличие у ближайших родственников бронхиальной астмы или поллиноза; распространенная сухость кожи; начало дерматита до 2-х летнего возраста.
Лабораторно-инструментальные методы исследования:
24
-определение содержания общего IgE в сыворотке крови (тест не яв-
ляется диагностическим);
-кожные тесты (PRIK-тест, скарификационные пробы, внутрикож-
ные пробы) выявляют IgE-опосредованные аллергические реакции, их проводят при отсутствии острых проявлений АД у больного;
-элиминационную диету и провокационный тест с пищевыми аллерге-
нами обычно выполняют для подтверждения диагноза пищевой аллергии особенно к злаковым и коровьему молоку;
-определение аллергеноспецифических IgE АТ в сыворотке крови
(РАСТ, ИФА и др.) предпочтительно для пациентов с ихтиозом, принимающих антигистаминные препараты или антидепрессанты, с сомнительными результатами кожных тестов или при отсутствии корреляции клиники и результатов кожных тестов, с высоким риском развития анафилактических реакций на определенный аллерген при проведении кожного тестирования.
Для оценки тяжести клинических симптомов АД в настоящее время наиболее широко используют шкалы SCORAD (Scoring Atopic
Dermatitis), EASY (Eczema Area and Severity Index), SASSAD (Six Area
Six Sign Atopic Dermatitis Severity Score). В нашей стране широкое распространение получила шкала SCORAD (рис. 1.4), которая учитывает распространённость кожного процесса (А), интенсивность клинических проявлений (В) и субъективных симптомов (С).
A.Распространённость кожного процесса — площадь поражённой кожи, которую рассчитывают по правилу «девятки» (см. рис.1.4, в скобках указана площадь поверхности для детей до 2 лет). Для оценки также можно использовать правило «ладони» (площадь ладонной поверхности кисти принимают равной 1% всей поверхности кожи).
B.Для определения интенсивности клинических проявлений подсчитывают выраженность 6 признаков (эритема, отёк/папулы, корки/мокнутие, экскориации, лихенификация, сухость кожи). Каждый признак оценивают от 0 до 3 баллов (0 - отсутствует, 1 - слабо выражен, 2 - выражен умеренно, 3 - выражен резко; дробные значения не допускаются). Оценку симптомов проводят на участке кожи, где они максимально выражены. Общая сумма баллов может быть от О (кожные поражения отсутствуют) до 18 (максимальная интенсивность всех 6 симптомов). Один и тот же участок поражённой кожи можно использовать для оценки выраженности любого количества симптомов.
C.Субъективные симптомы - зуд кожных покровов и нарушения сна - оценивают у детей старше 7 лет. Пациенту или его родителям предлагается указать точку в пределах 10-сантиметровой линейки, соответствующую, по их мнению, степени выраженности зуда и нару-
25
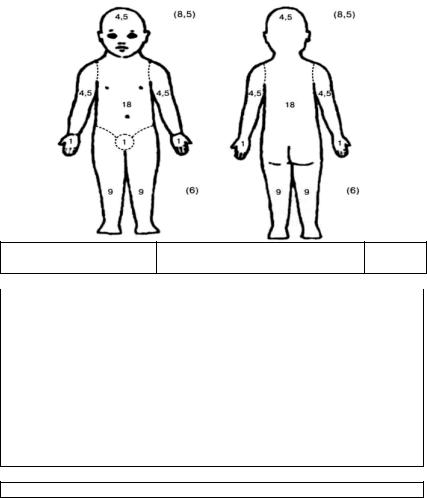
шений сна, усреднённую за последние 3 сут. Сумма баллов субъективных симптомов может колебаться от 0 до 20.
Общую оценку рассчитывают по формуле: А/5 + 7В/2 + С. Общая сумма баллов по шкале SCORAD может составлять от 0 (кли нические проявления поражения кожи отсутствуют) до 103 (максимально выраженные проявления АД).
Рис. 1.4. Определение степени тяжести АД
Укажите площадь поражения (%)
А: Эпидемиология.
В: Интенсивность |
|
Общий балл |
|
|
|
||
Критерий |
Выраженность (балл) |
|
0 |
– отсутствует |
|||
0 |
1 |
2 |
|
3 |
|||
|
|
|
|
||||
Эритема |
|
|
|
|
|
1 |
– слабо |
Отёк/папула |
|
|
|
|
|
2 |
– умеренно |
Корки/мокнутие |
|
|
|
|
|
||
Экскориации |
|
|
|
|
|
3 |
– сильно |
Лихенификация |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
* - сухость кожи оценивается вне очагов островоспалительных изме-
нений и участков лихенификаций
С: Субъективные симптомы
26

Зуд + нарушение сна =
А/5 + 7В/2 + С = Способ расчета
Табл. 1.4. Оценка степени тяжести АД
Легкое течение |
Средне-тяжелое |
Тяжелое течение |
Ограниченные |
Распространенный ха- |
Диффузный характер |
участки пораже- |
рактер поражения кожи |
поражения кожи в вы- |
ния кожи, слабая |
с умеренной экссудаци- |
раженной экссудацией, |
эритема или лихе- |
ей, гиперемией и/или |
гиперемией и/или лихе- |
низация, слабый |
лихенизацией, умерен- |
низацией, постоянным |
зуд кожи, редкие |
ный зуд, более частые |
сильным зудом и прак- |
обострения 1-2 |
обострения 3-4 раза в |
тически непрерывное |
раза в год |
год с короткими ремис- |
рецидивирующее тече- |
|
сиями |
ние |
Впрактической работе для постановки диагноза «АД», как правило, достаточно определения клинических параметров. Первым и обязательным клиническим параметром является зуд. Из остальных четырех параметров необходимо установить не менее трех. К ним относятся:
- характерная локализация поражения кожи; - наличие у ближайших родственников атопического заболевания; - распространенная сухость кожи; - появление дерматита в возрасте до 2-х лет.
Врасшифровке диагноза «АД» наибольшее практическое значение имеют две характеристики: фаза заболевания, тяжесть кожного поражения.
Степень тяжести АД можно также определить по продолжительности периодов обострения и ремиссии, выраженности зуда, распространенности кожного процесса, увеличению периферических лимфатических узлов (табл. 1.4).
27
Дифференциальный диагноз АД проводится с: иммунодефицитами, красным плоским лишаем, инфекциями и инвазиями, метаболическими заболеваниями, розовым лишаем Жильбера, вульгарным ихтиозом, неопластическими заболеваниями, дерматитами, многоформной экссудативной эритемой, экссудативно-катаральным диатезом (см. «Экссудативно-катаральный диатез»).
Лечение, задачи лечения: уменьшение выраженности симптомов болезни; обеспечение длительного контроля над заболеванием, путем предотвращения или снижения тяжести обострения; изменение естественного течения заболевания. Полное излечение пациента в некоторых случаях невозможно.
Схема лечения: Основные направления терапии АД: устранение причинных факторов, вызывающих обострение (диета, гипоаллергенный быт), лечебно-косметический уход за кожей; наружная противовоспалительная терапия, антигистаминные препараты.
Вспомогательное лечение: энтеросорбция, лечебный плазмаферез, фототерапия, цитостатики, антибиотики, витамины, иммуномодуляторы, пробиотики.
Показания к госпитализации: обострение АД, сопровождающееся нарушением общего состояния; распространенный кожный процесс, сопровождающийся вторичным инфицированием; рецидивирующие кожные инфекции; неэффективность стандартной противовоспалительной терапии; необходимость проведения аллергологического обследования.
Диета при АД должна исключать продукты, роль которых в развитии АД доказана. Для детей первого года жизни оптимальным питанием является грудное молоко. При его отсутствии при легких проявлениях АД используют адаптированные смеси с низкой степенью гидролиза (гипоаллергенные смеси – НаН гипоаллергенный, Хипп ГА, Хумана ГА и др.). При выраженных проявлениях АД показано назначение смесей на основе высокой степени гидролиза белка (Алфаре, Нутрилон Пепти ТСЦ, Нутрамиген и др.). Прикормы детям с АД рекомендует водить на 1 месяц позже, чем здоровым.
Наружная терапия АД включает в себя уход за кожей (увлажнение и смягчение) и использование лекарственных средств, наносящихся на кожу. Наружная терапия АД является обязательной частью лечения. Основными задачами наружной терапии при АД являются: а) купирование зуда и воспаления; б) повышение барьерной функции кожи, восстановление водно-липидного ее слоя; в) проведение адекватного ухода за кожей.
Уход за кожей должен осуществляться в зависимости от фазы АД:
28
1.Острая и подострая фазы с мокнутием кожи:
-показано применение влажно-высыхающих повязок, примочек, орошений термальной водой;
-пораженные участки кожи следует своевременно очищать от гноя, корок, чешуек;
-купание детей в эту фазу дерматита не противопоказано, если соблюдаются все правила купания;
-при невозможности купания, применяют очистку кожи специальными мицелловыми растворами (Далианж);
-использование кремов и мазей в этой фазе АД не показано, так как их применение может спровоцировать мокнутие.
2.Острая и подострая фазы без мокнутия кожи:
-ежедневное купание с последующим использованием кремов с ненасыщенной текстурой;
-из средств ухода за кожей предпочтение отдается орошениям термальной водой, использованию эмульсий предпочитаются специальное мыло, гель, мусс.
3.Хроническая фаза:
-основным является применение достаточного количества увлажняющих и главным образом смягчающих средств;
-обязательным является нанесение увлажняющих/смягчающих средств после купания (табл. 1.10);
-некоторым больным, имеющим выраженную сухость кожи, можно рекомендовать неоднократную ванну (душ) в течение дня для усиления гидратации кожи с последующим нанесением на нее увлажняющих/смягчающих средств.
Для наружной терапии АД применяют: топические глюкокортикоиды (ТГК), Элидел, традиционные лечебные средства (анилиновые красители, нафталан, деготь, ихтиол, АСД фракция III). В зависимости от остроты воспалительного процесса для лечения применяют: лосьоны, болтушки, кремы, гели, липогели, мази. Правила выбора лекарственных препаратов при АД представлены в табл. 1.5.
Табл. 1.5. Выбор лекарственной формы нестандартных наруж-
ных противовоспалительных препаратов
Характер воспалительного |
Лекарственная форма |
|
процесса |
||
|
Примочки, аэрозоли, влажно-
Острое воспаление с мокнутием высыхающие повязки, лосьоны, растворы
29

Острое воспаление без мокну- |
Водные болтушки, кремы, ли- |
|
тия |
покремы, пасты, аэрозоли |
|
Подострое воспаление |
Кремы, липокремы, пасты |
|
Хроническое воспаление, ин- |
Мази |
|
согревающие компрессы |
||
фильтрация и лихенизация в |
||
мази с кератолитическими сред- |
||
очагах |
||
ствами |
||
|
||
|
Кремы с добавлением увлаж- |
|
Ремиссия, скрытое течение |
няющих средств, липосомаль- |
|
|
ные кремы, лосьоны |
В настоящее время для наружной терапии применяют или топические глюкокортикостероиды или нестероидные противовоспалительные препараты (табл. 1.6).
Табл. 1.6. Выбор препарата для наружной противовоспалитель-
ной терапии. Ступенчатая терапия АД (EAACI\AAAAI)
Тяжелый АД, не |
Системные иммуносупрессоры |
|
Топические ГКС |
||
поддающийся ле- |
||
Антигистаминные препараты 2-го поколения |
||
чению |
||
Фототерапия |
||
|
||
|
Системные антигистаминные препараты 2-го по- |
|
Умеренные и вы- |
коления |
|
раженные сим- |
тГКС средней и высокой активности |
|
птомы АД |
При стабилизации – ингибиторы кальциневрина |
|
|
(2-я линия) (Элидел) |
|
|
Системные антигистаминные препараты 2-го по- |
|
Легкие и умерен- |
коления |
|
тГКС средней и высокой активности |
||
ные симптомы |
||
При стабилизации – ингибиторы (1.я линия) |
||
АД |
||
кальциневрина (2-я линия) на чувствительные |
||
|
||
|
участки кожи (Элидел) |
|
Только сухость |
Увлажняющие средства, элиминация триггеров |
|
кожи |
||
|
Из ГКС наиболее часто применяют Элоком, Адвантан, Локоид. Указанные препараты выпускают в разных формах. Принципы назначения разных форм ГКС представлены в табл. 1.7.
30

Табл. 1.7. Принципы наружной терапии АД
Эмульсия |
|
Эритема |
|
|
|
Отек |
|
|
ОСТРАЯ |
Везикулы |
|
|
СТАДИЯ |
Выраженный зуд |
|
Крем |
|
|
|
|
ПОДОСТРАЯ |
Вскрытие везикул |
|
|
Экссудация |
||
|
СТАДИЯ |
Корки |
|
Мазь |
|
Шелушение |
|
|
|
||
|
ХРОНИЧЕСКАЯ |
Шелушение |
|
|
Лихенификация |
||
Жирная мазь |
СТАДИЯ |
||
Дисхромия |
|||
|
Методика применения ТГКС
-наружные кортикостероиды назначают в период выраженного обострения АД;
-ограничить длительность такого лечения несколькими днями;
-не применять высокоактивные глюкокортикостероиды для лечения детей, особенно раннего возраста (табл. 1.8);
-на кожу лица и складок не наносить высокоактивные глюкокортикостероиды;
-наносить кортикостероидные препараты только на наиболее пораженные участки кожи;
-исключить длительное применение кортикостероидов.
Табл. 1.8. Классификация топических глюкокортикоидов по степе-
ни активности
Класс (степень ак- |
Наименование препарата |
тивности) |
|
IV (очень сильные) |
Клобетазол |
III (сильные) |
Флутиказон, Целестодерм В, Элоком, |
|
Адвантан, Локоид, Триамцинолон |
II (средней силы) |
Алкометазон |
I (слабые) |
Гидрокортизон, Преднизолон |
|
31 |

Табл.1.9. Минимальный разрешенный возраст применения на-
ружных ГКС
Препарат |
С какого возраста можно |
Частота использования |
|
|
применять |
(доза) |
|
Адвантан |
с 6-месячного |
1 раз в сутки |
|
Афлодерм |
с 6-месячного |
1 -3 раза в сутки |
|
Локоид |
с 6-месячного |
1-3 раза в сутки (обычно не |
|
более 30-60 г в неделю) |
|||
|
|
||
Элоком |
с 6 месяцев |
1 раз в сутки |
Противопоказаниями к применению наружных кортикостероидов являются:
1.Туберкулезный или сифилитический процессы в области нанесения препарата;
2.Вирусные заболевания, в том числе простой герпес, ветряная оспа, опоясывающий лишай в области нанесения препарата;
3.Кожные реакции на вакцинацию в области нанесения препарата;
4.Наличие повышенной чувствительности к компонентам препарата.
Табл. 1.10. Средства дерматологической косметики для ухода за сухой и атопичной кожей (выборочно)
Програм- |
Гигие- |
Увлажне- |
Питание |
Противовоспа- |
ма |
на |
ние |
|
лительное сред- |
|
|
|
|
ство |
Атодерм |
Мусс и |
Крем Ато- |
Крем Ато- |
Крем Атодерм |
|
мыло |
дерм РР; |
дерм, крем |
РО Цинк |
|
Ато- |
Крем Гид- |
Атодерм РР |
|
|
дерм |
рабио |
|
|
Локобейз |
|
Локобейз |
Локобейз |
|
|
|
Репеа |
Репеа |
|
|
|
Локобейз |
Локобейз |
|
|
|
липокрем |
липокрем |
|
Лаборато- |
Мыло, |
Термальная |
Крем Эс- |
Спрей, крем Cu- |
рия Урьяж |
гель |
вода Урьяж, |
мольянт, Эс- |
Zn; крем и гель |
|
Cu-Zn |
крем Гид- |
мольянт Экс- |
Прурисед |
|
|
ролипидик |
трем |
|
32
Лаборато- |
Мыло, |
Молочко |
Крем Экзоме- |
Лосьон Сители- |
рия Дюкре |
гель |
Экзомега |
га |
ум, крем Эпите- |
|
Реальба |
|
|
лиаль |
Системная терапия АД представлена антигистаминными препаратами, стабилизаторами тучных клеток.
Антигистаминная терапия – важный этап лечения АД. Антигистаминные препараты I поколения (димедрол, пипольфен, супрастин, тавегил и др.) из-за выраженных побочных явлений для лечения применяются все реже.
Табл. 1.11. Основные возрастные дозы антигистаминных пре-
паратов
Препарат |
Доза |
Путь введения, |
|
|
кратность |
|
|
|
Аллергодил |
Не назначают до 6 лет. Взрослым |
Внутрь на ночь |
|
по 1т (2мг) |
|
Гисманал |
До 6 лет: 0,2 мг/кг. 6-12 лет: 5 мг в |
Внутрь 1 раз |
|
сутки |
|
|
|
|
Димедрол |
До 1 года: 0,002-0,005, от 2 до 5 |
Внутрь, в/в, в/м, |
|
лет: 0,002-0,005 от 2 до 5 лет: 0,005 |
п/к 1-3 раза |
|
-0,0015, от 6 до 12 лет6 0,015-0,03 |
|
|
|
|
Кларитин |
2-12 лет 5 мг (1/2 таб. или 1ч.л) |
Внутрь 1 раз |
|
|
|
Супрастин |
В зависимости от возраста по ¼- |
Внутрь 2-3 раза, |
|
1/3-1/2 таблетки |
в/м, в/в |
|
|
|
Кетотифен |
В зависимости от возраста по 1/3- |
Внутрь 2 раза |
|
1/2-1 т или 0,05 мг/кг |
|
|
|
|
Пипольфен |
1-2 года, 0,0025г (суточная 0,0075- |
Внутрь 3-4 раза |
|
0,01г), 3-4 года, разовая 0,005г (су- |
Парентерально: |
|
точная 0,015г), 5-6 лет, разовая |
3-5 раз. |
|
0,0075-0,01г (Суточная 0,025- |
|
|
0,03г), 7-9 лет, разовая 0,01г (су- |
|
|
точная 0,03г), 10-14 лет, разовая |
|
|
0,015(суточная 0,045г), |
|
|
Инъекции: 500мкг1мг/кг при в/м |
|
|
введении, при в/в- 1/3 дозы от в/м. |
|
33
Зиртек |
2-6 лет: 2,5 -5 мг (таблетки, капли) |
1-2 раза |
|
|
Старше 6 лет: 10 мг (таблетки, ка- |
|
|
|
пли) |
|
|
Перитол |
6 мес.- 2 года 400 мкг/кг/ сутки, 2- |
3 |
раза |
|
6 лет: 6мг/сутки, 6-14 лет: 12 мг |
|
|
|
сутки. |
|
|
Лоратадин |
Детям старше 2 лет. При массе |
1 |
раз в сутки |
|
более 30 кг – 10 мг. |
|
|
Дезлоратадин |
С 1 г до 5 лет по 1,25 мг; с 6 лет до |
1 |
раз в сутки |
|
11 лет – 2.5 мг |
|
|
Предпочтение при лечении АД следует отдавать препаратам II поколения: Лоратадин, Дезлоратадин, Цетиризин, Фексофенадин.
Антибактериальная терапия
Местное применение антибактериальных препаратов разумно в очагах, колонизированных staphylococcus aureus. Системное применение антибиотиков может быть оправдано у пациентов с подтвержденной бактериальной инфекцией кожи на больших участках.
Комбинированная терапия: тридерм, фуцирокт, фуцидин Г.
Системная иммуномодулирующая терапия применяется в случаях тяжелого течения АД, рефрактерного к стандартной терапии местными средствами.
Системные глюкокортикоиды преднизолон (перорально) или триамцинолон (внутримышечно) можно назначать короткими курсами для купирования тяжелых обострений АД.
Течение АД чаще всего волнообразное, рецидивирующее. Исходы. У 60% детей с АД симптомы заболевания со временем
полностью исчезают. У остальных детей проявления АД сохраняются и рецидивируют на протяжении всей жизни. АД может быть частью так называемого аллергического марша, когда последовательно после АД развивается бронхиальная астма, а затем поллиноз.
Прогноз при АД зависит от возраста детей. Считают, что дети, заболевшие АД на 1-м году жизни имеют лучший прогноз заболевания. С другой стороны, нередко при раннем развитии АД заболевание протекает тяжелее. Неблагоприятное влияние на прогноз оказывают другие сопутствующие заболевания (поллиноз, аллергический ринит).
Профилактика
34

Табл. 1.12. Рекомендации по первичной профилактике пищевой
аллергии у детей раннего возраста с высоким риском развития аллергии
Стратегия профилак- |
Метод или мероприятие |
тики |
|
Идентификация ребенка |
Установление наличия в семье атопии |
высокого риска прена- |
|
тально или в раннем |
|
постнатальном периоде |
|
Исследования |
Повышенный уровень IgE в крови |
Исключение воздействия пищевых аллергенов на ребенка |
|
В периоде беременности |
Не рекомендуется |
В грудном возрасте |
Диета кормящей матери с исключением |
|
яиц, коровьего молока, орехов, дополни- |
|
тельным введением 1500 мг кальция в |
|
сутки |
В питании ребенка |
Грудное вскармливание желательно до 6- |
|
ти месяцев |
Восполнять дефицит грудного молока гипоаллергенной гидролизо-
ванной смесью
Прикорм вводить с 6-ти месячного возраста, начиная с наименее ал-
лергенных продуктов
Вводить 1 раз в неделю или в месяц, если ребенок переносит:
С 9-12 месяцев (коровье молоко, с 1 года куриные яйца, с 3-х лет орехи, рыбу)
Исключить воздействие |
Всем, кто контактирует с ребенком, не |
неблагоприятных неспе- |
курить ни до его рождения, ни после |
цифических факторов |
Устранить все возможные загрязнения |
|
воздуха |
|
Устранить риск вирусных инфекций (со- |
|
хранять грудное вскармливание!) |
Вопросы к экзамену. Атопический дерматит. Этиология Патогенез.
Классификация (стадии развития, периоды и фазы болезни, возрастные клинические формы, распространенность поражения и тяжесть течения). Основные клинико-этиологические и клинико-патогенетические варианты. Методы диагностики. Оценка степени тяжести (SCORAD). Дифференциальный диагноз. Современные подходы к терапии. Течение. Исходы. Прогноз. Профилактика. 35
БРОНХИАЛЬНАЯ АСТМА (БА) – хроническое аллергическое воспаление бронхов, сопровождающееся их гиперреактивностью и периодически возникающими приступами затрудненного дыхания в результате бронхиальной обструкции, обусловленной бронхоконстрикцией, гиперсекрецией слизи, отеком стенки бронхов. Бронхиальная обструкция (под влиянием лечения или спонтанно) обратима.
Нарушение бронхиальной проходимости проявляется одышкой, свистящими хрипами в легких, нередко слышимыми на расстоянии, кашлем, чувством стеснения в груди.
Факторы, влияющие на риск развития БА, можно разделить на факторы обуславливающие развитие заболевания (внутренние) и факторы, провоцирующие появление симптомов. Некоторые факторы относятся к обеим группам.
Эпидемиология. БА астма является весьма распространенным заболеванием и встречается с частотой 1,5-10%.
Факторы риска. Вероятность развития БА увеличивается, если в анамнезе имеется: атопический дерматит, аллергический риноконъюнктивит, отягощенный семейный анамнез по БА или другим аллергическим заболеваниям.
Классификация. Выделяют четыре степени тяжести БА: легкая интермиттирующая, легкая персистирующая, среднетяжелая персистирующая, тяжелая персистирующая.
По течению: период обострения, период ремиссии. Ремиссия может быть полной и неполной.
Тяжесть обострения: легкая, средней тяжести, тяжелая, крайней тяжести (астматический статус).
Этиология. Различают три основные группы причин, способствующих развитию БА: предрасполагающие (отягощенный аллергический анамнез, атопия, гиперреактивность бронхов); причинные (аллергены, вирусные инфекции, медикаменты); вызывающие обострение (триггеры): инфекции, неблагоприятные метеоусловия, табачный дым, стресс, физическая нагрузка.
Сенсибилизацию дыхательных путей вызывают различные аллергены: бытовые, эпидермальные, пищевые, грибковые, пыльцевые. В последние годы возрастает значение промышленных аллергенов.
Патогенез
Морфологической основой бронхиальной гиперреактивности при БА является аллергическое хроническое воспаление стенки дыхательных путей, характеризующееся наличием слизи в просвете бронхов, содержащей различные клеточные элементы, дисплазией и десквамацией эпителия, увеличением числа бокаловидных клеток, утолщением
36
базальной мембраны, инфильтрацией собственной мембраны слизистой оболочки лимфоидными клетками и гранулоцитами с преобладанием эозинофилов в инфильтрате и секрете.
Основным иммунологическим маркером сенсибилизации является повышение уровня общего IgЕ в сыворотке крови больного и наличие специфических IgЕ антител к аллергенам. Существенная часть IgЕ фиксирована на тучных клетках и базофилах.
Тучная клетка занимает одно из ведущих мест в аллергической реакции. В результате активации тучной клетки комплексами антиген + антитело происходит высвобождение медиаторов аллергии (гистамин и др.), а также образование новых медиаторов (простагландины, лейкотриены и др.). Под действием этих медиаторов развивается немедленный ответ – острый бронхоспазм, отек слизистой бронхов, гиперсекреция бронхиальной слизи. Эти же медиаторы ответственны и за продолжительную активацию эозинофилов, нейтрофилов, тромбоцитов и Т-лимфоцитов, за формирование воспаления в тканях и развитие отсроченной реакции.
Снижение уровня кальция в межклеточной среде ведет к подавлению синтеза лейкотриенов.
При БА эозинофилы часто обнаруживаются в большом количестве в жидкости бронхоальвеолярного лаважа. При обострении заболевания выявляются признаки активации эозинофилов и повышенной секреции ими медиаторов (основной протеин, эозинофильный катионный протеин, эозинофильный нейротоксин, цитокины, хемокины и др.).
При БА выявляется вторичная недостаточность антиоксидантных ферментов, что может привести к увеличению уровня свободных радикалов, которые способны индуцировать секрецию хемокинов, что приводит к усилению инфильтративного компонента воспаления.
Имеет место выраженная корреляционная зависимость концентрации оксида азота в воздухе, выдыхаемом больными БА, не принимающими кортикостероидные препараты, и интенсивностью воспаления в дыхательных путях. Этот показатель высоко чувствителен для контроля за эффективностью базисной терапии.
Особенностью детской БА является наличие диссоциативных нарушений внутри нейро-иммуно-эндокринного комплекса. Частота интра- и перинатальной патологии у детей с БА достигает почти 80%. Тканевая гипоксия, возникающая при патологическом течении беременности и родов, приводит к нарушению синтеза ферментов, макроэргических соединений, нарушению энергетического обмена. Патологическое течение родов может приводить к поражению стволовых
37

структур мозга, регулирующих функции респираторной системы, что способствует формированию бронхолегочной патологии.
Дисбаланс функционального состояния симпатического и парасимпатического отделов вегетативной нервной системы играет большую роль в патогенезе БА. Для многих больных характерно преобладание парасимпатического отдела вегетативной нервной системы и извращенные реакции на адреналин. На функциональное состояние эффекторных клеток бронхов и легких оказывают влияние аутоантитела против адренергических рецепторов.
Исследования. Общий анализ крови и мочи, кал на яйца глист, кожные пробы, показатели функции внешнего дыхания (пикфлоуметрия – после 6 лет, спирография - после 6 лет, пробы с бронхолитиками, проба с функциональной нагрузкой). Больные с БА должны быть об - следованы на наличие аллергического ринита. По показаниям: опреде-
ление общего и специфических IgЕ, иммунологическое обследование, рентгенография грудной клетки и придаточных пазух, ЭКГ, ЭХО-КГ, бронхоскопия (по особым показаниям), исследование мокроты.
Исследования амбулаторно, приказ МЗ РФ № 301: исследование неспровоцированных легочных объемов, консультация аллерголога.
По показаниям: ЭКГ, консультация пульмонолога, КТ органов грудной клетки, бронхоскопия, определение уровня кислорода в крови, кожные пробы.
Анамнез, клиника. В анамнезе у детей с БА выявляются различные аллергические заболевания. В периоде обострения выявляется малопродуктивный кашель, экспираторная одышка, вздутие грудной
Наследственно обусловленный повышенный уровень IgE
Сенсибилизация различными группами аллергенов
Образование комплекса IgE + аллерген
Фиксация комплекса на тучной клетке, базофилах бронхов
Дегрануляция тучных клеток и базофилов |
|
|
Са++ |
||
|
|
|
Выделение медиаторов воспаления: гистамин, цитокины, липидные медиаторы и др.
38
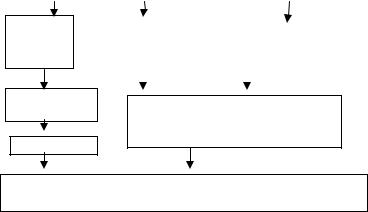
Активация Th2 клеток
Выделение IL4,
IL 13, IL 5
Синтез IgE
Активация |
|
|
|
|
|
Дисссоциативные нарушения |
|||
эозинофилов |
|
|||
|
нейро-иммуно-эндокринного |
|||
|
|
|
комплекса |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Выделение медиаторов эозинофилов: протеины, ферменты, цитокины, хемокины, липидные)
Формирование хронического аллергического воспаления дыхательных путей с гиперреактивностью бронхов
Рис.1.5. Схема патогенеза БА
клетки, коробочный оттенок перкуторного звука, рассеянные сухие хрипы, иногда вынужденное положение ребенка. Симптомы БА могут усиливаться ночью. Эквивалентами приступа БА может быть спастический ночной кашель.
У детей раннего возраста описывают следующие особенности БА: внутриутробная сенсибилизация плода; сенсибилизация пищевыми аллергенами у детей первого года жизни; сенсибилизация пыльцевыми аллергенами у детей 3-4 лет; наличие фоновой патологии (ПЭП, атопический дерматит, острые аллергические реакции, повторные ОРИ, рецидивирующий обструктивный бронхит).
Диагноз
39
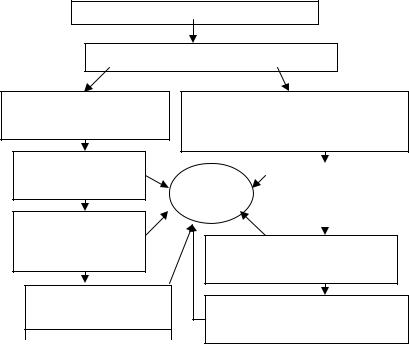
Анамнез, отягощенный по аллергии (+)*
Аускультация, ПСВ во время визита
Во время визита симпто-
мы отсутствуют
Тест с физической
нагрузкой
Пикфлоуметрия в
домашних
условиях
Провокационный тест с метахолином или гистамином
Наличие симптомов во время визита (сви-
стящие хрипы при аускультации, падение ПСВ, симптомы длительной обструкции)
Диаг- |
Тест с ингаляцион- |
||
ным бронходилата- |
|||
ноз |
|||
тором |
|||
|
|
|
|
|
|
|
|
Исключение контакта с при-
чинно-значимым аллергеном
Назначение противовоспали-
тельных средств
Рис. 1.6. Алгоритм диагностики бронхиальной астмы (Enidence Based Medicine – согласно медицине, основанной на доказательствах)
* - аллергодиагностика обязательна для всех пациентов с подозрением на бронхиальную астму
Наличие типичного приступа - достаточное основание для диагностики БА. При отсутствии приступов значение играет выявление в анамнезе повторных эпизодов затрудненного свистящего дыхания, признаков обструкции бронхов, ночного кашля, положительного аллергологического анамнеза.
Диагностика БА у детей младшего возраста основывается в первую очередь на клинических признаках, оценке симптомов и данных физикального обследования. О высокой вероятности диагноза БА говорят: частые эпизоды свистящих хрипов (больше 1 в месяц), кашель или хрипы, вызванные физической нагрузкой, кашель по ночам в отсутст-
40

вие ОРИ, отсутствие сезонных изменений хрипов, а так же сохранение симптомов в возрасте старше 3 лет.
Для подтверждения диагноза БА у детей в возрасте до 5 лет используют пробное лечение бронхолитиками короткого действия и ингаляционными стероидами. Улучшение на фоне этой терапии и ухудшение после ее прекращения говорит в пользу диагноза БА.
Степени тяжести БА диагностируют на основании следующих признаков.
Ступень 1: интермиттирующая бронхиальная астма: короткие обострения; симптомы реже 1 раза в неделю; ночные симптомы не чаще 2 раз в месяц; ОФВ1 или ПСВ>80% от должных значений; вариабельность показателей ПСВ или ОФВ1 < 20%.
Ступень 2: легкая персистирующая бронхиальная астма: сим-
птомы чаще 1 раза в неделю, но реже 1 раза в день ; обострения могут влиять на физическую активность и сон; ночные симптомы чаще 2 раз в месяц; ОФВ1 или ПСВ > 80% от должных значений; вариабельность показателей ПСВ или ОФВ1 = 20-30%.
Ступень 3: персистирующая бронхиальная астма средней сте-
пени тяжести: ежедневные симптомы; обострения могут влиять на физическую активность и сон; ночные симптомы чаще 1 раза в неделю; ежедневный прием ингаляционных β2-агонистов короткого действия; ОФВ1 или ПСВ от 60 до 80% от должных значений; вариабельность показателей ПСВ или ОФВ1>30%.
Ступень 4: тяжелая персистирующая бронхиальная астма:
ежедневные симптомы; частые обострения; частые ночные симптомы; ограничение физической активности; ОФВ1 или ПСВ<60% от должных значений; вариабельность показателей ПСВ или ОФВ1>30%.
Тяжесть обострения БА диагностируется на основании: учащения дыхания, участия вспомогательной мускулатуры, интенсивности свистящего дыхания, выраженности вздутия грудной клетки, ЧСС, вынужденности положения, изменения поведения, степени ограничения физической активности, объема терапии (препараты и способы их введения).
Табл. 1.13. Критерии тяжести приступа бронхиальной астмы
Признаки |
Легкий |
Средне- |
Тяжелый |
Астматиче- |
|
|
тяжелый |
|
ское состоя- |
|
|
|
|
ние |
Физиче- |
Сохранена |
Ограниче- |
Резко сни- |
Резко снижена |
ская ак- |
|
на |
жена, по- |
или отсутству- |
41
тивность |
|
|
ложение |
ет |
|
|
|
|
вынужден- |
|
|
|
|
|
ное |
|
|
|
|
Ограниче- |
|
|
|
Разговор- |
|
на, произ- |
Затруднена |
Отсутствует |
|
Сохранена |
носит от- |
||||
ная речь |
|||||
|
дельные |
|
|
||
|
|
|
|
||
|
|
фразы |
|
|
|
|
Не изме- |
|
Возбужде- |
Спутанность |
|
Сфера соз- |
нена, ино- |
Возбужде- |
ние, испуг |
сознания, ко- |
|
«дыха- |
|||||
нания |
гда возбу- |
ние |
тельная |
матозное со- |
|
|
ждение |
|
стояние |
||
|
|
паника» |
|||
|
|
|
|
||
|
Нормаль- |
Выражен- |
Резко вы- |
|
|
|
ная экспи- |
раженная |
|
||
|
ная или |
|
|||
Частота |
раторная |
экспира- |
Тахипноэ или |
||
дыхание |
|||||
одышка. |
торная |
||||
дыхания |
учащенное |
брадипноэ |
|||
|
до 30% |
Более 30- |
одышка |
|
|
|
50% от |
более 50% |
|
||
|
нормы |
|
|||
|
нормы |
от нормы |
|
||
|
|
|
|||
Участие |
|
|
|
Парадоксаль- |
|
вспомога- |
Нерезко |
|
Резко вы- |
||
|
ное торакоаб- |
||||
тельной |
выражено |
Выражено |
|||
ражено |
доминальное |
||||
мускула- |
|
|
|
дыхание |
|
туры |
|
|
|
||
|
|
|
|
||
Частота |
Увеличена |
Увеличена |
Резко уве- |
Брадикардия |
|
пульса |
личена |
||||
|
|
Выражен- |
|
|
|
|
|
ное сви- |
Резко вы- |
|
|
Дыхание |
Свистящие |
стящее на |
раженное |
«Немое лег- |
|
хрипы, |
вдохе и |
свистящее |
|||
при ау- |
обычно в |
выдохе |
или ослаб- |
кое», отсутст- |
|
скультации |
конце вы- |
или моза- |
ление про- |
вие дыхатель- |
|
ных шумов |
|||||
|
доха |
ичное про- |
ведения |
|
|
|
|
ведение |
дыхания |
|
|
|
|
дыхания |
|
|
|
ПСВ (%) |
|
|
|
|
|
от нормы |
70-90% |
50-70% |
Менее 50% |
|
|
или наи- |
|
||||
|
|
|
|
||
лучших |
|
|
|
|
42
значений |
|
|
|
|
|
больного |
|
|
|
|
|
Pa CO2 |
<35 мм рт. |
<35-40 мм |
> 40 мм рт. |
|
|
ст. |
рт. ст. |
ст. |
|
||
|
|
||||
SaO2 |
> 95% |
90-95% |
< 90 % |
|
|
|
Бронхос- |
Бронхос- |
Использо- |
|
|
Объем |
пазмоли- |
пазмоли- |
|
||
вались вы- |
|
||||
бронхос- |
тическая |
тическая |
Использова- |
||
сокие дозы |
|||||
пазмоли- |
терапия не |
терапия не |
препара- |
лись высокие |
|
тической |
проводи- |
проводи- |
дозы препара- |
||
тов. Воз- |
|||||
терапии в |
лась или |
лась или |
тов. Возможна |
||
можна пе- |
|||||
последние |
использо- |
использо- |
редозиров- |
передозировка |
|
сутки, осо- |
вались |
вались |
адреномимети- |
||
ка адрено- |
|||||
бенно в |
низкие/ |
низкие / |
миметиков |
ков и/или тео- |
|
последние |
средние |
средние |
филлина |
||
и/или тео- |
|||||
4-6 часов |
дозы пре- |
дозы пре- |
филлина |
|
|
|
паратов |
паратов |
|
||
|
|
|
Лабораторные исследования
Дополнительные исследования необходимы для определения степени тяжести, характера сенсибилизации, механизмов развития БА.
Спирометрия, пикфлоуметрия позволяют оценить наличие и степень выраженности нарушений функции внешнего дыхания.
Рентгенологическое исследование выявляет эмфизему, а в некот о-
рых случаях ателектазы, пневмонию, признаки пневмоторакса. В мокроте можно выявить эозинофилы, спирали Куршмана.
Кожные тесты, исследование специфических IgE подтверждают аллергическую природу БА и характер сенсибилизации.
Дифференциальный диагноз БА необходимо проводить с синдромом хронической аспирации пищи, инородным телом, муковисцидозом, облитерирующим бронхиолитом, аномалиями бронхолегочной системы, сердечной недостаточностью, бронхолегочной дисплазией, обструктивными бронхитами (см. «Бронхиты», табл. 1.18).
При наличии следующих симптомов следует заподозрить отличное от БА заболевание (Педиатрия, клинические рекомендации, 2009).
Данные анамнеза:
-появление симптомов заболевания в возрасте до 2 лет;
-респираторный дистресс-синдром и/или применение ИВЛ;
-неврологическая дисфункция в неонатальном периоде;
-отсутствие эффекта от применения бронхолитиков;
-свистящие хрипы, связанные с кормлением или рвотой;
43
-затруднения глотания и/или рецидивирующая рвота;
-диарея;
-плохая прибавка массы тела;
-сохранение потребности в оксигенотерапии более 1 нед после обострения заболевания.
Физикальные данные:
-деформация пальцев рук в виде «барабанных палочек»;
-шумы в сердце»
-стридор;
-очаговые изменения в легких;
-крепитация при аускультации;
-цианоз.
Результаты лабораторных и инструментальных исследований:
-очаговые или инфильтративные изменения на рентгенограмме органов грудной клетки;
-анемия;
-необратимая обструкция дыхательных путей;
-гипоксемия.
Лечение, задачи лечения. Основная цель терапии БА у детей - достижение стойкой (устойчивой) ремиссии, предупреждение прогрессирования заболевания, исключение побочных эффектов противоастматических средств; предотвращение связанной с БА смертности.
Схема лечения. Основные направления в терапии БА: элиминаци-
онные мероприятия; превентивная (контролирующая) терапия; фармакотерапия острого периода болезни; аллерген-специфическая терапия; реабилитация; обучение пациентов.
Вспомогательные методы: физиолечение, спелеотерапия, лазеротерапия, антигистаминные препараты, специфическая иммунотерапия причинно-значимыми аллергенами, методы регулируемого дыхания, иглорефлексотерапия, психотерапия, борьба с полипрагмазией.
Тактика лечения и профилактики БА определяется характером воспалительного процесса. План лечения обострения должен основываться на данных диагностики БА и динамики клинических проявлений. Необходимо подобрать схему лечения, дозы препаратов, технологии их применения.
Показания для госпитализации: невозможность или неэффектив-
ность (в течение 1-3 ч) лечения в домашних условиях; дети из группы высокого риска по развитию осложнений; необходимость установления природы обострений и подбора средств терапии при впервые возникших симптомах БА.
44
Показания к переводу в ОИТАР: не купирующийся приступ БА более 6 часов, резистентность к симпатомиметикам, другие признаки астматического состояния.
Программа ведения ребенка, больного БА включает: разработку индивидуальных планов медикаментозной терапии; разработку индивидуальных планов купирования обострений БА; мониторинг состояния ребенка с периодическим исследованием показателей функции внешнего дыхания и/или данных пикфлоуметрии и ведением дневника симптомов; просвещение и обучение больных детей и членов семьи; использование немедикаментозных методов терапии.
При лечении БА используются: а) препараты, купирующие при-
ступ заболевания, б) средства, предупреждающие развитие симптомов БА.
Препараты, купирующие приступ заболевания: короткодейст-
вующие β2-агонисты (сальбутамол, беротек, тербуталин, фенотерол и др.), антихолинергические препараты (ипратропиум бромид), корот-
кодействующие теофиллины (аминофиллин). Более 4 раз в сутки эти препараты применять не рекомендуют.
Средства, предупреждающие развитие симптомов БА: глюко-
кортикоиды (ингаляционные - бекламетазон, будесонид, флутиказон, флютиказон, триамцинолон); таблетки или сиропы - гидрокортизон, метилпреднизолон, преднизон), кромоны (интал, тайлед), β2-агонисты длительного действия (формотерол, сальмотерол, тербуталин), тео-
филлины длительного высвобождения (теопек, ретард, теотард, ретафил), антилейкотриеновые препараты (монтелюкаст, зафирлукаст).
Первоочередным мероприятием при лечении БА является купиро-
вание приступа (табл. 1.14).
Табл. 1.14. Лечение бронхиальной астмы у детей на догоспи-
тальном этапе
Диагноз |
Медикаментозная терапия |
Результат |
|
|
|
Бронхиаль- |
Вентолин через небулайзер в течение 5- |
Купирова- |
ная астма |
10 минут |
ние |
легкий при- |
или |
приступа |
ступ |
Беродуал через небулайзер в течение 5- |
|
|
10 минут |
|
|
Оценить терапию через 20 минут |
|
|
При неудовлетворительном эффекте |
|
|
повторить аналогичную ингаляцию |
|
45
|
бронхолитика |
|
Бронхиаль- |
Вентолин через небулайзер в течение 5- |
Купирова- |
ная астма |
10 минут |
ние присту- |
средне- |
или |
па |
тяжелое обо- |
Беродуал через небулайзер в течение 5- |
|
стрение |
10 минут |
Госпитали- |
|
и Преднизолон перорально |
зация в ста- |
|
или |
ционар |
|
Пульмикорт через небулайзер в течение |
|
|
5-10 минут |
|
|
Оценить терапию через 20 минут |
|
|
При неудовлетворительном эффекте |
|
|
повторить аналогичную ингаляцию |
|
|
бронхолитика |
|
Бронхиаль- |
Вентолин через небулайзер в течение 5- |
|
ная астма |
10 минут |
|
тяжелое обо- |
или |
|
стрение |
Беродуал через небулайзер в течение 5- |
Госпитали- |
|
10 минут |
зация детей |
|
и Преднизолон внутривенно или перо- |
в стационар |
|
рально |
|
|
или Пульмикорт через небулайзер в те- |
|
|
чение 5-10 минут |
|
|
|
|
Бронхиаль- |
Вентолин через небулайзер в течение 5- |
|
ная астма |
10 минут |
|
|
или |
|
Астматиче- |
Беродуал через небулайзер в течение 5- |
Госпитали- |
ский статус |
10 минут |
зация в |
|
и Преднизолон перорально |
|
|
ОРИТ |
|
|
или |
|
|
|
|
|
Пульмикорт через небулайзер в течение |
|
|
5-10 минут |
|
|
Интубация трахеи, ИВЛ |
|
Препараты для снятия приступа БА лучше вводить ингаляционно, через небулайзер. К преимуществам небулайзерной терапии относят: легкость техники ингаляции, высокую эффективность лечения, быстрое улучшение состояния больного, возможность точного дозирования препарата и изменения дозы при необходимости.
46
При легком приступе БА используют препараты β2-агонистов, ипратропиума бромида (или их комбинации) вводимые ингаляционно.
После ликвидации острого легкого приступа БА необходимо продолжить применение указанных препаратов еще 1-2 дня. Если ребенок получает базисную терапию (недокромил натрия, кромогликат натрия, ингаляционные кортикостероиды), следует продолжить прием препаратов. Необходимо контролировать состояние ребенка, исследовать ПСВ с помощью пикфлоуметра.
При средне-тяжелом приступе БА, при отсутствии эффекта от применения β2-агонистов и/или ипратропиума бромида, возможно введение эуфиллина в/в струйно медленно в течение 10-15 минут на изотоническом растворе хлористого натрия.
После ликвидации приступа БА продолжают бронхоспазмолитическую терапию каждые 4 часа бодрствования еще 1-2 дня. Возможен перевод ребенка на пролонгированные бронхолитики (β2-агонисты, метилксантины) до нормализации клинических и функциональных данных. Если ребенок получает базисную терапию (недокромил натрия, кромогликат натрия, ингаляционные кортикостероиды), продолжить их прием, увеличить дозу препарата в 1,5-2 раза на 7-10 дней, или использовать комбинированные препараты (противовоспалительный препарат + бронхоспазмолитик).
При тяжелом приступе БА через небулайзер вводят β2-агонисты периодически с интервалом 20 минут в течение часа, затем каждые 1-4 часа, или проводят длительную небулизацию. Бронхоспазмолитический эффект может быть усилен добавлением ипратропиума бромида или использованием комбинированного препарата. Если больной не может создать пик потока на выдохе п/к вводится адреналин 0,01 мл/кг/доза или 1:1000 (1 мг/мл) (максимальная доза до 0,3 мл). Одновременно с бронхоспазмолитиками вводятся системные глюкокортикостероиды парентерально или внутрь в дозе 5 мг/кг. Повторное введение глюкокортикостероидов при недостаточном эффекте через 6 часов. Оксигенотерапия через маску или носовой катетер. При недостаточном эффекте от указанной терапии вводят эуфиллин внутривенно (при необходимости капельно).
После ликвидации тяжелого приступа БА продолжают бронхоспазмолитическую терапию каждые 4 часа бодрствования. β2-агонисты короткого действия применяют еще 3-5 дней в форме дозирующего аэрозоля или через небулайзер. Следует назначить системные кортикостероиды парентерально или per os на 3-5 дней в дозе 1-2 мг/кг/сут до купирования бронхиальной обструкции. Перевести пациента на пролонгированные бронхолитики (β2-агонисты, метилксантины). Если
47
ребенок получает базисную терапию (ингаляционные кортикостероиды) - продолжить прием, увеличить дозу препарата в 1,5-2 раза на 7-10 дней. Препараты лучше вводить с помощью небулайзера.
Необходимо несколько дней наблюдать за состоянием больного с мониторированием ПСВ с помощью пикфлоуметра, и пульсоксиметрией.
Эффективность проводимого лечения оценивается по следующим вариантам:
«Хороший» ответ - состояние стабильное, уменьшилась одышка и количество сухих хрипов в легких; ПСВ увеличилось на 12-15% от исходного.
«Неполный» ответ - состояние нестабильное, симптомы в прежней степени, в легких сохраняются участки с плохой проводимостью дыхания, нет прироста ПСВ.
«Плохой» ответ - симптомы прежней степени или нарастают, ПСВ ухудшается (см. также прил. 1).
Основные принципы интенсивной терапии БА:
−оксигенотерапия с поддержанием SaO2 более 95%;
−продолжение терапии β2-агонистами;
−использование системных глюкокортикостероидов парентерально до 10 мг/кг/сут или per os;
−применение метилксантинов (эуфиллин) в/в 4,5-5 мг/кг в теч е- ние 20-30 минут, в последующем - непрерывная инфузия в дозе 0,6-0,8 мг/кг/час или дробно в соответствующих дозах через каждые 4-5 часов под контролем концентрации теофиллина в крови.
Инфузионная терапия при БА включает изотонический раствор
хлорида натрия и 5% раствор глюкозы в соотношении 1:1. Объем жидкости для введения рассчитывают в соответствии с физиологическими потерями (в среднем 50 мл/кг/сут). Количество внутривенно вводимой жидкости у детей раннего возраста составляет 10-20 мл/кг массы, общий объем -150-300 мл, скорость введения 30-45 мл/час (10-15 капель в минуту), длительность инфузии в зависимости от объема.
При проведении интенсивной терапии необходимо осуществлять мониторинг жизненных функций: ЧСС, ЧДД, ЭКГ, пульсоксиметрия, РаО2, РаСО2.
Астматический статус – самое тяжелое проявление БА. Астматический статус необходимо диагностировать при некупируемом приступе БА на протяжении 6 часов и более; при развитии резистентности к симпатомиметическим средствам; нарушении дренажной функции бронхов; возникновении гипоксемии (РО2 < 60 мм рт. ст.), гиперкапнии (РСО2 >60 мм рт. ст.).
48
Причинами развития астматического статуса могут быть: ОРИ, неадекватная терапия приступа БА, передозировка симпатомиметиков, надпочечниковая недостаточность.
В клинической картине астматического статуса выделяют 3 стадии.
I стадия – относительной компенсации - характеризуется клини-
кой тяжелого приступа БА с нарушениями бронхиальной проходимости и резистентностью к симпатомиметикам. Характерно нарастание эмфиземы, тахикардии. Артериальное давление повышается. Больной становится беспокойным, появляется акроцианоз. При лабораторном исследовании выявляют: гипоксемию, гиперкапнию, респираторный или метаболический ацидоз.
II стадия – декомпенсации - характеризуется нарастанием дыхательной недостаточности, нарастанием спазма и отека слизистой оболочки бронхов. В легких при аускультации перестают выслушиваться дыхательные шумы («молчание в легких»). При сохраняющейся тахикардии начинает снижаться артериальное давление. При лабораторном исследовании выявляют нарастающие проявления гипоксемии, гиперкапнии, респираторного или метаболического ацидоза.
III стадия – гипоксическая кома – проявляется тяжелой дыхательной недостаточностью, синдромом «молчания» в легких, генерализованным цианозом, потерей сознания, падением артериального давления, сердечной недостаточностью.
Лечение астматического статуса проводится в зависимости от стадии заболевания.
При I стадии астматического статуса вводят в/в 2,4% раствор эуфиллина из расчета 4-6 мг/кг на 250-500 мл 5% раствора глюкозы. Проводят ингаляции 2% раствора соды или 3% раствора калия йодида. Внутривенно вводят изотонический раствор натрия хлорида в дозе 4060 мл/кг. Больные должны получать увлажненный кислород, витаминные препараты (кальция пантотенат, витамины В5, В6, С). Для коррекции ацидоза применяют соду. При отсутствии эффекта от перечисленной терапии назначают преднизолон по 1-2 мг/кг/сутки. Для профилактики бактериальных осложнений показаны антибиотики.
При II стадии астматического статуса увеличивают дозу пред-
низолона до 3-5 мг/кг. Для коррекции гипокалиемии внутривенно вводят раствор калия хлорида. При признаках недостаточности кровообращения показаны инотропные дозы допамина, сердечные гликозиды, мочегонные. При отсутствии эффекта от перечисленного лечения решается вопрос о проведении лечебной бронхоскопии.
При III стадии астматического статуса проводят адекватную вентиляцию легких и посиндромную терапию, направленную на под-
49
держание деятельности сердца, коррекции электролитных нарушений. Дозы преднизолона увеличивают до 4-8 мг/кг. При потере сознания начинают дегидратационную терапию (маннитол, мочегонные, дексаметазон, сернокислая магнезия).
Базисная терапия БА направлена на купирование проявлений аллергического воспаления и предупреждение приступов БА. В настоящее время принят ступенчатый подход к проведению лечения. Сущностью ступенчатого лечения является увеличение или уменьшение объема терапии в зависимости от контроля симптомов БА.
Для лучшего контроля за БА более предпочтительна комбинированная терапия (ингаляционный глюкокортикоид + β2-агонист длительного действия). В качестве комбинированных препаратов наиболее часто используют Симбикорт (будесонид/формотерол) и Серетид (флутиказон/сальмотерол).
Препараты и методы, которые не следует использовать при при-
ступе БА: антигистаминные препараты, седативные препараты, фитопрепараты, горчичники, банки, сульфат магния, препараты кальция, муколитики, антибиотики, пролонгированные бронхолитики.
Табл.1.15. Объем базисной терапии у детей младше 5 лет в зави-
симости от степени тяжести БА
Степень тя- |
Препараты базисной терапии |
||
жести |
Препараты выбора |
Альтернативные препараты |
|
Ступень 1, |
Нет |
|
|
интермитти- |
|
||
необходимости |
|
||
рующая БА |
|
||
|
|
||
Ступень 2, |
|
Теофиллин с медленным |
|
|
высвобождением |
||
легкая |
|
||
Низкие дозы ИГК |
Кромоны |
||
персисти- |
|||
|
Антилейкотриеновый пре- |
||
рующая БА |
|
||
|
парат |
||
|
|
||
|
|
Средние дозы ИГК+ теофиллин |
|
Ступень 3, |
|
с медленным высвобождением |
|
среднетяже- |
|
Средние дозы ИГК + ингаля- |
|
|
ционный, длительно дейст- |
||
лая перси- |
Средние дозы ИГК |
||
вующий β2-адреномиметик |
|||
стирующая |
|
||
|
Высокие дозы ИГК |
||
БА |
|
||
|
Средние дозы ИГК + антилей- |
||
|
|
котриеновый препарат |
|
Ступень 4, |
Высокие дозы ИГК+ один |
|
|
или более следующих пре- |
|
||
50

тяжелая |
паратов при необходимо- |
|
персисти- |
сти: |
|
рующая БА |
теофиллин с медленным |
|
высвобождением, ингаля- |
|
|
|
ционный, длительно дейст- |
|
|
вующий β2-адреномиме- |
|
|
тик, антилейкотриеновый |
|
|
препарат, системный ГК |
|
Табл. 1.16. Объем базисной терапии у детей 5 лет и старше в за-
висимости от степени тяжести БА
Степень |
Препараты базисной терапии |
||
|
Альтернативные препара- |
||
тяжести |
Препараты выбора |
||
ты |
|||
|
|
||
Ступень 1, |
|
|
|
интермитти- |
Нет необходимости |
|
|
рующая БА |
|
|
|
Ступень 2, |
|
Теофиллин с медленным |
|
|
высвобождением |
||
легкая |
|
||
Низкие дозы ИГК |
Кромоны |
||
персисти- |
|||
|
Антилейкотриеновый |
||
рующая БА |
|
||
|
препарат |
||
|
|
||
|
Низкие/средние дозы |
Средние дозы ИГК+ пе- |
|
Ступень 3, |
роральный, длительно |
||
ИГК + ингаляционный, |
|||
действующий β2- |
|||
среднетяже- |
длительно действующий |
||
адреномиметик |
|||
лая перси- |
β2-адреномиметик |
||
Высокие дозы ИГК |
|||
стирующая |
средние дозы ИГК + |
||
Средние дозы ИГК + ан- |
|||
БА |
теофиллин с медленным |
||
тилейкотриеновый препа- |
|||
|
высвобождением |
||
|
рат |
||
|
|
||
|
Высокие дозы ИГК + инга- |
|
|
|
ляционный, длительно |
|
|
|
действующий β2- |
|
|
Ступень 4, |
адреномиметик + один или |
|
|
более следующих препара- |
|
||
тяжелая |
тов при необходимости: |
|
|
персисти- |
|
||
теофиллин с медленным |
|
||
рующая БА |
|
||
высвобождением, |
|
||
|
антилейкотриеновый пре- |
|
|
|
парат |
|
|
|
пероральный длительно |
|
|
51

действующий β2-
адреномиметик, системный ГК
Немедикаментозные методы лечения БА включают: диетотера-
пию, респираторную терапию, массаж и вибромассаж; лечебную физкультуру, спелеотерапию, горноклиматическое лечение, физиотерапию, фитотерапию, психотерапию. Эффективность немедикаментозных методов лечения БА изучена недостаточно. Перечисленные методы характеризует выраженная постепенность наступления положительного эффекта, слабая эффективность (по сравнению с медикаментозными методами лечения). К положительным моментам следует отнести возможность уменьшения зависимости от длительного применения медикаментов.
Осложнения БА: ателектазы, медиастинальная и подкожная эмфизема, спонтанный пневмоторакс, эмфизема легких, легочное сердце, асфиксия.
Профилактика. Выделяют три уровня профилактики БА: первичный, вторичный, третичный.
Первичная профилактика своей задачей ставит предупреждение развития аллергической сенсибилизации. Основными мероприятиями первичной профилактики БА являются: предупреждение патологического течения беременности, исключение (ограничение) пассивного курения, сохранение естественного вскармливания до 4-6 месячного возраста.
Вторичная профилактика направлена на предупреждение развития у детей БА с генетически детерминированным высоким риском развития атопии, а также у детей с атопическим дерматитом и другими аллергическими заболеваниями. Основное мероприятие: превентивная терапия цитеризином.
Третичная профилактика предусматривает предупреждение прогрессирования БА и неблагоприятного ее исхода при помощи адекватных мер лечебного и реабилитационного характера. Основные мероприятия: элиминационный режим, гипоаллергенная диета, профилактика ОРИ, санация очагов инфекции, рациональное использование медикаментов при лечении интеркурентных заболеваний. Важное значение имеют: лечение гастроэзофагеального рефлюкса, регулярная базисная терапия, лечение ожирения.
52

Вопросы к экзамену. Бронхиальная астма. Факторы риска. Классифи-
кация. Патогенез. Клинические проявления в приступном периоде. Осложнения в приступном периоде. Патогенез и клиника астматического статуса. Осложнения при длительном течении астмы, протекающей с частыми рецидивами. Диагностика. Функция внешнего дыхания. Принципы лечения. Лечение в приступном периоде. Базисная терапия. Аллергенспецифическая иммунотерапия. Неотложная терапия астматического статуса. Профилактика.
Глава III. Заболевания органов дыхания
БРОНХИТЫ
Бронхит (Б) – острое воспаление слизистой оболочки бронхов, вызываемое различными инфекционными, реже физическими или химическими факторами.
Эпидемиология. Б являются одними из самых частых проявлений ОРИ. Частота острого Б составляет 200-400 на 1000 детского населения. Обструктивные формы Б встречаются у 20-30% от всех детей, болеющих Б.
Этиология. Б чаще всего вызываются вирусами - рино-, РС, короновирусами, парагриппа и метапневмовирусами. У старших детей возможна микоплазменная этиология заболевания, а у детей первых месяцев жизни – хламидийная. Часто выделение бактерий в мокроте не дает оснований говорить о бактериальной этиологии Б, т.к. речь идет о неинвазивном размножении флоры без характерных для микробного воспаления признаков. В этих случаях применение антибиотиков не влияет на течение Б.
Бактериальные Б развиваются у детей с нарушениями очищения бронхов (инородное тело, стеноз гортани, интубация, трахеостома, привычная аспирация пищи, муковисцидоз). Бактериальная этиология Б встречается у 10-15% детей и представлена пневмококками, стафилококками, гемофильной палочкой.
Роль загрязнения воздуха (промышленные газы, пассивное курение, печи, дровяные и газовые плиты) связана с развитием гиперреактивности бронхов, особенно у детей первых 6 лет жизни; заболеваемость Б - наиболее чуткий индикатор загрязнения воздуха.
Патогенез. Развитию Б предшествует воздействие на организм предрасполагающих факторов (охлаждение или перегревание, загряз-
53
ненный воздух, пассивное курение, снижение иммунитета, очаги хронической инфекции и др.). Инфекция (чаще вирусы) попадают в организм воздушно-капельным путем. Размножение вирусов происходит в клетках дыхательной системы. При различной этиологии Б в патогенезе имеются особенности, связанные с этиологией заболевания. В развитии воспалительного процесса в стенке бронхов принимают участие интерлейкины, простагландины, клеточные медиаторы, нервная система, Основными проявлениями воспаления бронхов, являются отек, гиперемия слизистой, повышенная выработка слизи, нарушение мукоцилиарного клиренса.
Классификация: острый (простой) Б, обструктивный Б, бронхиолит, рецидивирующий (обструктивный, необструктивный) Б.
Исследования. По показаниям: общий анализ крови и мочи, серологическое исследование, посев с миндалин на микрофлору, посев на дифтерию, рентгенологическое исследование грудной клетки, иммунофлюоресцентное исследование слизи носоглотки на антигены вирусов, ЭКГ, ЭХОЭГ.
Исследования амбулаторно, приказ МЗ РФ № 259: анализ крови (тройка). По показаниям: рентгенография легких, общий анализ крови.
Анамнез, клиника
Острый Б. В анамнезе контакты с больными ОРИ. Клинические проявления простого Б складываются из: 1) клиники респираторного синдрома (гиперемия зева, кашель, насморк, конъюнктивит и др.). Особенности респираторного синдрома зависят от этиологии заболевания (вирусы гриппа, аденовирусы, микоплазма и т.д.).
2)Бронхолегочной синдром характеризуется: чаще нормальным перкуторным звуком над легкими, жестким дыханием, рассеянными разнокалиберными (средне- и крупнопузырчатые) влажными и сухими хрипами. Количество хрипов изменяется при кашле. Отсутствует локальность изменения аускультативных и перкуторных данных. Кашель
–обязательный признак Б. Вначале заболевания он сухой, затем становится влажным. Мокрота серозно-слизистая. Одышки практически не бывает.
3)Интоксикационный синдром: капризность, снижение эмоцио-
нального тонуса, легкая бледность кожи, ухудшение аппетита.
54

Предрасполагающие факторы: охлаж-
дение или перегревание, загрязненный воздух, пассивное курение, снижение иммунитета, очаги хронической инфекции у ребенка или у членов семьи, неблагоприятные бытовые условия, патология перинатального периода, фоновая патология и т.д.
Этиологические факторы:
вирусы, бактерии, микоплазмы, хламидии
|
|
|
|
|
|
Грипп |
Аденовирусная ин- |
РС-инфекция |
|
|
|
фекция |
|
|
|
Воздушно-капельный путь передачи инфекции |
|
||
|
Проникновение вируса через слизистую дыхательных путей |
|
||
|
Репродукция вируса в клетках дыхательной системы |
|
||
|
Выработка провоспа- |
Попадание вируса в |
Попадание вируса в кровь, |
|
|
лительных медиато- |
кровь, развитие вирусе- |
развитие вирусемии. |
|
|
ров. |
мии. Поражение эндо- |
Распространение вируса |
|
|
Вирусемия, токсиче- |
телия сосудов (экссуда- |
бронхогенно или гемато- |
|
|
ские и токсикоаллер- |
тивный тип воспаления, |
генно на нижние дыха- |
|
|
гические реакции. |
с выпадением фибрина). |
тельные пути. |
|
|
Развитие воспали- |
Некроз эпителия→ ак- |
Развитие многоклеточного |
|
|
тельных процессов в |
тивация тромбокиназы |
сосочкообразного разрас- |
|
|
органах дыхательной |
→ образование фибрина |
тания эпителия (формиро- |
|
|
системы. |
→ появление пленчатых |
вание БОС). |
|
|
|
налетов. |
|
|
|
|
|
|
|
Повреждение эпителия дыхательных путей, угнетение барьерных
свойств стенки бронхов, нарушение нервной регуляции и трофики бронхиального дерева
Нервная система:
активация: а) системы
NANC**
б) холинергической системы в) симпатической системы
Тучная клетка, базофил, мак-
рофаг → арахидоновая ****
кислота → выработка гистамина, ФАТ*, простагландинов, цитокинов, лейкотриенов
Увеличение проницаемости сосудов, сокращение бронхов, секре-
ция слизи, хемотаксис
55

Развитие воспалительных изменений в стенке бронхов
Рис. 1.7. Схема патогенеза бронхитов
* ФАТ - Фактор активации тромбоцитов (усиливает выработку слизи, вызывает спазм мускулатуры бронхов);
**- NANC – неадренергически-нехолинэнергическая система;
***- мукоцилиарный клиренс – способность бронхиального дерева
ксамоочищению (реснитчатый эскалатор);
****- арахидоновая кислота синтезируется из мембранных фосфолипидов. Ее метаболитами являются простагландины, лейкотриены.
Диагноз простого Б чаще всего клинический. Дополнительные методы исследования необходимы для проведения дифференциального диагноза в первую очередь с пневмонией.
Лабораторные исследования Рентгенологические данные: усиление легочного рисунка, отсутст-
вие теней очаговой инфильтрации, малоструктурность корней легкого. Гемограмма. Изменения в крови отражают этиологию заболевания.
При вирусном процессе вначале Б отмечается незначительный лейкоцитоз, затем – лейкопения, лимфоцитоз, моноцитоз. СОЭ обычно ускорено незначительно (15-19 мм/ч).
Исходы при остром Б – выздоровление через 10-14 дней. Осложнения развиваются редко.
Обструктивный Б – острый бронхит, протекающий с синдромом диффузной бронхиальной обструкции. Обструктивный бронхит встречается преимущественно у детей первых 4-х лет жизни.
Респираторный синдром (смотри «острый Б»).
Бронхолегочной и бронхообструктивный синдромы: жесткое дыха-
ние без локальных изменений, удлинение выдоха, свистящее дыхание (хрипы, слышные на расстоянии), разнообразные сухие хрипы преимущественно на выдохе, разнокалиберные рассеянные влажные хрипы. Изменение аускультативной картины после кашля.
При обструктивном Б обязательным является наличие бронхообструктивного синдрома, степень выраженности которого различна (табл. 1.17). Степень дыхательной недостаточности чаще всего выражена в меньшей степени, чем степень бронхообструктивного синдрома.
Табл.1. 17. Шкала оценки тяжести обструктивногосиндрома
56
Ба |
Частота ды- |
Свистя- |
Степень выражен- |
|
Участие |
|
лл |
хания |
|
щие |
ности эмфиземы |
|
вспомога- |
ы |
|
|
хрипы |
|
|
тельной |
|
|
|
|
мускулату- |
||
|
|
|
|
|
|
ры |
0 |
Соответствует |
Нет |
нет |
|
Нет |
|
|
возрастной нор- |
|
|
|
|
|
|
ме |
|
|
|
|
|
1 |
1-2 мес. < 50 |
Терми- |
Грудная клетка визу- |
|
+ |
|
|
2-12 мес. < 40 |
нальные на |
ально не вздута, ло- |
|
|
|
|
1-5 лет < 30 |
выдохе |
кальный коробочный |
|
|
|
|
6-8 лет < 25 |
(асульта- |
перкуторный звук |
|
|
|
|
тивно) |
|
|
|||
|
|
|
|
|
|
|
2 |
1-2 мес. |
50-60 |
На выдохе |
Грудная клетка визу- |
|
++ |
|
2-12 мес. |
40-50 |
и |
ально умеренно |
|
|
|
1-5 лет 30-40 |
на вдохе |
вздута, коробочный |
|
|
|
|
6-8 лет 25-30 |
|
перкуторный звук |
|
|
|
|
|
|
|
над всей поверхно- |
|
|
|
|
|
|
стью умеренный |
|
|
3 |
1-2 мес. < 60 |
Слышны |
Грудная клетка визу- |
|
+++ |
|
|
2-12 мес. < 60 |
на |
ально резко вздута, |
|
|
|
|
1-5 лет < |
40 |
расстоя- |
выраженный коро- |
|
|
|
6-8 лет < 30 |
нии |
бочный перкуторный |
|
|
|
|
|
|
|
звук |
|
|
Примечание: бронхообструктивный синдром отсутствует - |
0-1 балл; |
|||||
бронхиальная обструкция Ι степени - 2-4 балла; бронхиальная обструкция ΙΙ степени - 5-8 баллов; бронхиальная обструкция ΙΙΙ степени: 9-12 баллов.
Интоксикационный синдром (смотри «острый Б»).
Диагноз обструктивного Б клинический. Дополнительные методы исследования необходимы для проведения дифференциального диагноза в первую очередь с пневмонией.
Лабораторные исследования Рентгенологические данные: вздутие легких (эмфизема), инфильт-
рация корней легких.
Гемограмма – смотри «острый Б».
Исход при обструктивном Б чаще благоприятный. Выздоровление наступает обычно через 10-14 дней. В некоторых случаях заболевание может принять затяжной или рецидивирующий характер. Возможна трансформация в бронхиальную астму. В редких случаях при тяжелом течении наблюдается неблагоприятный исход.
57
Бронхиолит – воспалительное заболевание нижних дыхательных путей с преимущественным поражением мелких бронхов и бронхиол.
Бронхиолитом болеют в основном дети первых месяцев жизни. Этиология – РС-вирусы, вирусы парагриппа и др.
Клиника бронхиолита складывается из: респираторного, интоксикационного бронхообструктивного синдромов. Главными особенностями заболевания являются: одышка (часто выраженная) экспираторного характера (чаще), субфебрильная температура, обилие влажных мелкопузырчатых хрипов над всей поверхностью легких, вздутие легких.
Диагноз бронхиолита клинико-рентгенологический.
Лабораторные исследования Рентгенологические данные: вздутие легких, усиление бронхоле-
гочного рисунка, мелкие ателектазы, мелкие очаговые инфильтративные тени.
Гемограмма – смотри «острый Б».
Исход при бронхиолите зависит от степени тяжести заболевания При тяжелом варианте бронхиолита возможен неблагоприятный исход. Осложнения (пневмония, пневмоторакс) развиваются редко.
Рецидивирующий бронхит – бронхит, который повторяется не реже 2-3 раз в год при длительности заболевания не менее 1-2 лет.
Патогенез. В основе патогенеза лежит повышенная чувствительность бронхиального дерева к вирусной инфекции, аллергическая предрасположенность, дисплазия соединительной ткани (пролапс митрального клапана, разболтанность суставов, повышенная эластичность кожи), морфо-функциональная незрелость стенки бронхов.
Анамнеза, клиника. Обострение необструктивного рецидиви-
рующего бронхита (РНОБ) протекает как острый бронхит с признаками ОРИ. Вне рецидивов клинические проявления отсутствуют.
Болеют дети 1-5 года жизни. Причина обострений – ОРИ.
Обострение рецидивирующего обструктивного бронхита (РОБ)
протекает как обструктивный бронхит. Особенности: более длительное течение рецидива бронхита. Часть случаев РОБ трансформируется в бронхиальную астму. Фактором риска такой трансформации являются: высокий уровень в крови IgE, положительные кожные пробы, атопия в анамнезе, три и более эпизодов обструктивного синдрома.
Диагноз. Анамнестические критерии: заболевание в большинстве случаев развивается после (или во время) ОРИ.
58

Клинические признаки: респираторный синдром (гиперемия слизистой зева, ринит), кашель в начале заболевания сухой, постепенно становится влажным, мокрота отделяется легко, имеет слизистый, реже - слизисто-гнойный характер (при бактериальном характере воспалительного процесса).
Синдром дыхательной недостаточности отсутствует или выражен умеренно на высоте патологического процесса.
Бронхолегочный синдром: неизмененный перкуторный звук либо коробочный оттенок; жесткое дыхание, сухие, крупно- и среднепузырчатые влажные хрипы, выслушиваемые с обеих сторон на вдохе, количество которых изменяется при кашле, иногда выслушиваются единичные мелкопузырчатые влажные хрипы. Симптомы интоксикации в виде снижения эмоционального тонуса (капризность, негативные реакции), легкой бледности кожи. Температура может быть нормальной или субфебрильной. Длительность лихорадки не превышает 2-3 дней, но при микоплазменной и аденовирусной инфекции лихорадка может сохраняться до 8-10 дней.
У детей старше 5 лет диагноз РОБ не применяется. В последние годы отношение к диагнозу РОБ становится все более негативным1.
Дифференциальный диагноз проводят с бронхиальной астмой, муковисцидозом, эзофагогастральным рефлюксом, длительно стоящим инородным телом. Главный отличительный признак бронхиальной астмы – наличие приступообразного появления бронхообструкции.
Табл. 1.18. Клинические критерии дифференциальной диагно-
стики бронхиальной астмы и обструктивного бронхита у детей раннего возраста с бронхообструктивным синдромом на фоне
ОРВИ (Национальная программа «Бронхиальная астма у детей,
2006)
Признаки |
Бронхиальная |
Обструктивный |
|
астма |
бронхит |
Возраст |
Старше 1,5 года |
Младше 1 года |
|
|
|
1 Согласно «Классификации клинических форм бронхолегочных заболеваний у детей», 2009 диагноз «рецидивирующий обструктивный бронхит» не предусмотрен.
59

Проявления бронхообструктив- |
В 1-е сутки |
На 3-й день ОРВИ |
|
ного синдрома |
|||
ОРВИ |
и позднее |
||
|
|||
|
|
|
|
Ранее бронхообструктивный |
2 и более раз |
Не отмечался или |
|
синдром отмечался |
был однократно |
||
|
|
|
|
Наследственная отягощенность |
|
|
|
аллергическими заболеваниями, |
Имеется |
Нет |
|
в том числе наличие бронхиаль- |
|||
|
|
||
ной астмы по материнской линии |
|
|
|
|
|
|
|
Наличие в анамнезе аллергиче- |
|
|
|
ских реакций на пищевые про- |
Отмечено |
Нет |
|
дукты, медикаменты, профилак- |
|||
|
|
||
тические прививки |
|
|
|
Избыточная бытовая антигенная |
|
|
|
нагрузка, наличие сырости, пле- |
Имеется |
нет |
|
сени в жилом помещении |
|
|
|
|
|
|
Табл. 1.19. Дифференциальный диагноз бронхитов (Баранов А.А.
с соавт., 1997)
Сим- |
Простой |
Обструктив- |
Брон- |
Бронхопневмо- |
|
птомы |
бронхит |
ный бронхит |
хиолит |
ния |
|
Темпе- |
Чаще субфеб- |
Чаще субфебрильная, мо- |
Фебрильная или |
||
ратура |
рильная, может |
жет быть нормальной; феб- |
субфебрильная, |
||
тела |
быть нор- |
рильная при микоплазмен- |
сохраняется дли- |
||
|
мальной |
ной и аденовирусной ин- |
тельно |
||
|
|
фекции |
|
|
|
Инток- |
Отсутствует |
Выражена больше, чем при |
Выражена значи- |
||
сикация |
или слабо |
простом бронхите, кратко- |
тельно, нарастает |
||
|
выражена |
временная |
|
|
в динамике болез- |
|
|
|
|
|
ни, при осложне- |
|
|
|
|
|
ниях может раз- |
|
|
|
|
|
виться токсикоз |
Кашель |
Сухой, затем |
Кашель |
Кашель |
Динамика от сухо- |
|
|
продуктивный |
сухой, |
малопродук- |
го до влажного |
|
|
с отхождением |
мокрота |
тивный, упор- |
кашля, глубокие |
|
|
слизистой |
отделяет- |
ный приступо- |
кашлевые толчки |
|
|
мокроты |
ся плохо, |
образный, |
со слизистой или |
|
|
|
вязкого |
нередко имеет |
слизисто-гнойной |
|
|
|
характе- |
спастический |
мокротой |
|
60
|
|
ра |
|
«обертон» |
|
|
Одыш- |
Отсутствует |
Экспираторная с участием |
ДН смешанного |
|||
ка |
|
вспомогательной мускула- |
типа разной степе- |
|||
|
|
туры |
|
|
ни |
|
Форма |
Не изменена |
Вздутие грудной клетки |
Может не изме- |
|||
грудной |
|
|
|
|
|
няться |
клетки |
|
|
|
|
|
|
Данные |
Нормальный |
Коробочный |
|
Коробоч- |
Укорочение пер- |
|
перкус- |
перкуторный |
перкуторный |
ный перку- |
куторного звука |
||
сии |
звук, редко с |
звук разной |
|
торный |
соответствует |
|
|
коробочным |
степени вы- |
|
звук разной |
очагу поражения, |
|
|
оттенком |
раженности |
|
степени |
коробочный отте- |
|
|
|
|
|
|
выражен- |
нок над другими |
|
|
|
|
|
ности |
участками. |
|
Жесткое дыха- |
Дыхание с |
|
Дыхание с |
Ослабленное, же- |
|
|
ние. |
удлиненным |
|
удлинен- |
сткое, бронхиаль- |
|
|
Диффузные |
выдохом, |
|
ным выдо- |
ное дыхание. |
|
|
средне – и |
жесткое, |
|
хом. Оби- |
Часто локальные |
|
|
крупнопузыр- |
сухие сви- |
|
лие мелко- |
его изменения! |
|
|
чатые хрипы, |
стящие хри- |
|
пузырча- |
Мелкопузырчатые |
|
Данные |
сухие хрипы. |
пы, реже – |
|
тых и кре- |
хрипы на ограни- |
|
аускуль |
При кашле – |
разнокали- |
|
питирую- |
ченном участке. |
|
тации |
хрипы изме- |
берные |
|
щих хри- |
Длительность (5-6 |
|
|
няются. Быст- |
влажные |
|
пов над |
дней) сохранения |
|
|
рая положи- |
хрипы. Из- |
|
всей по- |
изменений |
|
|
тельная дина- |
менчивость |
|
верхностью |
|
|
|
мика |
хрипов при |
|
легких. |
|
|
|
|
кашле. Быст- |
|
|
||
|
|
рая положи- |
|
|
|
|
|
|
тельная ди- |
|
|
|
|
|
|
намика |
|
|
|
|
Показа- |
Лейкопения, |
Лейкопения, |
|
Лейкопе- |
Нейтрофильный |
|
тели |
лимфоцитоз; |
лимфоцитоз; |
|
ния, лим- |
лейкоцитоз со |
|
пери- |
нормальная |
нормальная |
|
фоцитоз; |
сдвигом влево, |
|
фериче- |
или слегка |
или слегка |
|
нормальная |
увеличение СОЭ |
|
ской |
ускоренная |
ускоренная |
|
или слегка |
более 20 мм/ч. |
|
крови |
(15-19 мм/ч) |
(15-19 мм/ч) |
|
ускоренная |
Нередко анемия. |
|
|
СОЭ |
СОЭ |
|
(15 -19 |
Изменения зависят |
|
|
|
|
|
|
мм/ч) СОЭ |
от этиологии |
|
|
|
|
|
|
пневмонии |
Рентге- |
Усиление |
Вздутие лег- |
|
Вздутие |
Инфильтрация |
|
нологи- |
бронхососуди- |
ких, усиле- |
|
легких, |
паренхимы очаго- |
|
ческие |
стого рисунка |
ние бронхо- |
|
усиление |
вого, сегментарно- |
|
данные |
за счет перива- |
сосудистого |
|
бронхосо- |
го, очагово- |
|
|
скулярной и |
рисунка |
|
судистого |
сливного, долево- |
|
61
|
перибронхи- |
|
и легочного |
го характера |
|
альной ин- |
|
рисунка. |
|
|
фильтрации, |
|
Мелкие |
|
|
расширение |
|
ателектазы, |
|
|
корней легких |
|
мелкие |
|
|
|
|
тени ин- |
|
|
|
|
фильтрации |
|
Лабораторные исследования Рентгенограмма легких выявляет усиленный легочный рисунок
при отсутствии очаговых тканей, малоструктурность корней легких; эмфизематозные изменения (при РОБ).
Анализ крови: нормальное или незначительное увеличение содержания лейкоцитов, может быть лейкопения, лимфоцитоз, моноцитоз, СОЭ не изменена у большинства больных.
Исходы. У детей без положительного индивидуального и семейного аллергологического анамнеза рецидивы Б постепенно могут исчезнуть. При наличии положительного аллергологического анамнеза у 50% детей возможно развитие бронхиальной астмы.
Лечение. Задачи лечения: воздействие на этиологические причины заболевания (вирусы, бактерии, микоплазмы); купирование проявлений Б (кашель, лихорадка, интоксикация и др.).
Схема лечения. Обязательными при лечении Б являются: обильное питье (около 100 мл/кг в сутки), массаж с дренажом грудной клетки.
Вспомогательная терапия: этиологическая (противовирусная - при среднетяжелых и тяжелых проявлениях ОРИ, антибактериальная терапия), и симптоматическое лечение.
Показания для госпитализации: затянувшееся течение Б, наличие серьезной фоновой патологии, выраженность бронхообструктивного синдрома, выраженность дыхательной недостаточности (для бронхиолита), по социальным причинам.
Показания для назначения антибиотиков при Б: 1) гипертермия бо-
лее 3-х дней, 2) наличие клинической картины бронхиолита и пневмонии, 3) ранний возраст больного (особенно дети первого года жизни), 4) наличие выраженных симптомов интоксикации, 5) затянувшееся течение заболевания, 6) подозрение на микоплазменную или хламидийную этиологию Б.
Препаратами первого ряда при Б являются: амоксициллин, амоксициллин/клавуланат (например, Амоксиклав, Уназин), азитромицин (Сумамед), кларитромицин (Клацид, Клеримед, Фромилид). Фузафунгин (аэрозоль «Биопарокс»), кроме антибактериального действия
62
уменьшает экссудацию и улучшает мукоцилиарный клиренс. Основой симптоматической терапии является назначение отхарки-
вающих и муколитических препаратов в зависимости от характера кашля и мокроты. В качестве противовоспалительной терапии применяют фенспирид (Эреспал). При выраженной лихорадке показаны жаропонижающие средства.
Лечение лихорадки
При наличии «бледной гипертермии» больному назначают парацетамол в разовой дозе 10-15 мг/кг или ибупрофен в разовой дозе 5-10 мг/кг.
Табл. 1.20. Критерии назначения жаропонижающих средств при
лихорадке
Группы детей |
Благоприятный тип |
Неблагоприятный тип |
|
лихорадки, «розовая |
лихорадки, «бледная» |
|
лихорадка» |
лихорадка |
Здоровые дети |
Выше 39,0-39,5 оС |
Выше 38,0 оС |
в возрасте |
|
|
старше 2 мес. |
|
|
Дети из груп- |
Выше 38,0-28,5 оС |
Выше 37,5 оС |
пы риска* |
|
|
* В группу риска по развитию осложнений включают: детей в возрасте до 2-х месяцев при наличии температуры выше 38 оС, с фебрильными судорогами в анамнезе, с хронической патологией органов кровообращения, с наследственными метаболическими заболеваниями.
Табл. 1.21. Муколитическая терапия при бронхитах
Препарат |
|
Показания к приме- |
Противопоказания и ог- |
|
|
нению |
раничения к применению |
|
Препараты центрального действия |
||
Бронхолитин, ко- |
|
Сухой навязчивый |
Продуктивный кашель, |
деин, кодипронт, |
|
кашель, сопровож- |
ранний возраст, про- |
дионин, глауцин |
|
дающийся болевым |
дуктивный кашель у |
гидрохлорид, бута- |
синдромом (плеврит, |
детей с заболеваниями |
|
мират (Синекод), |
|
коклюш) |
ЦНС, отек легких, |
тусупрекс, Пансиве- |
|
инородные тела, аспира- |
|
рин (Седотуссин) |
|
|
ция |
Увлажняющие
63

Ингаляции хлорида |
Непродуктивный ка- |
|
Сухой плеврит, ино- |
или бензоната на- |
шель |
|
родные тела дыхатель- |
трия, соды, хлорида |
|
|
ных путей, аспирация |
аммония, эвкалип- |
|
|
жидкостей, отек легких |
та, бальзама Эвкаба- |
|
|
|
ла, водного пара |
|
|
|
|
Обволакивающие |
|
|
Экстракты эвка- |
Непродуктивный ка- |
|
Нет |
липта, акации, лак- |
шель при заболева- |
|
|
рицы, дикой вишни, |
ниях дыхательных |
|
|
липы, глицерин, мед |
путей |
|
|
|
Местноанастезирующие |
||
Бензокаин, циклаин, |
проведение меди- |
|
Все другие ситуации |
Татракаин |
цинских манипуля- |
|
|
|
ций на дыхательных |
|
|
|
путях |
|
|
|
Отхаркивающие2 |
|
|
Бронхикум эликсир, |
Заболевания дыха- |
|
Продуктивный кашель, |
Бронхоцин, Гексап- |
тельных путей у де- |
|
ранний возраст ребенка, |
невмин, Геделикс, |
тей старше 3 лет. |
|
высокий риск развития |
Глицерам, Грудной |
Кашель, ассоцииро- |
|
аспирации, бронхорея |
сбор (№1 - №3), |
ванный с бронхос- |
|
любой этиологии, отек |
Грудной эликсир, |
пазмом |
|
легких |
Доктор Мом, Колд- |
|
|
|
рекс, Мукалтин, |
|
|
|
Пектуссин, Термо- |
|
|
|
псис, Туссин |
|
|
|
|
Муколитики |
|
|
Ацетилцистеин, |
Кашель, обусловлен- |
|
В зависимости от пре- |
карбоцистеин, бром- |
ный трудностью от- |
|
парата |
гексин, карбоци- |
хождения густой и |
|
|
стеина лизиновая |
вязкой мокроты |
|
|
соль (Флуифорт), |
|
|
|
амброксол (Лазол- |
|
|
|
ван), дорназе, Мес- |
|
|
|
на, |
|
|
|
|
Противовоспалительные |
||
2 Традиционные отхаркивающие средства недостаточно эффективны, а у детей младшего возраста могут вызвать рвоту
64
Фенспирид (Эрес- |
|
ОРЗ, бронхиты, |
Все другие ситуации |
пал) |
|
|
|
|
Комбинированные препараты |
||
Бронхолитин, стоп- |
|
ОРЗ, бронхиты, ино- |
Непродуктивный ка- |
тусин, синекод, ло- |
|
гда бронхоспазм |
шель |
рейн, солутан |
|
|
|
При отсутствии эффекта от применения парацетамола (ибупрофена) применяют литические смеси, включающие: дипразин (пипольфен) 2,5% раствор в дозе 0,15-0,3 мг/кг внутривенно или внутримышечно, дроперидол 0,25% раствор в дозе 0,05-0,15 мг/кг массы, анальгин 50% раствор в дозе 5 мг/кг (0,1 мл/год жизни).
Физические методы охлаждения (холод к голове и на крупные сосуды, растирание уксусно-спиртовым раствором) применяют только после введения сосудорасширяющих препаратов.
Противовирусная терапия при Б назначается в случаях среднетяжелого или тяжелого течения ОРВИ в первые дни заболевания. Наиболее часто для этой цели используют: Арбидол, Циклоферон, Альгирем (Римантадин), Анаферон детский, Афлубин, Виферон.
Особенности лечения острого Б
Лечение острого Б обычно проводится амбулаторно. Постельный режим назначают до нормализации температуры. Диета, обогащенная витаминами и молочно-растительная пища (для детей в возрасте старше 1 года). Обильное питье. Антибактериальная, противовирусная, противокашлевая терапия назначаются по принципам, изложенным выше.
Антигистаминные препараты показаны: при наличии фоновых аллергических заболеваний, у больных с обильной жидкой мокротой.
Особенности лечения обструктивного Б
Лечение обструктивного Б отличается от лечения острого Б только терапией обструктивного синдрома.
Бронхоспазмолитическая терапия (шаг 1): β2-агонисты - сальбутамол (Вентолин), формотерол (Форадил), фенотерол (Беротек). Препараты можно вводить через небулайзер. Показано применение холиноблокатора атровента (ипратропиум бромид). При отсутствии эффекта – через 20-40 минут вводится повторная доза препаратов.
Шаг 2: повторная доза β2-агонистов + ингаляционные глюкокортикоиды.
Шаг 3: стероиды внутримышечно (дексаметазон 0,5-0,75 мг/кг или преднизолон 3-5мг/кг).
Поддерживающая терапия: β-адреномиметик (аэрозоль, перо-
65
рально), в том числе с ипратропия бромидом (Беродуал), и/или эуфиллин по 4-5 мг/кг 3-4 раза в сутки.
Особенности лечения бронхиолита
Питание не изменяют, или объем питания может быть уменьшен. При признаках обезвоживания 1-2-й степени показана оральная регидратация (регидрон, Оралит и др.). Инфузионная терапия назначается при клинике эксикоза 2-й степени. Принципы инфузионной терапии: ограничение суточной жидкости потребления на 20-30-50% (в зависимости от степени тяжести состояния). Внутривенно вводится 1/3 часть от рассчитанного объема.
Оксигенотерапия – основа лечения бронхиолита с признаками дыхательной недостаточности II-III степени. Принципы лечения ДН изложены в разделе «пневмония».
Купирование бронхообструктивного синдрома проводится по принципам, изложенным в разделе «обструктивный бронхит».
При выраженном беспокойстве можно осторожно назначить седативную терапию.
При тяжелом течении бронхиолита за рубежом применяют аэрозоль рибавирина непрерывным или интермиттирующим методом.
Симптоматическое лечение проводится по принципам лечения простого Б.
Особенности лечения рецидивирующего бронхита (РБ)
Схема лечения РОБ и РБ. Обязательным является: обильное пи-
тье (около 100 мл/кг в сутки), массаж с дренажом грудной клетки, бронхоспазмолитическая терапия (при РОБ), лечение выявленной сопутствующей патологии, кетотифен, бактериальные вакцины, кромоны.
Вспомогательная терапия: этиологическая (противовирусная - при среднетяжелых и тяжелых проявлениях ОРИ), антибактериальная и симптоматическая.
Лечение рецидивирующего обструктивного бронхита при его обо-
стрении проводится по тем же правилам, что и лечение «Обструктивного бронхита». Базисным лечением при рецидивирующем обструктивном бронхите является кетотифен по 0,05 мг/кг/сут в течение 3-6 месяцев. Вместо кетотифена можно использовать: интал, Тайлед, дитек, беротек (через небулайзер). При недостаточном эффекте в лечение следует добавить ингаляции стероидов (лучше через небулайзер). При частых обострениях Б и ОРИ назначают рибомунил.
Из отхаркивающих и муколитических препарат наиболее предпочтителен Лазолван или АЦЦ.
66

Антигистаминные препараты при РОБ и РБ показаны только при наличии сопутствующих аллергических заболеваний. Показанием для применения антибиотиков является появление обильной гнойной мокроты и выявление сопутствующего тонзиллита и синусита. В качестве противовоспалительной терапии показано назначение фенспирида (Эреспала) в дозе 4 мг/кг. Уменьшению частоты ОРИ способствуют бактериальные лизаты.
Табл. 1.22. Бактериальные лизаты (бактериальные вакцины)
Препарат |
Путь введе- |
До 7 |
Старше |
Схема применения |
|
ния |
лет |
7 лет |
|
|
|
|
|
|
Бронхомунал |
Перорально |
3,5мг |
7,0 мг |
1 раз в день – в течение |
|
|
|
|
10 дней каждого из 3 мес. |
Рибомунил |
Перорально |
0,25 |
0,5мг |
1 раз в день – в течение |
|
|
мг |
|
4 дней из каждых 3 нед. |
ИРС-19 |
Интраназально |
1 нажатие (1 |
2 раза в день – в течение |
|
|
|
доза) |
|
2 нед. |
|
|
|
|
|
Имудон |
табл. для рас- |
1 табл. |
6-8 раз в день в течение |
|
|
сасывания |
|
|
10-20 дней |
|
|
|
|
|
Применение физиотерапевтических процедур не оказывает существенного влияния на течение рецидива Б.
Профилактика Б соответствует профилактическим мероприятия при ОРИ: санитарно-оздоровительные меры, специфическая и неспецифическая профилактика. Наиболее эффективными профилактическими мерами являются: разобщение здоровых и больных детей, мытье рук, закаливание. С профилактической целью можно применять бактериальные лизаты (ИРС 19, Имудон, бронхомунал, рибомунил), Арбидол, Анаферон детский и др.; иммуномодуляторы.
Вопросы к экзамену. Бронхиты. Этиология. Патогенез бронхитов. Роль
инфекционных, физических и химических факторов в развитии бронхитов. Роль загрязнения атмосферного воздуха, пассивного и активного курения. Классификация. Острые бронхиты: острый (простой) бронхит, острый бронхиолит, рецидивирующий бронхит, обструктивный бронхит. Первичные и вторичные бронхиты. Особенности клинической картины. Течение бронхитов. Диагностика. Дифференциальный диагноз. Лечение. Исходы. Профилактика.
67
ПНЕВМОНИЯ (П) – острое инфекционное заболевание легких, преимущественно бактериальной этиологии, характеризующееся очаговым поражением респираторных отделов с внутриальвеолярной экссудацией.
Эпидемиология. П в РФ встречается у 4-17 детей на 1000 детского населения. При использовании только клинических критериев диагностики заболеваемость П увеличивается до 20-80 на 1000 детей.
Этиология. Основным возбудителем П у детей является стрептококк пневмонии (пневмококк). На этиологию П у детей существенное влияние оказывают: место инфицирования, возраст ребенка, наличие легочных осложнений, иммунодефицитные состояния.
Ведущими бактериальными возбудителями типичных П у детей в возрасте 1-6 месяцев являются: кишечные палочки и другие представители грамотрицательной кишечной микрофлоры, стафилококки. Реже типичные П в этом возрасте вызываются гемофильной палочкой (10%) и маракселлой.
Основными возбудителями атипичных П являются: хламидия трахоматис и микоплазмы.
Во всех возрастных группах в15% случаев П вызываются вируса-
ми.
Таб.1. 23. Этиология внебольничных пневмоний у детей
Возбудитель |
0 - 3 |
3 мес - |
Старше |
Ослож- |
Аспирация |
|
мес |
5 лет |
5 лет |
ненная |
|
-Str. pneumoniae |
+ |
++ |
+++ |
+++ |
+ |
H. influenzae |
+ |
+++ |
+ |
+++ |
+ |
Streptococcus viridans |
+++ |
- |
- |
- |
- |
Staphilococcus aureus |
++ |
++ |
+ |
++ |
++ |
M. catarrhalis |
+ |
+ |
+ |
+ |
+ |
Enterobacteriaceae |
+++ |
+++ |
+ |
+ |
+ |
spp |
- |
+ |
+ |
++ |
++ |
Streptococcus |
+ |
+ |
+++ |
+ |
- |
pyogenes |
+++ |
+ |
+/- |
+/- |
- |
M.pneumoniae |
|
|
|
|
|
Chlamydphilla/ |
+ |
- |
- |
- |
- |
Chlamydia |
+/- |
- |
- |
+/- |
++ |
U.urealyticum |
|
|
|
|
|
Анаэробы |
|
|
|
|
|
68
Внебольничные П у детей в возрасте от 6 месяцев до 6 лет. Ос-
новные бактериальные возбудители типичных П: стрептококк пневмонии (более 50%), гемофильная палочка (до 10%). Атипичные П в этом возрасте вызываются микоплазмами (10%) и еще реже – хламидиями.
Внебольничные П в возрасте от 7 до 15 лет вызываются как виру-
сами, так и бактериями. Основными бактериальными возбудителями типичных П являются: пневмококки (40%) и редко - гемофильная палочка и стрептококки. Атипичные П в этом возрасте чаще всего вызываются микоплазмами (20-40%) и редко – хламидиями (7-24%).
У детей с иммунодефицитами П вызываются: вирусами (ЦМВ,
герпеса и др.), грибами, пневмоцистами.
Классификация
По этиологии: бактериальная, вирусная, грибковая, паразитарная, хламидийная, микоплазменная, смешанная.
По месту инфицирования: внебольничная, внутрибольничная (после 48-72 часов после госпитализации).
Также выделяются:
Аспирационная (при заболеваниях, сопровождающихся рефлюксом, дисфагией, у больных с нарушением сознания);
Вентиляционная – развивается у пациентов на ИВЛ: ранняя – в первые 5 суток и поздняя – после 5 суток ИВЛ;
У новорожденных: внутриутробные (которые проявились в первые 72 часа жизни), постнатальные.
По клинико-рентгенологическим данным: очаговая пневмония,
моноили полисегментарная, очагово-сливная, долевая (крупозная), интерстициальная).
По степени тяжести: средней тяжести и тяжелая. Тяжесть пневмонии определяется выраженностью клинических проявлений и наличием осложнений.
Осложнения: легочные: булла, абсцесс, плевриты, пневмоторакс, пиопневмоторакс, абсцесс.
Внелегочные осложнения: ДВС-синдром, недостаточность кровообращения, инфекционно-токсический шок.
По течению: острое (до 1,5 мес.), затяжное (1,5-6 месяцев). Патогенез. В основе патогенеза П лежит снижение иммунитета,
часто развивающееся вследствие вирусных заболеваний. Важную роль играет также нарушение мукоцилиарного клиренса (см. «Бронхиты»).
В настоящее время выделяют следующие основные механизмы развития П:
1. Микроаспирация секрета ротоглотки;
69

2.Вдыхание аэрозоля, содержащего микроорганизмы;
3.Гематогенное распространение микроорганизмов из внелогочного очага инфекции;
4.Непосредственное распространение инфекции из соседних пораженных органов.
Экзогенный путь ин- |
Предшествующее |
Эндогенный путь инфици- |
||
фицирования (пневмо- |
воздействие виру- |
рования (стафилококки, |
||
кокки, микоплазма) |
са на респиратор- |
стрептококки, протей, |
||
|
ный тракт |
кишечная палочка |
||
Аспирация |
|
|
|
|
пищи |
Инфекционный агент |
|
|
|
|
|
|
||
|
|
воздействие на эндотелий |
||
Бронхогенный путь распространения |
капилляров |
|
||
инфекции |
|
|
|
|
торможение функции реснитчатого эпителия |
|
|
||
нарушение мукоцилиарного клиренса |
|
|
||
возникновение сегментарного ателектаза |
нарушение функции |
|||
|
|
|||
развитие пневмонического фокуса |
нейтрофилов, макро- |
|||
фагов, Т-лимфоцитов |
||||
|
|
|||
нарушения в малом круге кровообращения (прекращение |
|
|||
капиллярного кровотока, патологического шунтирование) |
Нарушения |
|||
|
|
|
||
|
|
|
микроцирку- |
|
уменьшение газообмена, нарушение диффузии |
|
ляции |
||
|
|
|||
|
|
токсикоз |
|
Недостаточность функции внешнего дыха- |
|||
|
|
||
|
|
|
гипоксемия |
|
|
|
гипокапния |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Нарушение метабо- |
|
|
|
|
гиперкапния |
|
|
|||||
лических процессов |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
Нарушение белково- |
|
|||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
го, углеводного, |
|
|||
|
Фиксация железа |
|
|
|
жирового, пигмент- |
|
||||||
|
|
|
|
|
|
|
|
ного обмена |
|
|||
|
|
|
|
|
|
|||||||
|
анемия |
|
|
|
|
|
|
70 |
|
|||
|
|
|
|
|
|
|
||||||
Эндокринные наруше-
ния
гипоксия ДВС
Нарушения КОС, микро-
элементного баланса
шок
Ацидоз
парез кишеч-
ника Органные
поражения
Синдром ССАДГ*
Рис. 1.8. Схема патогенез пневмонии
* ССАДГ – синдром стимуляции антидиуретического гормона.
Факторами, предрасполагающими к микроаспирации являются:
-возраст до 6 мес.;
-энцефалопатии;
-дисфагия (срыгивание, рвота, гастроэзофагеальный рефлюкс);
-синдром бронхиальной обструкции;
-механизм нарушения защитных барьеров (зонд, интубация, трахеомаляция, повторная рвота при парезе кишечника, тяжелых заболеваниях;
-ИВЛ;
-развитие критического состояния вследствие основного заболевания;
-пороки развития сердца, легких;
-нейромышечная блокада.
Исследования. Общий анализ крови и мочи, рентгенография орга-
нов грудной клетки. По показаниям: посев мокроты на флору, (включая M.pneumoniae, а также U.urealyticum у новорожденных), исследование показателей КОС, определение хламидий в слюне и других биологических жидкостях, спирограмма, экспресс диагностика вирусных антигенов иммунофлюоресцентным методом, определение титра антител к хламидиям, микоплазмам.
Исследования амбулаторно, приказ МЗ РФ № 263: общий анализ крови, рентгенография легких. По показаниям: микробиологическое исследование мокроты (включая M.pneumoniae, а также U.urealyticum у новорожденных), серологические исследования на инфекции и вирусы, томография легких.
Анамнез, клиника. Примерно у половины детей развитию П предшествует ОРИ. Наиболее характерные признаки П: температура тела более 38 0С в течение 3-х суток и более, одышка, втяжение уступчивых мест грудной клетки, кашель, интоксикация.
Фебрильная температура важный признак П. Температура ниже 38 0С с 95% с большой вероятностью свидетельствует против П – кроме атипичных. Отсутствие лихорадки у ребенка старше 6 месяцев ставит под сомнение наличие П. Без применения антибиотиков лихорадка держится более трех дней.
Одышка выявляется тем чаще, чем обширнее поражение легких (20-60%). Цианоз очень редкий признак дыхательной недостаточности.
71
Интоксикационный синдром: плохой аппетит, возбуждение или апатия, нарушение сна, плаксивость, бледность, тахикардия.
Синдром респираторно-катаральных изменений: насморк, кашель,
конъюнктивит и др. Особенности его проявлений зависят от этиологии предшествующей ОРИ (встречается в 40-50% случаев).
Аукультативно-перкуторные изменения: изменение перкуторного звука выявляется тем чаще, чем обширнее зона пневмонической инфильтрации (при долевых процессах – в 75%).
Ослабленное дыхание, локальное жесткое дыхание, бронхиальное дыхание над зоной инфильтрата – 70%, локальные мелкопузырчатые хрипы – менее 50%, рассеянные влажные хрипы – 25%, рассеянные сухие хрипы – 10%.
Внимание! У 20-30% при П отсутствуют локальные перкуторные и аускультативные изменения. Отсутствие у пациента локальных изменений со стороны легких не исключает наличия П.
В зависимости от этиологии и клинических проявлений П условно делят на типичные и атипичные.
Табл. 1.24. Признаки типичных и атипичных внебольничных пневмоний у детей первых месяцев жизни (В.К. Таточенко, 2006)
Признак |
Пневмония типичная |
Пневмония атипичная |
Лихорадка |
Выражена, Т > 38 0С |
Нет или субфебрильная |
Одышка |
Нет или незначительная |
Выражена |
|
Влажный, нечастый |
Начинается с кашля, ка- |
Кашель |
|
шель стокато, упорный, |
|
|
нарастающий |
Катар |
Часто отсутствует |
Отсутствует или скудный |
Конъюнкти- |
Отсутствует |
В анамнезе, и при мико- |
вит |
|
плазмозе |
Лимфаденит |
Отсутствует |
При хламидиозе |
Хрипы |
Нет или локализо- |
Рассеянные |
ванные |
|
|
|
|
|
Перкуссия |
Часто укорочение |
Коробочный звук |
Рентгеноло- |
Чаще односторонний |
Двусторонние множествен- |
гическая |
очаг или инфильтрат; |
ные очаги с поражением |
картина |
вовлечение плевры |
интерстиция |
|
Кишечная палочка, ста- |
C. trachomatis, M. pneumo- |
Возбудитель |
филококки, реже пнев- |
niae, U. urealyticum |
|
мококк, H. influenzae |
|
72
Осложнения (см. «классификация пневмоний»).
Особенности клиники П разной этиологии
Пневмококковые пневмонии. Крупозная П у детей старшего возраста характеризуется температурой 40 0С и выше, ознобом. Возможен кашель с ржавой мокротой. Нередко наблюдают герпетические высыпания, покраснение щеки на стороне поражения, боли в грудной клетке. Возможно расстройство сознания (бред, страхи). При исследовании легких выявляют локальные перкуторные (укорочение); аускультативные (ослабление дыхание, бронхофония, непостоянные крепитирующие хрипы) изменения.
При рентгенологическом исследовании обнаруживают чаще одностороннее, как лобарное, так и очаговые (в т.ч. шаровидные) тени или затемнения 1-2 сегментов. В анализе крови - лейкоцитоз выше 15-
20×109/л со сдвигом формулы крови влево, увеличение СОЭ до 20-40 мм/ч и выше.
Пневмококковые П у детей младшего возраста протекают при не-
большом объеме инфильтрата, с умеренным токсикозом. Часто отсутствует одышка. При массивных инфильтратах в процесс вовлекается плевра (син – и метапневмонические плевриты). Иногда развивается пиопневмоторакс и внутрилегочные тонкостенные полости (буллы). В
анализах крови наблюдают лейкоцитоз выше 15-20×109/л со сдвигом формулы крови влево, увеличение СОЭ до 20-40 мм/ч и выше.
Стафилококковые пневмонии чаще формируются у детей первых месяцев жизни, а также у больных иммунодефицитами. При внутрибольничном заражении стафилококки вызывают П особенно у детей, получавших пенициллин. Характерно наличие предшествующего ОРИ.
При исследовании легких выявляют укорочение перкуторного звука, локальные изменения дыхания, рассеянные влажные и сухие хрипы (признак гнойного бронхита). У таких больных часто развивается выраженный пневмонический токсикоз, одышка, кашель, стонущее дыхание. При плевральной пункции в случаях развития плеврита можно обнаружить сливкообразный гной.
При рентгенологическом исследовании вначале выявляется нечетко ограниченный инфильтрат, который быстро увеличивается в размерах; признаки плеврита; воздушные полости (иногда с уровнем жидкости).
В анализе крови нередко обнаруживают лейкоцитоз выше 25×109/л, увеличение СОЭ выше 30-40 мм/ч.
73
Стрептококковыми пневмониями болеют дети 2-7 лет. Харак-
терно острое начало, фебрильная температура, токсикоз. При исследовании легких нередко имеет место отсутствие четких перкуторных признаков, малое количество хрипов. Со стороны сердца возможно развитие атриовентрикулярной блокады.
При рентгенологическом исследовании выявляют множественные округлые очаги инфильтрации в разных фазах (от инфильтрации до абсцесса), увеличение прикорневых лимфатических узлов; выраженный интерстициальный компонент воспаления (рассеянные небольшие очаги, часто с полостями). Часто выявляют двусторонний плеврит с жидким гноем. В крови можно обнаружить увеличение титров АСЛ – О.
Пневмониями, вызванные гемофильной палочкой болеют дети до 5 лет. Для этой этиологии П характерно острое начало, фебрильная температура, токсикоз.
При рентгенологическом исследовании выявляют очаги инфильтрации, иногда плевральный выпот геморрагического характера.
В анализах крови - нормальное число лейкоцитов и СОЭ. Антибиотики типа пенициллина неэффективны.
Микоплазменные пневмонии чаще наблюдают у детей школьного возраста. Характерна сезонность заболеваемости, увеличение числа больных каждые 4-5 лет.
Вклинической картине характерным является упорный кашель, высокая температура при относительно нетяжелом состоянии. У многих детей имеет место постепенное начало заболевания, скудные катаральные проявления.
При исследовании легких выслушиваются рассеянные мелкопузырчатые хрипы, чаще асимметричные.
При рентгенологическом исследовании обнаруживается негомогенная инфильтрация обоих легких, часто асимметричная.
Ванализах крови наблюдают отсутствие лейкоцитоза, нормальное или умеренно повышенное СОЭ.
Хламидийные пневмонии характерны для детей первых 6 месяцев
жизни. В анамнезе у матери фиксируют выделения из гениталий во время беременности или эрозии. У детей на первом месяце жизни возможны конъюнктивиты. Температура обычно нормальная. Характерен нарастающий кашель (стокато – коклюшеподобный, без реприз).
При исследовании легких выявляют одышку без клинических признаков бронхиальной обструкции. При аускультации в легких выслушивают рассеянные влажные хрипы.
74
При рентгенологическом исследовании обнаруживают вздутие и усиление легочного рисунка, множество мелких очажков (напоминает картину милиарного туберкулеза).
В анализе крови часто выявляют выраженный лейкоцитоз (выше
20-30×109/л) и эозинофилию (выше 5%).
Вирусные пневмонии могут развиться при тяжелой форме гриппа (клиника геморрагического инфаркта легкого), аденовирусной инфекции, РС-инфекции, парагриппе. Клиника этих П трудноотличима от клиники бронхита.
Диагноз вирусной П оправдан при выявлении на рентгенограмме негомогенной пневмонической инфильтрации без четких контуров, при отсутствии в крови сдвигов, характерных для бактериальных П.
Диагноз. При постановке диагноза П учитывают: нарушение общего состояния, повышение температуры тела (лихорадка более трех дней), наличие кашля, одышку различной степени выраженности и характерные физикальные проявления (локальные нарушения дыхания и перкуторного звука). Рентгенологическое подтверждение базируется на выявлении очаговых или инфильтративных изменений на рентгенограмме.
На этапе верификации диагноза допускается постановка диагноза острой П только по клиническим признакам. Следует помнить, что мелкие (менее 1-2 см в диаметре), разрозненные очаги инфильтрации, как правило, не выявляются при рентгенологическом исследовании легких. При этом придается большое значение изменениям в динамике со стороны крови - ускорение СОЭ, нейтрофильный лейкоцитоз со сдвигом влево.
Лабораторные исследования
При П наиболее характерными являются следующие гематологи-
ческие сдвиги: лейкоцитоз выше 10×109/л – выявляют у 50% больных. Высокий лейкоцитоз характерен для деструктивной П, П, вызванной хламидией трахоматис. П с низким числом лейкоцитов наблюдают при выделении микоплазмы и гемофильной палочки. Для П характерна СОЭ выше 20 мм/ч. Отсутствие гематологических изменений не позволяет исключить П.
Рентгенологическое исследование. Гомогенная тень (полисегмен-
тарная, долевая очаговая) характерна для бактериальных П; тяжистые, негомогенные тени – для атипичных П (микоплазма). По форме пневмонической тени очень трудно судить о ее этиологии.
75

Диссеминированный процесс у грудных детей характерен для хламидиоза или пневмоцистоза; у детей старшего возраста – для стрептококковой этиологии П.
Очагово-сливные плотные тени с выбухающей границей характерны для деструктивных П; при наличии вогнутой границы – говорят о наличии ателектатического компонента.
Прикорневые затемнения – реакция корней на ОРИ или туберкулезный бронхоаденит. Диагноз «прикорневая пневмония» неправомочен.
Рентгенологический контроль показан только при массивных и осложненных П, а также при отсутствии эффекта от лечения.
При неосложненных П повторная рентгенограмма выполняется в случаях полного клинического эффекта не ранее чем через 3-4 недели (т.к. рассасывание пневмонического инфильтрата происходит именно в эти сроки).
Наличие бронхиальной обструкции с высокой степенью вероятности исключает типичную этиологию П. Эти проявления возможны при атипичных П и внутрибольничном заражении.
Важное место в диагностике П принадлежит определению этиологического агента (возбудителя) путем бактериоскопии и посевов мокроты и промывных вод бронхов. Обнаружение бактериального агента из верхних дыхательных путей не обязательно свидетельствует о том, что он является возбудителем П.
Начало осмотра: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Т0 > 380 > 3 дней |
|
Нет |
|
|
|
|
|
Нет |
|
Асимметрия |
|||||||||||||
и/или одышка и/или |
|
|
|
|
|
|
|
|
|
|
|
влажных |
|||||||||||
|
|
|
Локальные |
сим- |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||
втяжение |
грудной |
|
|
|
|
|
|
|
|
хрипов |
|||||||||||||
|
|
|
птомы: |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||
клетки (без |
обструк- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
укорочение |
пер- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
ции) |
|
|
|
|
|
|
|
|
|
|
|
нет |
|
|
|
|
|||||||
|
|
|
|
куторного звука |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
и/или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
ослабленное |
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Признаки токсикоза |
|
||||||||||||||||||
|
|
|
|
|
бронхиальное |
|
|
||||||||||||||||
|
|
|
|
|
дыхание |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
и/или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
локальные хрипы |
|
|
Да |
|
|
|
Нет |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
Да |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОРВИ |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
76

Рентгенография или начало лечения
Рис. 1.9. Диагностический алгоритм пневмоний (по В.К. Та-
точенко, 2006 г)
Посевы крови на стерильность выявляют возбудителя в 10-20% случаев, а при наличии плеврита в 40%.
Посевы мокроты из трахеи полуколичественным методом дают хорошие результаты для пневмококков, но не для гемофильной палочки и стафилококков.
Выделение атипичных патогенов из дыхательных путей свидетельствует о наличии инфекции или носительстве, однако, не обязательно говорит о ее роли в развитии П.
Нарастание титров АТ к пневмотропным микроорганизмам не имеет диагностического значения из-за феномена поликлональной активации иммунной системы. Для подтверждения роли атипичной флоры имеет значение выявление антител класса IgM, однако, это происходит только на второй-третьей неделе заболевания.
В повседневной практике методы этиологической диагностики рекомендуются только при рефрактерных к лечению случаях, а также при внутрибольничном инфицировании.
У всех детей с ОРЗ и кашлем классифицируют как имеющие (В.К. Таточенко, 2006):
1.Вероятно тяжелую П при наличии хотя бы одного из следующих симптомов, независимо от уровня температуры:
-учащение дыхания при отсутствии обструкции; -втяжение межреберий в отсутствие обструкции; - стонущее кряхтящее дыхание; - цианоз носогубного треугольника;
Признаки токсикоза (больной вид, отказ от еды и питья, сонливость, нарушение сознания, резкая бледность при повышенной температуре).
2.Вероятно имеющие П – при отсутствии указанных в п. 1 пр и- знаков, при наличии хотя бы одного из следующих симптомов:
3.– температура > 38 0С более 3 дней;
4.Локальные физикальные признаки пневмонии;
5.Асимметрия хрипов, особенно при наличии конъюнктивита и других симптомов микоплазменной инфекции.
77

В тех сл учаях, когда П развивается на фоне других различных заболеваний легких, сердца, крови, после травм, ранений, отравлений и т.д. устанавливается диагноз вторичной П: инфаркт-пневмонии, гипостатические, застойные П, аспирационные и т.д.
Дифференциальный диагноз П проводят с различными заболеваниями как системы дыхания, так и другими инфекционными заболеваниями. Выраженное преобладание признаков интоксикации, особенно в начале заболевания, делает необходимым дифференциальный диагноз с такими инфекционными заболеваниями как тифы, ангины и др., первичной манифестацией которых является общая интоксикация. Необходимо помнить о туберкулезе легких, особенно в тех случаях, когда при рентгенологическом исследовании выявляется инфильтрат округлой или овальной формы с четкими контурами в верхних долях легких на фоне петрификатов. При этом в мокроте и в промывных водах с бронхов могут определяться микобактерии туберкулеза.
Наличие респираторно-катаральных проявлений требует исключе-
ния ОРИ, бронхитов (см. табл. 1.19).
При появлении выраженных инфильтративных изменений в легких,
следует исключить экссудативный плеврит и опухоли, для чего необ-
ходимы дальнейшее инструментальное (рентгенологическое, бронхологическое) и лабораторное обследование.
При затяжном течении П ее следует дифференцировать с застой-
ными явлениями в легких кардиального генеза, со злокачественными новообразованиями легких, особенно в тех случаях, когда имеется о б- струкция бронха.
Табл. 1.24. Дифференциальный диагноз пневмонии
Признак |
Пневмония |
Гнойный плеврит |
Лихорадка |
Характерна |
Характерна, выраже- |
|
|
на |
Интоксикация |
Имеется |
Выражена |
Дыхательная недос- |
В зависимости от |
В зависимости от |
таточность |
варианта пневмонии |
объема выпота |
Ограничение экскур- |
Не характерно |
Характерно |
сии грудной клетки |
|
|
Тупой звук при пер- |
Не характерен |
Характерен |
куссии |
(часто укорочение) |
|
Резко ослабленное |
Локальное ослабле- |
Характерно |
или отсутствующее |
ние дыхания |
|
дыхание |
|
|
78
Анализ крови |
Различная степень |
Большая степень вы- |
|
выраженности воспа- |
раженности измене- |
|
лительных изменений |
ний по сравнению с |
|
|
пневмонией |
Рентгенологические |
Инфильтративные |
Затемнение реберно- |
данные |
изменения в легких в |
диафрагмального |
|
зависимости от фор- |
угла |
|
мы |
|
Смещение органов |
Не характерно |
В здоровую сторону |
средостения |
|
|
Лечение. Задачи лечения: санация возбудителя, купирование дыхательной недостаточности, лечение изменений, развившихся в различных органах и системах (токсикоз, сердечно-сосудистая недостаточность, нарушения КОС и т. д.).
Схема лечения. Обязательным при П является назначение антибиотиков и оксигенотерапия (при ДН II-III степени).
Вспомогательное лечение: режимные моменты, рекомендации по питанию, симптоматическое (синдромальное) лечение.
Показания для госпитализации: дети первого полугодия жизни;
осложненная П; признаки гипоксии или выраженной дегидратации; наличие тяжелой сопутствующей патологии; отсутствие эффекта от стартовой антибактериальной терапии в течение 36-48 часов; госпитализация по социальным показаниям.
Принципы антибактериальной терапии пневмоний
1.Стартовая антибактериальная терапия назначается эмпирически (без выделения возбудителя) сразу после установления диагноза или при наличии подозрения на П.
2.Назначаемый антибактериальный препарат должен быть эффективным против всех наиболее вероятных возбудителей П. При выборе препарата необходимо опираться на все имеющиеся данные, касающиеся возможной этиологии заболевания (бактериологическое мониторирования для данного региона, методические рекомендации и т. д.).
3.Предшествующая у больного антибактериальная терапия в значительной степени изменяет микробный пейзаж у больного, что необходимо учитывать при назначении лечения (см. ниже).
4.Показаниями для замены антибактериального препарата является отсутствие эффекта от лечения (см. ниже).
5.При выделении возбудителя у больного при назначении антибиотика следует опираться на вид возбудителя, и/или результаты исследования чувствительности возбудителя к антибиотикам.
79
Табл. 1.25. Выбор стартового препарата при внебольничной пневмонии у детей (Методические рекомендации по пневмонии, 2009)
Возраст, форма |
А н т и б и о т и к и |
|
|
Стартовый |
Замена при неэф- |
|
препарат |
фективности |
1-6 мес., типич- |
Внутрь: защищенный |
Парентерально: це- |
ная (фебрильная, |
пенициллин, |
фалоспорины II-III |
с инфильтратив- |
в/в : Цефазолин или |
поколения, ванкоми- |
ной или очаговой |
оксациллин + аминогли- |
цин, карбопенемы |
тенью) |
козид в/в, в/м; |
|
1-6 мес., атипич- |
Внутрь: современный |
Внутрь: |
ная (афебрильная |
макролид * |
ко-тримоксазол |
с диффузными |
|
|
изменениями) |
|
|
6 мес. – 15 лет, |
Внутрь: амоксициллин |
Амоксициллин |
типичная, неос- |
или/и современный мак- |
/клавуланат, цефа- |
ложненная (го- |
ролид (при непереноси- |
лоспорины I-II поко- |
могенная тень) |
мости лактамов) |
ления |
6-15 лет, атипич- |
Внутрь: современный |
Доксициклин (старше |
ная, (негомоген- |
макролид |
12 лет) |
ная тень) |
|
|
6 мес. – 15 лет, |
Парентерально: пени- |
Парентерально: це- |
осложненная |
циллин, ампициллин, |
фалоспорины II-ΙΙΙ |
плевритом или |
или цефазолин. До 5 лет |
поколения |
деструкцией |
- цефуроксим, амокси- |
|
|
циллин/клавулановая |
|
|
кислота |
|
* Современные макролиды: азитромицин, кларитромицин, мидекамицин, рокситромицин, спирамицин.
Табл. 1.26. Стартовая терапия при внутрибольничной пневмо-
нии (В.К. Таточенко, 2009)
Терапия до |
Вероятный возбу- |
Рекомендуемые препараты |
пневмонии |
дитель |
|
|
|
|
80
Не проводи- |
Пневмококк, мико- |
Парентерально: ампициллин, |
лась |
плазма |
цефазолин. Внутрь: макролид. |
|
|
|
Амоксиампи- |
Стафилококк, мико- |
В/м, в/в: оксациллин, амокси- |
циллин |
плазма |
циллин/клавуланат. |
|
|
Внутрь: макролид |
|
|
|
Макролид |
Н. Influenzae , ус- |
Внутрь, в/м, в/в: амоксицил- |
|
тойчивый пневмо- |
лин/клавуланат, цефуроксим, |
|
кокк |
цефтриаксон, цефотаксим. |
Цефазолин, |
Е, coli, др. гр-отр. |
Парентерально: амоксицил- |
оксациллин, |
флора, резистентный |
лин/клавуланат, цефуроксим, |
линкомицин |
стафилококк |
цефтриаксон, цефотаксим, ами- |
|
|
ногликозид, ванкомицин, ком- |
|
|
бинации препаратов |
Аминогликозид |
Пневмококк, Не |
Парентерально: ампициллин, |
|
ферментирующая |
при отсутствии эффекта: цефа- |
|
флора. Резистент- |
лоспорины ІІІ-ІV поколения, |
|
ный стафилококк |
тикарциллин/клавуланат, ри- |
|
|
фампицин, карбопенем, ванко- |
|
|
мицин, по жизненным показа- |
|
|
ниям фторхинолоны |
Аминогликозид |
Резистентная гр-отр. |
Парентерально: цефепим, кар- |
+ цефалоспо- |
флора, резистентный |
бопенем, тикарциллин/ клаву- |
рин II-III |
стафилококк |
ланат, рифампицин, ванкоми- |
|
|
цин, по жизненным показаниям |
|
|
фторхинолоны или аминоглико- |
|
|
зиды в высоких дозах |
6. При внебольничных П стартовыми препаратами являются пенициллины т.к. основные возбудители П (пневмококк, гемофильная палочка) остаются чувствительными к ним.
7.При внутрибольничных П необходимо определение микрофлоры и чувствительности ее к антибиотикам.
8.У детей, получающих лечение в амбулаторных условиях, не следует использовать инъекционные формы антибиотиков.
9.При тяжело протекающих П антибиотики следует вводить внутривенно.
10.Пользоваться сочетаниями антибиотиков следует при неясной этиологии заболевания или при тяжелом течении П.
81
11.После получения эффекта от парентерального введения антибиотиков следует переходить на оральные их формы (ступенчатый метод лечения).
12.Необходимо соблюдать наиболее оптимальные сроки лечения П (см. ниже).
13.Антибактериальная терапия не нуждается в сопроводительном лечении антигистаминными и противогрибковыми препаратами.
14.В амбулаторных условиях для лечения П не использую гентамицин.
Чувствительность бактериальных возбудителей к антибиотикам.
В настоящее время пневмококки остаются чувствительными к пенициллину. Чувствительность их к гентамицину почти отсутствует, а к бисептолу – снижена.
Гемофильная палочка: чувствительна к амоксициллину, цефалоспоринам ΙΙ-ΙV поколений.
Стафилококк ауреус: сохранена чувствительность к оксациллину, защищенным пенициллинам, линкосамиду, макролидам, аминогликозидам.
Хламидии и микоплазмы: высокочувствительны к макролидам, тетрациклинам.
Полный эффект лечения: падение температуры тела ниже 37,5 0С через 24-48 ч при неосложненной и через 3-4 суток при осложненной П на фоне улучшения общего состояния и аппетита, уменьшения одышки. В эти сроки рентгенологические изменения не нарастают или уменьшаются.
Частичный эффект: сохранение фебрильной температуры тела после указанных выше сроков при уменьшении выраженности токсикоза, одышки, улучшении аппетита и отсутствии отрицательной рентгенологической динамики. Наблюдается обычно при деструктивных П и/или при метапневмоническом плеврите. Смена антибиотика не требуется.
Отсутствие эффекта: сохранение лихорадки при ухудшении общего состояния и/или нарастании патологических изменений в легких или плевральной полости (увеличение объема выпота или его цитоза). При хламидиозе, пневмоцистозе отмечается нарастание одышки и гипоксемии. Отсутствие эффекта требует смены антибиотика.
Длительность стартовой антибактериальной терапии.
Показанием к переходу на альтернативные препараты являются отсутствие клинического эффекта от препарата первого выбора в течение
82

36-48 часов при нетяжелой и 48-72 часов при тяжелой П, а также развитие серьезных нежелательных лекарственных реакций.
Длительность антибактериальной терапии должна быть достаточной для подавления жизнедеятельности возбудителя. При адекватном выборе антибиотика для этого достаточно 6-7 дней. Считают, что антибактериальное лечение следует продолжить еще 2-3 дня после наступления эффекта от проводимого лечения. Лучше всего поддаются лечению пневмококковые П (6-7 дней), хуже П, вызванные гемофильной палочкой (10-14 дней). Наибольший срок лечения у деструктивных П – несколько недель.
Табл. 1.27. Ступенчатая антибактериальная терапия пневмоний
у детей
Стартовый препарат |
Препараты замены |
|||
Азитромицин в/в для детей |
Сумамед per oss |
Макролиды: |
||
старше 15 лет) |
Амоксициллин кла- |
Азитромицин |
||
Амоксициллин клавуланат |
вуланат per oss |
Медикамицин |
||
в/в |
Цефуроксим per oss |
Джозамицин |
||
Цефуроксим в/в, в/м |
Цефтриаксон per oss |
|
|
|
Цефтриаксон в/в |
|
|
|
|
|
|
|
|
|
Лечение дыхательной недостаточности включает следующие ос-
новные компоненты:
1. Восстановление проходимости дыхательных путей. 2. Ингаляцию кислорода. 3. ИВЛ. 4. Улучшение дренирования мокроты. 5. Коррекцию сопутствующих нарушений.
При I степени ДН необходимость в оксигенотерапии отсутствует. Достаточно проветривания помещений, пребывания ребенка на верандах, в коридорах.
При ДН II оксигенотерапия показана. При ее проведении необходимо учитывать следующие положения: 1. Концентрация кислорода в составе кислородо-воздушной смести должна быть минимально достаточной. 2. Кислород больному ребенку должен поступать согретым и увлажненным. 3. Режимы оксигенотерапию зависят от способа доставки кислорода к пациенту, выраженности дыхательной недостаточности, наличия и характера осложнений.
Улучшение дренирования мокроты включает применение: муколитиков (Эреспал, лазолван и др.), использование механического удаления мокроты (санация верхних дыхательных путей, санация трахеи при наличии интубационной трубки).
83
Коррекция сопутствующих нарушений включает: а) ликвидацию острой сердечной недостаточности (ограничение объема жидкости, сердечные гликозиды, мочегонные, допамин с кардиотоническим эффектом), б) устранение обезвоживания организма (смотри инфузионная терапия П), в) восстановление адекватного функционирования системы микроциркуляции, улучшение реологических свойств крови и ее транспортной функции (допамин в дозе 1-3 мкг/кг/мин, никотиновая кислота по 0,5-1 мл внутривенно однократно; кавинтон по 1 мг/кг внутривенно капельно); г) воздействие на свертывающие свойства крови (применение гепарина при гиперкоагуляции в дозе 50-100 ЕД/кг /сутки внутривенно равномерно).
Гидратация при П должна проводиться осторожно и преимущественно перорально. Объем суточной жидкости у детей с П должен быть меньше, чем СЖП (суточная жидкость поддержания), но не менее 700-
1000 мл.
Показания для проведения инфузионной терапии: выраженный эк-
сикоз, коллапс, нарушения микроциркуляции, угроза развития ДВСсиндрома. Объем внутривенно вводимой жидкости не должен превышать 20-30 мл/кг/сутки. В составе инфузионных сред коллоидные растворы должны составлять 1/3 от общего объема.
Введение ингибиторов протеаз (контрикал, Трасилол, гордокс) показано только в первые три дня развития заболевания, т.к. затем они не эффективны.
Исходы. П – серьезное заболевание, исходы при которой зависят от: возраста ребенка, этиологии П, жилищных условий, наличия фоновой патологии (недоношенность, гипотрофия, анемия, заболевания нервной системы и др.). У части детей с П развиваются легочные и внелегочные осложнения. В России 50-70% всех летальных исходов при П связано с госпитальными пневмониями. Летальность от внебольничных П зависит от несвоевременной госпитализации и неадекватного лечения.
Профилактика П включает предупреждение ОРИ, гриппа, соблюдение режима туда и отдыха, рациональное питание, занятие физкультурой, систематическое проветривание помещений, достаточное пребывание на свежем воздухе.
Большое внимание должно уделяться своевременному выявлению и устранению экзогенных и эндогенных факторов риска развития П.
Важная роль должна отводиться неспецифической профилактике, повышающей устойчивость организма к неблагоприятным факторам внешней среды, в частности к переохлаждению. Этому способствует
84

закаливание и активное физическое воспитание, рациональное питание.
Для профилактики внутрибольничных П необходимо изменить подходы к госпитализации детей с ОРИ и устранить необоснованное профилактическое использование антибиотиков.
Одной из эффективных мер профилактики является вакцинация. Вакцинация против гриппа снижает не только заболеваемость гриппом, но и смертность, в первую очередь, от гриппа и П.
Применение вакцины против инфекции, вызванной Н. influenzae типа В (в Российской Федерации зарегистрирована вакцина Акт-Хиб), у детей первых месяцев жизни сокращает на 80% заболеваемость тяжёлой П данной этиологии и на 22-26% заболеваемость всеми тяжёлыми П.
Полисахаридная пневмококковая вакцина (в Российской Федерации зарегистрирована вакцина Пневмо-23) иммуногенна лишь у детей старше 2 лет; у взрослых её эффективности составляет 83% в отношении «вакцинных» серотипов, 74% - всех серотипов пневмококка, у детей - 94% в отношении инвазивных форм пневмококковой инфекции. Применение этой вакцины рекомендуют детям из группы риска тяжёлого течения пневмококковой инфекции (с врождённой аспленией или удалённой селезёнкой; с нейтропенией; с дефицитом компонентов комплемента; страдающим хронической ликвореей).
Вопросы к экзамену. Острые пневмонии. Этиология. Патогенез. Классифи-
кация. Внебольничные и внутрибольничные пневмонии. Клиническая картина. Критерии тяжести. Диагностика. Рентгенологические признаки. Течение. Показания к госпитализации больных острой пневмонией. Лечение.
Особенности антибактериальной терапии внутри- и внебольничных пневмоний. Исходы. Профилактика.
ЛЕГОЧНЫЕ ОСЛОЖНЕНИЯ ПНЕВМОНИЙ
Согласно действующей классификации пневмоний к легочным осложнениям относят: буллы, абсцесс, плевриты, пневмоторакс, пиопневмоторакс.
В тоже время для обозначения перечисленных патологических состояний на практике часто пользуются понятиями «острая бактериальная деструкция легких» (ОБДЛ), «острая деструктивная пневмония» (ОДП), и др.
Этиология (см. «Парапневмонический выпот и эмпиема»).
85

Классификация. Из множества предложенных классификаций бактериальных деструкций легких наиболее приемлема следующая:
I. Острая бактериальная деструкция.
По генезу - первичная (аэробронхогенная), вторичная (гематогенная).
По клинико-рентгенологическим формам:
деструкция с внутрилегочными осложнениями:
а) абсцессы; б) буллы;
деструкции с плевральными осложнениями:
а) пиоторакс (плащевидный, тотальный (эмпиема плевры), отграниченный;
б) пиопневмоторакс и пневмоторакс (напряженный, ненапряженный, отграниченный).
По течению - острое, затяжное, септическое.
II. Хронические формы (исходы острой деструкции):
хронический абсцесс, хроническая эмпиема плевры, приобретенные кисты плевры.
Деструктивная пневмония чаще всего проявляется буллами, пиопневмотораксами, абсцессом, пиотораксом.
Патогенез деструктивных пневмоний
Аспи-
рационное инфицирование
ОРВИ (респираторные вирусы)
1. Нарушение мукоцилиарного клиренса
2.Нарушение системы альвеолярных макрофагов
3.Нарушение системы местного иммунитета (IgA)
4. Нарушение системы гуморального иммунитета
Активация пневмококков
Активация условно-патогенной флоры
Развитие инфекционно-воспалительного про-
цесса в легких
Деструкция
(полость или полость с гноем)
Ингаля-
ционное (неаспирационное) инфицирование
Прорыв гноя в бронх |
|
|
Нефункционирующий |
|
|
|
Эпителизация |
|
||||||||
(дренирующий бронх) |
|
|
дренирующий бронх |
|
|
|
полости |
|
||||||||
|
|
|
|
|
|
|
86 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Спадение |
|
формиро- |
|
распростране- |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||||||
|
полости |
|
вание |
|
ние процесса |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
Формирование |
|
|||||||||
|
|
|
|
хрониче- |
|
на плевру |
|
|
|
|
||||||
|
|
|
|
ского |
|
|
|
|
|
|
|
кистообразной по- |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
облитерация |
|
|
|
|
|
|
|
|
лости (выздоров- |
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
абсцесса |
|
|
|
|
|
|
) |
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||||
Рис. 1.10. Схема патогенеза деструктивной пневмонии
Исследования (см. «Парапневмонический выпот и эмпиема»).
Анамнез, клиника
1.Буллы – тонкостенные воздушные полости, развивающиеся на разных этапах пневмонического процесса. Буллы выявляются исключительно рентгенологически и имеют различные размеры, форму, которая может быстро изменяться (игра буллы). В этих полостях чаще нет гноя, что обусловливает благоприятную клиническую картину. К моменту образования булл больные перестают лихорадить, улучшается аппетит, нормализуется картина периферической крови. Дыхательных нарушений, как правило, не наблюдается. В большинстве случаев буллы со временем самостоятельно исчезают.
2.Абсцесс легкого характеризуется фебрильной температурой, проявлениями дыхательной недостаточности, интоксикацией (бледность кожного покрова с мраморным рисунком, вялость, сонливость). Физикальная картина представлена снижением дыхательных экскурсий на стороне поражения, укорочением перкуторного звука в проекции пораженной доли. Поскольку при наличии абсцесса легкого бывает, как правило, выражен реактивный плеврит, то данные аускультации и перкуссии могут соответствовать картине пиоторакса (см. ниже). Диагностика абсцесса легкого в фазе инфильтрации затруднительна. В фазе сформировавшегося абсцесса - диагноз рентгенологический.
3.Пневмоторакс. В основе пневмоторакса лежит разрыв легкого
или пристеночной буллы. Выделяют скрытый и напряженный пневмотораксы. В анамнезе выявляется различная бронхолегочная патология. При напряженном пневмотораксе клиническая картина развивается внезапно и характеризуется одышкой, беспокойством, вздутием пораженной половины грудной клетки, цианозом. В некоторых случаях появляется кашель, проявления сосудистого коллапса. При объективном исследовании выявляют выраженный тимпанит и резко ослабленное дыхание на стороне поражения, отставание пораженной половины грудной клетки в акте дыхания, смещение органов средостения в здоровую сторону.
87
Скрытый пневмоторакс выявить клинически очень трудно из-за небольшого количества воздуха в плевральной полости.
4. Пиопневмоторакс представляет собой результат прорыва воздуха из легкого в плевральную полость, пораженную эмпиемой. Выделяют напряженный и скрытый вариант пиопневмоторакса.
Напряженный пиопневмоторакс клинически проявляется кардиореспираторной катастрофой. Основные симптомы: боль в грудной клетке, диспноэ, выраженная дыхательная недостаточность, цианоз, тахикардия, нитевидный пульс, снижение артериального давления, лихорадка, выраженная интоксикация. Пораженная половина грудной клетки вздута, дыхание над ней или резко ослаблено или отсутствует. Перкуторно над гноем тупой звук. Над скоплением воздуха - тимпанит. Границы сердца смещены в здоровую сторону.
Скрытый пиопневмоторакс проявляется картиной гнойного плеврита и появлением воздуха в плевральной полости (см. ниже).
Диагноз
Буллы диагностируют исключительно по результатам рентгенологического исследования (различного размера и формы воздушная тонкостенная полость).
Пневмоторакс. Напряженный пневмоторакс диагностируют на основании характерных клинических проявлений и подтверждают результатами рентгенологического исследования, при котором выявляют наличие воздуха в плевральной полости, отсутствие легочного рисунка, в различной степени коллабированное легкое, смещение органов средостения в здоровую сторону. Ограниченный пневмоторакс выявляют только по результатам рентгенологического исследования (небольшое количество воздуха в плевральной полости).
Абсцесс легкого. Данная форма легочной деструкции может иметь несколько вариантов: абсцесс, заполненный гноем (не с сообщающийся с бронхиальным деревом), абсцесс с уровнем жидкости (при дренировании полости абсцесса через бронх). При рентгенологическом исследовании выявляют полость с уровнем гноя и выраженной пиогенной оболочкой.
Пиопневмоторакс. Диагноз напряженного пиопневмоторакса устанавливается на основании описанной характерной клинической картины и подтверждается результатами рентгенологического исследования, при котором выявляют затемнение реберно-диафрагмального синуса, уровень жидкости, над которым имеется воздух. Легкое коллабировано. Средостение смещено в здоровую сторону. Диагноз скрытого (ненапряженного) пиопневмоторакса – рентгенологический.
88
В анализе крови для всех форм деструктивной пневмонии характерно снижение гемоглобина и эритроцитов, лейкоцитоз со сдвигом нейтрофильной формулы влево, высокая СОЭ.
Дифференциальный диагноз
Абсцесс легкого. Инфильтративную фазу абсцесса по рентгенограмме трудно отдифференцировать от пневмонического инфильтрата, однако округлость форм и более интенсивное затемнение в центре позволяют с большей уверенностью говорить об абсцедировании. Абсцесс с уровнем жидкости следует дифференцировать с нагноившейся врожденной кистой легкого.
Пневмоторакс дифференцируют с большими воздушными полостями (буллами), лобарной эмфиземой, диафрагмальной грыжей.
Пиопневмоторакс необходимо дифференцировать с пневмотораксом.
Буллы дифференцируют с врожденными и приобретенными кистами, ограниченным пневмотораксом, кистозной гипоплазией легкого.
Лечение, задачи лечения: декомпрессия (при напряжении в плевральной полости), купирование воспалительных изменений в плевре и легких; эрадикация возбудителя.
Схема лечения. Обязательное лечение: антибактериальная терапия, борьба с интоксикацией, лечение дыхательной недостаточности, обеспечение эффективного бронхиального дренажа (муколитики, дренирующее положение, вибромассаж), дренирование плевральной полости в режиме активной аспирации (при напряжении в плевральной полости).
Вспомогательное лечение: хирургическое лечение, диетотерапия, режим, санационная бронхоскопия, иммунозаместительная терапия, энзимотерапия, витаминотерапия.
Показания для госпитализации: все дети с осложнениями пневмо-
нии подлежат госпитализации.
Особенности терапии см. в разделе «Парапневмонический выпот и эмпиема».
Парапневмонический выпот и эмпиема. Парапневмониче-
ским (синпневмоническим) плевритом называют плеврит, который возник одновременно с пневмонией. Метапневмоническим плевритом называют плеврит, который развился на фоне обратного развития пневмонии. В развитии метапневмонического плеврита принимают участие иммунопатологические процессы.
Эмпиема – гнойное воспаление плевры.
89
Эпидемиология. Парапневмонический выпот и эмпиема встречаются с частотой 3,3 на 100 000 детей. Парапневмонический выпот и эмпиема более часто встречаются у мальчиков, чем у девочек, более часто поражаются новорожденные и дети раннего возраста. Более часто заболевание возникает зимой и весной, что, вероятно, связано с его инфекционной природой.
Предрасполагающие факторы: иммунодефициты, аспирация, состояние после хирургического вмешательства и травмы.
У здорового ребенка плевральный выпот обычно возникает вторично по отношению к острой бактериальной пневмонии и реже в результате хронических инфекций, таких как легочный туберкулез.
Этиология. Установлено, что эмпиема вызывается вируснобактериальными ассоциациями, вирусным компонентом которых наиболее часто являются вирусы гриппа, парагриппа и аденовирусы.
Из бактерий, чаще выделяют золотистый стафилококк, пневмо-
кокк, Haemophilus influenzae, пиогенный стрептококк и Klebsiella
рnеumоniae. У трети детей эмпиема вызывается анаэробами, в том числе бактероидами, анаэробными палочками и Fusobacterium. Частота выделения возбудителей в плевральном выпоте составляет около 17%. Даже при использовании новейших молекулярных методов, этиологический фактор обнаруживается только в 75% случаев.
Патогенез. Инфекция, поражает примыкающее легкое или сосудистую ткань и активирует иммунную защиту и воспаление плевры. Возрастающая проницаемость сосудов позволяет клеткам, участвующим в воспалительном процессе (нейтрофилы, лимфоциты и эозинофилы), мигрировать в плевральную полость. В процессе принимает участие ряд цитокинов, таких как интерлейкин-1 (ИЛ1), ИЛ-6, ИЛ-8, ФНО-α, ФАТ (фактор активации тромбоцитов), вырабатываемых мезотелием, ограничивающим плевральную полость. Результатом является экссудативная стадия плеврального выпота. В полости плевры накапливается прозрачная жидкость с малым количеством лейкоцитов (простой парапневмонический выпот).
Вторая стадия плеврита фибринозно-гнойная. В плевральной полости начинается отложение фибрина, что ведет к развитию перегородок и ограниченных полостей. Повышается количество лейкоцитов, жидкость сгущается (осложненный парапневмонический выпот), что в конечном итоге приводит к образованию гноя (эмпиема).
Третья стадия – организация - фибробласты инфильтрируют плевральную полость, тонкая внутриплевральная мембрана реорганизуется в толстую и неэластичную. Эти плотные плевральные мембраны могут привести к неподвижности легкого, нарушению его функции, а также
90
к появлению постоянной полости, потенциально открытой для инфекции. В этом случае может произойти спонтанное заживление, либо развитие хронической эмпиемы.
Исследования. См. «Пневмония». Начальное обследование при подозрении на выпот в полость плевры включает: рентгенограмму органов грудной клетки, УЗИ органов грудной клетки, бактериологическое исследование крови (включая анаэробную флору), посев мокроты (при возможности), АСЛО, развернутый анализ крови с подсчетом эритроцитов, лейкоцитов и лейкоформулой, электролиты крови, общий белок сыворотки крови, С-реактивный белок (по показаниям).
Анамнез, клинка. Существуют два варианта начала заболевания. Первый вариант: у ребенка присутствуют классические симптомы пневмонии. При появлении плеврального выпота эти симптомы усиливаются. Может возникать боль в груди, ребенок принимает вынужденное положение на пораженной стороне.
У ребенка с парапневмоническим выпотом или эмпиемой обычно выявляют типичную картину пневмонии (кашель, локальные аускультативные и перкуторные изменения, недомогание, потеря аппетита), хотя возможно и более тяжелое состояние, чем обычно, иногда появляется плевральная боль в груди. Воспаление в нижних долях легких может сопровождаться болью в животе. Характерны лихорадка, выраженная интоксикация, признаки дыхательной недостаточности.
При объективном осмотре плевральный выпот диагностируется по одностороннему тупому звуку при перкуссии, ослаблению (отсутствию) дыхания и сколиозу. Также может появиться цианоз из-за нарушения вентиляционно-перфузионного соотношения. Выпот часто виден на рентгенограмме органов грудной клетки.
Второй вариант возможен у детей, которым поставлен диагноз пневмония, но они не получали обычного в этом случае лечения. Если ребенок продолжает температурить или его состояние не улучшается в течение 48 часов после начала лечения пневмонии, необходима переоценка состояния с учетом возможного развития осложнений. К моменту выздоровления при исследовании больного обязательно выявляется ослабление дыхания и притупление перкуторного звука над пораженной областью, это происходит из-за утолщения плевры и не должно становиться причиной для беспокойства.
Диагноз. У детей, которым уже поставлен диагноз «пневмония» выраженная лихорадка и отсутствие положительной динамики в течение 48 часов после начала антибиотикотерапии может быть сигналом возможности выпота в плевральную полость.
Лабораторные исследования
91
При рентгенологическом исследовании выявляется затемнение ре-
берно-диафрагмального угла – это ранний признак появления плеврального выпота, уровень жидкости может быть восходящим к латеральной стенке грудной клетки в переднее-задней проекции. Если снимок выполняется в положении лежа на спине (у маленьких детей), жидкость представлена как гомогенное затемнение целого легкого. Только по результатам рентгенографии невозможно дифференцировать эмпиему и плевральный выпот. Рентгенологическая картина приходит в норму к 3-6 месяцам.
УЗИ также может выявить присутствие жидкости в плевральной полости. Хотя УЗИ и не может подтвердить наличие инфекции, тем не менее, позволяет оценить размеры выпота, дифференцировать свободную и осумкованную жидкость (оценивается ее эхогенность). Также при помощи ультразвука выявляются истончения плевры, дифференцируются вторичные и туберкулезные выпоты (например, присутствие небольших узелков на поверхности плевры). В некоторых сложных случаях показано КТ.
Общий анализ крови не позволяет выявить различия у детей с бактериальной и вирусной этиологией заболевания. Наиболее часто выявляют лейкоцитоз, сдвиг формулы крови влево, увеличение СОЭ.
Исследование плевральной жидкости. Необходимо произвести по-
сев плевральной жидкости, и цитологическое ее исследование. Если в жидкости присутствуют лимфоциты, необходимо исключить туберкулез и злокачественные новообразования. Парапневмонический плевральный выпот сопровождается появлением полиморфноядерных лейкоцитов. Преобладание лимфоцитов должно настораживать в отношении туберкулеза или злокачественных новообразований.
Лечение, задачи лечения: купирование воспалительных изменений в плевре и легких; эрадикация возбудителя; эвакуация содержимого из плевральной полости.
Схема лечения. Обязательное лечение: лечебно-диагностическая плевральная пункция, антибактериальная терапия, инфузионная терапия, антипиретики.
Вспомогательное лечение: режим, диета, иммунокорригирующая терапия, противовоспалительная терапия, оксигенотерапия, интраплевральная фибринолитическая терапия.
Показания для госпитализации. Все дети с подозрениями на забо-
левания плевры должны быть госпитализированы.
Начальные мероприятия.
Внутривенное введение жидкости показано в тех случаях, если ребенок находится в состоянии дегидратации или не может или не хочет
92
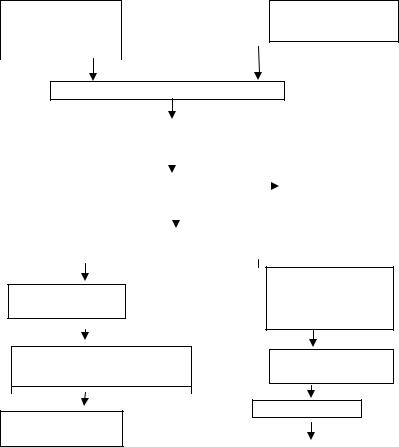
пить. Основой дезинтоксикационной терапии является управляемая инфузионная гемоделюция. Главные компоненты инфузионной терапии: коллоиды (инфукол, реамберин), кристаллоиды (10-15мл/кг массы тела), растворы глюкозы.
Антибиотикотерапия. Стартовая терапия назначается эмпирически. Во всех случаях антибиотики должны вводиться внутривенно. У детей с ослабленным иммунитетом назначают препараты с широким спектром действия. Внутривенное введение антибиотиков продолжается до понижения температуры тела ребенка или до удаления дренажа. Затем назначаются препараты для орального применения, такие как ко-амоксиклав (60-90 мг/кг сут в 3 приёма в/в или внутрь) на период 1-4 недели или дольше, если остаются проявления заболевания.
На фоне полного благополучия. Клинически подозревается парапневмонический выпот.
Пневмония. Неудачное лечение в течение 48 часов.
Рентгенография органов грудной клетки
|
Выпот в плевраль- |
|
|
|
|
|||
|
|
ную полость? |
|
|
|
|
||
|
|
|
|
|
Плевральная |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пункция, ис- |
|
|
|
|
|
|
|
|
|
|
|
Консультация |
|
|
|
следование |
||
|
|
детского хирурга |
|
|
|
плеврального |
||
|
|
|
|
|
|
|
|
содержимого |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Массивная антибактериальная терапия |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
Дренирование плевральной полости
Повышенная эхогенность или осумкованная жидкость на УЗИ. Густой гной.
Фибринолитическая
терапия
93
 Хирургическое лечение, активное дренирование плевральной полости
Хирургическое лечение, активное дренирование плевральной полости
Положительная динамика
Удалить дренаж
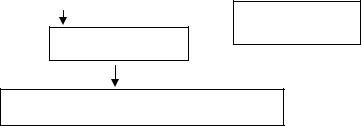
Отрицательная динамика
Переход на ступенчатую терапию, выписка
Повторный осмотр детского хирурга, позднее хирургическое вмешательство
Рис. 1.11. Алгоритм диагностики и лечения плевральной ин-
фекции у детей
Дифференциальный диагноз
Табл. 1.28. Дифференциальный диагноз плевритов
Признак |
Сухой |
Серозный |
Гнойный |
Пиопневмо- |
|
плеврит |
плеврит |
плеврит |
торакс на- |
|
|
|
|
пряженный |
Боли в |
Резко |
Слабая, уме- |
Слабая, уме- |
Слабая, уме- |
грудной |
выражена |
ренная |
ренная |
ренная |
клетке |
|
|
|
|
Лихо- |
Зависит |
37,5-38,5 0С |
39-40,5 0С |
39-40,5 0С |
радка |
от при- |
|
|
|
|
чины |
|
|
|
|
заболе- |
|
|
|
|
вания |
|
|
|
Состоя- |
Зависит |
Средней, тя- |
Тяжелое |
Тяжелое или |
ние |
от основ- |
жести или |
|
очень тяжелое |
больного |
ного за- |
тяжелое – за- |
|
|
|
болева- |
висит от коли- |
|
|
|
ния |
чества выпота, |
|
|
|
|
этиологии |
|
|
Одышка |
Легкая |
Степень ДН зависит от количест- |
Респираторная |
|
|
|
ва плеврального выпота |
катастрофа |
|
Смеще- |
Нет |
В здоровую сторону, степень смещения зависит от |
||
ние сре- |
|
количества выпота воздуха (при пиопневмотораксе) |
||
достения |
|
|
|
|
Перкус- |
Легкое |
От легкого |
От легкого |
От легкого |
сия |
укороче- |
укорочения до |
укорочения до |
укорочения до |
|
ние звука |
тупости |
тупости |
тупости. Тим- |
|
|
|
|
панит над воз- |
94
|
|
|
|
духом |
Аускуль- |
Шум |
Резкое ослаб- |
Резкое ослаб- |
Резкое ослаб- |
тация |
трения |
ление или от- |
ление или от- |
ление или от- |
|
плевры, |
сутствие ды- |
сутствие ды- |
сутствие ды- |
|
ослабле- |
хания, иногда |
хания, иногда |
хания, иногда |
|
ние ды- |
шум трения |
шум трения |
шум трения |
|
хания |
плевры |
плевры |
плевры |
Гемо- |
Измене- |
Умеренные |
Выраженные воспалительные |
|
грамма |
ния зави- |
изменения |
изменения в крови, свойственные |
|
|
сят от |
(лейкоцитоз, |
пиемическим очагам |
|
|
этиоло- |
сдвиг формулы |
|
|
|
гии и |
влево, ускоре- |
|
|
|
характера |
ние СОЭ) |
|
|
|
сопутст- |
|
|
|
|
вующей |
|
|
|
|
пневмо- |
|
|
|
|
нии и |
|
|
|
|
ОРВИ |
|
|
|
Рентге- |
Утолще- |
Затемнение |
Затемнение |
Затемнение |
нография |
ние плев- |
реберно- |
реберно- |
реберно- |
|
ры |
диафрагмаль- |
диафрагмаль- |
диафрагмаль- |
|
|
ного синуса, |
ного синуса, |
ного синуса, |
|
|
выявление |
выявление |
выявление |
|
|
жидкости в |
жидкости в |
жидкости в |
|
|
латеропози- |
латеропози- |
латеропози- |
|
|
ции, смещение |
ции, смещение |
ции, смещение |
|
|
средостения в |
средостения в |
средостения в |
|
|
здоровую сто- |
здоровую сто- |
здоровую сто- |
|
|
рону |
рону |
рону, уровень |
|
|
|
|
жидкости над |
|
|
|
|
гноем, колла- |
|
|
|
|
бирование |
|
|
|
|
легкого |
Микро- |
Выпот |
Лимфоциты, |
Нейтрофилы |
Нейтрофилы |
скопия |
отсутст- |
полинуклеары |
|
|
выпота |
вует |
|
|
|
Цвет |
Нет |
Светло- |
Сливкообразный, мутный, ино- |
|
|
|
желтый, про- |
гда с хлопьями или геморрагиче- |
|
|
|
зрачный |
ским компонентом |
|
Цитоз |
Отсутст- |
Менее 3000 в 1 |
Более 5000 в 1 мкл, нейтрофилы |
|
|
вует |
мкл, лимфоци- |
|
|
|
|
ты, полинук- |
|
|
|
|
леары |
|
|
Белок |
- |
Ниже 30 г/л |
Выше 30 г/л |
|
95
Доза антибиотиков не должна быть чрезмерной во избежание пенетрации плевры. При плеврите на фоне внебольничной пневмонии назначают: Цефуроксим, Ко-амоксиклав, Пенициллин, Амоксициллин, Клиндамицин. При аллергических реакциях на пенициллин назначается клиндамицин.
Установлено, что анальгетики (анальгин 50% 0,1 мл на год жизни) и антипиретики (ибуклин 20-40 мг/кг/сут в несколько приемов) способствуют более быстрому купированию проявлений плеврита.
Иммунокорригирующая терапия. Показания для назначения: дети младшего возраста, тяжелое течение заболевания, выраженные клини- ко-лабораторные проявления иммунологической вторичной недостаточности. Назначают: иммуноглобулины для внутривенного введения, переливание гипериммунной антистафилококковой или иной плазмы (10 мл/кг массы тела).
Интраплевральная фибринолитическая терапия сокращает срок госпитализации и рекомендована для использования при осложненных плевральных выпотах (густая жидкость или ее осумкование) или эмпиеме. Фибринолитики могут лизировать фибриновые перемычки при осумкованных эмпиемах и открывать лимфатические поры. С этой целью за рубежом применяется Урокиназа.
Физиотерапия при данной патологии положительного эффекта не дает.
С противовоспалительной целью показан Вобэмзим (1 таблетка на
6 кг массы тела/сут за 30 минут до еды 1 месяц), а при лихорадке ж а- ропонижающие средства.
Особенности лечения метапневмонического плеврита. При при-
знаках прогрессирования пневмонии следует заменить антибактериальную терапию. Показано назначение ибупрофена или индометацина, применение которых сокращает лихорадочный период. При отсутствии признаков деструкции возможно использование глюкокортикоидов.
Лечение больного проводится совместно с детским хирургом. Хирургическое лечение показано в том случае если эмпиема находиться в стадии организации, и если ее симптомы достоверны. Если у пациента имеется обширный выпот или ребенок находится в неудовлетворительном состоянии (респираторный дистресс-синдром и недостаточная оксигенация), рекомендуется немедленно перевести ребенка для дальнейшего лечения в хирургическое (реанимационное) отделение.
Консервативное лечение плевральной инфекции состоит из антибиотикотерапии изолированно или в комбинации с простым дренированием. Многие небольшие парапневмонические выпоты поддаются
96

антибиотикотерапии без необходимости дальнейшего вмешательства. Выпот, сдавливающий легкое и нарушающий его функцию у температурящего ребенка требует проведения дренирования или рассмотрения возможности раннего хирургического вмешательства. Для контроля за постановкой дренажа или проведением торакоцентеза используется УЗИ. Дренаж перекрывают, если извлечено жидкости более 10 мл/кг. Окончательной ясности в вопросе о целесообразном объеме эвакуируемой жидкость нет. У взрослых считают, что дренаж должен быть перекрыт на 1 час, если извлечено 10 мл/кг жидкости. У взрослых, также как и у старших детей и подростков, не следует эвакуировать более 1,5 литров жидкости одномоментно, или скорость дренирования не должна превышать 500 мл/час.
Исходы. Прогноз для детей, перенесших эмпиему, обычно благоприятный. Проведенные исследования показали, что, несмотря на различия в подходах к лечению, большинство детей полностью выздоравливают, и функция легких у них приходит в норму.
Вопросы к экзамену. Легочные осложнения пневмоний. Особенности развития, клинической картины, рентгенологических изменений при легочной деструкции. Диагноз. Дифференциальный диагноз. Особенности лечения легочных деструкций. Исходы.
ИНФЕКЦИОННЫЙ ТОКСИКОЗ (ИТ) – особый синдром,
развивающийся в результате инфекционного процесса и характеризующийся фазовыми изменениями ЦНС, нарушениями периферического кровообращения, органными, электролитными и метаболическими сдвигами.
Нейротоксикоз – особая реакция организма на инфекционное заболевание. Ведущие проявления нейротоксикоза – неврологические расстройства и нарушения периферического кровообращения. Отсутствуют выраженные признаки обезвоживания.
Факторы риска развития ИТ: недоношенные дети, наличие в анамнезе судорог и других перинатальных поражений нервной системы, искусственное вскармливание, перенесенное за несколько недель до данного заболевания ОРИ, ранний возраст.
97

Этиология. Наиболее часто ИТ развивается при гриппе, аденовирусной инфекции, парагриппе. Реже – при пневмонии, сепсисе, менингите, энцефалите.
Патогенез
Воздействие вирусов, токсинов бактерий
Активация гипоталамо-гипофизарно-надпочечниковой системы
Гиперсимпатикотония
Спазм периферических сосудов, централизация кровообращения
К
О
М
П
Е
Н
С
А
Ц
И
Я
Нарушения в микро- |
|
Нарушение кровообращения в мозге и |
циркуляторном русле |
|
внутренних органах |
Парез сосудов, децентрализация кровообращения
Интерстициаль- |
|
|
|
|
|
|
|
Отек |
|
Сердечно- |
|
ДВС- |
|
ные отеки |
|
|
|
|||
|
|
|
сосудистая |
|
синдром |
|
|
мозга |
|
|
|||
|
|
|
|
|||
|
|
|
|
недостаточ- |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
ность |
|
|
|
|
|
|
|
|
|
Циркуляторная гипоксемия, повреждение клеточных мембран
Отек- |
|
III стадия |
|
|
|
|
Нарушение функции жиз- |
||
набухание |
|
ДВС- |
|
ненно важных органов (поч- |
мозга |
|
синдрома |
|
ки, легкие, печень и др.), |
|
|
|
||
|
|
|
|
декомпенсированный ацидоз |
|
|
|
||
|
|
|
|
|
Рис. 1.12. Схема патогенеза инфекционного токсикоза
С
У
Б
К
О
М
П
Е
Н
С
А
Ц
и
я
Д
Е
К
О
М
П
Е
Н
С
А
Ц
И
Я
98
Классификация. Выделяют три степени тяжести токсикоза (табл.
1.29).
Табл.1.29. Степени тяжести токсикоза
Степень тяжести |
Нарушение пери- |
Степень тяжести по- |
токсикоза |
ферического кро- |
ражения нервной сис- |
|
вообращения |
темы |
Ι степень тяжести |
Компенсированное |
Прекома |
ΙΙ степень тяже- |
Субкомпенсирован- |
Среднемозговая кома |
сти |
ное |
|
ΙΙΙ степень тяже- |
Декомпенсирован- |
Кома стволовая, тер- |
сти |
ное |
минальная |
Исследования. Общий анализ крови и мочи, электролиты крови, показатели КОС, коагулограмма, ЭКГ, ЭхоКГ, исследования, направленные на выявление патологии почек, печени, надпочечников, и др.
Анамнез, клиника. Развитию ИТ всегда предшествует какое либо инфекционное заболевание. Клиника ИТ складывается из нескольких синдромов (см. рис. 1.13).
99
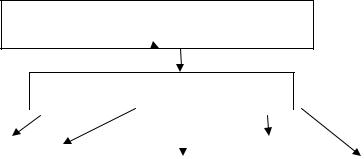
Клиника заболевания, при котором развился
токсикоз
Инфекционный токсикоз
|
|
|
|
|
|
|
|
|
|
|
|
Невро- |
|
|
|
|
|
|
Клиника |
|
|
|
|
|
|
|
|
|
|
|
|
||||
Наруше- |
|
|
|
|
|
|
|||||
логиче- |
|
|
Клиника |
|
синдро- |
|
|
Клини- |
|||
ские |
|
ния мик- |
|
пораже- |
|
мов ин- |
|
|
|||
|
|
|
|
|
ка на- |
||||||
|
роцирку- |
|
|
|
|
||||||
рас- |
|
|
ния орга- |
|
фекци- |
|
|
руше- |
|||
|
ляторно- |
|
|
|
|
||||||
строй- |
|
|
нов ми- |
|
онного |
|
|
ния |
|||
|
го русла |
|
|
|
|
||||||
ства |
|
|
шеней, |
|
токси- |
|
|
элек- |
|||
|
|
|
|
|
клиника |
|
коза: |
|
|
тролит- |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
полиор- |
|
гипер- |
|
|
ного |
|
|
|
|
|
||||||||
|
|
|
|
|
ганной |
|
терми- |
|
|
балан- |
|
|
|
|
|
|
недоста- |
|
ческий, |
|
|
са, КОС |
|
|
|
|
|
|
точности |
|
судо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
рожный |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис 1.13. Клинические проявления при инфекционном токси-
козе
В зависимости от ведущего синдрома выделяют различные варианты ИТ: инфекционно-токсический шок, синдром Рейе, гемолитикоуремический синдром, синдром Уотерхауза-Фридериксена, гипертермический синдром.
Табл.1.30. |
Классификация нарушений периферического крово- |
||
обращения (Папаян А.В. с соавт., 1979) |
|
||
|
|
|
|
Показате- |
Компенси- |
Субкомпенси- |
Декомпенсирован- |
ли |
рованная |
рованная |
ная |
|
(Ι степень) |
(ΙΙ степень) |
(ΙΙΙ степень) |
Пульс |
Умеренное |
Учащение до |
Тахикардия (свыше |
|
учащение до |
180-220 в 1мин |
220 в 1 мин) сменя- |
|
150-180 в 1 |
|
ется брадикардией и |
|
мин |
|
брадиаритмией. |
100

|
|
|
Определяется на |
|
|
|
|
крупных артериях. |
|
Дыхание |
Ум. учаще- |
Гипервентиля- |
Тахипноэ сменяется |
|
|
ние до 60-70 |
ция (80 и чаще в |
брадипноэ |
|
|
в мин |
1 мин) |
|
|
Темпера- |
38-39,5оС |
Гипертермия |
Гипертермия. В |
|
тура |
|
40оС и выше |
период терми- |
|
|
Не нарушено |
Уменьшение |
нальной комы ги- |
|
Соотношение |
потермия |
|||
ректальной и |
|
разницы |
Уменьшение раз- |
|
кожной тем- |
|
|
ницы до 0,5оС |
|
пературы |
Нормальной |
Бледная, мра- |
||
Кожа |
Мраморность кожи |
|||
|
окраски или |
морность кожи |
||
|
гиперемиро- |
на конечностях |
на конечностях и |
|
|
вана |
|
туловище, геморра- |
|
|
|
|
гическая сыпь, ги- |
|
Симптом |
Отрицатель- |
Положительный |
постазы |
|
«белого |
ный или сла- |
|
Резко положитель- |
|
пятна» |
бо положи- |
|
ный или двухфаз- |
|
|
тельный |
Снижение до 2-3 |
ный |
|
Диурез |
Олигурия со |
Анурия |
||
|
снижением |
мл/ч |
||
|
почасового |
|
|
|
|
диуреза до 5- |
|
|
|
Артери- |
10 мл/ч |
|
|
|
Повышено за |
Гипертензия с |
|
||
альное |
счет систо- |
Гипертензия сме- |
||
давление |
лического |
повышением |
||
|
|
диастолического |
няется гипотензией |
|
|
|
давления |
|
|
Метабо- |
ВЕ = 7 |
ВЕ = -10 |
рН = 7,20-7,00 |
|
лический |
ммоль/л |
ммоль/л и более. |
||
ацидоз |
|
Снижение рН до |
|
|
|
|
7,25-7,20 |
|
|
Гематок- |
Повышен на |
Повышен более |
Информативность |
|
рит |
0,05-0,07 л/л |
чем на 0,07 л/л |
||
снижается в связи с |
||||
|
|
|
||
|
|
|
присоединяющейся |
|
ЭКГ и |
Удлинение |
Удлинение Q- |
анемией |
|
Брадиаритмия. При- |
||||
ФКГ |
Q-T |
Т; укорочение Т- |
||
|
Р, зубец Т сли- |
знаки прекращения |
||
|
|
сердечной деятель- |
||
|
|
вается с Р |
||
|
|
|
101

ДВСсиндром
Эффект от оксигенотерапии
|
|
ности. Смещение S- |
|
|
Т ниже изолинии, |
|
|
отрицательный Т в |
|
|
левых грудных от- |
Гиперкоагу- |
Гиперкоагуля- |
ведениях |
ция, ΙΙ фаза |
Гипокоагуляция, ΙΙΙ |
|
ляция, Ι фаза |
тромбогеморра- |
фаза тромбоге- |
тромбоге- |
гического син- |
моррагического |
моррагиче- |
дрома |
синдрома |
ского син- |
Отсутствует |
|
дрома |
|
Отсутствует |
Благоприят- |
|
|
ный |
|
|
Табл. 1.31. Классификация неврологических расстройств при токсикозах (по Папаяну. АВ. и Цыбулькину Э.К., 1979)
Неврологические |
Сознание |
Мышечный тонус, |
расстройства |
|
двигательная актив- |
|
|
ность |
Прекома: |
|
|
ирритативная |
Сохранено, воз- |
Не изменен, беспо- |
фаза |
буждение |
койство, гиперкинезы |
сопорозная фаза |
Сохранено, за- |
Закономерных изме- |
|
торможено |
нений нет, двигатель- |
|
|
ная заторможенность |
Среднемозговая |
Отсутствует |
Повышен, двигатель- |
(мезэнцефалоди- |
|
ный автоматизм |
энцефальная) ко- |
|
|
ма |
|
|
Стволовая, (бульОтсутствует |
Снижен, двигательная |
|
барная) кома |
|
активность отсутствует |
Терминальная |
Отсутствует |
Снижен, двигательная |
кома |
|
активность отсутствует |
Судороги |
Сухожильные реф- |
Вегетативная нерв- |
|
лексы |
ная система |
Отсутствуют |
Повышены |
Признаки повышен- |
|
|
ной активности симпа- |
|
|
тической части вегета- |
102
|
|
|
тивной нервной систе- |
|
||
|
|
|
мы с расстройствами |
|
||
Отсутствуют |
|
Повышены |
периферического кро- |
|
||
Типичны |
|
Гиперрефлексия |
вотока Ι-ΙΙ степени |
|
||
Редки, чаще свя- |
Гипорефлексия |
Резкое повышение то- |
|
|||
заны с клиниче- |
|
нуса симпатической |
|
|||
скими признака- |
|
части вегетативной |
|
|||
ми гипоксии |
|
|
нервной системы с рас- |
|
||
|
|
|
стройствами перифери- |
|
||
|
|
|
ческого кровотока ΙΙ-ΙΙΙ |
|
||
Отсутствуют |
|
Арефлексия |
степени |
|
|
|
|
Признаки угнетения |
|
||||
|
|
|
обеих частей вегета- |
|
||
|
|
|
тивной нервной систе- |
|
||
|
|
|
мы, сосудистый кол- |
|
||
|
|
|
лапс |
|
|
|
|
|
|
Признаки угнетения |
|
||
|
|
|
кровообращения и ды- |
|
||
|
|
|
хания |
|
|
|
Табл. 1.32. |
Модифицированная шкала Глазго для детей млад- |
|||||
шего возраста |
|
|
|
|
|
|
|
|
|
|
|
||
Признак |
Характер ответа |
|
Оценка в |
|||
|
|
|
|
баллах |
|
|
Открывание |
Спонтанное |
|
4 |
|
|
|
глаз |
На речь |
|
3 |
|
|
|
|
На боль |
|
2 |
|
|
|
|
Нет ответа |
|
1 |
|
|
|
Вербальный |
Гуление |
|
5 |
|
|
|
ответ |
Раздраженный крик |
|
4 |
|
|
|
|
Крик на боль |
|
3 |
|
|
|
|
Стоны на боль |
|
2 |
|
|
|
|
Нет ответа |
|
1 |
|
|
|
Двигательная |
Нормальные спонтанные движения |
6 |
|
|
||
реакция |
Отдергивание на прикосновение |
5 |
|
|
||
|
Отдергивание на боль |
|
4 |
|
|
|
|
Ненормальное сгибание |
|
3 |
|
|
|
103
|
Ненормальное разгибание |
2 |
|
Нет ответа |
1 |
Диагноз ИТ основывается выявлении основных проявлений этого синдрома: неврологических нарушений и расстройств микроциркуляции.
Лабораторные исследования при ИТ необходимы для выявления органных поражений и определения их функционального состояния.
Дифференциальный диагноз ИТ проводят с нейроинфециями, энцефалитическими реакциями, сепсисом, течением инфекционных заболеваний.
Таб. 1.33. Дифференциальный диагноз инфекционного токсикоза
(Баранов А.А., соавт, 1997)
Клиниче- |
Инфекционный |
Энцефалитиче- |
Энцефалит |
ский при- |
токсикоз |
ская реакция |
|
знак |
|
|
|
Сознание |
От сопора до |
Вне судорог – |
От ясного до |
|
комы (при раз- |
ясное или со- |
комы |
|
ной степени ток- |
мнолентность |
|
|
сикоза) |
|
|
Температура |
Фебрильная |
От субфебриль- |
От нормальной |
|
|
ной до фебриль- |
до фебрильной |
|
|
ной |
|
Судороги |
Характерны для |
Генерализован- |
Чаще очаговые |
|
Ι-ΙΙ степени ток- |
ные, чаще кло- |
|
|
сикоза |
нико-тонические |
|
Делирий |
Не характерен |
Кратковремен- |
Отсутствует |
|
|
ный |
|
Аритмия |
При токсикозе |
Отсутствуют |
Выражены при |
дыхания |
ΙΙΙ степени |
|
поражении |
|
|
|
ствола |
Нарушение |
При токсикозе |
Отсутствуют |
Четкие |
гемодинами- |
ΙΙΙ степени |
|
|
ки |
|
|
|
Внутриче- |
При токсикозе |
Нормальное или |
Нормальное |
репное дав- |
ΙΙ-ΙΙΙ степени |
несколько по- |
или несколько |
ление |
|
вышено |
повышено |
Патологиче- |
Двусторонние, |
Двусторонние, |
Чаще односто- |
104
ские рефлек- |
несколько дней |
кратковремен- |
ронние, стой- |
сы |
|
ные |
кие |
Очаговая |
Отсутствует |
Отсутствует |
Четко выраже- |
симптомати- |
|
|
на |
ки |
|
|
|
Содержание |
Чаще повышено |
Чаще повышено |
Нормальное |
белка в |
(при токсикозе |
|
или повышен- |
СМЖ |
ΙΙ-ΙΙΙ степени) |
|
ное |
Цитоз СМЖ |
Отсутствует |
Отсутствует |
При менинго- |
|
|
|
энцефалите |
Течение |
Несколько дней |
Несколько дней |
Длительное |
Остаточные |
При перенесен- |
Отсутствуют |
Часто очаго- |
явления |
ной тяжелой |
|
вый невроло- |
|
гипоксии |
|
гический де- |
|
|
|
фект |
Сочетание |
Обязательный |
Только невроло- |
Преимущест- |
неврологи- |
признак |
гические нару- |
венно невроло- |
ческих на- |
|
шения |
гическое на- |
рушений с |
|
|
рушения |
нарушения- |
|
|
|
ми сознания |
|
|
|
Лечение, задачи лечения: лечение основного заболевания, нормализация нарушений периферического кровообращения, устранение гиперсимпатикотонии, устранение гипоксии, купирование неврологических нарушений, лечение синдромов ИТ, лечение полиорганной недостаточности.
Схема лечения: Обязательное лечение: ликвидация гиперсимпатикотонии, нормализация микроциркуляции и гемодинамики, купирование проявлений полиорганной недостаточности, коррекция КОС и электролитных нарушений, терапия заболевания, вызвавшего развитие ИТ.
Вспомогательное лечение: диета, элиминация токсинов, профилактика ДВС-синдрома, поддержание энергетического обеспечения метаболизма, лечение синдромов ИТ.
Диета при ИТ проводится по принципам, изложенным в разделе «Пневмония».
Показания для госпитализации: все дети с ИТ должны быть госпи-
тализированы.
ИТ Ι степени
105
Интенсивный этап лечения решает следующие задачи: проведение нейровегетативной блокады, поддержание энергетического обеспечения метаболизма, нормализация микроциркуляции и гемодинамики, элиминация токсинов.
1.Нейровегетативная блокада: пипольфен 2,5% раствор по 0,15 мл/кг массы тела внутримышечно или внутривенно каждые 6-8 часов.
2.Коррекция гемоциркуляторных нарушений.
а) воздействие на сосудистый тонус: папаверин 2% раствор по 1-2 мг/год жизни внутримышечно или внутривенно. В последующем вводят эуфиллин 2,4% раствор по 6 мг/кг массы тела внутривенно каждые 6 часов на растворе глюкозе.
б) воздействие на сосудистую проницаемость и стабилизация клеточных мембран: аскорбиновая кислота 5% раствор по 1 мл внутривенно однократно.
3.Улучшение реологических свойств крови: трентал по 10 мг/кг массы тела внутривенно.
4.Коррекция водно-электролитных нарушений. Суточное количество жидкости при ИТ Ι степени назначается в объеме СЖП (суточной жидкости потребления). Основной путь введения жидкости – оральный. В качестве растворов для орального введения используют: Оралит, регидрон, цитроглюкосалан.
5.Коррекция дыхательной недостаточности.
6.Нормализация метаболизма в нейронах головного мозга: пирацетам 20% раствор по 50-100 мг/кг массы тела внутривенно в растворе глюкозы 3-4 раза в сутки.
7.Элиминация эндо- и экзотоксинов: смекта, полифепан.
8.Лечение синдромов, характерных для ИТ Ι степени:
а) гипертермический синдром: парацетамол по 10-15 мг/кг на прием; физическое охлаждение. При отсутствии эффекта от антипиретиков применяют литические смеси, включающие димедрол, пипольфен, папаверин, анальгин.
б) судорожный синдром: 0,5% раствор седуксена в разовой дозе 0,3-0,5 мг/кг (но не более 10 мг на одно введение); 20% раствор оксибутирата натрия по 50-100 мг/кг; 25% раствор магния сульфата по 0,2 мл/кг внутримышечно. При отсутствии эффекта назначают гексенал 5% раствор по 3-5 мг/кг внутримышечно.
9. Лечение заболевания, при котором развился синдром ИТ.
Инфекционный токсикоз ΙΙ степени
Интенсивный этап лечения решает следующие задача: проведение нейровегетативной блокады, поддержание энергетического обеспече-
106
ния метаболизма, нормализация микроциркуляции и гемодинамики, элиминация токсинов.
1.Нейровегетативная блокада – дроперидол 0,25% раствор по 0,05- 0,1 мл/кг массы тела внутривенно, только после ликвидации гиповолемии. Препарат вводят каждые 8-10 часов.
2.Коррекция гемоциркуляторных нарушений: пентамин 5% раствор по 0,05-0,1 мг/год внутривенно, однократно (противопоказан при гиповолемии). Затем вводят 2,4% раствор эуфиллина по 4-6 мг/кг массы тела внутривенно на растворе глюкозы каждые 6 часов.
3.Воздействие на сосудистую проницаемость и стабилизация клеточных мембран: преднизолон по 1-10 мг/кг/сутки внутривенно каждые 4 часа.
4.Улучшение реологических и коагуляционных свойств крови: никотиновая кислота по 0,5-1,0 мл внутривенно, однократно; кавинтон по 1 мг/кг массы тела внутривенно капельно; гепарин (при выявлении признаков гиперкоагуляции) по 50-200 ЕД/кг массы тела в сутки внутривенно, равномерно; плазма свежезамороженная по 5-8 мл/кг массы тела внутривенно, капельно, однократно. Для профилактики ДВСсиндрома также применяют курантил 0,5% раствор по 2-3 мг/кг/сутки внутривенно.
5.Коррекция вводно-электролитных и метаболических расстройств. Суточный объем жидкости уменьшается на 25% от СЖП. Примерно половина рассчитанного объема водится внутрь, остальная часть жидкости вводится внутривенно. Выбор кровезамещающих растворов определяется клиническими проявлениями токсикоза (отек мозга, сердечная недостаточность, и т.д.). В состав инфузионных сред следует включить растворы калия хлорида (4-7,5-10%). Количество вводимого калия рассчитывается по номограмме Абердина. Рассчитанное количество калия вводится только капельно, равномерно в течение суток. Препараты кальция (хлорид кальция, глюконат кальция) назначают из расчета 0,25-0,15 мл/кг/сутки.
6.Коррекция дыхательной недостаточности: оксигенотерапия.
7.Нормализация метаболизма в нейронах головного мозга: пирацетам 20% раствор по 50-100 мг/кг массы тела внутривенно в растворе глюкозы 3-4 раза в сутки.
8.Элиминация экзо- и эндотоксинов: а) лазикс по 1-3 мг/кг в сутки внутривенно; б) альбумин 10% по 10 мл/кг массы тела внутривенно капельно.
9.Для уменьшения активности лизосомальных ферментов показаны протеолитические ферменты: трасилол и контрикал (внутривенно капельно в дозе 500 ЕД/кг на 50-100 мл 5% раствора глюкозы).
107
10. Лечение синдромов, развивающихся при токсикозе ΙΙ степени: гипертермический синдром, судорожный синдром, сердечная недостаточность. При сердечной недостаточности показаны сердечные гликозиды внутривенно (0,05% раствор строфантина или 0,06% раствор коргликона по 0,1-0,2 мл 1-2 раза в сутки).
10. Лечение заболевания, при котором развился синдром инфекционного токсикоза.
Инфекционный токсикоз ΙΙΙ степени
Реанимационный этап решает следующие задачи: стабилизация центральной гемодинамики, восполнение ОЦК, ранняя искусственная ИВЛ, коррекция жизнеугрожающего синдрома.
1.Коррекция гемоциркуляторных нарушений, нормализация системной гемодинамики: преднизолон по 5-10 мг/кг массы тела внутривенно одномоментно.
2.Далее необходимо внутривенно ввести свежезамороженную плазму или альбумин по 10-20 мл/кг массы тела капельно или кристаллоиды (физраствор) в дозе 30 мл/кг/час (до стабилизации показателей гемодинамики).
3.Допамин. В дозе 2-5 мкг/кг/мин препарат нормализует нарушения микроциркуляции и обладает диуретическим эффектом. В дозе 6-9 мкг/кг/мин допамин оказывает инотропное действие (кардиостимулирующий эффект). В дозе свыше 10 мкг/кг/мин допамин повышает уровень артериального давления. Допамин разводят 5% раствором глюкозы или физиологическим раствором до общего объема 100 мл. В этом случае параметр введения 1 мл/час соответствует скорости введения препарата 1 мкг/кг/мин.
Интенсивный этап лечения решает следующие задача: проведение
нейровегетативной блокады, поддержание энергетического обеспечения метаболизма, нормализация микроциркуляции и гемодинамики, элиминация токсинов.
1.Нейровегетативная блокада (неглубокая): дроперидол 0,25% раствор по 0,05 мл/кг массы тела внутривенно, только после ликвидации гиповолемии. Препарат вводят каждые 8-10 часов.
2.Воздействие на сосудистый тонус: эуфиллин 2,4% раствор по 4- 6 мг/кг массы тела внутривенно каждые 6 часов.
3.Улучшение реологических и коагуляционных свойств крови: кавинтон по 1 мг/кг массы тела внутривенно капельно.
4.Гепарин (при гиперкоагуляции) по 50-100 ЕД/кг тела в сутки внутривенно, равномерно.
5.Коррекция водно-электролитных нарушений. Суточный объем жидкости уменьшается на 50% от СЖП. Весь рассчитанный объем
108

жидкости вводится внутривенно. В состав инфузионных сред следует включить растворы калия хлорида (4-7,5-10% растворы). Количество вводимого калия рассчитывается по номограмме Абердина. Рассчитанное количество калия вводится только капельно, равномерно в течение суток. Препараты кальция (хлорид кальция, глюконат кальция) назначают из расчета 0,25-0,15 мл/кг/сутки. Выбор кровезамещающих растворов определяется клиническими проявлениями токсикоза (отек мозга, сердечная недостаточность, и т.д.).
6.Лечение синдромов, развивающихся при токсикозе ΙΙΙ степени: инфекционно-токсический шок, острая сердечная недостаточность.
7.Нормализация метаболизма в нейронах головного мозга: пирацетам 20% раствор по 50-100 мг/кг массы тела внутривенно в растворе глюкозы 3-4 раза в сутки.
8.Элиминация экзо- и эндотоксинов: а) лазикс по 1-3 мг/кг в сутки внутривенно; б) альбумин 10% по 10 мл/кг массы тела внутривенно капельно, в) плазмаферез по схеме.
9.Лечение заболевания, при котором развился синдром инфекционного токсикоза.
Вопросы к экзамену. Первичный инфекционный токсикоз. Причины.
Патогенез. Клинические синдромы. Диагностика. Дифференциальный диагноз. Лечение. Показания и особенности инфузионной терапии. Коррекция сердечно-сосудистых расстройств и дыхательной недостаточности.
ХРОНИЧНКИЕ НЕСПЕЦИФИЧЕСКИЕ БРОНХОЛЕГОЧНЫЕ ЗАБОЛЕВАНИЯ (ХНБЛЗ) представляют собой хронический воспалительный процесс, имеющий в своей основе необратимые морфологические изменения в виде деформации бронхов и пневмосклероза в одном или нескольких сегментах, бронхоэктазов и сопровождающийся рецидивами воспаления в бронхах или легочной ткани.
Этиология. К формированию ХНБЛЗ проводят: ателектазы различного генеза, включая врожденные; аспирация инородных тел, хроническая аспирация пищи. Неблагоприятному исходу процесса способствуют ранний возраст, сопутствующие заболевания, поздно начатое и неправильное лечение. Из эндогенных факторов следует назвать врожденные микродефекты бронхиальных структур, иммунодефицит, цилиарную дисфункцию.
109
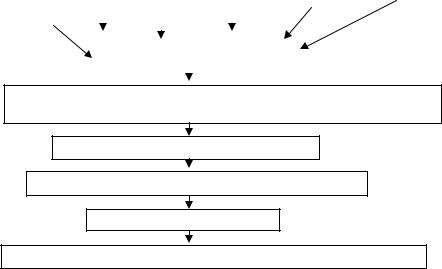
Патогенез ХНБЛЗ разработан недостаточно. Центральное место в патогенезе ХНБЛЗ занимает инфекция. В результате развития и персистирования воспалительного процесса развивается повреждение цилиарного эпителия бронхов, гиперплазия бокаловидных клеток, разрушение реснитчатого эпителия.
Следствием длительных воспалительных изменений является формирование необратимых расширений бронхов с выраженными структурными изменениями их стенок и функциональной неполноценностью.
Страдает функция бронхов – нарушение мукоцилиарного клиренса, часто присоединяется бронхиальная обструкция.
Неблагопри- |
|
Нарушения |
|
Наслед- |
|
Наруше- |
|
Анома- |
|||||
ятная эколо- |
|
местной |
|
ственная |
|
ние дре- |
|
лии |
|||||
гия |
|
защиты |
|
предрас- |
|
нажной |
|
бронхо- |
|||||
|
|
|
|
|
|
|
|
поло- |
|
функции |
|
легочной |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
системы |
|||
Нарушения |
|
|
|
Аспираци- |
|
женность |
|
бронхов |
|
|
|||
|
|
|
|
|
|
|
|||||||
|
|
|
онный син- |
|
|
|
|
|
|
|
|
||
иммунитета |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
дром |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
Инфекция: бактерии, вирусы |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повреждение цилиарного эпителия бронхов, гиперплазия бокаловидных клеток,
разрушение реснитчатого эпителия
Повышение выработки медиаторов воспаления
Усиление и углубление воспалительного процесса в бронхах
Развитие гнойного эндобронхита
Ухудшение дренажной функции бронхов, развитие бронхиальной обструкции
Рис. 1.14. Схема патогенеза ХНБЛЗ
Между этиологическими факторами ХНБЛЗ, воспалением и бронхиальной обструкцией существует взаимосвязь («порочный круг», рис.
110

1.15).
|
|
|
|
|
|
|
Бактериальная инфекция |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Воспаление |
|
|
|
|
|
|
|
|
|
|
|
||||
|
Колонизация |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гиперсекреция |
|||||||
|
бактериями |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
Бронхиаль- |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
ная об- |
|
|
|
|
|
|
|
|
|
|
|
||
|
Размножение |
|
|
|
|
струкция |
|
|
|
|
|
|
|
Застой слизи |
|
|||||||||
|
|
бактерий |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нарушение дренажной |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Нарушение защитных |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
функции бронхов |
|||||||||||||
|
|
механизмов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рефлекторные механизмы |
|
|
Бронхоспазм (аллергия) |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 1.15. «Порочный круг» при ХНБЛЗ (Середа Е.В., 2002)
Классификация
Хроническая патология легких у детей включает:
1.Инфекционно-воспалительные болезни легких;
2.Врожденные пороки развития бронхолегочной системы;
3.Наследственные болезни легких;
4.Поражения легких при других наследственных заболеваниях;
5.Аллергические болезни легких.
Инфекционно-воспалительные болезни легких представлены: хроническим бронхитом, бронхоэктатической болезнью.
Хронический бронхит (ХБ) – хроническое распространенное воспалительное поражение бронхов.
ХБ рассматривается в настоящее как самостоятельная нозологическая единица. Первичный ХБ – хроническое распространенное воспалительное поражение бронхов, протекающее с повторными обострениями. В МКБ-10 выделяют: простой, слизисто-гнойный, неуточненный ХБ. ХБ может быть и вто ричным (синдром при основной патологии).
Бронхоэктатическая болезнь (БЭБ) – приобретенное хроническое воспалительное заболевание бронхолегочной системы, характеризующееся гнойно-воспалительным процессом в расширенных деформированных бронхах с инфильтративными и склеротическими изменения-
111

ми в перибронхиальном пространстве.
БЭБ – это самостоятельная нозологическая форма. Под термином «бронхоэктазы» понимают необратимые расширения бронхов, которые могут локализоваться или охватывать целые отделы бронхиального дерева. Любая форма бронхоэктазов связана с бактериальной инфекцией. Основную роль в появлении бронхоэктазов играет повреждение бронхиальной стенки инфекцией. БЭБ, как отдельную нозологическую форму, следует отличать от бронхоэктазов, развивающихся при других заболеваниях. К ним относят: врожденные аномалии бронхолегочной системы, синдром Вильямса-Кембелла, трахеобронхомегалию, муковисцидоз, первичные иммунодефициты, первичную цилиарную дискинезию, синдром Картагенера, дефицит альфа-1- антитрипсина, синдром Элерса-Данлоса, синдром Марфана.
Пороки развития бронхолегочной системы представлены поро-
ками развития легких: агенезия легких, аплазия легких, секвестрация легких, кисты легких, гипоплазия легких.
Распространенные пороки развития стенки трахеи и бронхов
включают: трахеобронхомегалию, трахеобронхомаляцию, синдром Вильямса-Кембелла, бронхиолоэктатическую эмфизему.
Ограниченные пороки развития стенки трахеи и бронхов пред-
ставлены: врожденными стенозами, врожденной лобарной эмфиземой, дивертикулами трахеи и бронхов, добавочными бронхами; пороками отдельных бронхов; трахеобронхопищеводными свищами.
Исследования: общий анализ крови и мочи, посев мокроты на флору и цитологическое исследование мокроты, биохимический анализ крови (общепринятые исследования), исследование газов крови, спирограмма (дети старше 5 лет); проба с бронхолитиком; рентгенография органов грудной клетки, бронхоскопия (с анализом бронхиального содержимого), исследование кала на яйца глист. По показаниям:
определение иммуноглобулинов в крови, рентгенография придаточных пазух носа, ЭХО-КГ, проба Манту, потовая проба, пнев-
мосцинтиграфия, бронхография, биопсия слизистой бронха с исследованием реснитчатого эпителия, КТ, ЯМР, ангиопульмонография, анализ на ά1-антитрипсин, анализ пота на хлориды.
Анамнез, клиника. В анамнезе у детей с ХНБЛЗ выявляют неоднократные пневмонии одной локализации, перенесенную тяжелую пневмонию типа стафилококковой, затяжноетечение сегментарной пневмонии, особенно в раннем возрасте; указания на врожденные пороки развития бронхолегочной системы, инородное тело бронхов, ателектазы у недоношенных детей, иммунодефицитное состояние, бронхолегочную дисплазию после ИВЛ, мукоциллиарную недостаточность, перенесенные в тяже-
112
лой форме коклюш и корь.Возможно выявление лихорадки, отставания в росте, недостаточной прибавку в массе тела, ограничение физической активности.
Характерны жалобы на упорный кашель чаще по утрам, ночью, с отхождением мокроты (в том числе и в отсутствии ОРИ) . Количество мокроты может варьировать от небольшого (20-50 мл в сутки) до 100 -150 мл, при наличии бронхоэктазов мокрота можетбыть слизисто-гнойная или гнойная.
Симптомокомплекс хронической интоксикации,гипоксии— быстрая утомляе-
мость, снижение работоспособности, нарушение концентрации внимания, ослабление памяти, бледность, тени под глазами, могут быть признаки дистрофии, наличие «барабанных палочек», «часовых стекол», асимметричная деформация грудной клетки.
Бронхолегочный синдром:выявляется укорочение звука при перкуссии локального характера или мозаичность картины. При аускультации на фоне жесткого дыхания наличие стойких локальных разнокалиберных влажных
исухих разнотембровых хрипов.
1.ХБ характеризуется наличием длительного кашля с мокротой, постоянством выслушивания влажных и сухих хрипов над легкими.
2.БЭБ характеризуется кашлем с большим количеством гнойной мокроты. Отмечается отставание детей в физическом развитии. Часто выявляют различные варианты деформации грудной клетки. Типичны разной степени выраженности дыхательная недостаточность, барабанные палочки, часовые стекла. Характерны жесткое дыхание, разнокалиберные влажные хрипы, трескучие хрипы типа «пулеметного треска», дистанционные хрипы.
Диагноз
1. Диагноз ХБ устанавливается на основании клиники и подтверждается при помощи, бронхоскопии, спирографии, бронхографии, компьютерной томографии. При этом следует исключить все другие причины формирования хронической бронхолегочной патологии.
Первичный ХБ диагностируется при наличии кашля с мокротой, постоянных хрипов в течение 3 месяцев и более. На протяжении года должно быть не менее 3 обострений. Общая продолжительность заболевания 2 года и более. Необходимо исключить заболевания, протекающие с вторичным бронхитом, который является компонентом хронических заболеваний легких и бронхов (муковисцидоз, первичная цилиарная дискинезия, пороки развития бронхолегочной системы и др.).
2. Диагноз БЭБ устанавливается с учетом оценки клиники. Помимо собственно документации наличия бронхоэктазов (бронхоско-
113
пия, бронхография, КТ) при рентгенологическом исследовании выявляют деформацию легочного рисунка, перибронхиальные уплотнения, ячеистый легочной рисунок, кольцевидные тени, смещение органов средостения. Необходимо провести дифференциальный диагноз между собственно БЭБ и бронхоэктазами, как проявлением основной патологии.
Лабораторные исследования Общий анализ крови- при обостренииХНБЛЗ регистрируютлейкоцитоз
нейтрофильного характера, увеличение СОЭ.
При рентгенологическом исследовании при ХБ выявляют: усиление и деформацию легочного рисунка без локального пневмосклероза.
Бронхоскопия при ХБ - картина простого, слизисто-гнойного эндобронхита. При ХБ имеется деформация бронхов различной степени выраженности и распространенности. При первичном ХБ выявляют изменения в слизистом и подслизистом слое бронхов с гиперплазией желез.
Бронхоскопия при БЭБ выявляет различные варианты бронхоэктазов, деформации бронхов и воспалительных изменений.
Бронхография при ХБ обнаруживает деформацию стенок бронхов, их втяжение и выбухание, искривление и оголенность бронхиальных стволов. При этом локальный пневмосклероз не выявляется. Существенным является положение, согласно которому трансформация ХБ в бронхоэктазы не происходит.
Бронхография при БЭБ - деформация бронхиального дерева, расширение дистальных участков бронхов, наличие цилиндрических и мешотчатых бронхоэктазов.
Спирография - нарушение функции внешнего дыхания рестриктивного, обструктивного или смешанного характера.
Анализ мокроты - наличие нейтрофилов, макрофагов, бактерий, (чаще грамотрицательная флора, устойчивая к антибиотикам).
Бактериологическое исследование мокроты - чаще всего выделяют гемофильную палочку, β-гемолитический стрептококк, пневмококк, разные виды стафилококков нередко идентифицируют микоплазмы как самостоятельно, так и в ассоциации с другими микроорганизмами.
Дифференциальный диагноз необходимо проводить с: туберкулезом; наследственной бронхолегочной патологией; врожденными аномалиями бронхолегочной системы; поражениями легких при системных заболеваниях; рецидивирующими бронхитами.
Таб. 1.34 Дифференциальный диагноз хронического бронхита
114
Признак |
Хронический бронхит |
Рецидивирующий |
|
|
бронхит |
Ведущий этиологи- |
Табачный дым |
Эпизод ОРВИ |
ческий признак |
|
|
Кашель с мокротой |
Наличие на протяжении |
В течение 3-4 не- |
|
3- мес. и более |
дель |
Хрипы в легких |
Тоже |
2- 4 недели |
Общая продолжи- |
2 года и более |
Не менее 1,5-2 лет |
тельность заболе- |
|
|
вания |
|
|
Бронхоскопия |
картина простого, слизи- |
Проявления эндоб- |
|
сто-гнойного, эндоброн- |
ронхита |
|
хита, деформация брон- |
|
|
хов различной степени |
|
|
выраженности и распро- |
|
|
страненности |
|
Микроскопия сли- |
Изменения в слизистом и |
Изменения неодно- |
зистой |
подслизистом слое брон- |
значны |
|
хов с гиперплазией желез |
|
|
|
|
Бактериологическое |
Гемофильная палочка, β- |
Пневмококк, гемо- |
исследование мок- |
гемолитический стреп- |
фильная палочка и |
роты |
тококк и др. |
др. в 45% |
Течение |
Рецидивы продолжаются |
Рецидивы прекра- |
|
до 7-9-12 лет |
щаются через 2-3 |
|
|
года |
Лечение, задачи лечения: купирование (снижение интенсивности) воспалительных проявлений, удлинение периода ремиссии, повышение качества жизни пациента, предупреждение прогрессирования заболевания и формирования осложнений.
Схема лечения. Обязательными при ХНБЛЗ являются: антибактериальная терапия, муколитическая терапия, позиционный дренаж, вибрационный массаж грудной клетки, противовоспалительное лечение, ЛФК.
Вспомогательное лечение: режим, диета, лечение бронхообструктивного синдрома, физиотерапия, лечебная бронхоскопия, мукорегуляторы, фитотерапия, эндобронхиальное введение антибиотиков, хирургическое лечение.
Показания для госпитализации: тяжелые обострения ХНБЛЗ, ос-
115

ложненное течение заболевания, наличие тяжелой фоновой патологии, необходимость углубленного обследования, госпитализация по социальным показаниям.
При обострении БЭБ, ХБ назначается постельный или полупостельный режим, диета с повышенным количеством белка (мясо, творог) и жиров (сливочное масло, рыбий жир).
Антибактериальная терапия при ХП и БЭБ применяется во всех случаях обострений заболевания.
Показания для антибактериальной терапии при лечении ХБ:
−обострение ХБ или его высокая активность вне обострения;
−развитие пневмонии или обострение легочного очага инфекции;
−присоединение микоплазменной или хламидийной инфекции;
−при симптомах, подозрительных на наличие бактериальной инфекции;
−при возникновении внелегочного очага бактериального процесса (синусит, отит и др.).
Табл. 1.35. Муколитические препараты при лечении ХНБЛЗ
Препарат |
Дозировка |
N-ацетилцистеин |
Внутрь после еды: детям до 2лет 100 мг 2 раза в |
день, 2-6 лет – 100 мг 3 раза в день, старше 6 лет – |
|
АЦЦ, Мукобене, |
200 мг 2-3 раза в день. В ингаляциях – 150-300 мг |
Мукомист и др. |
на процедуру. |
|
|
Месна, Мистаброн |
В ингаляциях – дозировки индивидуальные |
Карбоцистеин |
Сироп 2%. Детям 2-5 лет – по 100 мг (по 5 мл – 1 ч. |
ложка) 2 раза в день, старше 5 лет по 5 мл 3 раза в |
|
Флюдитек |
день |
|
|
Карбоцистеина |
Сироп 450 мг/5мл: внутрь 2-3 раза в сутки детям 1- |
лизиновая соль |
5 лет - по 2,5 мл (225 мг). 5-12 лет – о 5п мл (450 |
Флуифорт |
мг), старше 12 лет – по 15 мл. |
|
Таблетки 30 мг, раствор для приема внутрь и для |
Амброксол |
ингаляций 7,5 мг/мл, сироп 15 мг/5 мл, 30 мг/5 мл. |
Внутрь детям до 5 лет – 7,5 мг, 5-12 лет – 15 мг, |
|
Лазолван |
старше 12 лет – 30 мг 2 – 3 раза в день. Принимают |
Медовен |
после еды, запивая небольшим количеством жидко- |
Фервекс от кашля |
сти. |
|
Ингаляции: младше 5 лет – по 2 мл, старше 5 лет – |
|
2-3 мл 1-2 раза в день. |
Пульмозим |
В ингаляциях по 2,5 мг 1-3 раза в день через небу- |
|
116 |

Дорназа альфа лайзер. Эндобронхиально по 1-2 ампулы на проце-
дуру.
Антибактериальная терапия строится с учетом результатов высева возбудителя из мокроты. При отрицательных результатах посевов лечение проводится с учетом наиболее вероятного возбудителя заболевания. Антибиотикотерапию можно начинать с защищенных пенициллинов, цефалоспоринов, аминогликозидов. При нетяжелых обострениях возможно оральное применение препаратов (см. также «Лечение пневмонии»). При недостаточной эффективности лечения показаны лечебные бронхоскопии, эндотрахеальное введение антибиотиков.
Важное место в лечении обострений ХБ и БЭБ занимает постуральный дренаж, который проводят 3-4 раза в день по 10-15 минут до еды.
Муколитическая терапия при ХНБЛЗ направлена на разжижение и удаление мокроты. Для этих целей рекомендуют применение муколитиков (табл. 1.35).
Лечение синдрома бронхиальной обструкции при ХНБЛЗ представ-
ляет сложную проблему. При проведении этого лечения предпочтение следует отдавать пролонгированным препаратам, к которым относят β2-агонисты длительного действия (Форадил, и др.).
Физиотерапия при ХНБЛЗ включает УВЧ, микроволновую терапию, лекарственный электрофорез. При катаральных проявлениях в легких, обструкции, гиповентиляции применяют электрофорез с платифиллином. При сильном кашле - электрофорез с 0,1% раствором дионина. В периоде стихания воспалительных изменений назначают индуктотермию или ультразвуковую терапию.
Санаторное лечение закрепляет результаты терапии обострения, улучшает предоперационную подготовку и реабилитацию после операции и включает в себя: ЛФК, подвижные игры, прогулки, спортивные упражнения.
Из средств фитотерапии применяют: зверобой, цветы ромашки, трава багульника и др.
Показано использование позиционного дренажа, вибромассажа грудной клетки, ЛФК.
Оперативное лечение рекомендуется при наличии хорошо отграниченного участка пневмосклероза с бронхоэктазами, а также (паллиативная операция) при обширных проявлениях, негативно влияющих на развитие ребенка. При тяжелых двусторонних процессах удаление наиболее пораженных сегментов уменьшает степень интоксикации и способствует физическому развитию ребенка.
117

Исходы. Прогноз при ХНБЛЗ зависит от вида заболевания и распространенности бронхолегочных изменений. Наиболее благоприятный прогноз при ХБ. Улучшение состояния и течения заболевания наблюдается в подростковом возрасте.
Прогноз при БЭБ более серьезный, чем при ХБ. Улучшение состояния с возрастом наблюдают только у 1/3 пациентов. Однако и прогрессирования заболевания также не происходит. Полного выздоровления даже после оперативного вмешательства нет.
Наиболее серьезный прогноз при кистозной гипоплазии легкого. На протяжении наблюдения сохраняются клинические проявления заболевания.
Профилактика ХНБЛЗ включает в себя весь комплекс мер, используемых при острых пневмониях (улучшение жилищных условий, рациональное питание, закаливание, лечение фоновой патологии и др.). Особое место занимает использование пневмококковых вакцин. Важным является своевременное удаление инородных тел, раннее распознавание и лечение ателектазов.
Вопросы к экзамену. Хронический бронхит. Бронхоэктатическая бо-
лезнь. Этиология. Патогенез. Клиническая картина. Диагностика. Показания к бронхологическому исследованию. Бронхологические методы исследования: бронхоскопия, бронхография. Неинвазивные методы исследования: рентгенологическое исследование легких, компьютерная томография (КТ), ядерно-магнитная резонансная томография (ЯМРТ). Радиоизо-
топные методы исследования. Дифференциальный диагноз. Лечение. Немедикаментозные методы лечения. Показания к хирургическому лечению. Исходы. Профилактика.
Глава IV. Белково-энергетическая недостаточность
ГИПОТРОФИЯ (Г) - хроническое расстройство питания, характеризующееся дефицитом массы по отношению к росту. В настоящее время для обозначения этого состояния все чаще употребляются термины: белково-энергетическая недостаточность, синдром недостаточности питания.
Эпидемиология Г изучена недостаточно. Частота Г зависит от экономического развития страны. В России тяжелая Г диагностируется у 2% детей. Легкие формы Г часто пропускаются.
Классификация. По времени возникновения различают пренаталь-
ную (внутриутробную, врождённую) и постнатальную (приобретенную) Г.
118
По степени тяжести выделяют Г первой, второй и третьей степени. При Г I степени дефицит фактической массы по отношению к долженствующей с учётом роста ребенка составляет 10-20%, при Г II
степени - 20-30%, при Г III степени - больше 30%.
Период заболевания: начальный, прогрессирования, реконвалесценции.
Первичные Г имеют в своей основе белково-энергетическая недостаточность. Вторичные Г сопровождают врожденные и приобретенные заболевания.
Гипостатура – вариант дистрофии с равномерным отставанием массы тела и роста от возрастных норм.
Основными клинико-патогенетическими вариантами Г являются:
алиментарный маразм, квашиоркор, маразм-квашиоркор.
Этиология. К развитию Г могут привести различные экзогенные и эндогенные факторы, которые, как правило, сочетано, обуславливают либо недостаточное поступление пищи в организм, либо недостаточное её усвоение. Этиологические факторы зависят от времени возникновения и соответственно формы Г: пренатальной или постнатальной.
Причины развития пренатальной Г, условно, можно разделить на три группы:
1.Преплацентарные: конституциональные особенности матери (инфантилизм, астеническое телосложение, возраст моложе 18 лет или старше 35 лет); сердечно-сосудистые, почечные, эндокринные и другие заболевания матери; токсикозы беременности; предшествующие медицинские аборты; недостаточное питание матери во время беременности; неблагоприятные социально-экономические, производственные или экологические условия, вредные привычки матери (курение, алкоголизм, наркомания); аномалии васкуляризации матки.
2.Плацентарные: тромбозы, гематомы, инфаркты плаценты, её гипоплазия, кальциноз, фиброз, плацентит.
3.Постплацентарные: аномалии пуповины, многоплодная бере-
менность, врождённые пороки развития плода, внутриутробная инфекция, наследственные факторы (хромосомные заболевания, моногенные синдромы, семейная аутосомно-доминантная предрасположенность к гипотрофии).
Многие этиологические факторы (преплацентарные и плацентарные) реализуются через хроническую плацентарную недостаточность, которая приводит к развитию хронической гипоксии плода и задержке физического развития.
119
Среди экзогенных факторов, вызывающих развитие постнатальной Г, существенное значение имеют алиментарные факторы - количественный недокорм.
Не менее важную роль в возникновении Г играют и качественные нарушения питания (качественный «недокорм»): дефицит витаминов и микроэлементов, недостаток или избыток какого-либо пищевого вещества (белка, жира или углеводов). При повышенной белковой нагрузке снижается утилизация белка, в организме накапливаются азотистые продукты, аминокислоты, аммиак, возникает ацидоз, что ведёт к появлению дистрофических изменений в мозговой ткани и паренхиматозных органах.
Особенно неблагоприятен избыток белка на фоне недостатка углеводов. Последнее наблюдается при длительном кормлении молочными смесями и известно как «молочное расстройство питания». Злоупотребление кашами может стать причиной так называемого «мучного расстройства питания», которое проявляется либо в виде паратрофии (пастозная форма), либо Г (атрофическая и гипертоническиспастическая формы). Иногда Г является следствием длительного водного голодания.
К развитию Г часто ведут острые и хронические инфекционные заболевания (вирусные инфекции, сепсис, кишечные инфекции, отоантрит, и т.д.); существенное значение имеет дисбиоз кишечника. Вредное влияние на питание ребёнка оказывают нарушение режима и дефекты ухода.
Причинами развития наиболее тяжелых форм пренатальной Г в настоящее время чаще являются эндогенные факторы: синдром мальабсорбции, пороки развития желудочно-кишечного тракта и других органов, наследственные нарушения обмена веществ (галактоземия, фруктоземия, некоторые аминоацидопатии и т.д.), иммунодефицитные состояния, эндокринные заболевания (адреногенитальный синдром), патология центральной нервной системы.
Патогенез
Основой патогенеза Г является хроническая стрессовая реакция (Е. В. Неудахин, 1992).
У детей с пренатальной Г повышено образование стрессреализующих гормонов: адреналина, СТГ, глюкокортикоидов. Однако при тяжёлой степени Г появляются признаки истощения коры надпочечников. Продукция инсулина и минералокортикоидов снижена. Увеличение синтеза глюкокортикоидов и снижение минералокортикоидов и инсулина характерно для хронической стрессовой реакции. При этом быстро расходуются углеводы, а для энергетического обес-
120
печения механизмов долговременной адаптации более активно используются липиды. По данным исследований В.Ф. Дёмина у новорожденных с пренатальной Г отмечается продолжительная гиперлипидемия за счёт нейтрального жира, эфиров холестерина и фосфолипидов. Эфиры холестерина необходимы для продукции ряда биологически активных веществ, в том числе – глюкокортикоидов; фосфолипиды - для образования клеточных мембран и сурфактанта.
Характер эндокринных и метаболических изменений, типичных для хронической стрессовой реакции, делает обоснованным понятие «стрессовый плод» по отношению к плоду с пренатальной Г. Хроническая стрессовая реакция у плода и новорожденного с пренатальной Г обуславливает гиповолемию, централизацию кровообращения и гипердинамическую реакцию миокарда, гипогликемию, уменьшение содержания гликогена в печени и сердце, гипокальциемию и гипомагниемию, метаболический ацидоз, накопление продуктов перекисного окисления липидов, полицитемию и повышение уровня гематокрита, гиперкоагуляционный синдром (у этих детей более высокий риск развития ДВС-синдрома), нарушение микрогемоциркуляции, возникновение иммунодепрессии.
Хронический стресс уменьшает опасность развития у новорожденных с пренатальной Г I и II степени синдрома дыхательных расстройств вследствие усиленного образования сурфактанта, но повышает риск возникновения кровоизлияний в мозг и лёгкие, а также некротического энтероколита.
У детей раннего возраста с постнатальной (приобретённой) и смешанной (пренатально-постнатальной) Г также определяются изменения, характерные для хронической стрессовой реакции. Результаты исследования вегетативного гомеостаза свидетельствуют о стадийности и зависимости выраженности изменений от степени Г: при I и II степенях отмечается нарастающая симпатикотония и усиливающаяся активность центрального контура регуляции, при III степени – «срыв адаптации», децентрализация регуляции с переходом на автономные уровни и преобладание парасимпатических влияний. Для детей с Г I и II степеней характерна дисфункция коры надпочечников с повышенной продукцией глюкокортикоидных фракций и пониженной - проминералокортикоидных (маркёр хронической стрессовой реакции). У детей с Г III степени наблюдается гипофункция (истощение) коры надпочечников.
О состоянии хронического стресса свидетельствует и переход обмена веществ с преимущественно углеводного на преимущественно липидный, в результате чего используется нейтральный жир подкож-
121
но-жировой клетчатки для энергетического обеспечения функций организма и образования фосфолипидов, необходимых клеточным мембранам. Для сердечно-сосудистой системы у детей раннего возраста с Г характерна склонность к централизации кровообращения на фоне гиповолемии, гипердинамическая реакция миокарда, лёгочная гипертензия, спастическое состояние прекапиллярных артериол, нарушение микрогемоциркуляции с развитием «сладж»-синдрома в микрососудах. Гемодинамические расстройства патогенетически связаны с хронической стрессовой реакцией. Стрессовым влиянием можно объяснить и развитие гиперкоагуляции и иммунодепрессии.
Т.О., Г - это проявление патофизиологической (хронической стрессовой) реакции организма, в связи с чем она должна рассматриваться как клиническим синдромом, а не как нозологическая единица.
Анамнез, клиника
Основными клиническими синдромами при Г являются: недоста-
точная упитанность, трофические расстройства, снижение пищевой толерантности, изменение функционального состояния ЦНС, нарушение иммунологической реактивности.
Г I степени проявляется умеренным похуданием ребёнка (дефицит массы тела 10-20%), что выражается в истончении подкожного жирового слоя, прежде всего на туловище. У детей отмечается бледность кожных покровов и слизистых оболочек, снижение тургора тканей и мышечного тонуса. Рост не нарушается. Аппетит и стул обычно остаются нормальными. Функции внутренних органов и психомоторное развитие не изменяются.
При Г II степени заметно ухудшается состояние ребёнка. Кожные покровы приобретают сероватый оттенок, становятся сухими. Из-за низкой эластичности кожа легко собирается в складки, особенно на внутренней поверхности бёдер. Тургор тканей и тонус мышц снижены. Подкожный жировой слой отсутствует на туловище и конечностях. Дефицит массы (20-30%) сопровождается отставанием в росте на 1-3 см. У детей плохой аппетит, снижена толерантность к пище. Они раздражительны или беспокойны. Обращают на себя внимание задержка в психомоторном развитии. У больных легко возникают ин- фекционно-воспалительные очаги в ушах, зеве, легких. Часто наблюдается анемия. Характер стула зависит от особенностей питания.
122

Факторы, способствующие развитию гипотрофии: хромосомные заболевания,
врожденные заболевания, алиментарный фактор, острые и хронические инфекционные заболевания, дисбактериоз кишечника, нарушения режима, дефекты ухода, синдром мальабсорбции, врожденные пороки развития, наследственные нарушения обмена, эндокринные заболевания, поражение ЦНС.
Гипотрофия I и II степени.
Нарастающая симпатикотония и усиливающаяся активность центрального контура регуляции.
Повышение образования стресс-реализующих гормонов (АКТГ, адреналин, глюкокортикоиды)
Дисфункция коры надпочечников с повышенной продукцией глюкокортикоидов и снижением минералокортикоидов (маркер хронической стрессовой реакции).
Быстрое расходование углеводов. Развитие гипогликемии и уменьшение содержания гликогена в печени и сердце.
Переключение обмена веществ с преимущественно углеводного на преимущественно липидный. В результате для энергетического обеспечения организма используется нейтральный жир подкожно-жировой клетчатки.
Развитие гипокальциемии и гипомагниемии. Развитие метаболического ацидоза.
Увеличение в крови продуктов перекисного окисления липидов Полицитемия и повышение уровня гематокрита Сердечно-сосудистая система – склонность к централизации кровообращения,
которая возникает на фоне гиповолемии и проявляется компенсаторной реакцией в виде увеличения сократительной способности миокарда, легочной гипертензией, спастическим состоянием прекапиллярных артериол, Нарушением микроциркуляции с появлением «сладж-синдрома». Стрессовые влияния - угнетение иммунитета (угнетение клеточного звена иммунитета)
Гипотрофия III степени
Срыв адаптации, децентрализация регуляции с переходом на автономные уровни. Истощение (гипофункция коры надпочечников)
Изменение функционального состояния ЦНС
Рис. 1.16. Схема патогенеза гипотрофии
Белковый стул (при перекорме молоком, творогом) обычно скудный, сухой, плотный, крошковатый с гнилостным запахом и щелочной реакцией, состоит в основном из известковых и магнезиевых солей.
123
Мучнистый стул обычно жидкий с кислой реакцией, с примесью зелени и слизи. При копрологическом исследовании определяется много внеклеточного крахмала, перевариваемой клетчатки, нейтрального жира и жирных кислот, слизи и лейкоцитов.
Голодный стул скудный, сухой, иногда крошковидный, обесцвеченный с гнилостным, зловонным запахом. В копрограмме много слизи, лейкоцитов, внеклеточного крахмала, нейтрального жира и жирных кислот. Часто развивается дисбиоз кишечника.
При Г III степени состояние ребёнка тяжёлое. Подкожный жировой слой отсутствует везде, даже на лице (дефицит массы тела более 30%). Лицо треугольной формы («лицо Вольтера»). Кожа с сероватоцианотичным оттенком, сухая, иногда с трещинами. Эластичность кожи и тургор тканей резко снижены. Может появиться пастозность тканей. Дефицит роста достигает 4-6 см. У многих детей имеются признаки стоматита, молочницы. Функции внутренних органов (лёгких, сердца, печени, почек) значительно нарушены. Аппетит отсутствует, отмечается выраженная жажда. Терморегуляция расстроена. У больных часто возникают гнойно-воспалительные очаги, могут развиваться септические состояния. Стул «голодный». Значительно угнетены функции центральной нервной системы.
При пренатальной Г отмечается дефицит массы тела по отношению к длине и массе соответственно сроку гестации.
Гипостатура в последние годы стала встречаться значительно чаще. Эта форма Г развивается у детей с врожденными и наследственными заболеваниями, а так же в тех случаях, когда повреждающие факторы оказывали длительное воздействие на организм ребенка. Возможно формирование гипостатуры с момента рождения.
Заболевание проявляется бледностью и сухость кожных покровов, снижением тургора тканей. Главной отличительной особенностью гипостатуры является пропорциональное отставание массы тела и роста по отношению к возрасту. Трофические нарушения кожи и подкожножировой клетчатки выражены значительно слабее, чем у детей с Г при аналогичном дефиците массы тела.
Как и при Г при гипостатуре имеет место проявления поражения ЦНС, признаки нарушения обмена веществ, метаболический ацидоз, снижение защитных реакций организма. При гипостатуре организму ребенка в большей степени, чем при Г удается приспособиться к существованию в новых условиях. В тоже время обменные нарушения, патология со стороны нервной системы имеют более стойкий характер, что проявляется плохими результатами лечения.
124
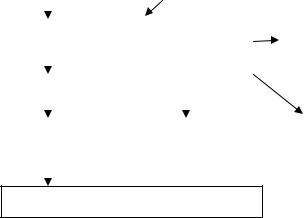
Квашиоркор – вариант Г, возникающий после отлучения ребенка от груди и переводе на растительную пищу, в результате чего развивается белковое голодание. Квашиоркор встречается на 2-4 году жизни.
|
Инфекция |
|
|
|
|
|
Дефицит белка в диете |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
↑ уровня |
|
Резкое снижение |
|
|
|
|
|
|
||||||
|
|
|
|
|
Отеки |
|
|||||||||
|
TNF-α , IL-1 |
|
висцерального пула |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
белка (альбумина, |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
липопротеидов и |
|
|
|
|
|
|
||||
|
↑ уровня IL6 |
|
|
|
|
|
|
|
|||||||
|
|
др.) |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изменение белково- |
|
Гормональ- |
|
|
Жировая ин- |
|
||||||||
|
синтетической |
|
|
ные наруше- |
|
|
фильтрация |
|
|||||||
|
функции печени |
|
|
ния |
|
|
печени |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повышение синтеза белков острой фазы
Рис. 1.17. Схема патогенеза квашиоркора (Педиатрия, нацио-
нальное руководство, 2009)
Основными особенностями квашиоркора являются: атрофия мышц с сохранением подкожно-жирового слоя, депигментация и посеребрение волос, выпадение волос, генерализованные отеки (лунообразное лицо), увеличенный в размерах живот, гепатоспленомегалия. Характерны выраженная задержка физического и психического развития, проявления рахита. При лабораторном исследовании выявляют тяжелую анемию, гипопротеинемию.
Диагноз Г у детей базируется на данных клиники, оценке показателей дефицита массы тела с учётом роста. Дефицит массы определяется по формуле:
Д = (ДМ – ФМ)/ДМ × 100, где Д - дефицит массы тела в %; ДМ - долженствующая масса с учётом роста; ФМ - фактическая масса.
Для оценки степени Г можно пользоваться таблицами центильных распределений массы по длине тела. При диагностике пренатальной Г используются данные клиники, оценочные таблицы Г. М. Дементьевой, В. Н. Ильина. На практике пренатальная Г у доношенных новорожденных часто диагностируется по массо-ростовому показателю, который в норме должен быть в пределах от 60 до 80; при Г I степени
125
- 59-55; при II степени - 54-50; при III степени - меньше 50. Помимо выявления Г, определения степени её тяжести, при осмотре ребёнка в большинстве случаев приходится решать вопрос: синдромом какого заболевания является Г у данного ребёнка? От этого зависит организация лечения.
Лабораторные критерии Г
Полицитемия, гиперкоагуляционный синдром, компенсированный (при Г I-II ст.) и декомпенсированный при Г III ст.
Гипогликемия, гипокальциемия и гипомагниемия, гипокалиемия, склонность к гипернатриемии.
Дислипидемия (гиперлипидемия за счет триглицеридов, фосфолипидов и эфиров холестерина при гипотрофии I-II ст. и за счет триглицеридов и НЭЖК при гипотрофии III ст.).
Повышение в моче уровней глюкокортикоидных гормонов и снижение минералокортикоидных при Г I-II ст.; снижение глюкокортикоидов и минералокортикоидов при Г III ст.
Гиперкатехоламинемия, гипоинсулинемия.
Угнетение иммунитета: уменьшение Т-лимфоцитов, повышение фагоцитарной активности нейтрофилов при I-II ст. Г и снижение – при III ст.
Изменения копрограммы: при молочном расстройстве питания:
щелочная реакция кала, повышение уровня кальция и магния.
При мучном расстройстве: кислая рН кала, повышение уровня внеклеточного крахмала, перевариваемой клетчатки, жирных кислот, слизи и лейкоцитов; признаки дисбиоза кишечника.
ЭКГ: метаболические нарушения в миокарде желудочков.
КИГ: признаки симпатикотонии при Г I-II ст. и ваготонии – при Г
III ст.
ЭХО КГ: компенсаторное увеличение сократительной способности миокарда при Г I-II ст. снижение сократительной способности миокарда при Г III ст.
В качестве скрининга Г используют показатели белкового обмена: протеинограмму (снижение белка и альбумина), уровень мочевины в крови (снижение), абсолютное количество лимфоцитов в периферической крови (снижение).
Дифференциальный диагноз Г проводят с гипостатурой, квашиоркором, нанизмом, конституциональной низкорослостью.
Табл. 1.36. Дифференциальный диагноз гипотрофии
Признак |
Гипотрофия |
Гипостатура |
Квашиоркор |
Нанизм |
|
126 |
|
|
|
Дефицит массы |
есть |
есть |
есть |
есть |
тела |
|
|
|
|
Дефицит дли- |
При Г 2-3 ст. |
Выражен |
есть |
есть |
ны тела |
|
|
|
|
Подкожно- |
истончен |
Истончен в |
нет |
нет |
жировой слой |
меньшей степе- |
|||
|
|
ни, чем дефицит |
|
|
|
|
массы |
|
|
Тургор тканей |
Изменен со- |
Изменен в |
Часто сохра- |
Не из- |
|
гласно степени |
меньшей степе- |
нен |
менен |
|
Г |
ни, чем дефицит |
|
|
|
|
массы |
|
|
Трофика тка- |
Нарушена в |
Выражена |
Нарушена |
Не на- |
ней |
зависимости |
меньше, чем |
|
рушена |
|
от степени Г |
степень дефи- |
|
|
|
|
цита массы |
|
|
|
|
тела |
|
|
Мышечный |
Снижен с |
Снижен |
Атрофия |
Нет |
тонус |
соответствии |
меньше, чем |
мышц |
|
|
со степенью Г |
дефицит мас- |
|
|
|
|
сы |
|
|
Психомоторное |
Нарушено в |
Изменено в |
Отставание в |
Нет |
развитие (п/мр) |
зависимости |
меньшей степе- |
п/мр. разви- |
|
от степени Г |
ни, чем дефицит |
|
||
|
массы |
тии |
|
|
Гепатомегалия |
При Г 3-й ст. |
редко |
Часто |
нет |
Отеки |
Редко |
Редко |
Характерно |
Нет |
Поражение |
В зависимо- |
Изменены в |
Встречаются |
нет |
внутренних |
сти от степени |
меньшей степе- |
|
|
органов |
Г |
ни, чем дефицит |
|
|
массы |
|
|
||
Отслойка эпи- |
Не характерно |
Не характерно |
характерно |
Нет |
дермиса, депиг- |
|
|
|
|
ментация волос |
|
|
|
|
Лечение, задачи лечения: восстановление дефицита массы тела, купирование клинических и параклинических проявлений Г, предупреждение развития осложнений.
Схема лечения. Обязательное лечение: диета, уход, режим, кор-
рекция водно-электролитных нарушений, витаминотерапия, стимулирующее лечение, ферментотерапия.
Вспомогательное лечение: частичное парентеральное питание, биопрепараты, β-адреноблокаторы, анаболические гормоны, санация очагов хронической инфекции, борьба с гиподинамией.
127
Показания для госпитализации: При Г I степени лечение обычно проводится в амбулаторных условиях, а при Г II и III степени - в стационаре.
В первую очередь осуществляются мероприятия по установлению причин, приведших к развитию Г (инфекционные, хронические заболевания ЖКТ, наследственные и врожденные энзимопатии, эндокринные заболевания, органические заболевания ЦНС). Большое внимание должно уделяться организации правильного режима дня, уходу за ребёнком. Для детей с Г наиболее оптимальной является температура воздуха 24-25 °C при относительной влажности 60-70%.
Согласно рекомендациям ВОЗ (2003) выделяется 10 шагов по выхаживанию детей с Г:
1.предупреждение/лечение гипогликемии;
2.предупреждение/лечение гипотермии;
3.предупреждение/лечение дегидратации;
4.коррекция электролитного баланса;
5.предупреждение/лечение инфекции;
6.коррекция дефицита микронутриентов;
7.осторожное начало кормления;
8.обеспечение прибавки массы тела и роста;
9.обеспечение сенсорной стимуляции и эмоциональной поддержки;
10.дальнейшая реабилитация.
Табл.1.37. Этапы выхаживания детей с белково-энергетической
недостаточностью
|
Шаги |
|
Ф А З А |
|
|
стабилизация |
|
реабилитация |
|
|
|
1-2 день |
3-7 день |
2-6 неделя |
1. |
гипогликемия |
ХХХХХХ |
|
|
2. гипотермия |
ХХХХХХ |
|
|
|
3. |
дегидратация |
ХХХХХХ |
|
|
4. |
электролиты |
ХХХХХХ |
ХХХХХХ |
ХХХХХХХХ |
5. |
инфекция |
ХХХХХХ |
|
|
6. |
микронутриенты |
Без железа |
|
С железом |
7. |
осторожное питание |
ХХХХХХ |
ХХХХХХ |
|
8. |
прибавка массы |
|
|
ХХХХХХХХ |
9. |
сенсорный стимул |
ХХХХХХ |
ХХХХХХ |
ХХХХХХХХ |
10. реабилитация |
|
|
ХХХХХХХХ |
|
128
Первый шаг. При сохраненном сознании и уровне глюкозы в крови менее 3 ммоль/л ребенку вводят 50 мл 10% раствора глюкозы через зонд и орально. Кормление начинают с 25% от обычного разового объема питания каждые 30 минут на протяжении 2-х часов. При наличии нарушения сознания (или гипогликемические судороги) внутривенно водят 10% раствор глюкоза из расчета 5 мл/кг. Всем детям с гипогликемией назначают антибиотики широкого спектра действия.
Второй шаг. Согревание ребенка начинают при ректальной температуре ниже 35,5 0С (лучистое тепло, теплая одежда).
Третий шаг. При наличии выраженных проявлений эксикоза начинают оральную регидратацию раствором ReSoMal (с пониженным содержание натрия) из расчета 5 мл/кг каждые 30 минут в течение 2 часов. В последующие 4-10 часов раствор вводят по 5-10 мл/кг/час, постепенно заменяя его на грудное молоко или молочную смесь. Кормление проводят каждые 2 часа без ночного перерыва.
Общее количество вводимой ребенку жидкости составляет 130 мл/кг/сутки, а при выраженных отеках – 100 мл/кг/сутки.
Количество жидкости, необходимой для внутривенного введения, будет равно: СЖП + жидкость возмещения обезвоживания минус (количество съеденной пищи + объем выпитой жидкости).
Основная часть жидкости вводится внутривенно в виде 10% раствора глюкозы.
Четвертый шаг. Коррекция гипокалиемии проводится из расчета 3-4 ммоль/кг/сутки; магния – 0,4-0,6 ммоль/кг/сутки. При возможности для коррекции электролитов следует использовать специальный элек- тролитно-минеральный раствор.
Пятый шаг. Своевременное предупреждение и лечение инфекции, которое проводится по общим принципам.
Шестой шаг. Коррекция дефицита железа начинается не ранее 2-й недели лечения в дозе 3 мг/кг/сутки. Доза цинка – 2 мг/кг/сутки; меди
– 0,3 мг/кг/сутки; фолиевой кислоты – 5 мг (в первый день), затем – 1 мг/сутки. В последующем переходят на витамино-минеральные комплексы. Возможно отдельное назначение витаминных препаратов: С, У, кальция пантотената, пиридоксина, ретинола.
Седьмой и восьмой шаги. Парентеральное питание на первом этапе лечения представлено препаратами аминокислот (Аминон, Альвезин), и концентрированными растворами глюкозы. Жировые эмульсии (Интралипид, Липофундин) начинают применять с 5-7 дня лечения в дозе 10 -15 мл/кг/сут. При тяжелых формах гипотрофии энтеральное питание начинают с кормления через зонд со скоростью поступления смеси не более 3 мл/мин (калорийная нагрузка не более 1
129
ккал/мл). Вначале следует использовать смеси на основе полного гидролиза белка (Алфаре, Нутрамиген, Прогестермил). Смеси (при тяжелой Г) должны содержать небольшое количество лактозы. Длительность периода зондового питания в зависимости от пищевой толерантности продолжается от нескольких дней до нескольких недель. Зондовое кормление постепенно отменяют и оставляют его только на ночное время. При достижении объема дневного кормления в 50-70% постоянное зондовое кормление отменяют.
При Г I и II степени диетотерапия проводится с выделением:
а) адаптационного периода (определение толерантности к пище); б) репарационного периода (промежуточный, этап коррекции); в) периода усиленного питания; г) переход на рациональное питание.
Диета является основой рационального лечения Г у детей раннего возраста. При её осуществлении необходимо соблюдать следующие принципы:
1. Использование на начальных этапах лишь легко усвояемой пищи (женское молоко, адаптированные смеси);
2. Систематический контроль питания с расчётом объёма пищи и пищевой нагрузки по белкам, жирам, углеводам и калориям.
Ι этап диетотерапии: определение толерантности ребенка к пище (адаптационный период, этап разгрузки, этап минимального питания).
Задачи Ι этапа диетотерапии:
-определение толерантности ребенка к пище;
-выведение из организма токсинов и недоокисленных продуктов обмена.
Суточный объем питания в первый день диетотерапии уменьшает-
ся от 20 до 80% в зависимости от степени Г (чем больше степень Г, тем с меньшего объема пищи начинается кормление на данном этапе).
При III степени Г продолжительность адаптационного периода может колебаться от 10 до 14 дней. Если разовая доза становится больше 50 мл, переходят на 8-разовое кормление (см. «первый» и «третий» шаги). Адаптационный период заканчивается увеличением суточного объёма пищи до необходимого количества (1/5 массы).
В качестве основной смеси используют или грудное молоко (донорское молоко) или адаптированную смесь. Все виды прикормов и иных пищевых добавок на этом этапе кормления отменяют.
Количество кормлений увеличивают (см. «первый» и «третий» шаги) в зависимости от степени Г и аппетита.
130

Продолжительность этапа определения толерантности ребенка к пище составляет 3-5-7-10 дней (в зависимости от степени Г). Чем выше степень Г - тем длительнее этот этап кормления.
На протяжении данного этапа постепенно (за 3-5-7-10 дней) увеличивается количество вводимой пищи, и к окончанию этапа доводят его до полного объема (рассчитанного тем или иным методом).
Недостающая часть питания возмещается глюкозо-солевыми растворами. В с вязи с тем, что ежедневное количество молока (смеси) увеличивается, количество вводимой жидкости постепенно уменьшается.
К моменту окончания этапа минимального питания ребенок должен получить полный необходимый объем пищи и прекратить получать внутривенные вливания и потребление жидкости через рот.
Полный объем пищи дается ребенку еще в течение 2-3 дней, после чего переходят ко ΙΙ этапу лечебного питания.
ΙΙ этап диетотерапии - промежуточный этап (этап коррекции дефицита основных пищевых ингредиентов).
|
|
|
|
|
|
П |
|
и |
т |
а |
н |
и |
е |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
щи |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
от90% |
|
|
|
100% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
необходимого |
|
|
|
|
-пи объема |
|
от 50% -рассчи |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
1день 2 день 3 день |
|
|
4 день |
5 день |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Питье |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
-внут |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ж |
и |
д |
к |
о |
с |
т ь |
|
||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
||||||||||
131
объем Рассчитанный
Рис.1. 18. Схема питания и восполнения объема жидкости при гипотрофии 2-й степени на Ι этапе диетотерапии (пример)
Задачи этапа: восполнение дефицита в питании у больного недостающих пищевых ингредиентов.
Методика проведения 2-го этапа. Для определения дефицита пищевых ингредиентов необходимо провести расчет питания.
Принципы расчета питания.
На 1-й неделе переходного периода количество белков и углеводов рассчитывается на фактическую массу +5% от нее, а жиры – на фактическую массу тела.
На 2-й неделе белки и углеводы рассчитываются на фактическую массу +10% от нее, а жиры – на фактическую массы тела.
На 3-й неделе белки и углеводы рассчитываются на фактическую массу тела +15% от нее, а жиры – на фактическую массу тела.
На 4-й неделе белки и углеводы рассчитываются на приблизительно долженствующую массы тела (фактическая + 20% от нее), а жиры на фактическую массы тела.
Недостающее количество белка, жира, углеводов вводится постепенно (в течение 5-7 дней - для каждого ингредиента) в следующей
последовательности: белки → углеводы → жиры.
Дефицит белка компенсируется: смесями с повышенным содержанием белка, творогом, белковыми модулями; дефицит жиров: жировыми модульными эмульсиями, сливками, растительным или сливочным маслом; углеводов – сахарным сиропом, кашами. Все пищевые добавки применяют в соответствии с возрастом.
После ликвидации дефицита всех ингредиентов, ребенку можно ввести положенные по возрасту (отмененные ранее) прикормы.
В периоде усиленного питания содержание белков и углеводов постепенно увеличивается и их начинают рассчитывать на долженствующую массу тела, а жиры на среднюю между фактической и долженствующей. При Г II ст. диета омолаживается (на 2-3 месяца).
Для расчета питания необходимо воспользоваться следующей таблицей:
Табл. 1.38. Расчет питания
Показатель |
Белки Жиры Углеводы Калории |
Должен получать на 1
кг массы тела
Должен получать всего
132

Получает всего
Дефицит
Для заполнения первой строки таблицы необходимо воспользоваться данные таблицы потребности в пищевых ингредиентах детей при Г (табл. 1.39).
Для заполнения строки 3 необходимо высчитать количество белка, жира, углеводов, содержащихся в получаемом ребенке суточном объеме смеси.
«Дефицит» - разность данных строки 2 и 3.
Табл. 1.39. Схема диетотерапии больного с гипотрофией (Бара-
нов А.А. с соавт, 1997)
Задачи |
Разгрузка и |
ΙΙ диетотерапии - промежу- |
Уси- |
||
этапов |
минималь- |
точный этап |
|
лен- |
|
диеты |
ное питание |
Кор- |
Кор- |
Коррек- |
ное |
|
|
рекция |
рекция |
ция жи- |
пита- |
|
|
белка |
углево- |
ров |
ние |
|
|
дов |
|||
Длитель- |
3-5-7-10 (в |
5-7 |
5-7 |
5-7 (всего |
До |
ность этапа |
зависимости |
|
|
15-20 |
выве- |
в днях |
от степени Г) |
|
|
дней) |
дения |
|
|
|
|
|
из Г |
Количество |
1/3-1/2-2/3-3/4- |
1 |
1 |
1 |
1 |
пищи от |
1 (в |
|
|
|
|
суточного |
зависимости от |
|
|
|
|
объема (1) |
степени Г) |
|
|
|
|
Потребность |
0,7-1,5-2,0 (в |
4,0 |
4,0 |
4,0-4,5 |
4,0-4,5 |
в белках |
зависимости от |
|
|
|
|
(г/кг) |
степени Г) |
|
|
|
|
Потребность |
2,0-3,0-4,0 (в |
4,0-4,5 |
5,0-6,0 |
5,0-6,0 |
6,0-6,5 |
в жирах |
зависимости от |
|
|
|
|
(г/кг) |
степени Г) |
|
|
|
|
Потребность |
8,0-10,0-11,0 (в |
11,0- |
12,0- |
13,0-14,0 |
15,0- |
в углеводах |
зависимости от |
12,0 |
13,0 |
|
16,0 |
(г/кг) |
степени Г) |
|
|
|
|
Калорий- |
60-80-100 |
100- |
110- |
120-130 |
130- |
ность |
|
110 |
120 |
|
140 |
(ккал/кг) |
|
|
|
|
|
133
ΙΙΙ этап диетотерапии – этап усиленного питания продолжается до выведения ребенка из состояния Г. На выведение ребенка из Г уходит несколько недель.
Каждую неделю необходимо проводить коррекцию диеты, которая приближается к норме за счёт постепенного расширения ассортимента продуктов, увеличения суточного объёма, уменьшения числа кормлений.
Девятый шаг – сенсорная стимуляция и эмоциональная поддержка. Дети с Г нуждаются в хорошем уходе, ласковом обращении, массаже, ЛФК, регулярном купании, прогулках на свежем воздухе.
Десятый шаг - дальнейшая длительная реабилитация - предусматривает возвращение к рациональному питанию, согласно возрасту и утвержденных рекомендаций. В этом периоде необходимо продолжить сенсорную и эмоциональную поддержку, адекватную иммунопрофилактику, витаминную и минеральную коррекцию, по показаниям проводить стимулирующую терапию.
Большое внимание уделяется ферментотерапии. Используется Креон, абомин, панкреатин, фестал, панзинорм, мексаза и другие ферменты. Назначаются препараты, обладающие анаболическим эффектом: рибоксин, оротат калия, L-карнитин, перитол, анаболические гормоны (последние, под контролем костного возраста), апилак в свечах, инсулин с глюкозой. Среди лекарственных негормональных средств с анаболическим эффектом особое место занимают препараты, содержащие L-карнитин. Препарат применяется за 30 минут до еды детям до 1 года по 0,03-0,075 г 3 раза в сутки, от 1 года до 6 лет – по 0,1 г 2-3 раза в сутки. Продолжительность курса – 1 месяц.
При сопутствующем дисбиозе кишечника применяются биопрепараты: Биовестин, Ацилакт, Аципол, Бактиспорин, Бактисубтил, Биобактон, Биоспорин, Биофруктолакт, Бифацид, Бифидумбактерин сухой, Бифидумбактерин-форте, Бификол, Бифилин, Бифиформ, Дюфалак, Колибактерин, Линекс, Лактофильтрум, Примадофилюс, Нутри- лин-В, Флонивин БС.
В комплексном лечении этих детей используются витамины (особенно токоферол, фолиевая кислота, один из препаратов витамина В12 - кобамамид);
витамино-минеральные комплексы: Алвитал, Алфавит, Биовиталь гель, Веторон Вибовит, Бэби Мультитабс, Бэби Мультитабс Малыш, Пангексавит, Пиковит, Центрум детский + Са, Центрум детскийэкстраватамин С, Юникап Ю.
Осложнения. Задержка физического и нервно-психического развития ребенка. Инфекционные осложнения (пневмонии, бронхиты, ОРИ,
134

кишечные инфекции, отиты и др.), баллонная и жировая дистрофия печения, развитие мальдигистии и мальабсорбции, гиповолемический шок, сердечно-сосудистая недостаточность, синдром внезапной смерти.
Профилактика Г у детей должна начинаться с укрепления здоровья женщины до беременности и во время беременности. При развитии Г у плода проводится её лечение с использованием сигетина, β- симпатомиметиков, эстрогенов, диатермии, сосудорасширяющих препаратов, улучшающих маточно-плацентарное кровообращение, а также мембраностабилизирующих средств. В профилактике постнатальной Г большое значение имеет рациональное естественное вскармливание, организация правильного режима и ухода за ребёнком, предупреждение и своевременное лечение заболеваний, осложняющихся развитием Г. Г – социальная болезнь, и, следовательно, для ее профилактики важны повышение уровня жизни населения и доступность медицинской помощи для всех слоев населения.
Вопросы к экзамену. Хронические расстройства питания. Классифи-
кация. Этиология. Патогенез. Клиническая картина. Диагностика. Дифференциальный диагноз. Осложнения. Лечение. Диетотерапия. Использование специальных лечебных продуктов питания. Профилактика.
Глава V. Рахит, нарушение фосфорно-кальциевого обме-
на
РАХИТ (Р). В настоящее время под Р понимают нарушение ми-
нерализации растущей кости, обусловленное временным несоответствием между потребностями растущего организма в фосфатах и каль-
ции и недостаточностью систем, обеспечивающих их доставку в организм ребенка. Р является самым частым заболеванием, связанным с нарушением фосфорно-кальциевого гомеостаза, у детей 1-го года жиз-
ни. Р и гиповитаминоз D это неоднозначные понятия!
В Международной классификации болезней 10-го пересмотра (МКБ-10) Р включен в раздел болезней эндокринной системы и обмена веществ (шифр Е55.0). При этом не отрицается значение гиповитаминоза D в его развитии.
Развитие костных признаков Р у детей раннего возраста обусловлено быстрыми темпами роста, высокой скоростью моделирования скелета и дефицитом в растущем организме фосфатов и кальция при не-
135
совершенстве путей их транспорта, метаболизма и утилизации (гетерохрония созревания). Поэтому в настоящее время Р относят к пограничным состояниям.
Эпидемиология. Частота Р у детей остается неизученной в связи с изменениями представлений о характере данной патологии. При исследовании уровня кальцитриола у детей с клиникой Р снижение уровня витамина D в крови было выявлено только у 7,5% обследованных детей. По данным современных авторов Р встречается у детей раннего возраста с частотой от 1,6 до 35%.
Факторы, способствующие развитию Р:
1.Высокие темпы роста и развития детей, повышенная потребность
вминеральных компонентах (особенно у недоношенных детей);
2.Дефицит кальция и фосфатов в пище;
3.Нарушение всасывания кальция и фосфатов в кишечнике, повышенное выделение их с мочой или нарушение утилизации их в кости;
4.Снижение уровня кальция и фосфатов крови при длительном алкалозе, дисбалансе цинка, магния, стронция, алюминия, обусловленных различными причинами;
5.Экзогенный и эндогенный дефицит витамина D;
6.Сниженная двигательная и опорная нагрузка;
7.Нарушение физиологического соотношения остеотропных гормонов - паратгормона и кальцитонина.
Этиология
Фосфорно-кальциевый обмен в организме обусловлен:
1.всасыванием фосфора и кальция в кишечнике;
2.взаимообменом их между кровью и костной тканью;
3.выделением кальция и фосфора из организма – реабсорбция в почечных канальцах.
Все факторы, приводящие к нарушению обмена кальция, частично компенсируются вымыванием кальция из костей в кровь, что приводит
кразвитию остеомаляции или остеопорозов.
Суточная потребность в кальции детей грудного возраста равна 50 мг на 1 кг массы. Важнейшим источником кальция являются молочные продукты. Всасывание кальция в кишечнике зависит не только от его количества в пище, но и от его растворимости, соотношения с фосфором (оптимальное 2:1), присутствия желчных солей, уровня pH (чем более выражена щелочная реакция, тем хуже всасывание). Главным регулятором всасывания кальция является витамин D.
Основная масса (более 90%) кальция и 70% фосфора находится в костях в виде неорганических солей. В течение всей жизни костная ткань находится в постоянном процессе созидания и разрушения, обу-
136
словленном взаимодействием трех типов клеток: остеобластов, остеоцитов и остеокластов. Кости активно участвуют в регуляции метаболизма кальция и фосфора, поддерживая их стабильный уровень в крови. При снижении уровня кальция и фосфора крови (произведение Ca
× P является постоянной величиной и равно 4,5-5,0) развивается резорбция кости за счет активации действия остеокластов, что увеличивает поступление в кровь этих ионов; при повышении данного коэффициента происходит избыточное отложение солей в кости.
Половина содержащегося в крови кальция связана с белками плазмы (главным образом с альбумином). Связанный с белками плазмы кальций является резервом для сохранения необходимого уровня ионизированного кальция.
Выделение кальция и фосфора почками идет параллельно содержанию их в крови. При нормальном содержании кальция его выделение с мочой незначительное, при гипокальциемии это количество резко уменьшается, гиперкальциемия увеличивает содержание кальция в моче.
Основными регуляторами фосфорно-кальциевого обмена наряду с
витамином D являются паратиреоидный гормон (ПГ) и кальцитонин
(КТ) – гормон щитовидной железы.
Под названием «витамин D» понимают группу веществ (около 10), содержащихся в продуктах растительного и животного происхождения, обладающих влиянием на фосфорно-кальциевый обмен. Наиболее активными из них являются эргокальциферол (витамин D2) и холекальциферол (витамин D3). Эргокальциферол в небольших количествах содержится в растительном масле, ростках пшеницы; холекальциферол – в рыбьем жире, молоке, сливочном масле, яйцах. Физиологическая суточная потребность в витамине D величина достаточно стабильная и составляет 400-500 МЕ. В период беременности и кормления грудным молоком она возрастает в 1,5, максимум в 2 раза.
137

Рис. 1.19. Схема регуляции фосфорно-кальциевого обмена в орга-
низме
Нормальное обеспечение организма витамином D связано не только с поступлением его с пищей, но и с образованием в коже под влиянием УФ-лучей. При этом из эргостерола (предшественник витамина D2) образуется эргокальциферол, а из 7-дегидрохолестерола (предшественник витамина D3) – холекальциферол.
138

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
25-гидроксилаза |
|
|
|
|
||||||
|
|
печень |
|
|
|
|
|
25(ОН)D-кальцифедеол |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
почки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
кальцифедеол |
|
|
|
|
|
1-ά-гидроксилаза |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
1,15(ОН)2-витамин-D-гормон - Кальцитриол |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
Низкий уровень |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
кальция в крови |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
Комплекс: кальцитриол + альфа-глобулин |
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Транспортная форма → активные метаболиты вита- |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мина D: кальцитриол, 24, 25-диоксикальциферол |
|
|||||||||||||||
|
|
Обеспечение мине- |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
рализации скелета |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Обеспечение мышечной |
|
|
|
Предотвращение |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
деятельности |
|
|
|
тетании |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
Взаимодействие с |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
рецепторами клеток- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
Участие в сокращении мышц |
|
|
|
|
|
|
|
||||||||||||||||||
|
|
мишеней |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
Образование комплекса: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мобилизация |
|
|||||||||||||
|
|
рецептор + кальцитриол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кальция из костей |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
Синтез белка |
|
|
|
|
|
|
Щелочная фосфатаза |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рассасывание |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
диафиза кости |
|
|||
|
БСК |
|
|
|
коллаген |
|
|
|
|
|
|
|
Синтез белковой |
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
стромы кости |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
Реабсорбция |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Захват |
|
|
кальция, фос- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
Минерализация скеле- |
|
|
|
|
|
|
|||||||||||||||||||
|
кальция из |
|
|
фора, амино- |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
кишечника |
|
|
кислот, цитра- |
|
|
|
|
|
|
та |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
тов в почках |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 1.20. Биотрансформация витамина D
При достаточной инсоляции (достаточно 10-минутного облучения кистей рук) в коже синтезируется необходимое организму количество витамина D. При недостаточной естественной инсоляции: климатогеографические особенности, условия проживания (сельская местность или промышленный город), бытовые факторы, время года и др. недостающее количество витамина D должно поступать с пищей или в виде лекарственных препаратов. У беременных женщин витамин D откладывается в виде депо в плаценте, что обеспечивает новорожденного некоторое время после рождения антирахитическими веществами.
Витамины D2 и D3 обладают очень малой биологической активностью. Физиологическое действие на органы-мишени (кишечник, кости, почки) осуществляется их метаболитами, образующимися в печени и
139
почках в результате ферментативного гидроксилирования. В печени под влиянием гидроксилазы образуется 25гидроксихолекальциферол 25(OH)D3-кальцидиерол. В почках в результате еще одного гидроксилирования синтезируется дигидроксихолекальциферол – 1,25-(OH)2D3- кальцитриерол, являющийся наиболее активным метаболитом витамина D. Кроме этих двух основных метаболитов в организме синтезируются другие соединения витамина D3 – 24,25(OH)2D3, 25,26(OH)2D3, 21,25(OH)2D3, действие которых изучено недостаточно.
Основная физиологическая функция витамина D (т.е. его активных метаболитов) в организме – регуляция и поддержание на необходимом уровне фосфорно-кальциевого гомеостаза организма. Это обеспечивается путем его влияния на всасывание кальция в кишечнике, на отложение его солей в костях (минерализация костей) и реабсорбцию кальция и фосфора в почечных канальцах.
Механизм всасывания кальция в кишечнике связан с синтезом энтероцитами белка связывающего кальций (БСК). Синтез БСК индуцируется кальцитриолом через генетический аппарат клеток, т.е. по механизму действия 1,25(OH)2D3 аналогичен гормонам.
В условиях гипокальциемии витамин D временно увеличивает резорбцию костной ткани, усиливает всасывание кальция в кишечнике и реабсорбцию его в почках, повышая тем самым уровень кальция в крови. При нормокальциемии он активирует деятельность остеобластов, снижает резорбцию кости и ее кортикальную порозность.
В последние годы показано, что клетки многих органов имеют рецепторы к кальцитриолу, который тем самым участвует в универсальной регуляции ферментных внутриклеточных систем. Активация соответствующих рецепторов через аденилатциклазу и ц-АМФ мобилизует кальций и его связь с белком-кальмодулином, что способствует передаче сигнала и усиливает функцию клетки, и соответственно, всего органа.
Витамин D стимулирует реакцию пируват-цитрат в цикле Кребса, обладает иммуномодулирующим действием, регулирует уровень секреции тиреотропного гормона гипофиза, прямо или опосредованно (через кальциемию) влияет на выработку инсулина поджелудочной железой.
Вторым важнейшим регулятором фосфорно-кальциевого обмена является паратгормон (ПГ). Продукция данного гормона паращитовидными железами усиливается при наличии гипокальциемии, и, особенно, при снижении в плазме и внеклеточной жидкости концентрации ионизированного кальция. Основными органами-мишенями для пара-
140
тгормона являются почки, кости и в меньшей степени желудочнокишечный тракт.
Действие паратгормона на почки проявляется увеличением реабсорбции кальция и магния. Одновременно снижается реабсорбция фосфора, что приводит к гиперфосфатурии и гипофосфатемии. Считается также, что паратгормон повышает способность образования в почках кальцитриола, усиливая тем самым абсорбцию кальция в кишечнике.
В костной ткани под влиянием паратгормона кальций костных апатитов переходит в растворимую форму, благодаря чему происходит его мобилизация и выход в кровь, что сопровождается развитием остеомаляции и даже остеопороза. Таким образом, паратгормон является основным кальцийсберегающим гормоном. Он осуществляет быструю регуляцию гомеостаза кальция, постоянная регуляция обмена кальция
– функция витамина D и его метаболитов. Образование ПГ стимулируется гипокальциемией, при высоком уровне кальция в крови его продукция уменьшается.
Третьим регулятором кальциевого обмена является кальцитонин (КТ) – гормон, вырабатываемый С-клетками парафолликулярного аппарата щитовидной железы. По действию на гомеостаз кальция он является антагонистом паратгормона. Его секреция усиливается при повышении уровня кальция в крови и уменьшается при понижении. Диета с большим количеством кальция в пище также стимулирует секрецию кальцитонина. Этот эффект опосредуется глюкагоном, который таким образом является биохимическим активатором выработки КТ. Кальцитонин защищает организм от гиперкальциемических состояний, снижает количество и активность остеокластов, уменьшая рассасывание костей, усиливает отложение кальция в кости, предотвращая развитие остеомаляции и остеопороза, активирует выведение его с мочой. Предполагается возможность ингибирующего влияния КТ на образование в почках кальцитриола.
На фосфорно-кальциевый гомеостаз, кроме трех выше описанных (витамин D, паратгормон, кальцитонин), оказывает влияние множество других факторов. Микроэлементы Mg, Al являются конкурентами кальция в процессе всасывания; Ba, Pb, Sr и Si могут замещать его в солях, находящихся в костной ткани; гормоны щитовидной железы, соматотропный гормон, андрогены активируют отложение кальция в кости, снижают его содержание в крови, глюкокортикоиды способствуют развитию остеопороза и вымыванию кальция в кровь; витамин А является антагонистом витамина D в процессе всасывания в кишечнике. Однако негативное влияние этих и многих других факторов на
141
фосфорно-кальциевый гомеостаз проявляется, как правило, при значительных отклонениях содержания этих веществ в организме. Регуляция фосфорно-кальциевого обмена в организме представлена на рис
1.19.
Патогенез
Основными механизмами патогенеза Р являются:
1.Нарушение всасывания кальция и фосфатов в кишечнике, повышенное выделение их с мочой или нарушение утилизации их в кости.
2.Снижение уровня кальция и фосфатов в крови и нарушение минерализации кости. Этому способствуют: длительный алкалоз, дефицит цинка, магния, стронция, алюминия.
3.Нарушение физиологического соотношения остеотропных гомонов – паратгормона и кальцитонина.
4.Экзо- и эндогенный дефицит витамина D, а также более низкий уровень метаболита витамина D. Этому способствуют: заболевания почек, печени, кишечника, дефекты питания.
Нарушения фосфорно-кальциевого обмена у детей раннего возраста чаще всего проявляются гипокальциемиями различного про-
исхождения с клиническими проявлениями со стороны костно-
мышечной системы. Наиболее частым заболеванием является Р. Причиной гипокальциемии может быть дефицит витамина D и нарушения его метаболизма, обусловленные временной незрелостью ферментных систем органов (почки, печень), регулирующих этот процесс. Реже встречаются первичные генетически детерминированные заболевания почек, желудочно-кишечного тракта, паращитовидных желез, костной системы, сопровождающиеся нарушениями фосфорнокальциевого гомеостаза со сходной клинической картиной.
Классификация (см. табл. 1.40).
Табл. 1.40. Классификация рахита
Степень тяжести |
Период болезни |
Характер течения |
1-я (легкая) |
Начальный |
Острое |
2-я (средней тя- |
Разгара |
Подострое |
жести) |
Реконвалесценции |
Рецидивирующее (прак- |
3-я (тяжелая) |
Остаточных явлений |
тически не встречается) |
Исследования: общий анализ крови и мочи, щелочная фосфатаза крови, кальций и фосфор крови, рентгенография костей.
142
Клиника. В настоящее время считают, что у детей при Р I степени обязательным является только наличие костных изменений. Т.О. ранее описываемые при этой степени тяжести рахита неврологические изменения к Р не относятся.
Для Р II степени характерны выраженные изменения со стороны костей: лобные и теменные бугры, четки, деформация грудной клетки, часто варусная деформация конечностей. Рентгенологически отмечается расширение метафизов трубчатых костей их чашеобразная деформация.
Для Р III степени характерны грубые деформации черепа, грудной клетки, нижних конечностей, задержка развития статических функций. Кроме этого определяются: одышка, тахикардия, увеличение печени.
Начальные признаки Р – размягчение краев большого родничка, краниотабес. Вопрос о так называемых начальных признаках Р в виде потливости, беспокойства, вздрагивания и др. окончательно не решен.
Период разгара – признаки остеомаляции костей или остеоидной гиперплазии, остеопороз. Наиболее выраженные клинические и рентгенологические изменения совпадают с выраженной гипофосфатемией.
Период реконвалесценции – обратное развитие клиники Р. При рентгенологическом исследовании появляется четкая линия обызвествления, в метафизарной зоне, нормализуется уровень фосфатов, сохраняется небольшая гипокальциемия, и умеренное повышение уровня щелочной фосфатазы.
Течение Р – острое и подострое, При остром течении преобладают проявления остеомаляции, а при подостром течении – остеоидной гиперплазии. Проявлениями остеомаляции являются: размягчение краев большого родничка, краниотабес, рахитический кифоз, искривление конечностей, рахитическая деформация грудной клетки.
К признакам остеоидной гиперплазии относят: рахитические четки, лобные и затылочные бугры, «нити жемчуга» и др.
Диагноз. В амбулаторных условиях для постановки диагноза Р достаточно клинических проявлений.
Лабораторное подтверждение Р I степени – небольшая гипофос-
фатемия и повышение активности щелочной фосфатазы.
Лабораторное подтверждение Р II степени – снижение уровня фосфатов, кальция, повышение активности щелочной фосфатазы.
Лабораторное подтверждение Р III степени – при рентгенологи-
ческом исследовании отмечается грубая перестройка рисунка и развития костей, расширение и размытость зоны метафизов, возможны пе-
143

реломы или смещения. В крови определяются выраженные снижение уровней фосфатов и кальция, повышение уровня щелочной фосфатазы.
Единственным надежным признаком диагностики Р является снижение уровня витамина D в крови (определение уровня 25-ОН-D3).
Дифференциальный диагноз Р проводят с: D-резистентными формами рахита, D-зависимыми формами рахита I и II типа, фосфатдиабетом, синдромом де Тони-Дебре-Фанкони, почечным тубулярным ацидозом, остеопорозом.
Табл. 1.41. Дифференциальный диагноз рахита
Признаки |
Витамин D- |
Фосфат- |
Почечный |
Болезнь де- |
|
дефицитный |
диабет |
тубуляр- |
Тони-Дебре- |
|
рахит |
|
ный ацидоз |
Фанкони |
Тип насле- |
Нет |
Доминант- |
Возможно |
аутосомно- |
дования |
|
ный. Сцеп- |
аутосомно- |
рецессив- |
|
|
ленный с Х- |
рецессив- |
ный или |
|
|
хромосомой |
ный или |
аутосомно- |
|
|
|
аутосомно- |
доминант- |
|
|
|
доминант- |
ный |
|
|
|
ный |
|
Сроки ма- |
1,5-3 меся- |
Старше 1 |
6 мес-2 года |
Старше 1-2- |
нифеста- |
ца |
года |
|
лет |
ции |
|
|
|
|
Первые |
Поражение |
Выражен- |
Полиурия, |
Беспричин- |
клиниче- |
костной |
ная дефор- |
полидип- |
ные повы- |
ские про- |
системы |
мация ниж- |
сия, плак- |
шения тем- |
явления |
|
них конеч- |
сивость, |
пературы, |
|
|
ностей, |
боли в |
полиурия, |
|
|
браслеты, |
мышцах, |
полидип- |
|
|
гипотония, |
гипотония |
сия, боли в |
|
|
|
|
мышцах |
Специфи- |
Краниота- |
Прогресси- |
Полиурия, |
Лихорадка, |
ческие |
бес, лобные |
рующая |
полидип- |
прогресси- |
признаки |
и затылоч- |
варусная |
сия, гипо- |
рующие |
|
ные бугры, |
деформация |
тония до |
множест- |
|
браслетки, |
конечно- |
атонии, |
венные ко- |
|
деформация |
стей |
адинамия, |
стные де- |
|
конечно- |
|
увеличение |
формации, |
|
стей |
|
печени, |
увеличение |
|
|
|
запоры, |
печени, |
144
|
|
|
вальгусная |
снижение |
|
|
|
деформация |
АД, запоры |
|
|
|
голеней |
|
Физиче- |
Без особен- |
Дефицит |
Снижение |
Снижение |
ское раз- |
ностей |
роста при |
роста и |
роста и |
витие |
|
нормальной |
массы |
массы |
|
|
массе |
|
|
Кальций |
снижен |
Норма |
Норма |
Чаще норма |
крови |
|
|
|
|
Фосфор |
снижен |
Резко сни- |
снижен |
Резко сни- |
|
|
жен |
|
жен |
Калий |
норма |
норма |
снижен |
снижен |
Натрий |
Норма |
норма |
снижен |
снижен |
КОС |
Чаще аци- |
Метаболи- |
Резкий ме- |
Резкий ме- |
|
доз |
ческий аци- |
таболиче- |
таболиче- |
|
|
доз |
ский ацидоз |
ский ацидоз |
Аминоаци- |
есть |
норма |
норма |
выражена |
дурия |
|
|
|
|
Фосфату- |
есть |
Резко вы- |
умеренная |
выраженная |
рия |
|
ражена |
|
|
Кальциу- |
снижена |
норма |
значитель- |
значитель- |
рия |
|
|
ная |
ная |
Рентгено- |
Бокаловид- |
Грубые бо- |
Острый |
Остеопороз, |
грамма |
ные расши- |
каловидные |
системный |
трабеку- |
костей |
рения ме- |
расширения |
остеопороз. |
лярная ис- |
скелета |
тафизов |
метафизов, |
Нечеткость |
черчен- |
|
|
утолщение |
контуров |
ность в |
|
|
коркового |
метафизов, |
дистальных |
|
|
слоя перио- |
концентри- |
и прокси- |
|
|
ста |
ческая ат- |
мальных |
|
|
|
рофия кос- |
отделов |
|
|
|
ти |
диафизов |
Эффект от |
Хороший |
Удовлетво- |
Незначи- |
Удовлетво- |
лечения |
эффект |
рительный |
тельный |
рительный |
витамином |
|
эффект при |
|
эффект при |
D |
|
высоких |
|
высоких |
|
|
дозах |
|
дозах |
Остеопороз – снижение костной массы и нарушение структуры костной ткани – может быть связан не только с Р, но и с другими факто-
145
рами. Причинами остеопороза являются: эндокринно -метаболические нарушения; нарушения питания и пищеварения; применение ряда лекарственных препаратов (гормоны, противосудорожные, антациды, гепарин); генетические факторы (несовершенный остеогенез, синдром Марфана, гомоцистинурия); длительная иммобилизация; злокачественные опухоли; хроническая почечная недостаточность. В этих случаях диагноз Р неправомерен, несмотря на клиническую схожесть.
Лечение. Задачи лечения: восстановление дефицита витамина D в организме, коррекция нарушения фосфорно-кальциевого обмена, купирование проявлений Р (деформация костей, мышечная гипотония, дисфункции внутренних органов).
Схема лечения. Обязательные мероприятия: препараты витамина
D, режим, солнечные и воздушные процедуры.
Вспомогательное лечение: диета, витаминотерапия, водные процедуры, массаж препараты кальция.
Показания для госпитализации: необходимость углубленного обследования (проведение дифференциального диагноза), отсутствие эффекта от назначения препаратов витамина D.
Режим, соответствующий возрасту ребенка, длительное пребывание на воздухе с достаточной инсоляцией (не менее 2-3 часов ежедневно).
Диета - естественное вскармливание, при искусственном вскармливании использование адаптированных смесей, соответствующих возрасту ребенка. Важным является своевременное введение прикормов.
Табл. 1.42. Лекарственные препараты витамина D
Наименование препарат |
|
Содержание |
|
|
витамина D |
Аквадетрим Витамина D3, Водный рас- |
1 |
мл – 30 капель; 1 капля – |
твор |
500 МЕ |
|
Видехол, масляный раствор D3, 0,125% |
1 |
капля 500 МЕ |
Видехол, масляный раствор, 0,25% |
1 |
капля -1000 МЕ |
Раствор эргокальциферола (витамина |
1 |
капля – 625 МЕ |
D2) масляный р-р, 0,0625% |
|
|
Раствор эргокальциферола (витамин |
1 |
капсула – 500 МЕ |
D2) в масле в капсулах |
|
|
Драже эргокальциферола (витамина D2) |
1 |
драже – 500 МЕ |
Раствор эргокальциферола (витамин D2 |
1 |
капле – 1250 МЕ |
146
в масле, 0,125% |
|
|
Раствор эргокальциферола (витамин D2 |
1 |
капля - 5000 МЕ |
в масле, 0,5% |
|
|
Оксидевит (кальцитриол, 1,25(ОН)2D2 |
1 |
капсуле – 1 мкг 0,00025 мг |
Рыбий жир в капсулах (Норвегия), |
1 |
капсула – 52 МЕ |
Меллер |
|
|
В настоящее время практически все педиатры согласились с тем, что специфическое лечение Р целесообразно проводить малыми лечебными дозами витамина D. Суточная доза витамина D при I-II степени Р при этом составляет 1500-2000 МЕ, курс – 100000–150000 МЕ;
при II-III степени – 3000-4000 МЕ, курс 200000-400000 МЕ. Это лече-
ние проводится в период разгара, подтвержденного биохимическими данными (снижение в крови кальция и фосфора, повышение щелочной фосфатазы). По окончании курса при необходимости целесообразно перейти на профилактическую (физиологическую) дозу витамина D. Рекомендованные в прошлом ударный, полуударный методы, повторные лечебные курсы в настоящее время не используются. При проведении специфической терапии следует осуществлять контроль за уровнем кальция в крови путем регулярной (1 раз в 10-14 дней) постановки реакции Сулковича (степень кальциурии).
Табл. 1.43. Современные кальцийсодержащие препараты
Название |
Содержание Ca |
Страна производитель |
Препараты, содержащие карбонат кальция |
||
УПСАВИТ кальций |
1250 |
Франция |
Аддитива кальций |
1250 |
Польша |
Кальций-D3-Никомед |
1250+D3 200 ед. |
Норвегия |
Витрум кальций |
1250+D3 200 ед. |
США |
Идеос |
1250+D3 400 ед. |
Франция |
Витакальцин |
624 |
Словакия |
Остеокеа |
1000 |
Великобритания |
Ca-Сандос форте |
1250 |
Швейцария |
|
Комплексные препараты |
|
Остеогенон |
Са 178, Р 82, факторы |
Франция |
|
роста |
|
Витрум остеомаг |
Ca, Mg, Zn, Cu, D3 |
США |
Берокка Ca и Mg |
Ca, Mg и витамины |
Швейцария |
Кальций СЕДИКО |
Ca, D3, вит. С |
Египет |
147
Кальцинова |
Ca, P, вит. D, А, С, В6 |
Словения |
Препараты кальция показаны недоношенным, детям, находящимся на естественном вскармливании, курсами по 2-3 недели. Дозу подбирают в зависимости от возраста, тяжести Р и степени обменных нарушений.
Препараты витамина D целесообразно сочетать с витаминами
группы В (В1, В2, В6), С, А, Е.
Для уменьшения выраженности вегетативных расстройств показано применение препаратов калия и магния (панангин, аспаркам) из расчета 10 мг/кг/сут на протяжении 3-4 недель.
Профилактика. В настоящее время неспецифическая антенатальная профилактика Р заключается в создании беременной женщине оптимальных условий для роста и развития плода: рациональное питание с достаточным поступлением не только белков, жиров, углеводов, но и микро- и макроэлементов (в том числе кальция и фосфора), витаминов (в том числе витамина D); запрещение беременной принимать токсические (особенно для плода) вещества – табак, алкоголь, наркотики; исключение возможностей контактов беременной с другими токсическими веществами – химические, лекарства, пестициды и пр. Беременная женщина должна вести физически активный образ жизни, максимально возможно (не менее 4-5 часов в сутки) быть на свежем воздухе, соблюдать режим дня с достаточным отдыхом днем и ночью. В этом случае нет необходимости дополнительного назначения беременной витамина D.
Антенатальная специфическая профилактика Р путем назначения 200-400 МЕ витамина D в сутки с 32 недели беременности в течение 8 недель (проводить только в зимний или весенний период года). Беременным из группы риска специфическая профилактика Р проводится независимо от сезона года.
Постнатальная неспецифическая профилактика Р включает в себя: естественное вскармливание; своевременное введение прикорма (лучше начинать с овощного пюре), соков; ежедневное пребывание на свежем воздухе, свободное пеленание, массаж, гимнастика, световоздушные и гигиенические ванны.
Физиологическая потребность ребенка в витамине D составляет 200 МЕ в сутки.
Постнатальная специфическая профилактика Р проводится детям только в период поздняя осень – ранняя весна в дозе 400 МЕ в сутки, начиная с 4-х недельного возраста. Дополнительное введение витамина D на 2-м году жизни нецелесообразно. Смеси, используемые при
148

искусственном вскармливании, содержат все необходимые витамины и микроэлементы в физиологических дозах, в связи с чем нет необходимости в дополнительном введении витамина D. Детям с малыми размерами родничка предпочтительнее использовать неспецифические методы профилактики Р.
Для недоношенных детей вопрос о профилактическом назначении витамина D должен решаться только после оптимизации потребления с пищей кальция и фосфора. Установлено, что у недоношенных детей гиповитаминоз D практически не выявляется. В развитии остеопении у них решающее значение имеет дефицит кальция и фосфатов. Традиционно считают, что профилактическая доза витамина D для недоношенных детей составляет 400-1000 МЕ в сутки.
Вопросы к экзамену. Рахит. Этиология. Патогенез. Классификация.
Клиническая картина. Диагностика. Дифференциальный диагноз. Лечение. Профилактика.
СПАЗМОФИЛИЯ (С) - своеобразное состояние детей раннего возраста, имеющих признаки рахита, обусловленное нарушением минерального обмена, гипофункцией паращитовидных желез, проявляющееся признаками повышенной нервно-мышечной возбудимости и наклонностью к судорогам.
Эпидемиология. С встречается почти исключительно у детей в возрасте первых 2-х лет, примерно у 3,5-4% всех детей.
Патогенез. Нарушения минерального обмена при С выражены более резко, чем при рахите и характеризуются некоторыми особенностями. Показателями изменений обмена являются гипокальциемия, резкая гипофосфатемия, гипомагниемия, гипонатриемия, гипохлоремия, гиперкалиемия и алкалоз. Дефицит кальция развивается за счет снижения содержания свободного и связанного кальция. Основными обменными нарушения при С являются гипокальциемия и алкалоз, которые объясняются снижением функции паращитовидных желез. Основные клинические проявления С (спазмы и судороги) объясняются резким недостатком кальция и вызванной этим повышенной возбудимостью нервов. Дополнительными факторами, способствующими возникновению судорог, считают недостаток натрия и хлора, а также выраженный недостаток магния и повышенную концентрацию калия (т.к. натрий понижает возбудимость нервно-мышечной системы). Возникновение судорог можно объяснить и недостатком витамина В1, который имеется при С. При его выраженном дефиците возникают резкие нарушения в гликолитической цепи с образованием пировино-
149
градной кислоты, которая играет большую роль в возникновении судорог.
С встречается в любые сезоны года, но чаще развивается весной. Провоцировать приступ С могут развитие какого-либо заболевания
с высокой температурой, частая рвота при желудочно-кишечных болезнях, а так же сильный плач, возбуждение, испуг и др. При этих с о- стояниях может наступить сдвиг в кислотно-щелочном равновесии в сторону алкалоза, с созданием условий для проявлений С.
Классификация (Е.М. Лепский, 1945):
1.Скрытая форма;
2.Явная форма (ларингоспазм, карпо-педальный спазм, эклампсия).
Исследования. Определение содержания кальция и фосфора плазмы крови; определение активности щелочной фосфатазы плазмы крови, исследование КОС, ЭКГ.
Анамнез, клиника. В анамнезе при С можно выявить раннее неправильное искусственное вскармливание, злоупотребление коровьим молоком, мучными продуктами, отсутствие профилактики рахита. Приступ С провоцируют лихорадочные состояния, частая рвота при желудочно-кишечных заболеваниях, испуг, возбуждение, сильный плач, повышенная ультрафиолетовая радиация.
У ребенка со С при осмотре должны быть выявлены признаки рахита.
Признаки скрытой С (симптомы повышенной возбудимости нерв- но-мышечного аппарата):
а) симптом Хвостека - легкое поколачивание по месту выхода лицевого нерва (между скуловой дугой и углом рта) вызывает сокращение или подергивание мышечной мускулатуры соответствующей стороны лица;
б) перонеальный симптом Люста - поколачивание позади и не-
много ниже головки малоберцовой кости вызывает тыльное сгибание и отведение стопы кнаружи;
в) симптом Труссо - сдавление сосудисто-нервного пучка на плече вызывает судорожное сокращение мышц кисти – «рука акушера»;
г) симптом Маслова - укол в пятку вызывает остановку дыхания вместо его учащения (проводится под контролем пневмограммы);
д) Симптом Эрба - размыкание катода, приложенного к срединному нерву, вызывает мышечное сокращение при силе тока менее 5 мА.
Признаки явной С:
а) ларингоспазм - внезапное затруднение на вдохе с появлением своеобразного шумного дыхания. При более выраженном сужении
150

голосовой щели - испуганное выражение лица, ребенок раскрытым ртом «ловит воздух», цианоз кожи, холодный пот на лице и туловище. Спустя несколько секунд появляется шумный вдох и восстанавливается нормальное дыхание. Приступы ларингоспазма могут повторяться в течение дня;
б) карпо-педальный спазм - тоническое сокращение мышц конечностей, особенно в кистях и стопах, от нескольких минут до нескольких дней, которые могут рецидивировать. При длительном спазме на тыле кистей и стоп появляется упругая отечность.
Спастическое состояние может распространяться и на другие группы мышц: глазные, жевательные (временное косоглазие или тризм), прогностически неблагоприятны спазмы дыхательных мышц (инспираторные или экспираторные апноэ), реже - спастическое состояние сердечной мышцы (остановка сердца и внезапная смерть). Встречаются спазмы гладкой мускулатуры внутренних органов, что приводит к расстройству мочеиспускания, дефекации;
в) эклампсия - клонико-тонические судороги с вовлечением в процесс поперечно-полосатых и гладких мышц всего тела; приступ начинается с подергиваний мимических мышц, затем присоединяются судорожные сокращения конечностей, дыхательных мышц, возникает цианоз. Сознание теряется обычно в начале приступа. Продолжительность приступа от нескольких минут до нескольких часов. Тонические и клонические судороги могут быть изолированными, сочетанными или последовательными. Клонические судороги чаще наблюдаются у детей на первом году жизни, тонические - у детей старше года.
Диагноз С основывается на выявлении у ребенка с рахитом признаков явной или скрытой С.
Лабораторные данные: а) биохимическое исследование крови - гипокальциемия (до 1,2-1,5 ммоль/л) на фоне относительно повышенного уровня неорганического фосфора.
б) увеличение цифр числителя или уменьшение знаменателя в форму-
ле Дьердя: |
Р04 -- НС03 –К+ |
|
Са++ Mg++ H+ |
Дифференциальный диагноз С проводят с заболеваниями, проявляющимися гипокальциемией: хронической почечной недостаточностью, гипопаратиреозом, синдромом мальабсорбции, приемом препаратов, снижающих уровень кальция
Табл. 1.44. Дифференциальный диагноз спазмофилии
Признак |
Спазмофи- |
Гипопа- |
ХПН |
Синдром маль- |
151
|
лия |
ратиреоз |
|
абсорбции |
Судороги |
Да |
Да |
+/- |
Возможны |
Рахитиче- |
Характерно |
Нет |
Остео- |
Остеопороз |
ские измене- |
|
|
пороз |
|
ния костей |
|
|
|
|
Хрониче- |
нет |
нет |
+/- |
характерно |
ская диарея |
|
|
|
|
Ув. мочеви- |
Нет |
Нет |
Да |
Нет |
ны, креати- |
|
|
|
|
нина |
|
|
|
|
Симптомы |
Да |
Да |
Да |
Да |
повышенной |
|
|
|
|
нервно- |
|
|
|
|
мышечной |
|
|
|
|
возбудимо- |
|
|
|
|
сти |
|
|
|
|
Уровень |
Нет |
Нет |
Нет |
Да |
ПТГ↓, фос- |
|
|
|
|
фор ↑ |
|
|
|
|
Кальций |
Да |
Да |
Да |
Да |
крови ↓ |
|
|
|
|
Лечение. Задачи лечения: нормализация нервно-мышечной возбудимости, показателей минерального обмена; купирование судорог и других проявлений С, лечение рахита.
Схема терапии
Обязательные мероприятия: купирование гипокальциемии, посиндромная терапия проявлений С, лечение рахита.
Вспомогательные методы лечения: режим, диета, витаминотера-
пия.
Показания для госпитализации: судороги, эклампсия, ларингос-
пазм.
Режим: максимально ограничить или крайне осторожно выполнять неприятные для ребенка процедуры.
Диета: исключение коровьего молока на 3-5 дней, углеводистое питание, постепенный переход на сбалансированную, соответствующую возрасту пищу.
При эклампсии: хлорид или глюконат кальция 10% раствор, 2-3 мл, внутривенно микроструйно. Оксибутират натрия 50-100 мг/кг внутривенно медленно или дроперидол 0,25% раствор 0,1 мг/кг, внутривенно медленно или седуксен 0,5% раствор, 0,15 мг/кг, внутримышечно или
152

внутривенно, или сернокислая магнезия 25% раствор, 0,8 мл/кг, внутримышечно, но не более 8,0 мл.
При карпо-педальном спазме: внутрь хлорид или глюконат кальция, фенобарбитал, бромиды.
При ларингоспазме: брызнуть на больного холодной водой, надавить пальцем на корень языка, по показаниям - искусственное дыхание, медикаментозная терапия, как при эклампсии.
После оказания неотложной помощи: препараты кальция внутрь,
хлористый аммоний 10% раствор, 1 ч.л. 3 раза в день, витамин D 4000 ME ежедневно с 4-5 дня; витаминотерапия.
Профилактика С в первую очередь связана с выявлением и лечением рахита. Важным является рациональное вскармливание ребенка. Особое внимание обратить на раннее введение в питание продуктов коровьего молока. Необходимо не допускать сильный плач, испуг.
Вопросы к экзамену. Спазмофилия как синдром гипокальциемии на
фоне острого рахита. Патогенез. Клиническая картина. Диагностика. Дифференциальный диагноз. Лечение. Исходы. Профилактика.
ГИПЕРВИТАМИНОЗ ВИТАМИНА D (ГД) возникает при передозировке витамина D или при индивидуальной повышенной чувствительности к нему.
Эпидемиология. В настоящее время благодаря пересмотру подходов к профилактике и лечению рахита ГД у детей встречаются редко.
Патогенез. Высокие дозы витамина D обладают токсическим действием на клеточные мембраны. Высокие дозы витамина D способствуют повышению в крови уровня кальция. Избыток кальция в организме приводит к его отложению в стенках сосудов внутренних органов (почки, сердце), что сопровождается нарушением функции пораженных органов.
Классификация (табл. 1.45).
Исследования. Общий анализ крови и мочи. Определение в крови уровней фосфора, кальция, кальцитонина, паратиреоидного гормона. Рентгенологическое исследование костей. Проба Сулковича.
По показаниям проводят исследования, необходимые для выявления патологии сердца, печени, почек (УЗИ почек, мозга, ЭКГ, рентгенография костей, общий анализ крови, общий анализ мочи, печеночные пробы и др.).
Консультации специалистов: уролог, нефролог, невролог, кардиолог.
153
Анамнез, клиника. Выраженная клиническая картина ГД отмечается при приеме суммарной дозы витамина D более 1 млн. МЕ, при сочетании приема витамина D с УФО или рыбьим жиром, а также при сочетании с большими дозами кальция в летнее время, у детей на искусственном вскармливании. Большое значение имеет длительность приема выше названной дозы (существовавший ранее ударный метод лечения рахита). Повышенная чувствительность к витамину D отмечается у детей, матери которых получали его во время беременности. Описаны случаи повышенной индивидуальной чувствительности к витамину D.
Клинически ГД проявляется картиной острого токсикоза (прием больших доз витамина D в течение 2-3 недель) или хронической интоксикации (прием витамина D на протяжении 6-8 месяцев и более).
Табл. 1.45. Классификация гипервитаминоза D у детей (Барлы-
баева И.А., Струкова В.И., 1976)
Степень |
Клинические проявления |
Период |
Течение |
тяжести |
|
|
|
|
|
|
|
I лег- |
Без токсикоза. Снижен аппе- |
Начальный |
Острое – |
кая |
тит. Раздражительность, на- |
Разгар |
до 6 ме- |
|
рушение сна. Задержка на- |
Реконвалесценция |
сяцев |
|
растания массы. Увеличение |
Остаточные явле- |
|
|
секреции Са с мочой. |
ния: кальциноз |
Хрони- |
|
Проба Сулковича +++ |
различных органов |
ческое |
|
|
и сосудов, их скле- |
- свыше |
|
|
роз с развитием |
6 меся- |
|
|
коарктации аорты, |
цев |
|
|
стеноза легочной |
|
|
|
артерии, хрониче- |
|
|
|
ская почечная не- |
|
|
|
достаточность и |
|
|
|
др. |
|
|
Умеренный токсикоз. Сни- |
|
|
II |
жен аппетит, рвота, задерж- |
|
|
средне |
ка или падение массы. Ги- |
|
|
тяже- |
перкальциемия, гипофосфа- |
|
|
лая |
темия, гиперцитремия, гипо- |
|
|
|
магниемия. Проба Сулкови- |
|
|
|
ча +++ или ++++ |
|
|
154

III Выраженный токсикоз.
тяже- Упорная рвота, значительная лая потеря массы, присоедине-
ние осложнений (пневмония, пиелонефрит, миокардит и др.). Резкие изменения биохимических показателей Са, Mg, P.
Примечание: ГД может протекать с преимущественным поражением нервной системы, ЖКТ, почек, сердечно-сосудистой системы.
Острая интоксикация витамином D проявляется клиникой нейро-
токсикоза или кишечного токсикоза: рвота, тошнота, обезвоживание, анорексия, гипотрофия, астения, запоры, полиурия, полидипсия. Поражение нервной системы варьирует от легкой заторможенности до тяжелых коматозных состояний с судорогами.
Хроническая интоксикация витамином D характеризуется раздра-
жительностью, нарушением сна, слабостью, появлением признаков гипотрофии, преждевременным закрытием большого родничка, изменениями со стороны сердечно-сосудистой и мочевыделительной систем, печени.
Проявления поражения сердечно-сосудистой системы варьируют от небольших функциональных нарушений до тяжелого миокардита с развитием недостаточности кровообращения. На ЭКГ выявляют расширение комплекса QRS, удлинение интервала PQ, сглаженность зубцов P и T в V 1 и V2; описаны случаи нарушения атриовентрикулярной проводимости; может быть ЭКГ картина инфаркта миокарда. Как правило, при ГД отмечается повышенное артериальное давление.
Поражение печени проявляется повышением активности сывороточных трансаминаз, диспротеинемией, повышением в крови холестерола, снижением альфа- и повышением беталипопротеидов; патологическими типами гликемических кривых.
Поражение почек может быть как в виде небольших дизурических явлений, так и в виде лейкоцитурии, незначительной гематурии, протеинурии, острой почечной недостаточности. Из-за частого присоединения инфекции возможно развитие пиелонефрита. У части детей может появиться нефрокальциноз, оксалатно-кальциевый уролитиаз. В далеко зашедших случаях формируется хроническая почечная недостаточность.
Диагноз ГД основывается на данных анамнеза (прием высоких доз витамина D), выявлении клинических проявлений заболевания.
155
Лабораторные исследования при ГД находят повышение уровня в крови и в моче фосфора и кальция, компенсаторное увеличение уровня кальцитонина и снижение паратиреоидного гормона, ацидоз. На рентгенограммах костей обнаруживаются расширение и уплотнение зон препараторного обызвествления.
Степени тяжести ГД диагностируют на основании следующих критериев:
Первая степень – уровень кальция в крови стабильно на верхней границе, интенсивное выделение его с мочой (реакция Сулковича ++), в клинической картине умеренные проявления токсикоза, полиурия, полидипсия, снижение веса.
Вторая степень – уровень кальция в крови выше нормы, но не превышает 12 мг%, с мочой его выделяется много (реакция Сулковича
+++ или ++++), в клинической картине выраженные явления токсикоза, полиурия, дистрофия.
Третья степень – уровень кальция в крови более 12 мг%, тяжелый токсикоз и обязательное поражение почек.
Дифференциальный диагноз ГД проводят с: интоксикациями различного генеза, (сопровождающиеся рвотой, снижением аппетита, падением массы тела), кальцинозом внутренних органов, заболеваниями почек (в том числе и ХПН).
Лечение. Задачи лечения: прекращение поступления в организм витамина D и препаратов кальция, купирование проявлений токсикоза, лечение патологических синдромов и проявлений ГД, предупреждение развития нефрокальциноза, пиелонефрита, ХПН.
Схема лечения.
Обязательные мероприятия: отмена витамина D и препаратов кальция, инфузионная терапия, мочегонные средства.
Вспомогательные методы лечения: глюкокортикоиды, кальцито-
нин, витамины А и Е.
Показания для госпитализации: лечение проводится в стационаре. Режим: ограничение инсоляции.
Диета с уменьшением в питании продуктов, содержащих большое количество кальция (молоко, сыры, творог и др.).
Лечение гиперкальциемических состояний заключается в отмене витамина D и препаратов кальция, назначении фитина для уменьшения всасывания кальция в кишечнике. Показано обильное введение жидкости (внутрь, внутривенно). При выраженной гиперкальциемии назначают препараты кальцитонина, наиболее популярным из которых считается синтетический кальцитонин лосося – миакальцик. По показани-
156

ям могут быть применены стероидные гормоны, гипотензивные средства.
Осложнения. При ГД могут развиваться: кальциноз различных органов и сосудов, их склероз с развитием коарктации аорты, стеноза легочной артерии, хроническая почечная недостаточность, пиелонефрит, комы.
Исходы. Последствиями ГД часто являются нефропатии: хронический пиелонефрит, интерстициальный нефрит, тубулопатии, нефрокальциноз. В тяжелых случаях возможен исход в ХПН.
Профилактика ГД в первую очередь сводится к ограничению использования высоких доз витамина D, исключению из арсенала врача спиртовых препаратов витамина D, исключению случаев передозировки витамина D и медикаментозных отравлений препаратом.
Вопросы к экзамену. Гипервитаминоз D. Причины. Классификация.
Клиническая картина. Диагностика. Дифференциальный диагноз. Осложнения. Лечение. Исходы. Профилактика.
Глава VI. Болезни почек и мочевых путей
ГЛОМЕРУЛОНЕФРИТЫ
Острый гломерулонефрит (ОГН) – острое диффузное иммунно-
воспалительное поражение почек, преимущественно клубочков, возникающее после бактериального, вирусного или паразитарного заболевания, спустя некоторый латентный период (период сенсибилизации). Чаще ОГН протекает с нефритическим синдромом, имеет циклическое течение. ОГН нередко отождествляют с постстрептококковым гломерулонефритом (ОПСГН).
Эпидемиология. По данным эндемического исследования, проведенного в 13 территориях России частота ОГН в детской популяции составляет 33:100 000. Болеют дети обоего пола, чаще в возрасте 6-12 лет, преимущественно мальчики. Заболевание встречается, как правило, в спорадическом варианте, число заболевших ОГН растет.
Предрасполагающими факторами развития ОПСГН являются:
отягощенная наследственность в отношении инфекционноаллергических заболеваний; повышенная семейная восприимчивость к стрептококковой инфекции; наличие у ребенка хронических очагов инфекции; гиповитаминозы, гельминтозы; частые ОРИ; охлаждения и
157
метеорологические факторы; вакцинации; прием аллергенов; наличие
HLA антигенов, DRw4, DRw6, B12.
Этиология ОГН инфекционная. Заболевание вызывают вирусные болезни (австралийский антиген, инфекционный мононуклеоз, ЦМВИ, Вирус Коксаки В4); бактериальные болезни (подострый бактериальный эндокардит, стрептококковая, стафилококковая инфекция, брюшной тиф); паразитарные болезни (малярия, шистосомоз, токсоплазмоз).
ОПСГН возникает после стрептококковых заболеваний (ангина, импетиго, скарлатина, рожа, лимфаденит и др.). Заболевание вызывают нефритогенные штаммы β-гемолитического стрептококка группы А (1, 2, 4, 12, 18, 25, 49 и др. типы). Этиология ОПСГН подтверждается высевом из очага стрептококка, обнаружением в крови антигенов и антител – АСО, антигиларунидазы, антистрептокиназы.
Патогенез ОПСГН предусматривает образование иммунных комплексов, состоящих из противострептококковых антител и стрептококков. В иммунных реакциях принимают участие комплемент, пропердин, медиаторы воспаления, факторы клеточного иммунитета. В результате активации свертывающей системы развивается локальный ДВС-синдром.
Главными следствиями развившегося воспалительного процесса в почках являются снижение клубочковой фильтрации, и формирование основных синдромов ОПСГН – мочевого, отечного и гипертензионного.
Макрогематурия развивается за счет повышения сосудистой, капиллярной и тканевой проницаемости, активации гиалуроридара, приводящей к деполимеризации гиалуроновой кислоты, входящей в состав основного вещества соединительной ткани и межклеточного вещества стенки сосудов – per diaрidesum эритроциты проникают в мочу, затем в процесс вовлекаются свертывающие системы тромбоцитов (их агрегация) и плазменные факторы (фактор XII, Хагемана), разворачивается местный ДВС-синдром, приводящий к макрогематурии.
Повышение артериального давления в своей основе имеет актива-
цию ренин-ангиотензин-альдостероновой системы, что приводит к усилению секреции АДГ гипофиза, что лежит в основе увеличения ОЦК.
Отеки при ОПСГН развиваются за счет стимуляции альдостерона, под действием которого увеличивается реабсорбция и задержка в организме натрия, воды. В развитии отеков также имеет значение повышение сосудистой и тканевой проницаемости за счет воспаления.
Накопление натрия в сосудистом русле повышает осмолярность плазмы, что способствует повышению секреции АДГ и повышению к
158
нему чувствительности дистальных канальцев и еще большей задержки воды и развитию гиперволемии. Дополнительному увеличению содержание натрия в организме способствует увеличение содержания ангиотензина II и альдостерона.
Важное значение также имеет активация кинин-каллекрииновой системы, что приводит к повышению сосудистой проницаемость и выходу жидкости из крови в тканевое пространство, с перераспределением жидкости и скоплением ее в рыхлой клетчатке.
Патогенез быстро возникающих нефротических отеков включает первичную задержку натрия и воды, активацию кининкаллекрииновой системы и гиалуронидазы с тотальным повышением сосудистой проницаемости с последующим выходом жидкой части крови в межтканевое пространство.
При медленно возникающих отеках развивается повреждение клу-
бочка, которое приводит к протеинурии, снижению коллоидноосмотического давления плазмы за счет уменьшения объема циркулирующей крови. Увеличение реабсорбции натрия, повышение секреции АДГ (вазопрессина) приводит к задержке воды в организме (в сосудистом русле, в результате чего развивается гиперволемия и увеличение жидкости в интерстициальном пространстве.
Патогенез
|
|
|
|
|
Стрептококк |
|
|
|
|
|
|
Антитела |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дополнительные системы: комплемент, |
|
|
||||||||||
|
|
|
Иммунные комплексы |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
пропердин, локальная активация гемо- |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
коагуляции, медиаторы воспаления, ПГ, |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Клеточный иммунитет |
|
|
|
Гломеру- |
|
|
|
|
|
|
|
Антитела к гломерулярной |
||||||||||||||
|
(макрофаги, Т-клетки), |
|
|
|
лонефрит |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
базальной мембране |
||||||||||||||||
|
|
Ig,Е |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повыше- |
|
|
|
|
|
|
|
|
|
|
|
||||
|
Увеличе- |
|
|
|
|
|
Снижение |
|
|
|
|
|
|
Отеки |
|
|
Мочевой |
|
|||||||||
|
|
|
|
|
|
|
|
ние АД |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
клубочковой |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
ние ОЦК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
синдром |
|
|||||||
|
|
|
|
|
|
|
фильтрации |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Наруше- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нарушение |
|
|
|
|
|
|
|||||||||
|
ние ССС |
|
|
|
|
|
Олигурия |
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
ЦНС |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
159
Рис. 1.21. Патогенез ОПСГН (Коровина Н.А с соавт., 1990)
Морфология ОПСГН (эндокапиллярный пролиферативный гломерулонефрит – по классификации ВОЗ) характеризуется увеличением клубочков в размерах, выявлением в мезангии больших плотных депозитов субэпителиального (С3-компонент, IgA); признаками эндокапилярного пролиферативного воспаления.
Табл. 1.46. Классификация первичного гломерулонефрита у де-
тей (Винница, 1976)
Форма гломерулонефрита |
Активность по- |
Состояние функ- |
|
чечного процесса |
ции почек |
1. Острый: |
Период начальных |
Без нарушения |
а) с острым нефритическим |
проявлений |
функции почек; |
синдромом, |
Период обратного |
С нарушением |
б) с нефротическим син- |
развития |
функции почек; |
дромом, |
Переход в хрони- |
Острая почечная |
в) с изолированным моче- |
ческий гломеру- |
недостаточность |
вым синдромом, |
лонефрит |
|
г) нефротический синдром с |
|
|
гематурией и (или) гипер- |
|
|
тензией. |
|
|
2. Хронический: |
Период обостре- |
Без нарушения |
а) гематурическая форма, |
ния |
функции почек; |
б) нефротическая форма, |
Период частичной |
С нарушением |
в) смешанная форма |
ремиссии |
функции почек; |
|
Период полной |
Хроническая по- |
|
клинико- |
чечная недоста- |
|
лабораторной ре- |
точность |
|
миссии |
|
3. Подострый (злокачест- |
|
|
венный) гломерулонефрит |
|
|
Наряду с клинической классификацией гломерулонефритов существует морфологическая классификация, позволяющая уточнить прогноз заболевания, повысить эффективность лечения.
Классификация первичных гломерулонефритов по морфоло-
гии (ВОЗ, 1980)
А. Небольшие изменения гломерул;
160
Б. Фокальные и/или сегментарные поражения (только с небольшими изменениями в остальных клубочках).
В. Диффузный гломерулонефрит:
1.мембранозный гломерулонефрит (мембранная нефропатия);
2.диффузный пролиферативный гломерулонефрит:
а) мезангиопролиферативный гломерулонефрит; б) эндокапиллярный пролиферативный гломерулонефрит;
3.мезангиокапиллярный (мембранознопролиферативный) гломерулонефрит:
1-й тип «классический»;
2-й тип лобулярный.
4.гломерулонефрит с плотными депозитами (болезнь плотных депозитов, мезангиокапиллярный гломерулонефрит), 2-й тип;
5.гломерулонефрит с полулуниями (экстракапиллярит);
а) склерозирующий гломерулонефрит.
Исследования: общий анализ крови и мочи, анализ мочи по Нечипоренко, длительность кровотечения, время свертывания, тромбоциты, протеинограмма, общие липиды, холестерин, триглицериды, креатинин, мочевая кислота; определение в крови калия, кальция, натрия, хлоридов, трансаминаз; серомукоид, щелочная фосфатаза, глюкоза крови, коагулограмма, показатели КОС, средние молекулы, группа крови и резус-фактор, титры АСЛО, ЦИК, суточная экскреция белка, оксалатов, кальция, фосфора, глюкозы, калия, натрия; проба по Зимницкому, проба Реберга, копрограмма, кал на скрытую кровь, ЭКГ.
По показаниям: β-липопротеиды, мочевина крови, маркеры гепатита, билирубин крови, иммунограмма, морфология мочевого осадка, посев мочи на флору, УЗИ паренхиматозных органов, радиоизотопная ренография, экскреторная урография, рентгенография органов грудной клетки, проба Манту, ФГДС, вирусологическое обследование, исследование в моче ферментов (холинэстераза, щелочная фосфатаза и др.).
Анамнез, клиника. Выделяют два варианта течения ОПСГН – циклическое (типичное) и ациклическое (моносимптомное).
В типичных случаях анамнез позволяет выявить предшествующее стрептококковое поражение зева, кожи и т. д. Через 2 -4 недели после перенесенной инфекции (латентный период), отмечается ухудшение общего состояния, уменьшение диуреза, потемнение мочи, появление головной боли, отеков на лице, голенях, иногда на животе, пояснице. Может быть кратковременное повышение температуры, тошнота, реже рвота, боли в поясничной области, иногда признаки эклампсии.
161
Объективно: ребенок бледен (за счет ангиоспазма), отеки, локализованные на лице и голенях. Отеки бывают «скрытыми» (выявляются положительной пробой Макклюра-Олдрича).
Со стороны сердечно-сосудистой системы обнаруживается тахикардия, реже брадикардия, приглушенность тонов, расширение границ относительной сердечной тупости, ослабление I тона на верхушке, усиление 2-го типа на аорте и легочной артерии, расширение границ сердца (за счет повышения артериального давления). В некоторых случаях развивается недостаточность кровообращения.
Моча цвета «мясных помоев» (макрогематурия). Олигурия диагностируется у половины детей, через 3-7 дней отмечается восстановление диуреза.
В периоде обратного развития симптомов появляется полиурия, купируются отеки, исчезает артериальная гипертензия, экстраренальные проявления заболевания (головные боли, нарушение самочувствия и др.). В последнюю очередь исчезает гематурия. Полное восстановление морфологических изменений в почках происходит через 1-2 года.
Ациклический вариант ОПСГН протекает, часто с изолированным мочевым синдромом. Заболевание характеризуется постепенным началом при отсутствии субъективных симптомов и экстраренальных проявлений. Через несколько лет может сформироваться хронический гломерулонефрит в различных формах.
Основными клиническими вариантами ОПСГН являются: нефро-
тический и нефритический синдромы (см. ниже).
Диагноз ОПСГН основывается на выявлении перенесенной стрептококковой инфекции и латентного периода после нее. Характерная триада симптомов (гематурия, умеренные отеки, повышение артериального давления) дает основание заподозрить ОГН.
Лабораторные исследования Общий анализ мочи. При ОПСГН чаще всего выявляют гематурию,
а в начале заболевания и лейкоцитурию. Лейкоцитурия - маркер им- мунно-воспалительного процесса в почках. Для ОГН характерной находкой является цилиндрурия (гиалиновые, зернистые, эритроцитарные). У многих больных обнаруживается протеинурия до 1-2 г/л/сутки.
В анализе крови: увеличение СОЭ, нейтрофилез; при наличии инфекционного очага – лейкоцитоз, умеренная анемия.
Биохимические исследования. Наблюдается диспротеинемия за счет умеренной гипоальбуминемии, гипер-α2 и γ-глобулинемии. При развитии выраженной олигурии у части больных в крови повышается уровень мочевины и креатинина, что рассматривается как нарушение функции почек острого периода. Возможно развитие ОПН.
162
При серологическом исследовании у 60-90% больных повышаются титры антистрептолизина О. Анти-М-протеиновые антитела появляются через 4-6 недель после перенесенной стрептококковой инфекции и сохраняются длительно. У 90% больных в крови повышаются ЦИК. В течение первых двух недель заболевания снижается уровень С2, С3, С4, фракций комплемента, который продолжается 4-6 недель.
Нарушения в системе свертывания характеризуются: увеличением протромбинового индекса, снижением уровня антитромбина III, угнетением фибринолитической активности, появлением в крови продуктов деградации фибриногена.
При УЗИ можно выявить незначительное увеличение почек в размерах, повышение их эхогенности.
Нефритический синдром – это симптомокомплекс, включающий экстраренальные симптомы (отеки или пастозность, повышение артериального давления, изменения со стороны сердца, ЦНС) и ренальные (олигурия, гематурия, протеинурия до 1г в сутки, цилиндрурия) проявления. В период начальных проявлений ОГН может наблюдаться нарушение функции почек, иногда развивается ОПН.
Нефротический синдром – симптомокомплекс, характеризующийся олигурией до анурии, массивной протеинурией (более 50 мг/кг/24 ч или более 3г/24 ч), гипо- и диспротеинемией (уменьшением альбуминов ниже 25 г/л, а также γ- глобулинов, увеличением α2 и β - глобулинов), гиперлипидемией и гиперхолестеринемией, что соответствует понятию полный нефротический синдром (НС). «Неполный» НС протекает без отеков. НС встречается при двух формах гломерулонефрита: нефротической и смешанной.
Диагностические трудности возникают при латентном, ациклическом варианте течения заболевания.
Биопсия почки - прижизненное морфологическое исследование почечной ткани с помощью чрезкожной пункции (закрытая биопсия) или оперативным методом (открытая, полуоткрытая биопсия).
Показания для биопсии при ОПСГН: атипичные проявления гломе-
рулонефрита, возраст до 3 лет, анурия, высокая азотемия, несоразмерная клинической картине; нарушения роста, гломерулонефрит в семье, длительное сохранение симптомов (задержка ремиссии), признаки системного заболевания, длительно сохраняющиеся гематурия и протеинурия.
Дифференциальный диагноз ОПСГН проводится с: хроническим гломерулонефритом, наследственным нефритом, геморрагическим васкулитом, транзиторным мочевым синдромом на фоне острого инфекционного заболевания, острым пиелонефритом, ревматизмом, сис-
163
темной красной волчанкой, ревматоидным артритом, инфекционным эндокардитом, интерстициальным нефритом, быстро прогрессирующим гломерулонефритом, IgA нефропатией (болезнь Берже), гемоли- тико-уремическим синдромом.
Табл. 1.47. Дифференциальный диагноз острого и хронического гломерулонефрита (Маковецкая Г.А., 1987, с изменениями)
Признаки |
Острый нефрит (неф- |
Хронический нефрит |
|
ритическая форма) |
(гематурическая форма) |
Клинические: |
|
Чаще у детей старшего |
Возраст к началу |
5-12 лет |
школьного возраста |
болезни |
|
|
Связь со стрепто- |
Прослеживается у |
Прослеживается как в |
кокковой, вирус- |
60% больных |
начале болезни, так и в |
ной инфекцией |
|
период обострения |
Развитие болезни |
Через 2-3 недели по- |
Чаще постепенное: |
|
сле перенесенного |
1) как исход острого за- |
|
стрептококкового или |
болевания возможно по- |
|
вирусного заболева- |
сле длительного латент- |
|
ния |
ного периода |
|
|
2) как первично- |
|
|
хроническое незаметное |
Симптомы ин- |
|
|
токсикации: |
Отмечается иногда |
Отмечается и вне обост- |
Головная боль |
То же |
рения |
Недомогание |
Имеется у части |
Жалобы отсутствуют |
Анорексия |
больных |
То же |
Усталость |
То же |
То же |
Отеки |
У 60-80% больных |
Могут отсутствовать |
Артериальная |
У 1/3-1/4 больных, |
При развитии ХПН |
гипертензия |
кратковременная |
|
Изменения в моче: |
|
|
Микрогематурия |
У 50% больных |
Имеется |
|
|
|
Макрогематурия |
У 30-40% |
Отсутствует вне обост- |
|
|
рения |
Цилиндрурия |
Встречаются эритро- |
Может не отмечаться |
|
цитарные цилиндры |
|
Протеинурия |
0,5-1,0 в сутки |
0,5-4,0 в сутки |
|
|
|
164
Цилиндрурия |
Эритроцитарные ци- |
Может не быть |
|
линдры |
|
Относительная |
В дебюте свыше 1020 |
Ниже 1017 |
плотность мочи |
|
|
Клубочковая |
Снижена значительно |
Снижена на 25-30% при |
фильтрация |
|
длительном лечении |
Олигурия |
Имеется в дебюте |
Нет |
Анемия |
Наблюдается редко |
Стойкая, у 1/3 больных |
Лейкоцитоз |
Отмечается у 15-30% |
Нет |
|
больных |
|
Увеличение СОЭ |
Отмечается у 75% |
Вне обострения СОЭ не |
|
больных |
увеличена |
Биохимические |
|
|
показатели крови: |
|
|
Гипопротеинемия |
Отсутствует |
Имеется |
|
|
|
Гиперфибриноге- |
Отмечается у всех |
Вне обострения не отме- |
немия |
больных |
чается |
Уровень серому- |
Повышен |
Нет повышения |
коида |
|
|
Гиперхолестери- |
Нет |
У 15-30% больных |
немия |
|
|
Осложнения: |
|
|
Острая сердечная |
Развивается у 1% |
Развивается реже, только |
недостаточность |
больных |
в терминальной фазе |
Гипертензионная |
Развивается у 2% |
Не развивается |
энцефалопатия |
больных |
|
Почечная недос- |
Возможно развитие |
Возможно развитие ХПН |
таточность |
ОПН |
|
Табл. 1.48. Дифференциальный диагноз острого гломерулонефрита и геморрагического васкулита (Игнатова М.С., с соавт., 1975,
Фокеева В.В. 1989 с изменениями)
Симптомы |
Острый гломеру- |
Геморрагический |
|
лонефрит |
гломерулонефрит |
Клинические: |
|
|
-возраст к началу забо- |
5-12 лет |
Чаще до 7 лет |
левания |
|
|
165
-связь со стрептококко- |
Прослеживается |
Не прослеживается |
вой инфекцией |
часто |
|
-связь с вирусной ин- |
Прослеживается |
Прослеживается |
фекцией |
|
часто |
Симптомы интоксикации |
Часто |
Редко |
(головная боль, недомога- |
|
|
ние, гипертермия) |
|
|
Отеки |
У 60-80% больных |
Редко |
Артериальная гипер- |
У 60-80% больных |
Нет |
тензия |
|
|
Боли в животе |
Редко |
У 50% больных |
Боли и припухлость |
Не бывает |
У 2/3 больных |
суставов |
|
|
Поражение кожи (гемор- |
Не бывает |
Практически всегда |
рагическая папулезная |
|
|
сыпь, преимущественно на |
|
|
конечностях вокруг суста- |
|
|
вов, ягодицах) |
|
|
Лабораторные измене- |
Появляются сразу |
Появляются через 1-3 |
ния в моче: |
|
недели от начала за- |
-протеинурия |
Часто до 1 г/л |
болевания. У 1/3 |
|
|
больных до 0,66 г/л |
-гематурия |
Часто, до макроге- |
У 1/2 больных, ча- |
|
матурии |
ще микрогематурия |
|
|
|
Олигурия |
Имеется |
Редко |
Клубочковая фильтра- |
Значительно сниже- |
В дебюте, как пра- |
ция |
на в дебюте |
вило, не изменена |
Табл. 1.49. Дифференциальный диагноз острого гломерулонеф-
рита и пиелонефрита (Маковецкая Г.А. 1987 с изменениями)
Показатель |
Острый гломеруло- |
Острый пиелонефрит |
|
нефрит |
|
Время появления |
Через 2-3 нед. после |
Через 7-12 дней после |
|
инфекции |
ОРВИ, или во время |
Возраст пациента |
Чаще 5-12 лет |
Любой |
Повышение АД |
У 60-80% |
Отсутствует |
Отеки |
У 60-80% |
Отсутствуют |
Лихорадка |
Редко |
Имеется |
Дизурия |
Отсутствует |
Часто |
166
Болезненность при |
- |
Характерно |
поколачивании |
|
|
Протеинурия |
В зависимости от |
Микропротеинурия (в |
|
формы |
среднем не выше 0,33 г/л) |
Гематурия |
До макрогематурии |
Микрогематурия у 1/3 |
|
|
больных |
Лейкоцитурия |
В дебюте микролей- |
Характерна, нейтро- |
|
коцитурия (лимфоци- |
фильная |
|
ты, моноциты) |
|
Цилиндрурия |
Гиалиновые, |
Лейкоцитарные |
|
Эритроцитарные |
|
Бактериурия |
Отсутствует |
Характерна |
Проба Зимницкого |
Не изменена |
У 1/2 нарушение ритма |
|
|
мочеотделения и сни- |
|
|
жение концентрацион- |
|
|
ной способности |
Клубочковая |
Снижена |
В тяжелых случаях |
фильтрация |
|
|
УЗИ |
Увеличение площа- |
Деформация чашечно- |
|
дей почек, визуализа- |
лоханочной системы, |
|
ция пирамид |
эктазия лоханки и ча- |
|
|
шечек |
С-реактивный белок |
+++ |
+, ++, +++ |
Повышение содер- |
В дебюте может по- |
При развитии ХПН |
жания мочевины |
вышаться |
|
Лечение. Задачи лечения: эрадикация стрептококковой инфекции, купирование ренальных и экстраренальных проявлений ОПСГН.
Схема лечения. Обязательные мероприятия: постельный режим,
диета, антибактериальная терапия.
Вспомогательное лечение: средства симптоматической терапии (мочегонные, гипотензивные), витаминотерапия, антигистаминные средства, эуфиллин, дезагреганты, мембраностабилизирующие препараты, антиоксиданты.
Показания для госпитализации: лечение ОГН проводится в стационаре.
Режим. Строгий постельный режим показан при экстраренальных симптомах и макрогематурии. Расширение режима показано при ликвидации гипертензии, отеков и уменьшении гематурии. Возможность перевода на расширенный режим решают по отсутствию жалоб, гипертензии и улучшению мочевого осадка.
167

Диета. Жидкость назначают из расчета диуреза предыдущего дня и потерь на перспирацию (15мл/(кг/сут) или 400 мл/(м2/сут)) для школьников. С увеличением диуреза количество выпиваемой жидкости увеличивают.
Ограничение натрия хлорида (бессолевой стол) назначают при олигурии и гипертензии. При нормализации артериального давления и увеличении диуреза разрешено подсаливание пищи (0,5-1,0 г/сут). Нормальное количество натрия хлорида (50 мг/(кг/сут)) при благоприятном варианте течения заболевания ребенок может получать с 4-5-й недели. В дебюте ОПСГН назначают стол 7а (по Певзнеру) сроком на 3-5 дней. На 3-5-7 день назначают переходный стол 7б. В рационе увеличивается количество белка и жира. В последующем больного переводят на стол 7в. Соль добавляют в готовые блюда.
Ограничение белка показано при олигурии и гипертензии. На период 5-7 дней сокращают потребление белка (до 1,0-0,5 г/(кг/сут)). Целесообразно также некоторое ограничение животных белков в течение 2- 3 недель. Калорийность сохраняют за счет увеличения в диете углеводов и жиров.
При олигурии показано ограничение калия. Из-за опасности гиперкалиемии исключают фруктовые или овощные соки. Противопоказаны калийсберегающие препараты. После схождения отеков целесообразно обогащение диеты калием (печеный картофель, фрукты и др.).
Больным с ОПСГН необходима антибактериальная терапия предпочтительно антибиотиками пенициллинового ряда (полусинтетические пенициллины типа амоксициллина или макролиды в обычных дозах). При отсутствии очагов инфекции длительность антибактериальной терапии 7-10 дней. При наличии очагов хронической инфекции по окончании курса антибактериальной терапии (4-6 недель) можно применять бициллин-5 или бициллин-1. Длительность бициллинотерапии до 6 месяцев. Бициллин-5 или бициллин-1 вводят 1 раз в 3 недели в дозировках: дошкольники – бициллин-5 – 750000 ЕД., бициллин-1 – 600000 ЕД.; школьники соответственно 1500000 ЕД и 1200000 ЕД.
Патогенетическая терапия ОГН может быть представлена в следующем виде (табл. 1.50).
Табл. 1.50. Патогенетическая терапия ОГН
Форма ОГН
с острым |
с нефроти- |
изолированным мо- |
нефротический |
нефритиче- |
ческим син- |
чевым синдромом |
синдром с гема- |
ским синдро- |
дромом |
|
турией и (или) |
168
мом |
|
|
гипертензией |
Антиагреган- |
Преднизо- |
Антиагреганты: |
Антиагреганты |
ты: |
лон |
Курантил, трентал, |
|
курантил |
|
никошпан |
|
Антикоагу- |
Препараты, |
Мембраностабили- |
Антикоагулян- |
лянты: гепа- |
уменьшаю- |
заторы: ксидифон, |
ты |
рин |
щие побоч- |
димефосфон, кар- |
|
|
ные эффек- |
сил, эссенциале, |
|
|
ты стерои- |
коринфар |
|
Никотиновая |
дов: аспар- |
Витаминотерапия: |
Преднизолон |
кислота |
кам, панан- |
а, В6, Е, С, рутин |
|
Эуфиллин |
гин, антаци- |
Антигистаминные |
Цитостатики |
Трентал |
ды |
препараты |
|
Для улучшения почечного кровотока применяют антиагреганты (курантил, персантил), которые назначают на 3-4 недели 2-3 раза в день в суточной дозе 1,5-3,0 мг/кг/сут.
Гепаринотерапия показана при: наличии признаков гиперкоагуляции; симптомов внутрипочечного (локального) внутрисосудистого свертывания крови (быстрое снижение функции почек при уменьшении содержания фибриногена и повышении содержания продуктов деградации фибрина в сыворотке крови); наличии ДВС-синдрома; выраженном отечном синдроме; выраженной гиперлипидемии.
Методы проведения гепаринотерапии: парентеральное введение (подкожно, внутримышечно) методом электрофореза (300 ЕД/кг) и методом аэрозоля (500 ЕД/кг), 100-200 ЕД/кг суточная доза в 4 инъекции. Препарат следует отменять постепенно под контролем показателей коагулограммы.
Никотиновая кислота активирует фибринолитическую систему крови, препятствует агрегации тромбоцитов, обладает сосудорасширяющим действием. Используют электрофорез 1% раствора никотиновой кислоты на область почек. Процедуры проводят ежедневно, число процедур 7-10.
Эуфиллин увеличивает просвет сосудов почек, дает легкий мочегонный эффект, уменьшает общее периферическое сопротивление. Препарат назначают на 1-2 недели в порошках или таблетках 3 раза в день в суточной дозе: до 9 лет – 15-18 мг/(кг/сут); 9-12 лет – 10-12,5 мг/(кг/сут); старше 12 лет – 10 мг/(кг/сут); трентал, никошпан.
Назначают витамины А, группы В, Е в возрастных дозах; мембраностабилизаторы - ксидифон, димефосфон, карсил.
169
Мочегонные при ОПСГН используют редко. Диуретики показаны при массивных отеках, артериальной гипертензии, гипертонической энцефалопатии. С целью увеличения диуреза назначают фуросемид (лазикс) в дозе 1,5-2,0 мг/кг внутримышечно или внутривенно 1-2 раза в сутки, затем еще 3 дня препарат вводят через рот в 1 приём.
Гипотензивные препараты показаны при уровне диастолического давления выше 95 мм рт. ст. и при гипертонической энцефалопатии.
При высокой гипертензии препаратами выбора являются каптоприл (капотен). Каптоприл назначается в суточной дозе 0,3 мг/кг/сут. Доза может быть увеличена до 2,0 мг/кг/сут в течение 3-5 дней. Возможно внутривенное введение 2,4% раствора эуфиллина на физиологическом растворе вместе с лазиксом (1-4 мг/кг). Основа лечения артериальной гипертензии – диуретики и антагонисты кальция.
При угрозе эклампсии внутримышечно применяют 1% раствор дибазола и 5% раствор папаверина (по 0,1 мг/кг/сут) и 1% раствор фуросемида (1,0-2,0 мг/кг).
При эклампсии для получения быстрого гипотензивного эффекта вводят диазоксид внутривенно струйно как можно быстрее в дозе 2-5 мг/кг (максимальная доза 100 мг) или метилдофа внутривенно в дозе 5-10 мг/кг (введение метилдофа можно повторять через 20-60 минут).
Для снятия судорог назначают 0,5% раствор седуксена (реланиума) в дозе 0,3-0,5 мг/кг внутримышечно или натрия оксибутирата в дозе 100-150 мг/кг, 10% кальция глюконат внутривенно. Лечение проводится на фоне оксигенотерапии.
Гемодиализ при ОПСГН показан в случае отсутствия реакции на лазикс, нарастании мочевины > 20-24 ммоль/л, калия > 7 ммоль/л, фосфора > 2 ммоль/л, < натрия до 130 ммоль/л, рН крови > 7,25.
Особое внимание необходимо уделить санации очагов инфекции. Тонзилэктомия проводится через 6 месяцев после начала ремиссии ОПСГН.
При ОГН с изолированным мочевым синдромом основой лечения являются антибиотики пенициллинового ряда, макролиды в сочетании с антиагрегантами.
При ОГН с нефритическим синдромом основой лечения являются антибиотики пенициллинового ряда, макролиды в сочетании с антиагрегантами и прямыми антикоагулянтами.
Осложнения. При ОПСГН возможно развитие: ангиоспастической энцефалопатии, острой почечной недостаточности, острой сердечнососудистой недостаточности.
170

Исходы. Выздоровление наступает в 85-90%. Летальный исход редко (<1%). В 10-15% случаем ОГН трансформируется в хронический гломерулонефрит.
Прогноз ближайший и отдаленный при ОПСГН с нефритическим синдромом благоприятный.
Вопросы к экзамену. Гломерулонефриты. Классификация. Острый
гломерулонефрит. Этиология. Патогенез. Особенности клинической картины в зависимости от преобладающего синдрома. Диагностика. Дифферен-
циальный диагноз. Лечение. Показания к иммуносупрессивной терапии. Исходы. Прогноз.
ХРОНИЧЕСКИЕ ГЛОМЕРУЛОНЕФРИТЫ
Хронический гломерулонефрит (ХГН) – группа гломерулопатий,
различных по морфологическим, клиническим, иммунологическим проявлениям, имеющая разную этиологию, патогенез и исходы.
ХГН могут являться следствием неизлеченного ОГН или иметь первично-хроническое течение заболевания, длящееся больше 1 года.
Эпидемиология ХГН неуточнена. По данным Американских авторов среди пациентов с ХГН только 10-15% составляют больные с относительно своевременно диагностированным ХГН.
Этиология. Инфекционные факторы развития ХГН: микробные возбудители (β -гемолитический стрептококк, стафилококк, возбудители туберкулеза и др.); вирусные: (вирусы гриппа, ЦМВ, гепатитов В и С, герпеса, Эпштейн-Барра, кори, краснухи).
Механические и физические воздействия: травма, инсоляция, пере-
охлаждение.
Аллергические и токсические воздействия: аллергия (особенно пи-
щевая), лекарственные факторы (препараты ртути, йода, золота, пенициллин, наркотики, сульфаниламиды), вакцинации.
От 15 до 26,3% больных с ХГН имели в анамнезе ОГН. В последние годы установлена связь между определённым фенотипом HLAсистемы и формированием ХГН.
Патогенез. В патогенезе ХГН играют роль: генетическая предрасположенность; сочетание нескольких факторов риска; приобретенные дефекты иммунной системы. Провоцируют проявления клинических и параклинических признаков воспаления в почках повторные охлаждения, вакцинации, вирусные и бактериальные инфекции, гепатит В, β -гемолитический стрептококк, хронический сепсис, малярия и др.
171
Чаще всего при ХГН развиваются изменения по III типу аллергической реакции с образованием циркулирующих иммунных комплексов (ИК), которые откладываются в клубочках. После образования ИК в реакцию вступает комплемент и некоторые его фракции. Депозиты ИК могут располагаться в различных отделах капиллярах клубочка. Отсюда формируются разные типы нефрита и морфологические изменения. В процессе удаления ЦИКов из организма образуется ряд медиаторов, способствующих фагоцитозу и их перевариванию. Если ЦИКов много развивается их повреждающее действие.
ЦИКи повреждают ткань почки, активируют медиаторы воспаления – гуморальные (систему комплемента, коагуляцию, кинины, метаболиты арахидоновой кислоты) и клеточные (нейтрофилы, тромбоциты, моноциты, макрофаги, лимфоциты).
Прогрессирование ХГН является следствием нарушенного взаимодействия между собственными клетками клубочка и клетками пришедшими в клубочек. Активированные моноциты и макрофаги выделяют биологически активные вещества, метаболиты О2, коллагеназу, которые повреждают ткани. Прогрессированию гломерулонефрита способствуют: иммунные механизмы, системная и внутрипочечная гипертензия, ишемия почки, протеинурия, гиперлипидемия, гиперкальциемия, гиперфосфатемия, высокобелковая диета.
Воспалительная реакция в почках протекает с пролиферацией (гиперклеточность) и расширением мезангиального матрикса. Накопление гломерулярного матрикса при длительном течении ХГН сопровождается склерозированием и облитерацией клубочка. Склеротические изменения в интерстиции повышают постгломерулярное сопротивление кровотоку, уменьшают почечный кровоток, повышают внутриканальцевое гидростатическое давление и тем самым снижают почечную фильтрацию. Хемокины, эндотелин привлекают в интерстициальное пространство макрофаги и другие клетки воспаления, факторы фиброгенеза, что ведет к интерстициальному фиброзу.
Воздействие этиологических факторов (инфекция, механиче-
ское и физическое воздействие, аллергия, токсические воздействия, наследственные факторы)
|
|
иммунологически необуслов- |
|
иммунологически обуслов- |
|||
|
ленный ХГН |
||
ленный ХГН |
|
||
|
|
||
|
|
|
Метаболические изменения
иммуноком- 172 подоцитов плексный механизм
(80-90%),

аутоим-
мунный
механизм
Повреждение эндотелия
капилляров клубочков
Экссудативно-
пролиферативные изменения, агрегация тромбоцитов, развитие локальной гиперкоагуляции
нарушение заряда гломеруляр-
ной базальной мембраны
Нарушение целостности клу-
бочкового фильтра
Потеря с первичной мочой
белка, липидов
Развитие белковой и жировой
дегенерации тубулярных клеток
Клинико-морфологические варианты хронического гло-
мерулонефрита
Рис. 1.22. Схема патогенеза ХГН
Классификация. Единая классификация ХГН отсутствует. В России принята клиническая классификация гломерулонефритов (см. «Острый гломерулонефрит»). Международные классификации основаны на иммуноморфологических критериях (см. «Острый гломерулонефрит»). Дополнительно к Отечественной классификации гломерулонефритов выделяют: рецидивирующее течение ХГН, прогрессирующее течение, быстропрогрессирующее течение.
В зависимости от чувствительности к стероидам выделяют: гормоночувствительный нефротический синдром (ГЧНС), гормонорезистентный нефротический синдром (ГРНС), часто рецидивирующий нефротический синдром, гормонозависимый нефротический синдром (ГЗНС).
Исследования. Общий анализ мочи с определением суточной протеинурии; протеинограмма, общий анализ крови, липидограмма, определение в крови уровня электролитов, иммунограмма, вирусологическое и бактериологическое исследование, биопсия почки (см. табл.
173
1.51). Определение антинейтрофильных цитоплазматических антител и антител к гломерулярной базальной мембране (диагностика БПГН).
Табл. 1.51. Показания к выполнению биопсии почки у детей с ХГН (Рациональная фармакотерапия у детей раннего возраста, 2007)
Клинические |
Показания для биопсии почек |
синдромы или |
|
заболевания |
|
Нефротический |
ГРН, СНС на первом году жизни, вторичный неф- |
синдром |
ротический синдром |
Протеинурия |
Персистирующая протеинурия более 1 г/сут, сни- |
|
жение функции почек, подозрение на системную |
|
или семейную патологию |
Гематурия |
Подозрение на наследственные заболевания, дли- |
|
тельная гломерулярная гематурия, протеинурия |
|
более 1 г/сутки |
Острый нефри- |
Прогрессирование заболевания через 6-8 недель от |
тический син- |
манифестации (нарастание протеинурии, стойкая |
дром |
АГ, снижение функции почек) |
Системные за- |
Для уточнения диагноза, снижение функции почек, |
болевания: вас- |
ОПН |
кулиты, нефрит, |
|
при СКВ |
|
БПГН |
Во всех случаях |
ХПН |
Для уточнения характера поражения почек с целью |
|
уточнения прогноза заболевания после замести- |
|
тельной терапии (в случае выраженного снижения |
|
СКФ и отсутствия уменьшения размеров обеих |
|
почек) |
Анамнез, клиника. У части детей в анамнезе выявляются проявления острого гломерулонефрита. Основными признаками ХГН являются: повышение артериального давления, отеки, мочевой синдром.
Дети с ХГН часто предъявляют жалобы на: боли в пояснице, утомляемость, головную боль, головокружение, дизурию (в то числе: учащённое мочеиспускание, болезненное мочеиспускание), боли в области сердца, сердцебиение.
При объективном исследовании можно выявить: отёки (от пастоз-
ности до анасарки), изменения сердечно-сосудистой системы (гипертензия, систолический шум на верхушке, признаки гипертрофии лево-
174
го желудочка, метаболические изменения миокарда), иногда признаки ХПН.
В зависимости от сочетания основных признаков ХГН выделяют следующие клинические его варианты: гематурический, нефротический, смешанный.
Основными проявлениями нефротического синдрома являются: массивные отеки, протеинурия выше 3 г/л в сутки, диспротеинемия (снижение уровня γ- глобулинов, повышение α2-глобулинов), гиперлипидемия (гиперхолестеринемия, повышение уровня общих липидов).
Ведущими признаками гематурического варианта ХГН считают:
стойкую гематурию (как микро- , так и макрогематурию), небольшую протеинурию (до 1-2 г/л в сутки), анемию. В некоторых случаях встр е- чается пастозность век, повышение артериального давления.
Для смешанной формы ХГН характерны: тяжелое состояние больных, неуклонно прогрессирующее течение заболевания, стойкая артериальная гипертензия, массивные отеки, гипокомплементемия (снижение С3 и/или С4 фракции комплемента), частое развитие ХПН.
Особенности различных вариантов ХГН
Нефротический синдром с минимальными изменениями
(НСМИ, НС) – симптомокомплекс, включающий массивную протеинурию (более 2-3 г/л/сут), гипоальбуминемию (ниже 25 г/л), гиперлипидемию и массивные отеки.
Эпидемиология. НС встречается с частотой 0,5 на 10000 детского населения. НСМИ является особенностью детей раннего и дошкольного возраста (1,5-7 лет), чаще болеют мальчики 2:1 и дети с отягощенным аллергологическим анамнезом.
Этиология. НС развивается вследствие нарушения проницаемости почечных клубочков. Наиболее частой причиной НС у детей является нефрит с минимальными изменениями (НСМИ). Кроме этого НС развивается при гломерулонефритах, внутриутробных инфекциях, системных заболеваниях соединительной ткани, геморрагических васкулитах. При НСМИ выявляются ассоциации с антигенами NLA В12, В13, ДR-5, DR-7. При атопическом НСМИ выявляется высокий уровень IgG в сыворотке крови.
Патогенез. Поражение капсулы Шумлянского-Боумена могут иметь различные механизмы. У части детей имеет место наследственно обусловленное поражение подоцитов. В некоторых случаях повреждение гломерулярного барьера происходит вследствие развития патологических иммунологических реакций, в основе которых лежит формирование иммунных комплексов. У части детей повреждение
175
клубочков происходит за счет отложения IgM, или развития склеротических изменений.
Следствием перечисленных механизмов является появление массивной протеинурии. Протеинурия – чаще альбуминурия, обусловлена утратой зарядно-селективной функции клубочкового фильтрационного барьера.
Гипопротеинемия приводит к снижению онкотического давления в крови. Развивающаяся гиповолемия способствует перемещению Na+ и Н2О в межклеточное пространство через валюмоосмоцепторы. Активация системы ренин – ангиотензин – альдостерон приводит к задержке Na+ , воды и усилению отеков. Компенсаторное увеличение синтеза АДГ ведет к увеличению ОЦК, что способствует уменьшению диуреза.
Клиническая классификация первичного ГН с НС (в соответст-
вии с классификацией Н. Сперанского с соавт., 1996, с дополнениями М.С. Игнатовой, Ю.Е. Вельтищева, 1982).
Клинические формы ГН с НС:
Нефротическая (клинически «чистый» НС).
Смешанная (НС в сочетании с гематурией и /или артериальной гипертензией).
Активность ГН:
III (экстраренальные проявления: отёки, артериальная гипертензия, максимальная выраженность мочевого синдрома и обменных сдвигов); II (умеренно выраженные мочевой синдром и обменные наруше-
ния);
I (минимальные мочевой синдром и обменные нарушения); 0 (нормализация всех показателей).
Течение:
Циклическое (без рецидивов); Рецидивирующее; Непрерывно рецидивирующее; Торпидное; Быстропрогрессирующее.
Функции почек:
ПН 0, ПН I, ПН IIа, ПН IIб (эквивалент ранней фазы ХПН), ХПН – хроническая почечная недостаточность.
Классификация НС с позиций чувствительности к глюкокор-
тикоидной терапии (International Study of Kidney Disease in Children, 1981).
176
Гормоночувствительный НС (ГЧНС) – полная клинико-
лабораторная ремиссия у больных наступает при лечении преднизолоном. Исключить вариант ГЧНС можно только в том случае, если проводилось лечение преднизолоном в дозе 2 мг/кг/сут или 60 мг/м2 (не более 80 мг/сут) в течение 6 недель.
Гормонорезистентный НС (ГРНС) – когда при лечении преднизо-
лоном в дозе 2 мг/кг/сут или 60 мг/м2 (не более 80 мг/сут) в течение 6 недель не исчезает протеинурия.
Часторецидивирующий НС (ЧРНС) – рецидивы ГЧНС возникают 4
и более раз в год, или 2 и более раз в 6 месяцев , при условии соблюдения правильных режимов лечения.
Гормонозависимый НС (ГЗНС) – обострения ГЧНС развиваются при снижении дозы преднизолона, или в течение 2 недель после его отмены (при правильном лечении).
НС с частичной гормоночувствительностью - вариант ГЧНС, ко-
гда при лечении преднизолоном в адекватных дозах наблюдается исчезновение отёков, уменьшение протеинурии, но полной ремиссии не наступает.
Исследования (см. «Гломерулонефриты»).
Анамнез, клиника. Характерно внезапное начало заболевания. Отеки появляются постепенно, при относительно удовлетворительном состоянии. Отеки обнаруживаются чаще на лице, веках (ошибочный диагноз - отек Квинке, или расценивается как прибавка в весе), на нижних конечностях, следы от носков, обуви. Отеки могут быть периферическими, полостными. Отеки – рыхлые, мягкие, асимметричные, подвижные. При массивных отеках наблюдаются трещины кожи с выходом транссудата. Артериальное давление чаще в норме или повышение давления кратковременное, в случаях, когда гипоальбуминемия достигает 5-8-10г/л (централизация кровообращения при развившемся гиповолемическом шоке). Иногда бывает разжиженный стул из-за отека слизистой оболочки кишечника.
Диагноз.
Исследование мочи. Суточная протеинурия от 3-6 до 20 г/сутки и больше. Относительная плотность мочи 1026-1030. Иногда в моче выявляют гематурию (6-10%), лейкоцитурию (4-9%).
Общий анализ крови увеличение СОЭ до 50-70 мм/час. Протеинограмма. Уровень общего белка в сыворотке снижен, ги-
поальбуминемия достигает 20-5 г/л (норма 35-50 г/л), гипер-α2, β- глобулинемия.
Другие исследования. Высокая гиперлипидемия. Иногда развивается гиперфибриногенемия – угроза тромботических осложнений. На-
177
рушение функции почек происходит только при тяжелых вариантах течения заболевания.
Фокально-сегментарный гломерулосклероз (ФСГ) встре-
чается в 7-10% всех почечных биопсий, проведенных в связи с протеинурией.
Впатогенезе ФСГ лежит дефект функции Т-лимфоцитов, повышенная продукция лимфокинов (интерлейкина-2), гиперлипидемия, липидурия.
Структурные изменения гломерулярной базальной мембраны, интрагломерулярные отложения гиалина и липидов, пролиферация мезангиальных клеток, разрастание мезангиального матрикса, склеротическая адгезия в капсуле Боумена приводит к образованию участков гиалиноза и склероза в клубочках. Болезнь встречается чаще у мальчиков 6-7 лет.
Вклинической картине характерна массивная протеинурия, микро-
имакрогематурия (80%), у 20-50% детей отмечается повышение артериального давления. Через 3-5 лет появляется нарушение функции почек с исходом в терминальную стадию ХПН.
Мембранозная нефропатия встречается у 7% детей с ГН. В
патогенезе играют роль ЦИК, образование аутоантител, направленных против поверхностных клеточных антигенов, находящихся в подоци-
тах. При морфологическом исследовании выявляют диффузное утол-
щение стенок капилляров клубочков.
Мембранозный ГН у детей клинически проявляется как нефротическая форма ХГН с полным нефротическим синдромом или с изолированным мочевым синдромом (выявляемым случайно), или НС с ми к- рогематурией. Неполный НС постепенно усиливается и приводит к развитию полного НС. У 30% больных имеется связь между ХГН и антигенами вируса гепатита В, приемом медикаментов.
Мезангиопролиферативный гломерулонефрит встречается у 40-60% больных ХГН.
Особенности патогенеза. Данный нефрит имеет иммунокомплексный механизм. Характерна гипокомплементемия. Дефицит в системе комплемента приводит к персистенции антигена и образованию иммунных комплексов. Выявляется селективное поражение тромбоцитов с образованием тромбоксанов (простагландины А2 и В2), приводящих к склерозу гломерул.
178
Особенности клиники: у 1/3 больных преобладает острое начало в виде нефритического синдрома с последующим рецидивированием гематурии и протеинурии или формированием смешанной формы. Имеется связь с перенесённой инфекцией. У 2/3 детей заболевание возникает незаметно, длительно протекает латентно с протеинурией, гематурией, отёками. Чаще выявляется у детей 10-12 лет. У 1/3 больных обнаруживается снижение почечных функций.
При морфологическом исследовании выявляют пролиферацию мезангиальных клеток, расширение мезангия, отложение иммунных комплексов.
Мезангиокапиллярный гломерулонефрит характеризуется пролиферацией мезангиальных клеток и расширением мезангия, утолщением и расщеплением стенок капилляров вследствие интерпозиции в них мезангия.
Ведущими клиническими симптомами являются нефритические отёки, микро- и макрогематурия, гипертензия, которая ухудшает прогрессирование ХГН. Иногда в дебюте нефрита развивается нефротический синдром.
Характерным является длительное снижение содержания в крови С3 и С4 фракций комплемента.
Данный вариант ХГН имеет прогрессирующее течение с формирование ХПН в течение 10 лет у половины больных.
Быстропрогрессирующий гломерулонефрит (БПГН)
Экстракапиллярный пролиферативный гломерулонефрит с полулуниями, подострый злокачественный гломерулонефрит (БПГН) – это синонимы одного заболевания, сущностью которого является чрезвычайно высокая активность гломерулонефрита, быстрое развитие и прогрессирование почечной недостаточности.
БПГН – может быть как самостоятельным заболеванием, так и являться проявлением других нефропатий. БПГН, развивающийся как самостоятельное заболевание, называется первичным. Вторичный БПГН является проявлением инфекционных, системных заболеваний, опухолевых процессов.
Различают 3 формы первичного БПГН: а) нефрит с антителами против антигенов гломерулярной базальной мембраны, б) иммунокомплексный БПГН, в) БПГН без иммунных комплексов.
В основе патогенеза БПГН лежит образование антител против базальной мембраны почек, или поражение мембраны иммунными комплексами. При иммунокомплексном варианте поражение мембраны
179
активирует сосудисто-тромбоцитарное и гемокоагуляционное звенья гемостаза, а также фибринолитическую систему, что приводит к изменению структуры эндотелия, образованию тромбов в сосудах почек. В результате происходит разрушение структуры базальной мембраны.
Морфологически при БПГН выявляется картина пролиферативного экстракапиллярного нефрита с образованием полулуний.
Клиника. Первые признаки БПГН нередко появляются после перенесённого острого инфекционного заболевания, чаще стрептококковой этиологии. Первыми симптомами нефрита являются отёки, макрогематурия, а так же повышение артериального давления. Повышение артериального давления обычно носит стойкий, выраженный и прогрессирующий характер. В дебюте заболевания сразу появляется олигоанурия, которая может быстро приводить к ОПН. У большей части больных в клинической картине заболевания преобладает нефротический вариант гломерулонефрита с гематурией и стойким повышением артериального давления. Со стороны крови обычно выявляется анемия и выраженная активность воспалительного процесса. Течение БПГН непрерывно-прогрессирующее. При выявлении в биоптате полулуний прогноз у больного обычно неблагоприятный.
Диагноз. В типичных случаях диагноз ХГН устанавливается на основании особенностей клиники (нефротический синдром, гематурия, смешанная форма) и результатов исследования мочи (протеинурия, гематурия, цилиндрурия). Существенное значение при постановке диагноза имеет определение степени активности воспалительного процесса (выраженность воспалительных изменений со стороны крови, степень изменений в протеинограмме и т. д.). Для подтверждения наличия нефротического синдрома важное значение имеет выявление гиперлипидемии или гиперхолестеринемии.
Для оценки иммунологической активности ХГН изучают изменения в иммунограмме (снижение фракций комплемента, повышение уровней ЦИК, изменение уровней иммуноглобулинов и др.).
Вирусологическое и бактериологическое исследование при ХГН в некоторых случаях позволяет уточнить генез заболевания, установить этиологию очагов хронической инфекции, своевременно диагностировать присоединение осложнений.
Дифференциальный диагноз ХГН необходимо проводить с: острыми гломерулонефритами, интерстициальным нефритом, наследственным нефритом, гломерулонефритами, развившимися на фоне системных заболеваний соединительной ткани.
180
Табл. 1.52. Дифференциальный диагноз признаки острого и хронического гломерулонефрита (Маковецкая Г.А. 1987, с измене-
ниями)
Признаки |
Острый нефрит |
Хронический |
|
(нефритическая |
нефрит (гемату- |
|
форма) |
рическая форма) |
Клинические: |
|
|
- возраст к началу болезни, |
5-10 лет |
Прослеживается |
- связь со стрептококковой |
Прослеживается у |
как в начале бо- |
и вирусной инфекцией, |
60% больных, |
лезни, так и в пе- |
|
|
риод обострения. |
- развитие болезни |
Через 1-2 недели |
Чаще постепенное: |
|
после перенесён- |
1) как исход остро- |
|
ного стрептокок- |
го заболевания |
|
кового или вирус- |
возможно после |
|
ного заболевания |
длительного ла- |
|
|
тентного периода, |
|
|
2) как первично- |
|
|
хроническое, неза- |
|
|
метное |
Симптомы интоксикации: |
|
|
- головная боль, |
Отмечается всегда |
Характерна |
- усталость, |
Отмечается всегда |
Характерна |
-недомогание, |
Отмечается всегда |
Жалобы отсутст- |
|
|
вуют |
- анорексия |
Имеется у части |
Жалобы отсутст- |
|
больных |
вуют |
|
|
|
Отёки |
У 60-80% больных |
Могут отсутствовать |
Артериальная гипертензия |
У 1/3-1/4 больных, |
При развитии ХПН |
|
кратковременная |
|
Лабораторные изменения: |
|
|
- макрогематурия, |
У 50% больных |
Отсутствует вне |
|
|
обострения |
- микрогематурия, |
Имеется |
Имеется |
- протеинурия, |
0,5-1,0 г в сутки |
0,5-4 г в сутки |
- цилиндрурия, |
встречается, эрит- |
Может не отме- |
|
роцитарные |
чаться |
181
- относительная плотность |
Нормальная |
Снижена |
мочи |
|
|
|
|
|
- клубочковая фильтрация, |
Снижена на 25- |
Снижена значи- |
|
30% |
тельно |
- олигурия, |
Имеется |
Нет |
- анемия, |
Наблюдается в |
Стойкая у 1/3 |
|
начале заболевания |
больных |
- лейкоцитоз, |
У 15-30% больных |
Нет |
- увеличение СОЭ |
У 75% больных |
Вне обострения |
|
|
СОЭ не увеличена |
Биохимические показатели |
|
|
крови: |
|
|
- гипопротеинемия, |
Обычно имеется |
Имеется |
- гипергаммаглобулинемия |
У всех больных |
Имеется |
|
|
Вне обострения |
- гиперфибриногенемия |
Есть |
нет |
|
|
|
- уровень серомукоида, |
Повышен |
Нет повышения |
- гиперхолестеринемия, |
Повышен |
У 15-30% больных |
- уровень лизолецитина |
Повышен |
Не повышен |
Осложнения: |
|
|
-острая сердечная недоста- |
У 5% больных, |
редко в терми- |
точность, |
|
нальной фазе, |
- гипертензионная энцефа- |
У 2% больных, |
не развивается, |
лопатия, |
|
|
- почечная недостаточ- |
Возможно разви- |
возможно развитие |
ность |
тие ОПН |
ХПН |
Лечение. Задачи лечения: купирование воспалительных изменений в почках (удаление антигена из внешней среды или организма больного, воздействие на иммунную систему больного, торможение медиаторов воспаления (комплемента, активности протеаз клеток, тромбоцитов, кининов, лимфокинов, гистамина, простагландинов)); ликвидация основных синдромов ХГН (отечный, гипертензионный и др.), лечение поражений ЦНС, сердечно-сосудистой системы; предупреждение осложнений гломерулонефрита и формирования ХГН.
Перед назначением терапии ХГН необходимо учесть:
1.тяжесть клинической симптоматики;
2.степень активности процесса;
182

3.особенности течения и проявления заболевания;
4.результаты предшествующего лечения;
5.результаты проведенного дифференциального диагноза.
Схема лечения. Обязательные мероприятия: режимные мероприя-
тия, диета, цитостатики и глюкокортикоиды; при гиперкоагуляции применяют гепарин и антиагреганты; НПВС (при отсутствии почечной недостаточности).
Вспомогательное лечение: диуретики и гипотензивные препараты; при гематурии - Σ-аминокапроновая кислота или дицинон, делагил, лечение осложнений заболевания.
Показания для госпитализации: ХГН лечится в специализирован-
ных отделениях.
Режим. Больные с ХГН находятся на постельном режиме до нормализации артериального давления, исчезновения (уменьшения) отеков.
Диета при обострении ХГН предусматривает ограничение объема жидкости, поваренной соли, количества белка (при снижении функции почек) на 2-4 недели. Жидкость назначается по диурезу предыдущего дня с учетом экстраренальных потерь (около 500 мл для детей школьного возраста). При малосимптомном течении заболевания ограничения режима и диеты нецелесообразны.
Особенности медикаментозной терапии ХНГ зависят от клиники заболевания, формы, морфологического варианта, функционального состояния почек, наличия осложнений.
Основными компонентами патогенетической терапии ХГН являются: глюкокортикоиды, гепарин, цитостатики, антиагреганты, ингибиторы АПФ, гиполипидемические препараты (статины). Перечисленные препараты назначаются чаще всего в различных сочетаниях в зависимости от формы заболевания и морфологического варианта ХГН.
Схематично лечение ХГН можно представить в следующем виде
(табл. 1. 53).
Табл. 1.53. Патогенетическая терапия ХГН
Форма ХГН
гематурическая форма |
нефротическая форма |
смешанная фор- |
|
|
ма |
Антиагреганты |
Преднизолон, метил- |
Антиагреганты |
|
преднизолон* |
|
Антикоагулянты |
Циклоспорин А |
Антикоагулянты |
Препараты, улучшаю- |
Иммуномодуляторы: |
Преднизолон, |
183
щие реологию крови и |
левамизол |
метилпреднизо- |
кровоток |
|
лон |
Мембраностабилизато- |
Мембраностабилизато- |
Плазмаферез |
ры |
ры: кетотифен (при на- |
|
|
личии аллергии) |
|
Противовоспалитель- |
Цитостатики: хлорбу- |
|
ные препараты: плак- |
тин, циклофосфан |
|
венил, резохин |
|
|
* см. рис. 1.23. |
|
|
Особенности лечения различных морфологических вариантов ХГН
Гормонорезистентный нефротический синдром с минимальными изменениями, мезангиопролиферативный гломерулонефрит:
циклофосфамид 10-12 мг/кг в течение 3-4 недель, затем поддерживающая доза на 6-12 месяцев. Циклофосфамид назначают совместно с преднизолоном по 1 мг/кг на протяжении 6-12 месяцев с постепенным снижением дозы. Возможно сочетание преднизолона с циклоспорином, или преднизолона с микофенолата мофетилом.
Фокальный сегментарный гломерулосклероз: преднизолон 1
мг/кг на протяжении до 12 месяцев альтернирующим курсом с постепенным снижением дозы до полной отмены вместе с циклоспорином. Так же применяют сочетание циклофосфамида и преднизолона длительностью до 6-12 месяцев. В некоторых случаях показана пульстерапия метилпреднизолоном в стартовой дозе 30 мг/кг внутривенно.
При отсутствии эффекта от иммуносупрессивной терапии назначают ингибиторы АПФ в виде монотерапии или в комбинации с антагонистами рецепторов ангиотензина II – каптоприл, эналоприл, лозартан.
184
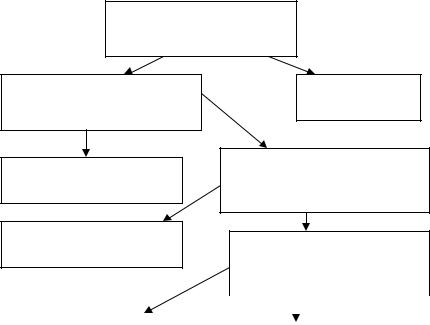
1-й эпизод НС
Преднизолон 2 мг/кг/24 ч 6 нед. (при частичной чувствительности + МП в/в 30 мг/кг №3), затем 1,5 мг/кг/48 ч 6 нед.
Первые 2-3 рецидива ГЧНС
Преднизолон 2 мг/кг/24 ч до исчезновения протеинурии в 3-х ан. мочи, затем 15 мг/кг/48 ч 4 нед.
Редкие рецидивы ГЧНС
Лечится так же, как первые 23рецидива
Редкие рецидивы ГЧНС
Лечатся так же, как первые 2-3 рецидива
ГРНС
Биопсия почечной ткани
ЧРНС и ГЗНС
Так же преднизолон + левамизол 2,5 мг/кг/48 ч 6-12 мес. Или: так же преднизолон + кетотифен 1,0-3,0 мг/24 ч 4-6 мес. (при наличии аллергии)
ЧРНС и ГЗНС
Так же преднизолон + хлорбутин 0,15-0,2 мг/кг/24 ч. 8-10 нед. или : так же преднизолон + циклофосфан 25 мг/кг/24 ч 8-12 нед.
|
|
|
|
|
|
|
Редкие рецидивы ГЧНС |
|
|
ЧРНС и ГЗНС |
|
|
||
|
Лечатся так же, как, как первые 2-3 рециди- |
|
||
Биопсия почечной ткани |
|
|
||
|
ва |
|
||
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Рис. 1.23. Алгоритм патогенетической терапии нефротического синдрома при первичном гломерулонефрите (Методическое посо-
бие для врачей, 2001)
Мембранопролиферативный гломерулонефрит: преднизолон в дозе 1 мг/кг альтернирующим курсом с постепенной отменой препарата. Общая длительность лечения до 1 года. Описаны схемы лечения, включающие сочетание циклофосфамида и преднизолона, преднизолона и циклоспорина. Во всех случаях предусматривается лечение от 9 до 12 месяцев.
Экстракапиллярный гломерулонефрит с полулуниями: показано назначение плазмафереза в сочетании с циклофосфамидом в дозе 12 мг/кг. Затем назначается терапия, включающая циклофосфамид, преднизолон, гепарин, дипиридамол.
Посиндромная терапия
185
Для коррекции артериальной гипертензии используют: каптоприл,
эналоприл, вальсартан, лозартан, амлодипин, нифедипин. Ингибиторы АПФ назначают не только для коррекции артериальной гипертензии, но и при отсутствии эффекта от иммуносупрессивной терапии.
Для лечения отечного синдрома используют: фуросемид по 1-2
мг/кг 1-2 раза в сутки (длительность терапии определяется индивидуально). При отеках, рефрактерных к фуросемиду назначают альбумин 20% по 0,5-1,0 г/кг внутривенно капельно. После введения альбумина вновь назначают фуросемид в виде монотерапии или в сочетании со спиролактоном в дозе 1-2 мг/кг 2-3 раза в сутки.
Следует иметь в виду, что длительная терапия глюкокортикоидами и цитостатиками имеет большое количество серьезных осложнений. К острым осложнениям глюкокортикоидной терапии относят: эйфорию, депрессию, нарушение сна, задержку жидкости.
Хронические осложнения глюкокортикоидной терапии проявляются: ожирением, миопатией, появлением стрий, атрофией кожи, задержкой роста, остеопорозом, гирсутизмом и др.
Применение цитостатиков приводит к: тошноте, рвоте, поносу, алопеции, инфекциям, тремору, тромбоцитопении, повышению уровня креатинина и др.
Осложнения. Осложнениями ХГН могут быть резкие нарушения водно-электролитного обмена, ОПН, отек мозга, отек сетчатки глазного дна с расстройством зрения. Возможен гиповолемический шок, почечная эклампсия. В некоторых случаях имеет место присоединение инфекционных заболеваний: перитонит, сепсис, рожа, пневмонии; развитие тромбоэмболических осложнений, ХПН.
Профилактика ХГН предусматривает предупреждение рецидивов заболевания (ограничение физической нагрузки, стрессов, переохлаждений, уменьшение числа инфекционных заболеваний, санация очагов хронической инфекции).
Прогноз при ХГН зависит от клинико-морфологического варианта заболевания, особенностей его течения, наличия или отсутствия осложнений, чувствительности или рефрактерности к лечению. При наличии ХГН с изолированным гематурическим синдромом или при гормоночувствительном варианте нефротического синдрома прогноз благоприятный.
У больных с фокально-сегментарным гломерулосклерозом средний срок развития ХПН составляет 6-8 лет. Даже после трансплантации почки у этих больных может развиться рецидив заболевания.
При быстропрогрессирующем гломерулонефрите, при наличии полулуний более чем в 50% клубочков, без проведения интенсивной те-
186

рапии выживаемость не превышает 6-12 месяцев. При поражении меньшего числа клубочков прогноз при проведении интенсивной терапии существенно улучшается.
Вопросы к экзамену. Хронический гломерулонефрит. Патогенез.
Классификация. Морфологические критерии, характеризующие хронизацию процесса. Особенности клинической картины в зависимости от формы. Диагностика. Дифференциальный диагноз. Течение. Лечение. Осложнения. Исходы. Прогноз.
ИНФЕКЦИЯ МОЧЕВЫВОДЯЩИХ ПУТЕЙ (ИМВП). Под тер-
мином ИМВП понимают инфицированность мочевых путей без четкого указания уровня поражения мочевой системы.
ИМВП у детей любого возраста характеризуется воспалительным процессом, сопровождающимся появлением в моче лейкоцитурии и бактериурии (или изолированной бактериурии). Различают симптоматическую бактериурию (когда имеются симптомы интоксикации, дизурии, болевой, абдоминальный синдром) и асимптоматическую бактериурию – когда нет клинических проявлений, и ИМВП протекает скрыто, или является случайной находкой при обследовании детей.
Частота симптоматической и асимптоматической (чаще) ИМВП в период новорожденности: 0,5%-2,0%. После 1-го месяца жизни происходит снижение частоты ИМВП у мальчиков достигая 1-2% в раннем возрасте, 0,5% в дошкольном возрасте, 0,1% - в пубертатном периоде.
Классификация ИМВП (J.Winbtrg, 1987)
I. Неосложненная ИМВП: асимтоматическая; симптоматическая; II. Осложненная ИМВП: асимтоматическая; симптоматическая. III. Уровни инфицирования и поражения при ИМВП (пиелонефрит,
цистит, уретрит).
Под осложненной формой ИМВП понимают инфицирование мочевых путей, возникающее на фоне нарушения уродинамики, как правило, обусловленной аномалиями их развития (рефлюксы, нейрогенный мочевой пузырь, и др.). Неосложненная ИМВП обусловлена транзиторной (функциональной) обструкцией мочевых путей.
Диагностически значимым для ИМВП считается присутствие колоний микроорганизмов одного вида в моче:
-100000 микробных тел в 1 мл мочи;
-10000 колоний микроорганизмов одного вида в 1 мл мочи, взятой катетером;
187
- любое количество колоний в 1 мл мочи, полученной путем надлобковой пункции.
ПИЕЛОНЕФРИТ (ПН) – неспецифическое микробновоспалительное заболевание почек с преимущественным поражением канальцев, чашечно-лоханочной системы и интерстиция.
Эпидемиология. Острый ПН занимает второе место после ОРИ по данным ВОЗ (от 12 до 54 на 1000 детского населения). В структуре заболеваний мочевой системы микробно-воспалительные заболевания почек составляют 70-80%. На первом году жизни мальчики и девочки болеют почти одинаково. Одной из причин частого ПН у мальчиков является физиологический фимоз. 85% детей заболевают ПН в первые 6 месяцев жизни, 30% - в период новорожденности. Заболеваемость на втором году жизни понижается, а затем снова возрастает на третьем году жизни и школьном и пубертатном периоде.
Девочки (за исключением детей первого года жизни) болеют чаще в силу анатомо-физиологических особенностей строения мочеполовой системы, особенностей их гормонального фона. У мальчиков после года заболевание чаще развивается на фоне аномалий мочевыводящих путей.
Этиология. Основной возбудитель ПН – кишечная палочка (до 90%). Грамположительные микроорганизмы являются этиологическим фактором в 8,4%. Смешанная флора наблюдается у 12-25% больных. Изучается роль хламидийной инфекции, уреаплазмы, микоплазмы в развитии ПН.
Вирусная инфекция способствует обострению персистирующей бактериальной инфекции. При длительной антибактериальной терапии возможна грибковая этиология ПН.
На характер микрофлоры оказывают влияние: возраст ребенка, пол, условия инфицирования (больничное, внебольничное), состояние иммунной системы, особенности питания, состояние экологии, аномалии развития мочевой системы и др.
Патогенез. Развитию ПН способствуют:
I. Эндогенные факторы риска развития ПН: ранний возраст ре-
бенка, особенности главного комплекса гистосовместимости, аномалии развития мочевых путей, отягощенная наследственность, недоношенность, перинатальные заболевания ЦНС, аномалии конституции, функциональные заболевания ЖКТ, и мочевой системы, нарушения иммунитета, салурия, эндокринные заболевания, железодефицитная анемия.
188
II. Экзогенные факторы риска развития ПН: неблагоприятные ус-
ловия экологии, нарушения питания, частые ОРИ, глистная инвазия, вредные привычки родителей, мастурбация, ранняя половая жизнь и т.д.
Важным моментом в развитии ПН является выраженность патогенных свойств микроорганизмов (адгезия, выделение уреазы и т. д.);
Факторы уропатогенности бактерий (E. Coli):
-реснички Р-фимбрии, которые дают возможность прикрепляться
куроэпителию, могут перемещаться против тока мочи;
-К-антигены бактерий препятствуют опсонизации и фагоцитозу;
-О-антигены определяют эндотоксический эффект;
-эндотоксин снижает перистальтику мочевых путей вплоть до полной блокады, функциональной обструкции.
Таким образом, адгезия бактерий к уроэпителию препятствует их механическому вымыванию из мочевых путей, эндотоксический эффект ведет к нарушению уродинамики, облегчает ретроградное передвижение микробов. В итоге - возбудители колонизируют почки, вызывают альтерацию почечной ткани, т. е. участвуют в формировании всех звеньев патогенеза.
Пути инфицирования почек: а) восходящий в 80% (при обструк-
тивном ПН); б) гематогенный (у новорожденных, у старших детей при остеомиелите); в) лимфогенный (при кишечных инфекциях, дисбактериозе).
Этапы патогенеза пиелонефрита
1-й этап. Преморбидный – пребывание уропатогенов в исходном биотоке, накопление в организме потенциальных возбудителей инфекции.
2-й этап. Транслокации – миграция уропатогенов в почки. Преодоление микроорганизмами иммунобиологических барьеров хозяина, прорыв микрофлоры в кровяное русло, лимфоток → гематогенная, лимфогенная диссеминация, заканчивающаяся инфицированием почки.
3-й этап. Колонизация – заселение уропатогенами почек.
4-й этап. Альтерация – инициация воспалительного процесса в почках (клиника воспаления). Продукция бактериями гистоповреждающих субстанций.
5-й этап. Санация – элиминация уропатогенов из почек, или этап персистенции.
В 80% случаев ПН развивается на фоне аномалии верхних и нижних мочевых путей при нарушении уродинамики.
Классификация
189
Табл.1. 54. Классификация пиелонефрита у детей (Всесоюзный симпозиум «Пиелонефрит у детей», 1980)
|
Формы пиелонефрита |
Активность бо- |
Функции почек |
|
|
|
|
лезни |
|
1. |
Первичный |
1. Острый |
1. Активная ста- |
1. Сохранение |
2. |
Вторичный: |
2. Хрони- |
дия (I, II, III сте- |
функции почек |
а) обструктив- |
ческий: |
пени активности). |
2. Нарушение |
|
|
ный |
а) рециди- |
2. Частичная кли- |
функции почек |
б) необструк- |
вирую- |
нико- |
(ПН I, II, III) |
|
тивный (тубуло- |
щий |
лабораторная ре- |
3. Хроническая |
|
патии, обменные |
б) латент- |
миссия. |
почечная недос- |
|
нарушения, по- |
ный |
3. Полная клини- |
таточность |
|
чечный дизэм- |
|
ко-лабораторная |
|
|
|
бриогенез) |
|
ремиссия |
|
Исследования. Общий анализ крови и мочи, моча на бактериурию, посев мочи, морфология мочевого осадка анализы мочи по Нечипоренко, Амбурже, Аддиса-Каковского.
В сложных случаях проводят исследования мочи на: хламидии, микоплазмы, уреаплазмы методами полимеразной цепной реакции (ПЦР, бактериологические методы, серологические методы); грибы (на среду обогащения Сабуро); вирусы (методами ПЦР, серологическими, вирусологическими); микобактерии туберкулеза (посев мочи, методы экспресс-диагностики).
Обязательные лабораторные исследования для характеристики функционального состояния почек: уровень креатинина, мочевины в крови; проба Зимницкого (у детей до 4-5 лет «свободная» проба Зимницкого); клиренс эндогенного креатинина, исследование рН, титруемой кислотности, экскреции аммиака); контроль диуреза; ритм и объем спонтанных мочеиспусканий.
Обязательные инструментальные исследования при микробновоспалительных заболеваниях мочевой системы:
-Измерение артериального давления;
-УЗИ органов мочевой системы;
-Рентгено-контрастные исследования (цистография, экскреторная урография).
Консультации специалистов (по показаниям): уролога, детского
хирурга; окулиста; невропатолога; оториноларинголога; стоматолога; фтизиатра.
190
Дополнительные методы диагностики
Мазок из влагалища у девочек, соскоб на энтеробиоз. У детей грудного возраста при остром течении ПН с признаками поражения ЦНС, сердечно-сосудистой системы, печени, почек - биохимический анализ крови (трансаминазы, калий, натрий, хлориды); кислотно-основное состояние; КТ, МРТ, радионуклидные исследования и др.
Анамнез, клиника. В анамнезе детей с ПН часто встречаются «беспричинные» повышения температуры, длительные субфебрилитеты, беспокойство, плач при мочеиспускании, дизурические расстройства, анорексия, срыгивания, рвота, проявления энуреза, боли в области поясницы, частые ОРИ, кишечные инфекции, дисбиозы кишечника.
Клиника ПН, зависит от возраста, наличия аномалий развития мочевой системы, обменных и иммунных нарушений, этиологии заболевания.
Описаны два основных варианта течения ПН 1. Острое начало, с относительно бурным развитием всех симптомов болезни.
2. Постепенное, последовательное появление основных признаков заболевания. У детей старшего возраста могут отмечаться все симптомы заболевания.
Лихорадка – один из важнейших признаков ПН. Температура может повышаться до высоких цифр, носить упорный характер, без катаральных явлений в зеве, сопровождаться многократной рвотой, головной болью, слабостью, утомляемостью. Иногда температура длительно субфебрильная.
Дизурические симптомы могут быть самого различного характера от энуреза до недержания мочи днем, императивные позывы, поллакиурия, натуживание, прерывистое мочеиспускание чаще при обструкции нижних отделов мочевыводящих путей.
Болевой симптом характеризуется разнообразием. Иногда боли слабо выражены, могут быть односторонними. У маленьких детей боли локализуются в околопупочной области, с иррадиацией боли в спину, лопатку, по ходу мочеточников, паховую область, бедро.
Интенсивность болей свидетельствует о резко выраженном отеке почки с нарушением гемо- и уродинамики. Возможно внезапное появление болей при нарушении оттока мочи при уретерогидронефрозе, мегауретере, пузырно-мочеточниковом рефлюксе, спазме мускулатуры, при подвижной почке (боль при беге, быстрой ходьбе).
Мочевой синдром проявляется помутнением мочи, изменениями в анализах мочи.
Объективно: интоксикационные проявления, боли (болезненность при поколачивании в поясничной области, болезненная пальпация жи-
191
вота, особенно по ходу мочеточников, с напряжением мышц брюшной стенки). Пастозность век, голеней, тени вокруг глаз. Повышение артериального давления не характерно, но оно может появиться при прогрессировании хронического ПН.
Для хронического ПН характерна субфебрильная температура в течение длительного времени с периодами подъема до фебрильных цифр. Течение или рецидивирующее, или латентное. Рецидивы протекают как острый ПН. При латентном течении - умеренные явления интоксикации и изменения в анализах мочи.
Уноворожденных детей и у детей раннего возраста в клинике ПН преобладают неспецифические проявления: интоксикация, повышение температуры, бледность, снижение аппетита, рвота или срыгивания, плохая прибавка в массе тела, поносы. Дизурические симптомы представлены беспокойством или плачем перед или вовремя мочеиспускания, натуживанием, прерывистой струей мочи.
Удетей в возрасте 1,5-2 лет ПН также может протекать малосим-
птомно, с преобладанием общеинтоксикационных проявлений заболевания. Иногда выявляется задержка мочи.
Среди детей 4-5 лет выявляют те или иные проявления болевого синдрома (чаще недифиренцированная боль); клиника дизурических проявлений становиться ярче, общеинтоксикационные проявления угасают.
У детей старшего возраста ПН проявляется болевым синдромом (в животе, поясничной области, над лобком), дизурическими симптомами, различными вариантами лихорадки, проявлениями интоксикации.
Диагноз ПН устанавливается при наличии дизурических проявлений, интоксикации, лихорадки, бактериурии (более 10.5 кое/мл микробных тел одного вида), нейтрофильной лейкоцитурии, снижения секреции водородных ионов (Н+) и солей аммония, титруемых кислот. В некоторых случаях выявляются признаки нарушения функционального состояния почек (изостенурия, гипостенурия); повышение в крови уровня мочевой кислоты, а в моче уровней уратов, оксалатов.
УЗИ почек - дает информацию в отношении размеров, формы почек, плотности паренхимы, соотношения коркового и мозгового вещества, размеров собирательной системы и строения мочевого пузыря. При ПН отмечается увеличение размеров почек с диффузным поражением за счет интерстициального отека. УЗИ позволяет выявить камни в почках и мочевом пузыре, дистопию и аномалию развития лоханок, мочеточников, мочевого пузыря, уменьшение размеров почек при склерозировании паренхимы.
192
Рентгенологическое обследования детей с ПН
Показания к проведению урографии: ИМВП; опухоли в животе;
немотивированные боли в животе; гипертензия; врожденные аномалии, которые могут сочетаться с аномалиями почек; признаки и симптомы поражения нижних мочевых путей; нефролитиаз; подозрение на пороки развития мочевой системы по результатам УЗИ.
Показания к проведению микционной цистографии: мочевая ин-
фекция; микрогематурия; боли в животе неясной этиологии; дизурические явления, поллакиурия, затрудненное и редкое мочеиспускание; различные варианты энуреза; патология верхних мочевых путей; аномалии наружных половых органов; атрезия анального отверстия и прямой кишки; повреждение мочевого пузыря и уретры; динамическое наблюдения после травмы нижних мочевых путей; опухоль живота и таза; заболевания нервной системы, вызывающие расстройства мочеиспускания; динамическое наблюдение в ходе консервативного и после хирургического лечения рефлюкс-нефропатии; изменения на УЗИ мочевого пузыря с опорожнением.
При микционной цистографии выявляют нарушения пассажа мочи, рефлюксы, обструкцию уретры, признаки нейрогенного мочевого пузыря.
При экскреторной урографии - проявления ПН, обструкции ПУС, пороки развития почек, мочеточников, снижение функции почек.
Степень активности ПН определяет по выраженности воспалительных изменений со стороны крови и мочи и других показателей активности воспалительного процесса.
Табл. 1.55. Классификация степеней активности пиелонефрита
(Всесоюзный симпозиум «Пиелонефрит у детей», 1980)
Степень |
Клиниче- |
Лабораторные показатели |
|
актив- |
ские сим- |
|
|
кровь |
моча |
||
ности |
птомы |
|
|
|
|
|
|
III |
Токсикоз, |
Лейкоцитоз со |
Массивная нейтрофиль- |
|
лихорадка, |
сдвигом влево, ↑ |
ная лейкоцитурия, ис- |
|
тошнота, ди- |
СОЭ, ↓ в крови |
тинная бактериурия. |
|
зурические |
альбуминов, ↑ α- |
Может быть гематурия, |
|
расстройства, |
глобулинов, β- |
протеинурия, аминоаци- |
|
пастозность |
липопротеидов |
догенез ↓ |
|
век |
|
|
II |
Симптомы |
Умеренная дис- |
Умеренная нейтрофиль- |
|
интоксика- |
протеинемия, ↑ β |
ная лейкоцитурия. Бак- |
193
|
ции, темпера- |
-липопротеидов, |
териурия, функция ами- |
|
тура нор- |
ДФА, умерен- |
ноацидогенеза ↓ |
|
мальная или |
ный лейкоцитоз, |
|
|
периодически |
↑ СОЭ |
|
|
субфебриль- |
|
|
|
ная |
|
|
I |
Нет |
Не изменены |
Пиурия определяется |
|
|
|
только при количествен- |
|
|
|
ном исследовании мочи, |
|
|
|
бактериурии нет. Функ- |
|
|
|
ция аминоацидогенеза |
|
|
|
нормальная или незначи- |
|
|
|
тельно ↓ |
0 |
Нет |
Не изменены |
Нормальный анализ мо- |
|
|
|
чи даже после провока- |
|
|
|
ционной преднизолновой |
|
|
|
пробы |
Диагноз острого ПН правомочен в течение 6 месяцев от начала заболевания.
Диагноз «первичный ПН» используется в тех случаях, когда при применении современных методов исследования не выявляется какаянибудь аномалия или другие изменения.
В диагнозе ПН необходимо указывать степень активности воспалительного процесса (таб. 1.55).
Дифференциальный диагноз ПН необходимо проводить с: гломерулонефритом, туберкулезом почек, тубулопатиями, интерстициальным нефритом, инфекцией мочевыводящих путей, циститом, вульвовагинитом, баланопоститом, острым аппендицитом.
Табл.1.56. Дифференциальный диагноз пиелонефрита и острого цистита (Маковецкая Г.А., 1987, с изменениями)
Признак |
Цистит |
Пиелонефрит |
Повышение температуры |
Не характерно |
Характерно |
тела выше 38 °С |
|
|
Симптомы интоксикации |
Не наблюдаются |
Наблюдаются часто |
Поллакиурия |
Наблюдается |
Не наблюдается |
Императивные позывы на |
Отмечаются всегда |
Не отмечаются |
мочеиспускание |
|
|
194
Императивное недержа- |
Отмечаются часто |
Не наблюдаются |
ние мочи, энурез |
|
|
Ощущение жжения во |
Отмечаются часто |
Не наблюдаются |
время мочеиспускания и |
|
|
после мочеиспускания |
|
|
Задержка мочи |
Наблюдается у |
Наблюдается |
|
маленьких детей |
|
Боли в пояснице |
Не наблюдаются |
Наблюдаются |
СОЭ |
Не изменена |
Повышена (20-25 |
|
|
мм/ч и выше) |
С-реактивный белок |
Отрицательный |
Положительный |
Протеинурия |
Отсутствует |
Наблюдается |
Признаки вагинита |
Наблюдаются у 1/3 |
Не наблюдаются |
|
больных девочек |
|
Концентрационная функ- |
Не изменена |
Может быть сниже- |
ция почек |
|
на |
Обнаружение в моче бак- |
Не наблюдается |
Наблюдается |
терий, покрытых антите- |
|
|
лами (метод иммуноф- |
|
|
люоресценции) |
|
|
Рентгенологические при- |
Паренхима почек |
Изменения чашеч- |
знаки |
не изменена. Дис- |
но-лоханочной сис- |
|
функция мочевого |
темы; различные |
|
пузыря |
анатомические и |
|
|
функциональные |
|
|
дефекты верхних и |
|
|
нижних мочевых |
|
|
путей |
Лечение. Задачи лечения: борьба с инфекционным процессом, восстановление уродинамики и функций почек, повышение сопротивляемости организма, предупреждение хронизации процесса и развития осложнений.
Схема лечения. Обязательные мероприятия: увеличение объема потребляемой жидкости, режим принудительных мочеиспусканий, антибактериальная терапия.
Вспомогательное лечение: режим, диета, дезинтоксикационная терапия, фитотерапия, физиолечение, стимулирующие средства, интерфероны, антиоксиданты, мембраностабилизаторы, витаминотерапия.
Показания для госпитализации: наличие выраженной интоксика-
195
ции и лихорадки, значительный болевой синдром, нарушение функции почек, повышение артериального давления, отсутствии эффекта от проводимого амбулаторно лечения, необходимость проведения углубленного обследования.
Режим постельный, длительностью 3-5 дней при наличии: интоксикации, лихорадки, озноба, болевого синдрома, выраженных дизурических расстройств.
По мере нормализации температуры, уменьшения или ликвидации экстраренальных симптомов, улучшения мочевого осадка режим расширяют.
Диета при экстраренальных проявлениях ПН должна быть с ограничением белка (до 1,5 /кг) и натрия хлорида (2-3 г/сут.). Показан дополнительный прием жидкости:
-до 7 лет – 500-700 мл;
-7-10 лет – 700-1000 мл;
-старше 10 лет – 1,0-1,5 л – клюквенный или брусничный морс, отвар из сухих яблок и груш. Рекомендуется прием слабощелочных минеральных вод (типа Славяновской, Смирновской) из расчета 2-3 мл/кг массы на прием в течение 20 дней, 2 курса в год.
При ликвидации экстраренальных симптомов используют диету с некоторым ограничением животных белков и жиров, исключением экстрактивных веществ, ограничением масла.
Важно соблюдение режима «регулярных» мочеиспусканий (через 2-3 часа в зависимости от возраста).
Антибактериальная терапия при ПН является основой лечения.
Стартовая антибактериальная терапия назначается эмпирически на основании знаний об этиологии заболевания.
Эффективность антибактериальной терапии оценивают через 3 дня после назначения препарата. При отсутствии эффекта (клиника, результаты исследования мочи) проводят изменение лечения. Коррекцию терапии желательно проводить с учетом результатов бактериологического исследования мочи.
В настоящее время в периоде обострения ПН рекомендуется в качестве стартовой терапии назначения защищенных пенициллинов (например, амоксиклав, Уназин), вводимых парентерально (внутривенно или внутримышечно в течение 3-7 дней с последующим переходом на ступенчатую терапию. Для стартовой терапии ПН так же используют цефалоспорины III поколения (цефтриаксон, цефотаксим, цефоперазон, цефтазидим, цефипим) и аминогликозиды (гентамицин, амикацин нетилмицин). Аминогликозиды в амбулаторных условиях не используют.
196
При тяжелых вариантах ПН эмпирическая антибактериальная терапия представлена: сочетаниями защищенных пенициллинов и аминогликозидов; сочетанием цефалоспоринов III-IV поколений и аминогликозидов; карбопенемами; пиперациллином/тазобактамом; тикарциллином/клавуланатом; фторхинолонами (только по жизненным показаниям), сочетанием ванкомицина и цефалоспоринов III-IV поколений; сочетанием ванкомицина и амикацина.
При стихании воспалительного процесса для лечения ПН используют защищенные пенициллины, цефалоспорины III поколения в оральных формах.
При лечении первого эпизода мочевой инфекции достаточно курса защищенного амоксициллина длительностью 5-7-10 дней. Препаратами выбора являются: амоксициллин/клавуланат, (например, амоксиклав), фосфомицин. Альтернативные препараты: цефуроксим, аксетил, нитрофурантоин, налидиксовая кислота. При асимптоматической бактериурии антибактериальная терапия не проводится.
Длительность антибактериальной терапии должна быть оптимальной, до полного подавления активности возбудителя (при остром ПН 2-3 недели); при обострении хронического ПН в условиях стационара антибактериальные препараты обычно назначаются непрерывно в течение 4 недель со сменой препарата каждые 7-10-14 дней.
Показанием для применения противорецидивной терапии являют-
ся: наличие пузырно-мочеточникового рефлюкса, рецидивы инфекции мочевых путей, первый эпизод инфекции мочевых путей до момента исключения аномалии развития мочевой системы (в среднем 1 месяц после достижения ремиссии в условиях антибактериальной терапии). Длительность профилактического лечения определяется индивидуально и может достигать 5 лет. Для длительной антимикробной профилактики применяют: фуразолидон, фурагин по 1 мг/кг, амоксиклав по 10 мг/кг, налидиксовую кислоту 15-20 мг/кг 1 раз в сутки, оксихинолин. Возможно длительное применение комбинированных растительных лекарственных средств (трава золототысячника, листья розмарина, корень любистока и др.).
Комбинированная антибактериальная терапия при ПН должна использоваться по строгим показаниям: тяжелое течение заболевания, необходимость расширить спектр антимикробного действия, наличие полирезистентности микроорганизмов к антибиотикам, подозрение на участие в воспалительном процессе внутриклеточных возбудителей (хламидии, микоплазмы, уреаплазмы).
В остром периоде ПН при выраженном синдроме эндогенной интоксикации показана инфузионно-корригирующая терапия. Состав и
197
объем инфузионной терапии зависят от стояния больного, показателей гомеостаза, диуреза и других функций почек.
Антиоксидантная терапия назначается по мере стихания микробного воспалительного процесса в почечной ткани, через 3-5 дней от начала антибактериальной терапии и проводится в течение 3-4 недель. Используют: витамин Е из расчета 1-2 мг/кг массы в сутки в завис и- мости от возраста; бета-каротин (Веторон по 1 капле на год жизни в зависимости от возраста ежедневно 1 раз в сутки в течение 4 недель); аскорбиновую кислоту (при отсутствии оксалурии и других противопоказаний); препараты, содержащие селен (триовит, селцинк и др.).
Средства, улучшающие почечный кровоток: (эуфиллин) – по пока-
заниям.
Иммуномодулирующая терапия в фазе максимальной активности не назначается и показана при стихании микробно-воспалительного процесса. Для лечения используют препараты рекомбинантного интерферона (виферон, реаферон). Виферон-1 (150 000 МЕ) назначается детям моложе 7 лет ректально по 1 свече дважды в день в течение 7 -10 дней, затем прерывисто 2-3 раза в неделю в течение 4-6 недель. Вифе- рон-2 (500 000МЕ) назначается детям старше 7 лет по 1 свече ректально дважды в день (курсовое лечение аналогично детям раннего возраста).
Лизоцим применяют перорально из расчет 5 мг/кг массы тела в сутки (не более 1 (200 мг в сутки) в течение 10 -20 дней или внутримышечно из расчета 2-5 мг/кг массы.
Бактериофаги показаны при упорном высеве однотипного возбудителя из мочи и кала при стойкой изолированной бактериурии.
Фитотерапия при ПН используется при прекращении непрерывной антибактериальной терапии; при поддерживающей антибактериальной терапии в дни, свободные от приема антибиотика, уросептика. Наиболее часто применяют: зверобой, толокнянку, шалфей, полевой хвощ, ромашку, шиповник, горец птичий.
Физиотерапия (см. «профилактика ПН»).
Лечебные мероприятия при обструктивном пиелонефрите
Лечение проводится совместно с детским урологом или детским хирургом. Решается вопрос о показаниях к оперативному лечению, катетеризации мочевого пузыря и др. Выбирая антибактериальные препараты у детей с обструктивным ПН, необходимо учитывать состояние функции почек и нефротоксичность антибиотиков.
Использование аминогликозидов при выраженной обструкции не показано. В случае назначения этих препаратов при небольшой обструкции лечение должно проводиться с индивидуальным подбором
198
дозы и мониторингом суточной концентрации препарата в крови. При снижении клубочковой фильтрации более 50% по пробе Реберга дозы этих препаратов должны быть уменьшены на 25-75%.
При ликвидации экстраренальных симптомов антибактериальную терапию продолжают уросептиками (препараты налидиксовой кислоты, оксихинолина и др.) курсами по 10-14 дней со сменой препараты.
Общая продолжительность непрерывной антибактериальной терапии 6-8 недель, при быстрой ликвидации клинических и лабораторных признаков активности – 4-6 недель.
При завершении непрерывной терапии в течение 3-6-9 месяцев продолжают поддерживающую терапию уросептиками ежемесячно по 7-10 дней, чередуя с отварами трав; или круглогодично по 1/3 суточной дозы уросептиков перед сном.
При выраженной активности обструктивного ПН с проявлениями синдрома эндогенной интоксикации, наряду с этиотропным лечением, важное значение имеет инфузионно-корригирующая терапия и нормализация уродинамики. Необходимо на несколько дней (2-4) катетеризировать мочевой пузырь. Показано назначение препаратов, улучшающих почечную гемодинамику (эуфиллин). При отсутствии острой задержки мочи возможно проведение «почечного дренажа» (назначается в утренние часы водная нагрузка в соответствии с возрастом и через 1 час фуросемид из расчета 1 мг/кг массы тела в сочетании с препаратами калия). При выявлении артериальной гипертензии – решение вопроса о назначении гипотензивных препаратов.
Осложнения: апостематозный нефрит, некроз почечных сосочков, карбункул почки, нефрогенная гипертония, нефролитиаз, вторично сморщенная почка, ХПН.
Профилактика ПН включает:
1. санацию очагов инфекции:
-при экстраренальных симптомах консервативная терапия тонзиллита, отита, аденоидов;
-при ликвидации экстраренальных симптомов санация полости
рта;
-при отсутствии экстраренальных симптомов, улучшении мочевого синдрома, при отсутствии нарушения функции почек проводят дегельминтизацию;
-аденотонзиллэктомия показана не ранее 6 месяцев после достижения клинико-лабораторной ремиссии.
2. Физиотерапевтическое лечение:
В активную стадию: СВЧ (противовоспалительный, улучшающий почечный кровоток эффект).
199
-в периоде стихания: ЭВТ (противовоспалительный, улучшающий почечный кровоток эффект); ультразвук (противовоспалительный, увеличивающий клубочковую фильтрацию эффект);
-в клинико-лабораторную ремиссию, для профилактики рецидива: тепловые процедуры (аппликации парафина, озокерита на область почек); аппликации грязи на область почек; электрофорез 1% раствора фурадонина; лечебные ванны (хлоридно-натриевые, минеральные, термальные) питье бутылочных минеральных вод (слабоминерализированные минеральные воды – гидрокарбонатно-кальциево- магниевые).
Противорецидивное лечение показано в случаях: наличия ПМР,
рецидивов инфекции МВП, первого эпизода ИМВП до момента исключения аномалии развития мочевой системы (в среднем 1 месяц после достижения ремиссии в условиях антибактериальной терапии).
Длительность профилактического лечения определяется индивидуально и может достигать 5 лет. Для длительной антимикробной профилактики применяют: фурагин по 1 мг/кг, ко-тримоксазол 2 мг/кг, амоксиклав (Уназин), Канефрон.
Фитотерапия (см. выше).
Исходы и прогноз ПН. Исходом хронического ПН является вто- рично-сморщенная почка при которой вначале происходит повышение клубочковой фильтрации (компенсаторная гипертрофия почечной паренхимы), а затем снижение клубочковой фильтрации (стадия декомпенсации).
При прогрессировании ПН уменьшается масса действующих нефронов, появляются признаки ХПН.
Прогноз при ПН зависит от своевременности диагностики, рациональности лечения и соблюдения диеты, правильности проводимого противорецидивного лечения, и своевременности урологической коррекции обструкции, наличия сопутствующих заболеваний.
Прогноз неблагоприятный при дизметаболических нарушениях, осложнившихся интерстициальным нефритом и ХПН.
Прогноз в отношении полного выздоровления ставится осторожно при условии нормальных показателей функции почек, отсутствии изменений в анализах мочи, отрицательных исследованиях на степень бактериурии на протяжении 5лет наблюдения за больным.
200

Вопросы к экзамену. Пиелонефрит. Понятие об инфекции мочевых
путей. Этиология. Предрасполагающие факторы (аномалии развития почек и мочевыводящих путей, нарушения метаболизма и другие). Патогенез. Классификация. Клиническая картина. Диагностика. Значение УЗИ почек для ранней диагностики. Показания к проведению рентгенологических исследований (цистография, внутривенная урография). Дифференци-
альный диагноз. Лечение. Подбор и длительность применения препаратов антибактериального действия. Исходы. Осложнения. Прогноз. Профилактика обострений.
Глава VII. Заболевания желудочно-кишечного тракта
ДИСКИНЕЗИИ СИСТЕМЫ ЖЕЛЧЕВЫДЕЛЕНИЯ
(ДСЖВ) - комплекс клинических симптомов (Римский консенсус, Рим, 1999), развившихся в результате моторно-тонической дисфункции желчного пузыря и желчевыводящих путей, без признаков органического их поражения (воспаление, камни).
Кинетика и биохимизм желчи
В норме желчный пузырь выполняет важные функции (табл. 1.57) по обеспечению нормального пищеварения и выделению желчи.
Табл. 1.57. Функции желчного пузыря
Функция |
Субстраты |
Накопительная |
Желчь |
Концентрационная |
Всасывание воды |
Реабсорбционная |
Аминокислоты, альбумин, неорганические ве- |
|
щества |
Сократительная |
Передвижение желчи |
Секреторная |
Слизь, ферменты, электролиты |
Ферментативная |
Ускорение действия панкреатической липазы |
Гормональная |
Выделение антихолецистокинина |
Регуляторная |
Поддержание состава желчи |
Последовательность основных функций жёлчного пузыря следующая:
– накопление в полости жёлчного пузыря жёлчи, секретируемой печенью;
201
–концентрирование накапливаемой жёлчи с целью создания резерва веществ, достаточного для упреждающего обеспечения пищеварения с участием жёлчи;
–периодическое, с должным упреждением выделение в двенадцатиперстную кишку жёлчи с необходимой концентрацией её компонентов, в должные интервалы времени и в необходимых для нормального пищеварения количествах.
Нормальная работа желчевыделительной системы обеспечивается центральной и вегетативной нервными системами, регуляторными пептидами (холецистокинин, ацетилхолин, оксид азота, нейропептид Y, соматостатин, эндорфины, половые гормоны, нейротензин).
Для нормального желчеотделения необходимы следующие условия: 1. ненарушенная функция печени, адекватный синтез и секреция желчных кислот; 2. сохранение концентрационной функции желчного пузыря; 3. сохранение моторной функции желчного пузыря; 4. адекватное функционирование сфинктерного аппарата билиарной системы;
5.отсутствие проявлений дуоденостаза.
Благодаря координации сократительной способности желчного пузыря и сфинктера Одди обеспечивается наполнение желчного пузыря в промежутках между приемами пищи.
Желчь представляет собой сложную биологическую жидкость. Основные компоненты желчи - желчные кислоты, холестерин, фосфолипиды и желчные пигменты. Желчные кислоты образуются в клетках печени из холестерина. Холестерин частично находится в желчи в чистом виде. Для того чтобы удержать холестерин от кристаллизации необходим лецитин. Лецитин сам по себе или вместе с желчными кислотами образует особые молекулярные структуры (мицеллы и везикулы), которые позволяют транспортировать холестерин от печени к кишечнику, не давая ему выпадать в виде кристаллов.
Существует индекс литогенности желчи, в котором учитываются взаимоотношения этих трех компонентов: холестерина, желчных кислот и лецитина. Нарушение биохимизма желчи сопровождает развитие всех заболеваний системы желчевыделения. Особенности нарушения физико-коллоидного состояния желчи, концентрация ее составных частей могут играть роль при постановке диагноза.
Эпидемиология. ДСЖВ занимают второе место в структуре всех гастроэнтерологических заболеваний в детской практике после хронического гастродуоденита. Частота ДСЖВ составляет от 50-60% до 9095% при различных заболеваниях органов пищеварения. Изолированные ДСЖВ встречаются у детей раннего и дошкольного возраста.
Этиология. Основными причинами развития ДСЖВ являются:
202
неврозы, депрессии, стрессы, отрицательные эмоции, нарушения вегетативной нервной системы, заболевания системы пищеварения, аномалии развития билиарной системы, расстройства нервно-гуморальной регуляции, аллергия, холецистэктомия.
Причины первичных дискинезий: стресс, нейрогуморальные нарушения, заболевания ЖКТ, очаги хронической инфекции. Вторичные дискинезии развиваются при: эндокринных заболеваниях, гепатитах, циррозах, хроническом холецистите, язвенной болезни.
Исследования: общий анализ крови и мочи, холестерин крови, билирубин и его фракции, трансаминазы, щелочная фосфатаза, копрограмма, УЗИ (так же УЗИ с функциональными пробами), ФГДС. По показаниям: определение амилазы крови и мочи, классическое и фракционное дуоденальное зондирование, ЭКГ, холецистография, контрастная внутривенная холангиохолецистография, рентгенография органов грудной клетки, бактериологическое исследование желчи, РПХГ, определение HBsAg,
Золотой стандарт исследования – манометрия сфинктера Одди с раздельным канюлированием панкреатического и желчного сегментов
(сложное и небезопасное исследование).
Исследования амбулаторно, приказ МЗ РФ № 262: УЗИ печени и желчного пузыря, определение уровня трансаминаз. По показаниям:
ЭКГ, общий анализ крови, глюкоза крови, холецистография, холангиография, ФГДС, билирубин крови и его фракции, щелочная фосфатаза.
Кскрининговым методам диагностики относят: биохимическое исследование крови, УЗИ органов брюшной полости, ЭФГДС.
Куточняющим методам исследования относят: УЗИ с функци о-
нальной пробой, динамическую холесцинтиграфию, ЭРХПГ, медикаментозные тесты с холецистокинином и морфином.
Патогенез. Основными причинами развития ДСЖВ являются нарушения вегетативной нервной системы, патологические висцеровисцеральные рефлексы, возникающие в результате заболеваний ЖКТ. Нарушениям моторики желчных путей способствуют изменение уровней нейромедиаторов и гуморальных факторов (холецистокинин), повышение давления в 12.п.к. вследствие спазма сфинктера Одди.
В результате нарушений в системе регуляции функций желчного пузыря и протоков, развиваются нарушения в работе сфинктерного аппарата, координации в работе сфинктеров и желчного пузыря, что приводит к нарушениям желчевыделения, застою желчи в билиарном тракте. Описаны более десяти вариантов дискоординации работы желчного пузыря и сфинктера Одди. Следствием моторных нарушений являются нарушение биохимизма желчи, и других функций желчного
203
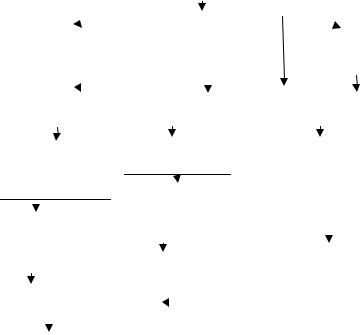
пузыря, присоединение хронического холецистита, формирование желчнокаменной болезни, нарушение дисбиоза кишечника.
|
Нарушение нейрогу- |
|
|
|
Заболевания |
|
Аномалии |
|
|
|
|
|
|
||||||||||||||||
|
моральных механиз- |
|
|
|
ЖКТ |
|
ЖП и про- |
|
|
|
|
|
|
||||||||||||||||
|
мов |
|
|
|
|
|
|
|
|
|
|
токов |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Спазм |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
Нарушение про- |
|
|
|
|
сфинкте- |
|
|
|
Дуоденобили- |
|
||||||||||||||||
|
|
|
|
|
|
|
ров |
|
|
|
|
||||||||||||||||||
|
|
|
дукции регули- |
|
|
|
|
|
|
|
арный рефлюкс |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
рующих гормонов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Застой желчи в билиарном тракте |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
Распад |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Нарушение |
|
|
|
|
|
Воздействие протео- |
|
||||||||||||||||||||
|
|
опорожне- |
|
|
желчной |
|
|
|
литических фермен- |
|
|||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
ЖП |
|
|
Выпадение |
|
|
|
тов ПЖ на слизистую |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
в осадок |
|
|
|
билиарного тракта, |
|
|||||||||||||
|
|
|
Гипертро- |
|
|
||||||||||||||||||||||||
|
|
|
|
|
компонен- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
фия стенки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Холецистит, холан- |
|
|
||||||||||||||
|
|
|
|
Образова- |
|
|
|
|
|||||||||||||||||||||
|
|
|
ЖП дила |
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
гит, реактивный ге- |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
ние камней |
|
|
|
|||||||||||||||
|
|
|
Дискине- |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
Желчнокаменная бо- |
|
|
|
Повы- |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
шение |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
Нарушение процессов переваривания и всасы- |
||||||||||||||||||||||||||
|
|
|
интра- |
||||||||||||||||||||||||||
|
|
|
вания избыточный рост бактерий в кишечнике |
||||||||||||||||||||||||||
|
|
|
дуоде- |
||||||||||||||||||||||||||
|
|
|
Рис. 1.24. Схема патогенез ДЖВС |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
Классификация |
функциональных |
расстройств |
билиарного |
|||||||||||||||||||||||
|
тракта (Рим, II). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Тип нарушений: а) по локализации – дисфункция желчного пузыря, дисфункция сфинктера Одди; б) по этиологии – первичные, вторич-
ные; в) по функциональному состоянию – гипофункция, гиперфунк-
ция.
Классификация дискинезий желчевыделительной системы
204
Ι . Этиопатогенетическая характеристика: первичные; вторичные.
ΙΙ. Тип нарушения моторики: гипертонически-гиперкинетический (гипермоторный); гипотонически-гипокинетический (гипомоторный); диссоциированный.
ΙΙΙ. Тип течения: латентное; с редкими обострениями; с частыми обострениями.
ΙV. Стадия: ремиссия; обострение.
V.Отдельные формы: дискинезия желчного пузыря (гипер- и гипотония, увеличение объема при сохранении эвакуаторной функции); дискинезия сфинктеров (гипертонус сфинктера Одди, диссинергия сфинктеров Одди и Люткенса).
Анамнез, клиника. В анамнезе детей с ДЖВС чаще всего выяв-
ляются: болевой синдром, диспепсические жалобы, астеновегетативные проявления. Следует иметь в виду, что при ДЖВС у 82% больных имелись нарушения интранатального периода с последующим развитием гипертензионно-гидроцефального синдрома, синдрома малых мозговых дисфункций, гипервозбудимости, эписиндрома. 64% детей находились на раннем и к тому же неправильном искусственном вскармливании; у 59% имелись указания на частые инфекции, в том числе и кишечные, бесконтрольное применение антибиотиков.
Клинические проявления различных форм патологии системы желчевыделения схожи. Характерны боли в области правого подреберья, приступообразные, колющие или ноющие, усиливающиеся при ходьбе и провоцируются погрешностями в диете. Часто выявляются пузырные симптомы: Ортнера, Керра, Егорова, френикус-симптом и др.
Характер астеновегетативных проявлений очень разнообразен и зависит от вида вегетативных нарушений (ваготония или симтпатотония). У таких детей часто выявляют: двигательную расторможенность, потливость, гиподинамию, сердцебиения, замкнутость, самообвинение. Диспептические проявления представлены: снижением аппетита, тошнотой, рвотой, отрыжкой, горечью во рту, изменениями частоты стула и т.д.
Диагноз.
Анализ крови – при ДСЖВ изменения, как правило не выявляются. Наличие воспалительных изменений в анализе крови требует исключения холецистита и других заболеваний воспалительного характера.
Биохимическое исследование крови – при холестазе увеличивается уровень общего и прямого билирубина, холестерина, щелочной фосфатазы, ЛДГ, иногда незначительное повышение уровней трансаминаз.
УЗИ – для оценки функционального состояния протоков и сфинктерного аппарата метод является малоинформативным.
205
Динамическая холесцинтиграфия – позволяет выявить: начальные функциональные изменения в желчных путях, рефлюксы в желчные протоки, определить нефункционирующий желчный пузырь, выявить нарушение оттока желчи.
Дуоденальное зондирование – имеет историческое значение. Гипермоторная дискинезия. Анамнез: постепенное начало забо-
левания. Связь с нервно-эмоциональным напряжением, гипокинезией, гипотонией, гиподинамией, дисгормональными нарушениями, инфекциями, наличием заболеваний ЖКТ, наследственная предрасположенность. Боли в правом подреберье без иррадиации, кратковременные, колющие, схваткообразные, связанные с физическим перенапряжением и отрицательными эмоциями. У детей старшего возраста боли иррадиируют в спину и под правую лопатку. Боли проходят или самостоятельно, или после приема спазмолитиков.
Следует иметь в виду, что при всех вариантах дискинезии болевые ощущения могут вообще отсутствовать, а кинические проявления заболевания могут маскироваться проявлениями основной патологии в системе пищеварения.
Подтверждающими признаками этой дискинезии являются: особенности анамнеза и болевого синдрома, продолжительность заболевания до 1 года, нормальная температура тела. Со стороны крови и других исследований отсутствуют признаки воспалительного характера.
При УЗИ выявляют спазм сфинктера Одди, гиперкинезию желчного пузыря (сокращение желчного пузыря после приема желчегонного завтрака более чем на 60% от первоначального объема на 30 минуте).
При спазме протоков желчный пузырь сокращается на 10-20 минуте. Результаты УЗИ часто и необоснованно выявляют гипомоторную дискинезию, в силу несовершенства существующей методики исследования.
Большее диагностическое значение имеют результаты манометрии сфинктера Одди, сцинтиграфии. Однако эти методы исследования пока не нашли широкого применения.
Гипомоторная дискинезия. Проявления заболевания возникают при нарушении режима питания, переохлаждении. Характерны тупые, длительные, ноющие боли, тошнота, отрыжка изжога. Длительность заболевания более 2-3 лет.
Подтверждающими признаками гипокинетической дискинезии являются выявление при УЗИ гипотонии сфинктера Одди, гипокинезии желчного пузыря (сокращение желчного пузыря после приема желче-
гонного завтрака менее 40% от первоначального объема на 40 мину-
206
те). УЗИ желчного пузыря с функциональной пробой необоснованно часто выявляет гипомоторные дискинезии. В связи с этим у детей предпочтительное использовать гепатобилиарную сцинтиграфию с фармакологическими тестами.
При исследовании щелочной фосфатазы и γ – глютамилтранспептидазы выявляют их повышение (признаки холестаза).
Дисфункция сфинктера Одди (билиарный тип) характеризуется приступообразными болями в эпигастрии и правом подреберье; положительными пузырными симптомами; повышением уровня трансаминаз в крови; расширением общего желчного протока; замедленным выведением контраста при ЭПРХГ. Косвенным признаком повышения тонуса сфинктера Одди является диаметр общего желчного протока более 10 мм и задержка контраста в нем более 45 мин. О дисфункции панкреатического протока говорит его расширение до 5 мм и замедленная эвакуация контраста из просвета.
На основании общепринятых методов диагностики можно установить только нарушения моторики желчного пузыря.
Дифференциальный диагноз ДЖВС проводится с хроническим холециститом, заболеваниями желудка, 12 п.к., поджелудочной железы (см. «Хронический холецистит», табл. 1.56).
Лечение. Задачи лечения: восстановление продукции желчи, нормализация тонуса сфинктерного аппарата и давления в 12 п.к., предупреждение развития воспалительных заболеваний системы пищеварения.
Схема лечения:
Обязательные мероприятия: режимные моменты, диета, использование психотерапевтических методов, миоспазмолитики (при гипермоторной ДЖВС), холецистокинетики (при гипомоторной ДЖВС).
Вспомогательное лечение: физиотерапия, фитотерапия, желчегонные средства, иглорефлексотерапия, ферменты, гепатопротекторы.
Показания для госпитализации: дискинезии ЖВС преимущественно лечатся амбулаторно. Госпитализация показана при вторичных дискинезиях.
Режим (соответствует тяжести и периоду заболевания).
Диета - стол № 5. Следует увеличить число приемов пищи до 5-6 раз в день. Исключить: экстрактивные вещества, пряности, копчености, маринады, жирные блюда, шоколад, какао, кофе. Рекомендовать: овощные салаты, винегреты, яйца всмятку, сыр, творог, вегетарианские супы, отварное мясо и рыбу, компоты, фруктовые соки.
При гиперкинезии не рекомендованы: холодные продукты, сало, свинина, торты, пирожные, сливки, сметана, яйца.
207
При гипокинезии показаны: хлеб с отрубями, черный (ржаной) хлеб, фрукты, овощи в большом количестве, сливки, сметана, яйца.
При повышении тонуса сфинктеров билиарной системы. Рекомендуют: покой, сухое тепло на место проекции желчного пузыря. Миотропные препараты: нитроглицерин под язык 2,5-5 мг (ребенку 7-12 лет), 5-10 мг 1 раз в сутки (ребенку старше 12 лет). Эффективны спазмолитики растительного происхождения: холагол (5-20 капель на прием на сахаре), хофитол (1 таблетка внутрь), гепабене.
Для лечения и предупреждения приступов боли используются ношпа, галидор или платифиллина гидротартрат курсами не более 3-х дней. Дюспаталин можно давать более длительно.
К средствам, устраняющим гипертонус желчного пузыря относят: платифиллин, Гимекромон (1/2 табл. ребенку 5-10 лет); 1 табл. ребенку 15 лет. Препарат назначается 3 раза в день за 30 мин. до еды, курсом 2 недели.
Для стимуляции желчеобразования используют холеретики, препараты, содержащие желчь или желчные кислоты: холензим, аллохол, циквалон, оксафенамид. При назначении препаратов, содержащих желчные кислоты, следует помнить, что они противопоказаны (кроме урсосана) при гепатитах, циррозах, язвенной болезни, эрозиях слизистой оболочки желудочно-кишечного тракта, панкреатитах, заболеваниях не связанных со стеатореей.
Эффективны новые комплексные растительные препараты: гепабене, Силимарин, сибектан. Сибектан можно комбинировать с желчегонными препаратами т.к. он может нивелировать отрицательные эффекты последних.
Показаны тюбажи по Демьянову с минеральной водой, минеральные воды средней минерализации 2 раза в день по 3 мл/кг на прием, физиотерапия, санаторно-курортное лечение.
ЛФК, ферментные препараты (при наличии клиники дуоденальной гипертензии, нарушении пищеварения) - Креон, мезим-форте, пензистал.
При функциональных нарушениях системы желчевыделения часто рекомендуют гепатопротекторы растительного происхождения: гепабене (при сочетании ДЖВС с поражениями печени), ЛИВ-52, гепатофальк, планта. Дифференцированный подход к лечению ДСЖВ представлен в табл. 1.58.
Табл. 1.58. Лечебные мероприятия при дисфункциональных расстройствах билиарного тракта (А.М. Запруднов, 2010)
208

Лечебные мероприятия
Дисфункциональные расстройства
Гипертония |
Гипотония |
|
|
Желчегонные |
|
Холеретики |
Холекинетики |
|
Синтетические: циквалон, окса- |
Истинные: холензим, аллохол и |
|
фенамид; растительные: олиме- |
др. |
|
тин, хофитол |
|
Растительные: гепабене, фламин |
|
Спазмолитики |
|
Быстродействующие |
нитраты |
Растительные препараты ком- |
(нитроглицерин), |
миотропные: |
бинированного действия: гепабе- |
платифиллин, дротаверин, мебе- |
не, хофитол |
|
верин, гимекромон. |
|
|
Растительные: холагол, холаго- |
|
|
гум |
|
|
Наркотические: |
дроперидол, |
|
нельзя морфин! |
|
|
|
Минеральные воды |
|
Низкой концентрации: Славяновская, |
Высокой минерализации (Ессентуки |
|
Смирновская, Арзни, Ессентуки №4 в |
№17, Моршанская, Баталинская и др. |
|
подогретом до 40-42 0С виде, по 180- |
температурой 18-20 0С, по 180-200 мл |
|
200 мл за 15-30 мин до еды 3 раза в |
за 15-30 мин. до еды 3 раза в день, |
|
день, курсом 3-4 нед. |
|
курсом 3-4 недели |
|
Физиотерапия |
|
Электрофорез с сульфатом магния, |
Ультразвук низкой интенсивности, |
|
новокаином, папаверином, индукто- |
синусоидальные модулированные |
|
термия на область правого подребе- |
токи на место проекции желчного |
|
рья, ультразвук высокой интенсивно- |
пузыря, электрофорез с хлористым |
|
сти на место проекции желчного пу- |
кальцием или прозерином на область |
|
зыря, электросон, гальванический |
правого подреберья, электросон, |
|
воротник по Щербаку, электрофорез с |
гальванизация хлористым кальцием, |
|
оксибутиратом натрия на область |
раствором брома на воротниковую |
|
симпатических шейный узлов. |
зону |
|
Профилактика. Активный образ жизни, санация очагов инфекции, рациональное питание. Лечение заболеваний, лежащих в основе дискинезии (патология ЖКТ, аллергия, вегетативные нарушения и т.д.).
209

Вопросы к экзамену. Болезни желчных путей. Классификация. Функ-
циональные нарушения желчевыводящих путей (нарушения кинетики и биохимизма желчи). Механизмы формирования. Типы дискинезий. Клинические проявления. Диагностика. Функциональные методы исследования (дуоденальное зондирование, холецистография. ретроградная холангиопанкреатография, УЗИ). Показания. Дифференциальный диагноз. Особенности лечения в зависимости от типа дискинезий. Профилактика.
ХРОНИЧЕСКИЙ ХОЛЕЦИСТИТ (ХХ) – хроническое воспаление стенки желчного пузыря преимущественно бактериального
происхождения. ХХ может быть первичным, или следствием перенесенного острого.
Эпидемиология. ХХ относительно редкое заболевание. Встречается у 6-15% детей, страдающих заболеваниями ЖКТ.
Этиология. Наиболее частые причины ХХ - бактериальная инфекция (кишечная палочка, кокки, энтерококки и др.). Значение в развитии ХХ имеют: нарушения питания, физическое и нервно-психическое перенапряжение, аллергия, эндокринная патология, гельминтозы.
Исследования: общий анализ крови и мочи, холестерин крови, билирубин и его фракции, трансаминазы, щелочная фосфатаза, копрограмма, УЗИ (так же УЗИ с функциональными пробами), ФГДС. По показаниям: определение амилазы крови и мочи, классическое и фракционное дуоденальное зондирование, ЭКГ, холецистография, контрастная внутривенная холангиохолецистография, рентгенография органов грудной клетки, бактериологическое исследование желчи, РПХГ, определение HBsAg,
Исследования амбулаторно, приказ МЗ РФ № 262: УЗИ печени и желчного пузыря, определение уровня трансаминаз. По показаниям:
ЭКГ, общий анализ крови, глюкоза крови, холецистография, холангиография, ФГДС, билирубин крови и его фракции, щелочная фосфатаза.
Патогенез. Пути распространения инфекции. Восходящий путь (при гипотонии сфинктера Одди, ахлоргидрии). Гематогенный путь: при хроническом тонзиллите, нарушении функции тонкокишечного эпителия и печени. Лимфогенный путь - при аппендиците, пневмонии, воспалительных заболеваниях брюшной полости.
Важными факторами, способствующими развитию ХХ, является: дискинезия билиарной системы, нарушение биохимизма желчи, рефлюксы, аномалии развития желчного пузыря, сопутствующая патология органов пищеварения. Снижение в желчи уровня IgA, нарушения
210
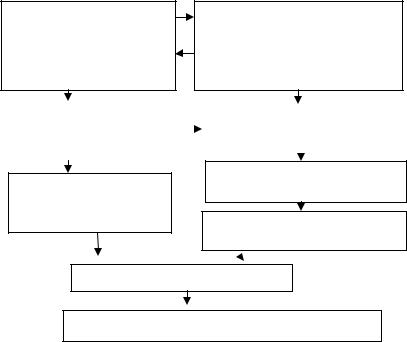
иммунологической реактивности, снижение концентрации желчных кислот (уменьшается бактерицидность желчи), облегчают развитие воспалительных изменений в желчном пузыре. Аутоиммунный компонент патогенеза способствует хронизации течения воспалительного процесса.
Воспалительный процесс локализуется обычно в области шейки желчного пузыря.
Предрасполагающие фак-
торы: инфекция, аллергия, обменные нарушения, гиподинамия, нарушения питания
Этиологические факторы: на-
рушение моторики ЖВП, рефлюксы, аномалии развития, камни в желчном пузыре, гастродуоденит
Снижение специфиче- |
|
|
Нарушение оттока и биохи- |
|
ских и неспецифических |
|
|
мического состава желчи |
|
|
|
|||
факторов защиты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Проникновение в ЖП
инфекции различными путями
Застой желчи в ЖП и желчных
протоках
Нарушение бактерицидности
желчи
Повреждение стенки ЖП
Формирование воспалительного процесса в ЖП
Рис. 1.25. Схема патогенеза ХХ
Классификация болезней желчевыделительной системы (по А.В. Мазурину, 1984, в модификации):
I.Функциональные нарушения:
Дискинезия: а) гипотоническая, гипокинетическая, б) гиперто-
ническая, гиперкинетическая; в) смешанная. 1. Дискриния желчного пузыря;
II, Механические нарушения: а) врожденные аномалии; б) гипер-
211
плазия лимфатических желез; в) микрокалькулез; г) синдром холестаза.
III, Воспалительные заболевания: а) холецистит: с сохранением функции желчного пузыря, - отключенный (нефункционирующий) желчный пузырь; б) холангит, в) холецистохолангит;
IV. Заболевания большого дуоденального сосочка и общего желчно-
го протока: а) функциональные: гипотония; гипертония; б) воспалительные; в) обтурационные.
V. Постхолецистэктомический синдром;
VI. Обменные заболевания: желчекаменная болезнь;
VII. Паразитарные: описторхоз, эхинококкоз, гельминтозы; VIII. Опухолевые образования.
IX. Травматические повреждения.
Анамнез, клиника. Проявления ХХ включают: болевой синдром, диспептические проявления, положительные пузырные симптомы, интоксикацию, лихорадку, астеновегетативные симптомы.
При сборе анамнеза необходимо уточнить особенности питания (жирная, жаренная пища), установить факторы, способствующие развитию заболевания; имеющиеся заболевания ЖКТ (гепатиты, заболевания желудка и др.). Выявить особенности болевого синдрома, особенности диспептических проявлений, лихорадки.
Болевой синдром при ХХ зависит от степени тяжести заболевания. В легких случаях боли могут быть не резко выраженными. Возможна их иррадиация в правое плечо и правую лопатку. Первичнохроническое течение заболевания характеризуется подострым течением, слабо выраженным болевым синдромом, преобладанием диспепсических расстройств (тошнота, рвота), наличием субфебрильной температуры.
Диагноз ХХ устанавливается на основании: болевого синдрома (см. критерии дискинезии), диспепсических, общеинтоксикационных проявлений, повышения температуры (чаще субфебрильная).
Лабораторные исследования Со стороны периферической крови изменения воспалительного ха-
рактера (исключить другие причины воспалительных изменений!). Биохимические исследования выявляют: диспротеинемию (повы-
шение уровня α-1, α-2, β, γ глобулинов), повышение уровней тимоловой пробы, фибриногена, СРБ, аминотрансфераз, щелочной фосфатазы, γ –глютамилтранспептидазы.
При УЗИ - стенка желчного пузыря толщиной более 3 мм, повышение ее плотности, большое количество хлопьев в желченном пузыре, дополнительные эхосигналы в паренхиме печени вокруг желчного пу-
212
зыря. Желчный пузырь увеличивается в размерах более чем на 5 мм2 от верхней границы нормы для пациентов данного возраста. Для ХХ характерно наличие паравезикулярной эхонегативности.
При термографии находят зоны повышенной энергетической яркости в области пузыря.
Дуоденальное зондирование. В желчи при микроскопии выявляют: слизь, обломки лейкоцитов, снижение уровня щелочной фосфатазы. При бактериологическом исследовании желчи обнаруживают более 100000 тысяч микробных тел в 1 мл желчи.
Дифференциальный диагноз проводят с дискинезиями желчных путей, заболеваниями желудка, поджелудочной железы.
Табл. 1.58. Дифференциальный диагноз дискинезий и хрониче-
ского холецистита
Признак |
Дискинезия ЖВП |
Хронический холе- |
|
|
цистит |
Температура тела |
Норма |
Субфебрилитет |
Интоксикация |
Нет |
Имеется |
Характер болей |
В зависимости от |
Боли обычно слабой |
|
вида дискинезии |
интенсивности |
Длительность заболева- |
1-3 года |
4-5 лет и более |
ния |
|
|
Воспалительные изме- |
Нет |
Есть |
нения в крови |
|
|
Диспротеинемия |
Нет |
Возможна |
УЗИ желчного пузыря |
Выявление вари- |
Уплотнение и утол- |
|
антов дискинезии |
щение стенки ЖП |
Моторные нарушения |
Характерны |
Характерны |
«Воспалительные» из- |
Не характерны |
Характерны |
менения в желчи |
|
|
Лечение. Задачи лечения: 1. борьба с инфекцией (антибактериальная терапия); 2. противовоспалительная терапия (коррекция побочных проявлений воспаления); 3. борьба с болью; 4. коррекция дискинезии системы желчевыделения; 5. ликвидация нарушений пищеварения.
Схема лечения. Обязательные мероприятия: режим, диета, анти-
бактериальная терапия (кроме легких обострений).
Вспомогательное лечение: желчегонные средства, спазмолитики,
213
ферменты, физиотерапия, гепатопротекторы, коррекция нарушений пищеварения, иммунокорригирующая терапия, витаминотерапия.
Показания для госпитализации: тяжелое состояние больного, выраженный болевой синдром, сочетанный характер поражения ЖКТ, невозможность проведения обследования и лечения в амбулаторных условиях, отсутствие эффекта от проведенной амбулаторно терапии.
При выраженной лихорадке и интоксикации – постельный режим. Диета № 5 или 5а. При наличии температуры, интоксикации, очагов хронической инфекции показана антибактериальная терапия.
Особенности антибактериальной терапии при ХХ. Антибактериальная терапия назначается только в период обострения заболевания. Стартовая антибактериальная терапия назначается эмпирически с учетом наиболее вероятных возбудителей заболевания. Используемые препараты должны создавать в желчи лечебную концентрацию. Хорошо поступают в желчь при отсутствии обструкции желчных путей следующие антибиотики: азлоциллин, мезлоциллии, доксициклин (детям старше 7 лет), современные макролиды (например, азитромицин), цефтриаксон. Для лечения ХХ так же можно использовать: ампициллин, цефазолин, линкомицин, меропенем, хлорамфеникол.
При легких обострениях возможно использование бактрима, нитрофурановых препаратов или даже ведение больного без применения антибактериальных средств. Длительность антибактериальной терапии 10-12 дней. После снятия воспалительных изменений в желчном пузыре показано назначение холеспазмолитика Одестона. Ферментные препараты (при наличии клиники дуоденальной гипертензии и нарушений пищеварения) – Креон, мезим-форте, пензистал.
Коррекция болевого синдрома: Дюспаталин, дротаверин, платифиллина гидротартрат, атропина сульфат. При выраженном болевом синдроме показаны анальгетики – анальгин, трамал.
Нарушение оттока желчи ликвидируют применением холеретиков (стимулируют образование и выделение желчи) и холекинетиками (усиливают поступление желчи в 12 п.к.). Желчегонные препараты применяют с учетом нарушений моторики билиарной системы. Холеретики показаны в период стихания воспалительного процесса и в фазе ремиссии (например, хофитол по 1-2-3 капсулы 3 раза в день перед едой).
В случаях выявления осадка или сгущения желчи в желчном пузыре показаны урсофальк, урсосан по 10-15 мг/кг в сутки на 2-3 месяца.
Физиолечение включает: грязевые аппликации на область правого подреберья (10 процедур), электрофорез с магнием.
Осложнения ХХ: желчекаменная болезнь, калькулезный холеци-
214

стит, перихолецистит, вторичные изменения печени (гепатит), нарушение полостного пищеварения, атрофический дуоденит, дуоденогастральный рефлюкс, рефлюкс-гастрит, хронический панкреатит.
Течение. По течению выделяют острые и хронические варианты холециститов. Острый холецистит – самое частое осложнение желчнокаменной болезни. Хроническое течение холецистита обычно первичное (без предшествующего острого холецистита). Возможно монотонное или рецидивирующее течение ХХ. Очень редко встречается не- прерывно-рецидивирующее течение ХХ.
Исходы. В детском возрасте ХХ протекает достаточно благоприятно. По мере увеличения длительности заболевания увеличивается частота сопутствующих заболеваний ЖКТ, возможно развитие желчнокаменной болезни.
Профилактика. Активный образ жизни, санация очагов инфекции, рациональное питание. Важно проводить лечение заболеваний, лежащих в основе дискинезии желчных путей (патология ЖКТ, аллергия, вегетативные нарушения и т.д.), а также организация своевременного лечения дискинезий системы желчевыделения. Медикаментозное растворение камней (при наличии).
Вопросы к экзамену. Холециститы. Этиология. Патогенез. Классифи-
кация. Клиническая картина. Диагностика. Дифференциальный диагноз. Течение. Исходы. Лечение. Профилактика.
ЖЕЛЧНОКАМЕННАЯ БОЛЕЗНЬ (ЖКБ) – обменное забо-
левание системы желчевыделения, характеризующееся образованием камней в желчном пузыре или в желчных протоках.
Эпидемиология. Частота ЖКБ в детском возрасте неизвестна. Чаще болеют девочки. В нашей стране среди взрослых ЖКБ встречается у 10-20% населения.
Факторы, способствующие появлению камней: наследственные факторы (нарушение обмена фосфолипидов, экскреции желчи в канальцы, регуляции липидного состава желчи и крови), аномалии развития системы желчевыделения, особенности питания, неблагоприятное влияние ксенобиотиков, дисбиозы кишечника, гиподинамия, воздействие невротизирующих факторов, токсикомания, алкоголь, курение.
Развитию ЖКБ так же способствуют: синдром короткой кишки; длительное парентеральное питание без энтерального компонента; цирроз печени; гемолитическая анемия; искусственные клапаны серд-
215
ца; паразитарная инвазия желчных путей; быстрое похудание; сахарный диабет; ожирение.
Классификация. У детей общепринятой классификации нет. Для практических целей может быть использована классификация ЖКБ, принятая съездом Научного общества гастроэнтерологов России в
2002 г.
І стадия – начальная или предкаменная; - густая неоднородная желчь;
-формирование билиарного сладжа с наличием микролитов; с наличием замазкообразной желчи; сочетание замазкообразной желчи с микролитами;
ІІ стадия – формирование желчных камней:
-по локализации: в желчном пузыре; в общем желчном протоке; печеночных протоках;
-по количеству конкрементов: одиночные, множественные;
-по клиническому течению: латентное, с наличием клинических симптомов – болевая форма с типичными желчными коликами;
-диспепсическая форма; под маской других заболеваний;
ІІІстадия – хронический рецидивирующий калькулезный холеци-
стит;
ІV стадия – осложнения.
Этиология и патогенез. Камнеобразование - стадийный процесс с
периодами активного роста и затихания. Факторы, приводящие к образованию желчных камней: а) выработка желчи, перенасыщенной холестерином (литогенная желчь); б) избыточная секреция холестерина в желчь; в) сниженная секреция фосфолипидов и желчных кислот; г) желчный стаз; д) инфекция желчевыводящих путей; е) гемолитическая анемия.
Воснове патогенеза ЖКБ лежит повышение литогенности желчи. Основными нарушениями при развитии ЖКБ являются нарушение синтеза и обмена холестерина, изменение соотношения желчных кислот, дискинезии системы желчевыделения. На первом этапе камнеобразования происходит нарушение синтеза печеночных ферментов, следствием чего являются избыточное количество холестерина и недостаточное количество желчных кислот, чему также способствует дисбиоз кишечника.
Вобразовании ядра будущего камня принимают участие: муцин, гликопротеиды, нарушения моторики желчных путей.
Вмеханизме образования пигментных камней принимают участие накопление в желчи меди и железа. Черные пигментные камни образуются при сочетании ЖКБ с циррозами печени, гемолитическими
216
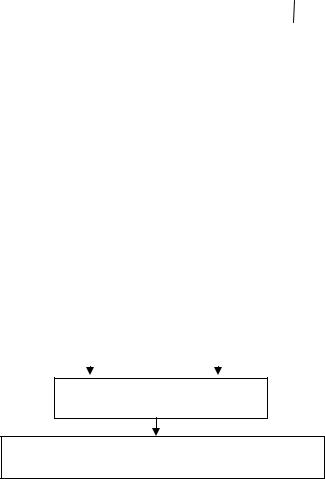
желтухами, ВПС. Коричневые пигментные камни образуются в случае вторичного инфицирования желчных путей.
Аномалии развития |
|
Наследственно де- |
|
Обмен ве- |
|
||||||||||||||
желчных путей |
|
терминированные |
|
ществ |
|
||||||||||||||
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
нарушения |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Особенности вегетативной нервной системы |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
Гиперсимпати- |
|
|
Асимпатикото- |
|
|
|
Ваготония |
|
|
||||||||
|
|
|
котония |
|
|
ния |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
ЖКБ, боле- |
|
|
|
ЖКБ, бессим- |
|
|
ЖКБ под «маской» |
|
|||||||||
|
|
вая форма |
|
|
птомное течение |
|
|
сопутствующих |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
заболеваний |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 1.26. Схема патогенеза холелитиаза (по Харитоновой Л.А.,
1998)
Состав камней, локализация. Чаще всего камни при ЖКБ у детей билирубиновые. Холестериновые камни рентгеннегативные. Возможны кальциевые, пигментные камни. Наиболее часто у детей камни локализуются в области дна желчного пузыря, а наиболее редко – в холедохе.
Нарушение обрабования и |
|
|
|
Гиперсекреция мукоидных |
|
танспорта холестерина и желч- |
|
|
|
субстанций |
|
ных кислот |
|
|
|
|
Дестабилизация везикул
ХС + ЖК на ХС + ФЛ
Кристаллизация холестерина с образованием конг-
ломератов желчных камней
Рис. 1.3. Патогенез холестеринового литиаза (Запруднов А.М.,
2010).
217
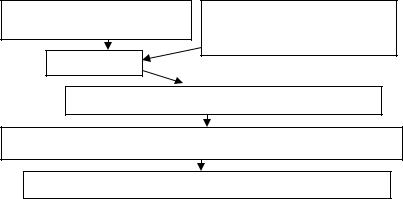
Примечание: ХС – холестерин; ЖК – желчные кислоты; ФЛ – фосфолипиды.
Аномалии и пороки развития
ЖВС
Холестаз
Нарушение синтеза билиру-
бина и энтеропатической циркуляции жечных кислот
Повышение концентрации свободного билирубина
Образование прочных нерастворимых связей с солями Ca, Mg, Fe
Образование агломератов пигментных желчных камней
Рис. 1.3. Патогенез билирубинового литиаза (Запруднов А.М.,
2010).
Исследования (см. «Хронический холецистит»). Так же необходимо определение щелочной фосфатазы, лейцинаминопептидазы, γ-ГТ, исследование липидограммы (с определением триглицеридов, фосфолипидов и НЭЖК). КТ не имеет преимуществ перед УЗИ. При подозрении на конкременты в желчных протоках, аномалии развития желчевыводящих путей проводится магнитно-резонансная холангиопанкреатография (МРХПГ). У взрослых «золотым стандартом» диагностики ЖКБ является ЭРХПГ. Ограничение к использованию данного метода у детей – инвазивность, травматичность. По диагностическому значению МРХРГ является аналогом ЭРХПГ. При отключенном желчном пузыре выполняют сцинтиграфию желчных путей.
Анамнез, клиника. При сборе анамнеза необходимо обратить внимание на наличие факторов риска развития ЖКБ; постепенное или острое развитие заболевания. Установить возможность связи ЖКБ с длительным приемом медикаментов, наличие аномалий желчного пузыря, дискинезий, особенности питания (пища с большим содержанием холестерина, сахарозы), наличие нарушений вегетативной нервной системы, стрессы, наследственную предрасположенность (до75%), наличие сопутствующих заболеваний органов пищеварения, в том числе и дисбиоза кишечника.
218
ЖКБ чаще всего протекает бессимптомно (латентная форма). Латентная форма – это одна из фаз течения ЖКБ, которая может длиться долго. Встречается у 50% детей с ЖКБ.
Диспептическая хроническая форма проявляется чувством тяже-
сти в эпигастрии и области правого подреберья, изжогой, метеоризмом, неустойчивым стулом. Обострение ЖКБ связано в погрешностями в диете (жирная, жаренная пища, острые блюда и т. д.).
Болевая хроническая форма - боли носят ноющий характер, локализуются в области правого подреберья и иррадиируют в правую лопатку. Положительные пузырные симптомы (Егорова, Ортнера, френикуссимптом). Характер болей зависит от размера камней. Детей, у которых имеются неподвижные камни, беспокоят тупые, ноющие боли в правом подреберье. Имеется связь болевого синдрома с состоянием вегетативной нервной системы. Так, у ваготоников боли чаще носят приступообразный характер.
Желчная колика (5-7% детей) - внезапно возникающие высокоинтенсивные боли в правом подреберье. Приступ болей провоцируется погрешностью в диете, стрессом, физической нагрузкой. Характерны тошнота, рвота, положительные пузырные симптомы.
Диагноз. При наличии клиники печеночной колики диагноз ЖКБ не представляет трудностей. В остальных случаях камни являются случайной находкой при УЗИ.
Лабораторные исследования Общий анализ крови. При развитии холецистита или холангита по-
является лейкоцитоз, нейтрофильный сдвиг формулы крови, увеличение СОЭ.
Дуоденальное зондирование (микроскопия, биохимическое исследование желчи). При дуоденальном зондировании в порции В обнаруживают мелкие камни, песок, кристаллы. Индекс литогенности (ИЛ) - частное от деления количества холестерина в желчи на количество холестерина, которое может быть растворено при данном соотноше-
нии желчных кислот, лецитина и холестерина. ИЛ =< 1 - желчь ненасыщенная (нелитогенная).
При биохимическом исследовании: повышение уровня в крови би-
лирубина, холестерина, ЛАП, желчных кислот.
Показатели липидного обмена - основное исследование при ЖКБ: уровень общих липидов снижается; триглицеридов, неэстерифицированных жирных кислот, фосфолипидов – повышается.
УЗИ. При УЗИ в просвете желчного пузыря выявляется округлое, подвижное плотное образование, за которым имеется «акустическая» тень.
219
Камни в желчных путях и желчном пузыре можно также выявить при помощи холецистографии, холецистохолангиографии.
Обзорная рентгенография области желчного пузыря выявляет конкременты с частотой менее 20%.
МРХПГ (магнито-резонансная холангиопанкреатография) –
выявляет конкременты в желчных протоках, в том числе и в печеночных, аномалии развития желчных путей.
Сцинтиграфия желчных протоков – используется для диагностики «отключенного» желчного пузыря.
Дифференциальный диагноз ЖКБ проводится с язвенной болезнью 12 п.к., хроническим гастродуоденитом, хроническим панкреатитом, хроническим холециститом.
Следует иметь в виду, что похожую на конкременты ультразвуковую картину могут давать дефекты заполнения желчного пузыря, особенности складчатости желчного пузыря, наличие сладжа, артефакты, связанные с дыхательными движениями. В сомнительных случаях следует повторить исследование.
При выявлении камней в желчном пузыре необходимо проведение дополнительных исследований для исключения: гемолитических анемий, мальабсорбции, гепатитов; исключить длительное применение фуросемида. Необходимо выполнить обследование на гельминты.
Лечение. Задачи лечения: создание условий для уменьшения воспалительного процесса, улучшения оттока желчи, уменьшения склонности к дальнейшему камнеобразованию.
Схема лечения. Обязательные мероприятия: режим, диета, препараты желчных кислот, улучшение оттока желчи, хирургическое лечение (при наличии показаний).
Вспомогательное лечение: использование гепатопротекторов, хирургическое лечение, литотрипсия.
Диета - стол № 5. Показано употребление большого количества растительной клетчатки, витамина С, уменьшение количества белка и жиров. Пищу рекомендуют принимать небольшими порциями 5-6 раз в день.
Показания для госпитализации – обострение ЖКБ.
Режим: (см. «Хронический холецистит»).
Лечение зависит от формы заболевания и степени операционного риска. Лечению подлежат больные с выраженной клинической симптоматикой. При бессимптомном течении ЖКБ показано только диспансерное наблюдение. У большей части больных при наличии хронической рецидивирующей формы ЖКБ приступ удается купировать консервативными методами лечения.
220
Для улучшения оттока желчи используют: парафиновые и озокеритовые аппликации, индуктотермию на область печени, электрофорез магния и спазмолитиков.
При длительном использовании медикаментов показаны гепатопротекторы: гепабене, хофитол, эссенциале.
Пероральное растворение камней применяется только тогда, когда соблюдаются нижеперечисленные правила:
1) ранняя стадия заболевания, 2) размеры конкрементов не более 10 мм, 3) сохранение сократительной способности желчного пузыря, 4) неосложненное течение ЖКБ.
Противопоказаниями для применения консервативной терапии являются: 1) наличие острого и хронического холецистита, 2) желчная колика, 3) отключенный желчный пузырь, 4) ожирение ІІІ степени, 5) хронический гепатит и цирроз печени, 6) хроническая диарея, 7) холедохолитиаз.
При тяжелом течении ЖКБ литолитическая терапия проводится в тех случаях, когда неблагоприятный риск оперативного вмешательства выше риска летального исхода ЖКБ.
Медикаментозное растворение камней эффективно только при наличии ренгенонегативных (холестериновых) камней. С этой целью применяют урсодил (урзофалк) длительно (на протяжении до 2-х лет). Хенофалк принимают на протяжении 1 года и более. Этот метод э ф- фективен только у 25% больных. При наличии билиарного сладжа эффективность лечения до 70%. Существует несколько схем приема препаратов.
Успешный литолиз не гарантирует от рецидивов камнеобразования.
Эффективность лечения оценивается в первые 3 месяца каждые 4 недели по данным УЗИ и биохимического исследования, а затем 1 раз в 6 месяцев.
Лечение печеночной колики: тепловые процедуры (грелки на поясничную область или живот, горячие ванны).
С целью купирования болей назначают спазмолитики: мебеверин, но-шпа, пинаверия бромид на протяжении 2-4 недель.
Противопоказания к назначению консервативного лечения: ослож-
ненное течение ЖКБ, отключенный желчный пузырь, ожирение III степени, хронические гепатиты и циррозы, хроническая диарея.
Хирургическое лечение ЖКБ проводится с учетом возраста ребенка, величины и места расположения камней, длительности заболевания, особенностей клиники.
221

Плановое оперативное вмешательство показано в возрасте от 3 до 12 лет при наличии диспептической формы ЖКБ и желчной колики. В возрасте 12-15 лет хирургическое вмешательство проводят только по экстренным показаниям. В настоящее время получили широкое распространение эндоскопические операции. Продолжают выполняться и открытые операции - холецистомия, холецистэктомия, холедохолитотомия.
В последние годы предложены альтернативные методы лечения ЖКБ: 1) прямое контактное растворение камней метил-(тред)- бутиловым эфиром. Широкому распространению метода препятствует большое число осложнений, частые рецидивы, необходимость наличия опыта у врача. Продолжает накапливаться материал по возможности применения при ЖКБ экстракорпоральной литотрипсии (дробление камней ударной волной).
Осложнения ЖКБ: деструктивный холецистит, холангит, механическая желтуха, вторичный билиарный цирроз печени, острый панкреатит, стриктура большого дуоденального сосочка, билиарная непроходимость кишечника, абсцесс печени, отключенный желчный пузырь и т. д.
Течение и прогноз. Радикальная операция при ЖКБ обеспечивает полное или почти полное выздоровление. При проведении органосберегающих операций процент рецидивов ЖКБ достаточно высок. Если оперативное вмешательство проведено в период ремиссии, то риск летального исхода составляет около 2%. При ранней диагностике ЖКБ и проведении адекватного лечения прогноз благоприятный.
Профилактика. Литогенность желчи значительно повышается при погрешностях в диете; дефиците в рационе витамина С; уменьшению экскреции холестерина в желчь способствует дозированная ходьба. Малоподвижный образ жизни способствует камнеобразованию.
Наиболее эффективны для профилактики рецидива ЖКБ урсофальк, хенофалк. Лучшая профилактика осложнения ЖКБ - своевременное оперативное лечение.
Для профилактики рецидивов камнеобразования используют: прием достаточного количества жидкости, дробное (не менее 4 раз) питание, снижение массы тела, профилактический прием урсодеоксихолевой кислоты, коррекцию дискинезий желчной системы.
Вопросы к экзамену. Желчнокаменная болезнь. Патогенез. Факторы, способствующие появлению камней. Клиническая картина. Диагностика. Значение рентгенологического и ультразвукового исследования в диагностике холелитиаза. Дифференциальный диагноз. Течение. Лечение. Неотложная терапия
222

при желчнокаменной колике. Показания к хирургическому лечению. Исходы. Профилактика.
ХРОНИЧЕСКИЙ ГАСТРОДУОДЕНИТ (ХГД) – хрониче-
ское воспалительное заболевание преимущественно антрального отдела желудка и 12 п.к., сопровождающееся нарушением регенерации слизистой оболочки желудка, расстройствами пищеварения и моторики.
Хронический гастрит – хроническое рецидивирующее очаговое или диффузное воспаление слизистой (подслизистой) оболочки желудка с нарушением процессов регенерации, склонностью к прогрессированию, развитию атрофии и секреторной недостаточности, сопровождающееся нарушениями пищеварения и обмена веществ.
Эпидемиология. ХГД самая частая патология органов пищеварения и составляет 80% от всех заболеваний желудочно-кишечного тракта. Частота ХГД (гастрита) у школьников составляет 4-20%. Хронический гастрит, как и дуоденит в изолированном виде встречается редко
– у 10-15% детей.
Факторы риска ХГД: раннее искусственное вскармливание, неполноценное по составу и нерегулярное питание, злоупотребление острой или горячей пищей, плохое пережевывание пищи, наследственная предрасположенность.
Этиология. Причины вызывающие ХГД: инфекции (хеликобактерии), нарушения питания, заболевания других органов системы пищеварения, эндокринная патология.
Выделяют экзогенные и эндогенные этиологические факторы ХГД. К экзогенным факторам относят: нарушение питания, длительный прием медикаментов, инфекции (хеликобактерии). Хеликобактерная инфекция (НР) принимает участие в развитии ХГД в более чем в 70% случаев. НР при поверхностных поражениях слизистой оболочки желудка и 12 п.к. выявляется у 30 -80% детей, а при эрозивно-язвенных процессах - у 90-100%.
К эндогенным факторам причисляют: заболевания других органов системы пищеварения, эндокринную патологию, нарушения ЦНС, заболевания обмена веществ. На долю аутоиммунного гастрита приходится 40% всех случаев заболеваний у детей.
Патогенез ХГД предусматривает воздействие алиментарного, ки- слотно-пептического, аллергического, аутоиммунного и наследственных факторов. Перечисленные факторы, оказывая повреждающее воз-
223
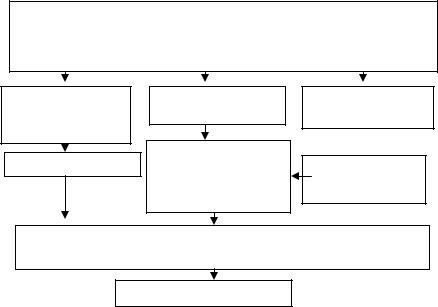
действие на слизистую оболочку желудка, подготавливают условия для присоединения НР – основного этиологического момента в развитии ХГД.
НР обладает уникальной способностью проникать через защитные барьеры слизистой оболочки путем продуцирования уреазы. Вокруг бактерий создается защитная щелочная оболочка, в результате чего НР проникают в крипты и железы слизистой оболочки желудка. Считают, что НР не только вызывает классический антральный гастрит, но и запускает аутоиммунные механизмы патогенеза гастрита.
НР вызывает следующую цепочку патологических изменений в слизистой оболочке: воспаление → атрофия → дисплазия → MALTлимфома (мальтома) или рак.
Помимо аутоиммунных механизмов в развитии ХГД принимают участие и другие компоненты иммунной системы. Происходит увеличение синтеза некоторых антител, активация Т-лимфоцитов, продукция γ- интерферона, цитокинов, белков теплового шока и др.
Результатом развившегося воспалительного процесса является нарушение секрето- и кислотообразования, выработки слизи, повреждение эпителия, микроциркуляторные расстройства.
Предрасполагающие и этиологические экзо- и эндогенные факторы:
наследственная отягощенность, нарушения питания, влияние медикаментов, инфекции, интоксикации, местные сосудистые и гипоксические состояния
Нарушение тро-
фики слизистой оболочки
Присоединение НР
Повреждение эпи-
телия
Расстройства регене-
рации эпителия, дистрофические изменения СОЖ
Аутоиммунные
нарушения
Дуоденогаст-
ральный рефлюкс
Нарушение секрето- и кислотообразования, выработки слизи, по-
вреждение эпителия, микроциркуляторные расстройства
Хронический гастрит
224
Рис. 1.27. Схема патогенеза ХГД
Классификация хронического гастрита, дуоденита, гастродуоденита у детей (2001г)
1.По происхождению: А) первичный (экзогенный):
2.Этиологические факторы: 1) инфекционный (H. Pylori (НР),
другие бактерии, вирусы, грибы); 2) токсический (реактивный): этиологические факторы – химический, радиационный, лекарственный, алкогольный, никотиновый, стрессовые состояния.
3.Топография: гастрит (антральный, фундальный, пангастрит);
дуоденит (бульбит, постбульбарный пандуоденит); гастродуоденит.
4. Формы поражения желудка и 12-перстной кишки.
По характеру эндоскопической картины: а) эритематозный/ экссу-
дативный, б) нодулярный, в) с эрозиями (с плоскими или приподнятыми эрозиями), г) геморрагический, д) с атрофией, е) смешанный.
5. По характеру морфологических изменений в слизистой оболоч-
ке желудка: а) поверхностный, б) диффузный. По характеру поражения: 1) с оценкой степени: воспаления, активности, атрофии, кишечной метаплазии, H. pylori. Без оценки степени: субатрофия, специфические, неспецифические.
6.Характер кислотной продукции желудка*: а) неизмененная, б)
пониженная, в) повышенная.
7.По периодам заболевания: 1) обострение, 2) период неполной ремиссии, 3) полная клиническая ремиссия, 4) клинико - эндоскопическая ремиссия, 5) клинико-эндоскопически- морфологическая ремиссия.
8.В) вторичный (эндогенный):
9.Этиологические факторы: аллергия, болезнь Крона, гранулема-
тоз, целиакия, при системных заболеваниях, саркоидоз.
10. Формы поражения желудка и 12-перстной кишки. Морфологически:
Степени тяжести: норма (0), слабая (1+), средняя (2+), сильная
(3+).
* Исследование кислотообразующей функции желудка потеряло былое диагностическое значение.
Классификация хронического гастрита (Сидней, 1990)
Ι. Морфологический.
1.Эндоскопическая характеристика:
а) эритематозный (поверхностный), эрозивный, геморрагический;
225
б) атрофический (умеренный, выраженный);
2.Гистологическая характеристика:
а) воспаление с эрозиями, кровоизлияниями; б) атрофический (умеренный, выраженный);
в) нарушение клеточного образования – метаплазия эпителия.
ΙΙ. Этиологический: 1. Связанный с желудочным хеликобактером (тип В); 2. Аутоиммунный (тип А); 3. Реактивный (тип С) *.
ΙΙΙ. Топографический: антральный; фундальный; пангастрит. ΙV. Активность: отсутствует; умеренная; выраженная.
* Под гастритом С понимают рефлюкс дуоденального содержимого. Иногда выделяют смешанный тип гастрита - присоединение аутоиммунных поражений к бактериальному гастриту.
Исследования: общий анализ крови и мочи, протеинограмма, билирубин крови, амилаза мочи, ФГДС, УЗИ органов брюшной полости.
По показаниям: анализ кала на скрытую кровь, исследования на хеликобактер, анализ желудочного сока, ЭКГ, рентгенография желудка, гистология и цитология биоптата.
Исследования амбулаторно, приказ МЗ РФ № 248: измерение АД, ФГДС, общий анализ крови, исследование на НР. По показаниям: био-
псия слизистой желудка и 12 перстной кишки, кал на скрытую кровь, рентгеноскопия желудка и 12 перстной кишки, рН-метрия, УЗИ желчного пузыря и поджелудочной железы.
Анамнез, клиника. При сборе анамнеза необходимо обратить внимание на: характер болей, их локализацию, связь с приемом пищи, временем суток; наличие и характер диспептических проявлений.
Проявления ХГД состоят из болевого, диспептического, астеновегетативного синдромов. Боли при ХГД могут быть постоянными или периодическими. Боли локализуются в эпигастральной или пилородуоденальной области. В некоторых случаях боли возникают ночью или натощак, уменьшаются после приема пищи или антисекреторных препаратов. Боли в животе или слабые или средней интенсивности, чаще связаны с приемом пищи.
Диспептические проявления при ХГД представлены: тошнотой, изжогой, тяжестью в эпигастрии, отрыжкой, изжогой, неприятным вкусом во рту, урчанием, переливанием жидкости в животе, метеоризмом, запорами или неустойчивым стулом.
Многие дети с ХГД предъявляют жалобы вегетативного характера: головные боли, повышенную потливость, тахикардию, одышку, нарушение аппетита, и др. Характер вегетативных проявлений зависит от типа вегетативных нарушений.
226
При объективном обследовании выявляют: боли в эпигастральной области, положительный симптом Менделя, наличие сопутствующих проявлений патологии желудочно-кишечного тракта и вегетативной нервной системы. У детей с ХГД имеет место бледность кожных покровов, повышенная потливость, сухость и обложенность языка белым налетом.
Диагноз ХГД клинико-инструментальный. Клинические проявления ХГД при постановке диагноза имеют ориентировочное значение.
Лабораторные исследования
Изменения банальных лабораторных показателей не характерны при ХГД.
ФГДС позволяет определить степень гиперплазии или атрофии слизистой оболочки, обнаружить воспалительные изменения (отек, гиперемия, повышение продукции слизи и жидкости, различные варианты рефлюксов), уточнить фазу заболевания, эффективность лечения. Основной метод диагностики ХГД - прижизненная гастробиопсия, которая помогает установить форму заболевания (поверхностный ГД, с поражением желез без атрофии или с атрофией, степень и тяжесть процесса, его динамику, выявить этиологию заболевания).
Исследование функционального состояния желудка с помощью фракционного исследования желудочного содержимого, внутрижелудочной рН-метрии позволяет судить о кислотообразующей и кислотонейтрализующей функциях желудка.
Диагностическая ценность методов исследования НР. Выделение культуры НР – чувствительность метода 33-97%, специфичность – 100%. Гистологический метод – чувствительность – 86-99%, специфичность – 86-100%. Обнаружение НР в слюне (метод ИФА) - чувствительность – 66%, специфичность – 98%. Уреазный тест - чувствительность – 65%, специфичность – 75-100%.
Подходы к определению степени тяжести ХГД. Для этой цели ис-
пользуют только морфологические критерии. 1. Воспаление - количество воспалительных клеток в слизистой оболочке желудка. 2. Атрофия – утрата клеточных желез (вне зависимости от выраженности воспаление). 3. Кишечная метаплазия – не всегда признак предракового состояния. 4. Активность воспаления – степень нейтрофильной инфильтрации собственной пластинки и межэпителиальных пространств слизистой оболочки желудка. 5. Степень обсемененности НР в гистопрепарате при его окраске по Граму или Гимзе.
Дифференциальный диагноз ХГД проводят с: функциональной диспепсией, эзофагитами, язвенной болезнью, холепатиями, панкреатитами. Основой дифференциальной диагностики являются дополни-
227
тельные исследования. При наличии клинических проявлений, указывающих на заболевание желудка (боли, чувство переполнения в подложечной области, тошноту, и т.д.) и при отсутствии признаков органических заболеваний (по данным ФГДС, биопсии) устанавливается диагноз функциональной диспепсии. См. также табл. 1.45.
Лечение. Задачи лечения: эрадикация инфекции, восстановление слизистой оболочки желудка, нормализация функционального состояния клеток слизистой оболочки, ликвидация нарушений пищеварения и моторики, предупреждение прогрессирования заболевания, лечение сопутствующих поражений ЖКТ.
Схема лечения. Обязательные мероприятия: эрадикация хеликобактера (при его наличии), подавление повышенной кислотности желудочного содержимого, коррекция болевого синдрома (при наличии).
Вспомогательное лечение: диета, восстановление слизистой оболочки желудки и двенадцатиперстной кишки, прокинетики, ферменты, миоспазмолитики, коррекция вегетативных нарушений, прием минеральных вод, физиотерапия.
Показания к госпитализации: впервые выявленная патология ЖКТ, сочетанный характер заболевания, выраженность болевого и диспептического синдромов, отсутствие эффекта от амбулаторного лечения, невозможность проведения обследования и лечения в амбулаторных условиях.
Лечение ХГД с секреторной недостаточностью включает применение диеты в стадии обострения. Стол №1 назначается на 1-2 недели. Затем постепенно переходят к столу № 2 (сокогонный стол, который назначают на 2 месяца). Важно соблюдать регулярность питания, тщательность прожевывания пищи. Строгое соблюдение диеты не обязательно.
Заместительная терапия включает натуральный желудочный сок, плантаглюцид в течение 3-4 недель, абомин в течение 3-4 недель, 1% раствор соляной кислоты с пепсином на протяжении 1 месяца, ферменты (прил. 1) в течение 3-4 недель.
Для улучшения трофических и регенераторных процессов рекомендуют назначать: липоевую кислоту 0,5% раствор по 1-2 мл, пантотенат кальция по 2 мл 10-20% раствора, ККБ по 50 мг, рибофлавина мононуклеотида по 1мл 1% раствора курсами по 7 дней, витамин U 0,05г 2 раза в день на протяжении 7 дней. Фитотерапия включает сок подорожника, облепиховое масло, настои трав трилистника, тысячелистника, мяты, ромашки, курсами по 30-60 дней.
В качестве средств симптоматической терапии при гастрите с по-
вышенной кислотообразующей функцией показаны: антациды и
228
адсорбенты (викалин, викаир, ротер, альмагель, фосфалюгель, маалокс, сукральфат). Курсы лечения этими препаратами от 2 до 6 недель. Антациды не рекомендуют применять совместно с другими препаратами (возможно нарушение их абсорбции и повреждение защитной оболочки).
Антисекреторные средства: атропин (7-10 дней), платифиллин (2 недели), метацин (2 недели); блокаторы Н2-гистаминовых рецепторов (ранитидин, фамотидин, зантак, ранисан). Курс лечения этими препаратами составляет 4-6 недель. Во избежание синдрома отмены эти препараты необходимо отменять постепенно.
Ингибиторы протонной помпы (омепразол, лансопразол, рабепразол и др.) при лечении ХГД назначают по 1 мг/кг. Основное показание для применения блокаторов Н2-гистаминовых рецепторов и ингибиторов протонной помпы – высокая кислотообразующая функция желудка. Омепразол не применяют вместе с другими антисекреторными препаратами из-за повышения риска возникновения инфекций пищеварительного тракта.
При наличии симптомов, связанных с нарушением моторики желудка и/или повышенной чувствительности желудка к растяжению, чувстве быстрого насыщения, переполнения, вздутия и тяжести в эпигастральной области показаны прокинетики (метоклопрамид по 10 мг 3 раза в день за 20 минут до еды).
Показаниями для применения прокинетиков (метоклопрамид, мотилиум) также являются: дуоденостаз, дуоденогастральный рефлюкс, гастростаз.
В качестве цитопротекторов назначают: биогастрон, ликвиритон (3- 4 недели), оксиферрискарбон (20-30 дней), сукральфат, облепиховое масло (30-40 дней), солкосерил.
При болях показаны спазмолитики – Дюспаталин, папаверин, дротаверин, платифиллин, атропин, метацин. При выявлении изменений вегетативного статуса по ваготоническому типу применяют: беллатаминал, белласпон, в сочетании со стимуляторами ЦНС растительного происхождения (элеутерококк, женьшень, плоды лимонника). При выявлении симпатотонии назначают: валериану, триоксазин, феназепам, нозепам, диазепам.
Минеральные воды (Ессентуки №4 и № 17, Арзни, Боржоми, Славяновская и др.) по 100-150 мл курсами по 30-40 дней, 2-3 курса в т е- чение года.
Физиолечение: при упорном болевом синдроме рекомендуют ультразвук (8-10 процедур) и гелий-неоновый лазер на эпигастрий (4-5 сеансов), КВЧ. В фазу стихания процесса используют: электросон (12-15
229

процедур), эндоназальный электрофорез с тиамином, электрофорез с новокаином, платифиллином, кальцием, цинком на область эпигастрия (курс 10-12 процедур). Начиная со 2-й недели обострения показаны: синусоидальные модулированные токи, ДМВ-терапия. В стадию стихания обострения назначают: аппликации озокерита, торфа, гальваногрязевые процедуры.
Антихеликобактерная терапия. Показаниями к назначению анти-
хеликобактерной терапии являются: язвенная болезнь желудка и язвенная болезнь двенадцатиперстной кишки независимо от фазы заболевания, НР-ассоциированный гастрит, атрофический гастрит, наличие инфицированных H. Pylori прямых родственников, а так же в некоторых случаях при наличии функциональной диспепсии (эффективность такого лечения пока не доказана). Схемы лечения НР при ХГД представлены в табл. 1.57. После эрадикационного лечения воспалительные изменения в слизистой оболочке исчезают в течение 2-6 месяцев.
Эффективность эрадикационной терапии можно повысить добавлением в лечение энтеросорбентов (СУМС, альгисорб и др.), иммуномодуляторов (деринат, виферон и др.). В период проведения эрадикационной терапии на срок не менее 4 недель возможно назначить пробиотики (бифидумбактерин форте, линекс, хилак форте и др.).
Табл. 1.59. Схемы лечения хеликобактерной инфекции (Форму-
лярная система, выпуск IX, 2008)
Терапия первой линии
1. Омепразол, лансопразол, ра- |
2. Омепразол, лансопразол, ра- |
бепразол, эзомепразол + |
бепразол, эзомепразол (все 2 |
Кларитромицин |
раза в сутки)+ |
Метронидазол |
Амоксициллин 2 раза в сутки) |
|
Кларитромицин (2 раза в сутки) |
Квадротерапия (терапия второй линии)
1. Омепразол, лансопразол, рабепразол, эзомепразол (все препа-
раты 2 раза в сутки) + субцитрат/субсалицилат висмута (4 раза в сутки) + метронидазол (3 раза в сутки) + тетрациклин (4 раза в сутки)
* терапию первой линии проводят сразу после установления диагноза ЯБ независимо от периода болезни (обострение, ремиссия) и осложнений. Продолжительность курса лечения 7-14 дней (14-ти дневный курс более предпочтительнее).
Профилактика. Рациональное питание, соблюдение требований гигиены, нормализация режима труда и отдыха, предупреждение обострений заболевания, своевременное лечение заболеваний желудочно-
230

кишечного тракта.
Вопросы к экзамену. Гастриты. Гастродуодениты. Хронический га-
стрит. Хронический гастродуоденит. Роль пилорического хеликобактера. Патогенез. Классификация. Клинические проявления. Диагностика. Функциональные методы исследования желудочной секреции (зондовые, беззондовые методы). Внутрижелудочная рН-метрия. Показания к рентгенологическому исследованию. Эзофагогастродуоденоскопия. Диффе-
ренциальная диагностика. Лечение. Особенности лечения гастрита хеликобактерной этиологии. Профилактика.
ЯЗВЕННАЯ БОЛЕЗНЬ (ЯБ) - хроническое рецидивирующее заболевание, склонное к прогрессированию и вовлечению в процесс других органов пищеварения. ЯБ является полиэтиологическим заболеванием, в возникновении которого играют роль: Helicobacter pilori (НР), нарушение взаимоотношений между факторами агрессии и факторами защиты в желудке, наследственная предрасположенность. Установлена взаимосвязь между ЯБ и ХГД.
Эпидемиология. Частота ЯБ составляет 1 случай на 600 детей. В последние годы отмечается как увеличение количества детей с ЯБ, так и «омоложение» заболевания. Инфицированность НР у детей 5-7 лет составляет 40-50%.
Этиология. Нарушение нейрогуморальной функции желудка, дефекты питания, стрессы, отрицательные эмоции, наследственная предрасположенность, хеликобактерная инфекция.
Патогенез. В основе патогенеза ЯБ лежит нарушение взаимоотношений между факторами агрессии и факторами защиты. Факторы агрессии: соляная кислота, пепсины, гистамин, желчные кислоты, дуоденогастральный рефлюкс. Факторы защиты: слизь, щелочи, регенераторная способность слизистой оболочки желудка, простагландины. Под влиянием нервно-психических нарушений, заболеваний системы пищеварения, эндокринных заболеваний, алиментарных факторов происходит сдвиг в сторону факторов агрессии, что приводит к повреждению слизистой оболочки.
Важным моментом в патогенезе ЯБ является колонизация слизи-
стой оболочки желудка Helicobacter pylori. Под влиянием Helicobacter pylori происходит запуск каскадных реакций цитокинового ряда IL-8 с модулированием хемотаксиса, хемокинеза, агрегацией и высвобождением ферментов из нейтрофилов, что усугубляет повреждение эпите-
231
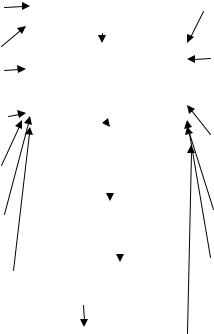
лия слизистой оболочки желудка. Влияние Helicobacter pylori приводит к замедлению миграции эпителия в случае образования дефекта, с последующей стимуляцией апоптоза. Это усиливает гибель клеток в краях язв и затрудняет их заживление. Снижение уровня эпидермального фактора роста при персистенции Helicobacter pylori вызывает задержку репарации, уменьшение синтеза простагландинов (PGE2), что приводит к нарушению микроциркуляции и трофики тканей.
|
|
|
|
|
|
|
Расстройство ре- |
|
|
|
|
|
|
Гипоксия |
|
|
|
|
|||||||
|
Психосомати- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
ческие факто- |
|
|
|
гуляции желудка |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дуодено- |
|
|
|
|
|
Эндокринные |
|
|
|
|
Нарушение есте- |
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
гаст- |
|
|
|
||||||||||
|
факторы |
|
|
|
|
ственной рези- |
|
|
|
|
|
|
|
ральный |
|
|
|
||||||||
|
|
|
|
|
|
|
стентности слизи- |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Деятельность же- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
стой оболочки |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
лудочно-кишечных |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Наруше- |
|
|
|
||||
|
гормонов |
|
|
|
Повышение актив- |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ние му- |
|
|
|
||||||||
|
|
|
|
|
|
|
ности кислотно- |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цинооб |
|
|
|
||||||||
|
Биогенные |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
пептического фак |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
амины |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Действие |
|
|
|
|||
|
|
|
|
|
|
|
Инфицирован- |
|
|
|
|
|
|
|
|
|
|
||||||||
|
Пищевая аллер- |
|
|
|
|
|
|
|
|
|
|
|
детерген- |
|
|
|
|||||||||
|
гия |
|
|
|
|
ность НР |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Наследст- |
|
|
|
||||
|
|
|
|
|
|
|
Морфологиче- |
|
|
|
|
|
|
|
|
||||||||||
|
Иммунологиче- |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
ские нарушения |
|
|
|
|
|
венность и |
|
|
|
||||||||||||
|
ские нарушения |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
особенности |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
Язвенная болезнь |
|
|
Нарушение реге- |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нерации СОЖ |
|
|
|
||||||||
|
Рис. 1.28. Схема патогенез ЯБ |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
Классификация язвенной болезни (Мазурин А.В., 1984)* |
|
|
|
|||||||||||||||||||||
1.Клинико-эндоскопическая стадия: а) свежая язва, б) начало эпи-
телизации язвенного дефекта, в) заживление язвенного дефекта слизистой оболочки при сохранившемся дуодените, г) клинико-эндо- скопическая ремиссия.
2.Фаза течения: а) обострение, б) неполная клиническая ремис-
232
сия, в) клиническая ремиссия.
3.По локализации: а) желудок, б) двенадцатиперстная кишка (луковица и постбульбарный отдел), в) двойная локализация.
4.Форма: Неосложненная. Осложненная: а) кровотечение, б) пенетрация, в) перфорация, г) стеноз привратника, д) перивисцерит.
5.Функциональная характеристика: Кислотность желудочного содержимого и моторика: а) повышены, б) понижены, в) нормальные.
6.Сопутствующие заболевания: а) панкреатит, б) гепатит, в) энте-
роколит (колит), г) эзофагит, д) холецистохолангит.
* В диагнозе следует указывать результаты исследования на хеликобактер.
Исследования: общий анализ крови и мочи, копрограмма, ФГДС, ЭКГ. По показаниям: протеинограмма, трансаминазы, щелочная фосфатаза, сывороточное железо, анализ кала на скрытую кровь, исследование на хеликобактер, анализ желудочного сока, рентгенография желудка, УЗИ органов брюшной полости, цитологическое исследование биоптата.
Исследования амбулаторно, приказ МЗ РФ №241: ФГДС, общий анализ крови, измерение АД. По показаниям: УЗИ желчного пузыря и поджелудочной железы, контрастная рентгенография желудка и 12 перстной кишки, исследование кислотообразующей функции желудка, рН-метрия, кал на скрытую кровь, биопсия слизистой желудки и 12 перстной кишки, тромбоциты крови, исследования на НР.
Анамнез, клиника. При сборе анамнеза необходимо обратить внимание на: рвоту (особенно «кофейной гущей»), вздутие живота, дегтеобразный стул, связь боли с приемом пищи, наличие ритмичности болей, голодные (ночные) боли, интенсивность болей, склонность
кзапорам.
Ванамнезе выявляют нарушение режима, питания, стрессы, заболевания желудка у близких родственников.
Основным проявлениям ЯБ является болевой синдром, для которого характерны: выраженность болей, «язвенноподобный» ритм болей (голод – боль – прием пищи – облегчение болей), наличие ночных и голодных болей (для ЯБДПК).
Выделяют ранние боли (появляются через 0,5-1 ч после еды и с о- храняются в течение 1-2 часов). Характерны для язв тела желудка.
Поздние боли возникают через 1,5-2 часа после еды. Эти боли по-
степенно усиливаются по мере продвижения желудочного содержимого в 12 п.к. (характерны для язв тела желудка).
Голодные (ночные боли) возникают через 1,5-2 часа после еды, постепенно усиливаются по мере продвижения желудочного содержимо-
233
го в 12 п.к., исчезают после очередного приема пищи. Характерны для язв 12 п.к. У детей боли не во всех случаях имеют описанные признаки.
Для ЯБ характерны диспептические проявления: изжога (частый и ранний признак), отрыжка, тошнота, запоры.
У многих детей с ЯБ выявляются симптомы вегетативной дисфункции: непереносимость закрытых помещений, чувство нехватки воздуха, нарушения сна, повышенная потливость и др.
При объективном исследовании выявляется болезненность или в области эпигастрия, или в области проекции луковицы 12 п.к. (в зависимости от локализации язв).
Для язвенной болезни характерно цикличное течение заболевания, сезонность обострений (весна и осень) Обострения чаще появляются после стрессов, нарушения питания, изменений погоды.
Диагноз ЯЗ устанавливается на основании учета данных анамнеза, клинических проявлений и результатов инструментальных исследований. У детей самая частая локализация ЯБ у детей - луковица двенадцатиперстной кишки.
Лабораторные исследования Общий анализ крови выявляет в некоторых случаях признаки по-
стгеморрагической анемии.
Анализ кала на скрытую кровь – положительная реакция при язвенном кровотечении.
ФГДС. Диагноз ЯБ подтверждается выявлением при ФГДС язвенного дефекта.
УЗИ – позволяет уточнить структурные изменения стенки желудка и прилегающих тканей.
Рентгенологическое исследование имеет вспомогательное значение
(уступает по чувствительности данным ФГДС).
Внутрижелудочная рН-метрия часто выявляет повышенную или сохраненную кислотообразующую функцию желудка.
Тесты для выявления НР (см. «хронический гастродуоденит»).
Дифференциальный диагноз ЯБ необходимо проводить со стрес-
совыми язвами (психоэмоциональные и физические травмы, оперативные вмешательства, шок, обморожение, тяжелое течение инфекционных заболеваний и т.д.). Лекарственные язвы развиваются при применении кортикостероидов, НПВС, резерпина, кофеина, цитостатиков и др. Вторичные симптоматические язвы возможны при: циррозе пече-
ни, хроническом гепатите, хроническом панкреатите, гиперпаратиреозе.
Дифференциальный диагноз также необходимо проводить с ХГД,
234
функциональной диспепсией.
Табл. 1.60. Дифференциальный диагноз язвенной болезни и ХГД
Признак |
Язвенная болезнь 12 |
ХГД |
|
п.к. |
|
Боль |
Ночная, голодная |
Часто связанная с |
|
|
приемом пищи |
Ритмичность болей |
Мойнигановский |
Не характерно |
|
ритм болей |
|
Интенсивность болей |
Высокоинтенсивные |
Слабые, умеренные |
Диспептические про- |
Характерны |
Характерны |
явления |
|
|
Вегетативные нару- |
Характерны |
Характерны |
шения |
|
|
Общий анализ крови |
Иногда постгеморра- |
Часто без изменений |
|
гическая анемия |
|
ФГДС |
Выявление язвенного |
Воспалительные из- |
|
дефекта |
менений разной ло- |
|
|
кализации |
Лечение. Задачи лечения: ликвидация язвенного дефекта, восстановление нарушенного пищеварения и моторики, предупреждение развития осложнений, лечение сопутствующих заболеваний органов пищеварения.
Схема лечения. Обязательные мероприятия: антихеликобактерная терапия, антациды, купирование болей, режим.
Вспомогательное лечение: диета, хирургическое лечение, лечение осложнений, прокинетики, фитотерапия, физиолечение, иглорефлексотерапия, прием минеральных вод, витаминотерапия, ЛФК.
Показания для госпитализации: впервые выявленная ЯБ (или подозрение на ЯБ), осложненное течение ЯБ, сочетанное течение ЯБ, отсутствие эффекта от амбулаторного лечения, частые рецидивы заболевания.
При обострении заболевания показан постельный режим. Диетические питание при ЯБ включает последовательное исполь-
зование вариантов диеты № 1, а затем диеты № 5. Не доказано, что строгое соблюдение противоязвенных диет способствует более быстрому заживлению язвы и предупреждает рецидивы. В период обострения заболевания пищу принимают до 5 раз в день с ограничением экс-
235

трактивных веществ, термическим щажением. По мере улучшения состояния диета расширяется.
Медикаментозная терапия ЯБ при выявлении (так и без выявления!) Helicobacter pilori проводится по схемам, используемым при лечении хронического НР-ассоциированного гастродуоденита. Используют или тройные схемы эрадикационной терапии или схемы квадротерапии (таб. 1.57). Более предпочтительно использовать 14-и дневный курс лечения. После применения эрадикационной терапии показаны препараты, нейтрализующие соляную кислоту (антациды или блокаторы). При обострении ЯБ без сопутствующих заболеваний органов пищеварения и осложнений допустимо проводить только курс эрадикации Helicobacter pilori без последующей монотерапии антацидами или блокаторами, что сокращает стоимость лечения и его сроки.
После окончания антихеликобактерной терапии лечение продолжают с использованием антисекреторных препаратов до заживления язвы. В том числе используют омепразол (не менее 2 недель), ранитидин или фамотидин в течение 4-7 недель.
При обострении неосложненной ЯБ 12 п.к. используют Н2- блокаторы (ранитидин, фамотидин) или ингибиторы протонной помпы (омепразол, лансопразол) в течение 4 недель. При отсутствии заживления курс лечения продолжают еще 4 недели. При обострении неосложненной язвы желудка курс лечения указанными препаратами составляет 4-8 недель.
При отсутствии Helicobacter pilori назначают антацидные средства на 4-6 недель; Н2-блокаторы (циметидин, ранитидин, фамотидин) на 4- 6 недель; биологические препараты (бифилакт, лактобактерин), биодобавки, обогащенные витаминами С, Е сульфатом цинка. Если симптомы болезни сохраняются дольше 6 недель, то препараты принимают на ночь еще 3-12 месяцев; также назначают сукральфат курсом 4-6 не-
дель; омепразол (или париет3) при длительно незаживающей язве, склонности к обострениям.
При тошноте или чувстве тяжести в эпигастрии – метоклопрамид, веро-метоклопрамид, домперидон, мотилиум.
При спастических болях в животе – Дюспаталин, дротаверин, дротаверин НС, дротаверин форте, инъекции платифиллина, но-шпа- форте.
Фитотерапия: а) обострение ЯБ (начиная с периода эпителизации
3 Ингибиторы протонного насоса по эффективности превосходят другие антисекреторные средства.
236
язвенного дефекта) - отвары и настои ромашки аптечной, валерианы, мяты перечной, кровохлебки лекарственной, тысячелистника, шиповника; б) ремиссия (стадия сформированного рубца) - аир болотный, алтей лекарственный, зверобой, сушеница топяная, подорожник большой, крапива двудомная.
Физиолечение (общие методики) применяют во все периоды заболевания. Местные процедуры (гальванизация, лекарственный электрофорез) показаны начиная со 2-й стадии болезни. Тепловые процедуры (парафин, озокерит) назначают в период заживления язвенного дефекта. Для рассасывания рубцов используют электрофорез с лидазой или террилитином.
Осложнения: кровотечение, перфорация язвы, пенетрация язвы, деформация и стеноз привратника, малигнизация язвы.
Кровотечение самый частый вид осложнения ЯБ. Незначительные кровотечения могут протекать скрыто. Массивные кровотечения проявляются геморрагическим шоком (бледность, головокружение, снижение АД, тахикардия, шум в ушах), кровавой рвотой, меленой, снижением уровня гемоглобина и эритроцитов в крови.
Перфорация язвы может протекать по нескольким вариантам. При перфорации в свободную брюшную полость появляются сильные («кинжальные») боли, признаки перитонита (доскообразный живот, симптомы раздражения брюшины, пареза кишечника), заостряются черты лица, появляются признаки обезвоживания. Диагноз подтверждается с помощью рентгенологического исследования.
Деформация и стеноз привратника чаще всего развиваются при ЯБ
12 п.к. Легкие и умеренные варианты этого осложнения клинически могут не проявляться. В более тяжелых случаях наблюдается чувство полноты и распирания в подложечной области, рвота (приносящая облегчение), потеря массы тела. Данное осложнение диагностируется при помощи ФГДС или рентгенологического исследования.
Пенетрация – проникновение язвы в соседние органы, возникает при значительной величине язвенного дефекта (10-15 мм). Проявляется упорным болевым синдромом, рвотой, не приносящей облегчения, изжогой, лейкоцитозом, увеличением СОЭ, повышением температуры тела.
Неотложная помощь при кровотечении включает: холод, голод,
покой. Область желудка обкладывают пузырями со льдом, промывают желудок ледяными растворами. Показана экстренная ЭФГДС для выявления локализации кровотечения с последующим применением методов терапевтического, эндоскопического и эндоваскулярного гемостаза. При снижении ОЦК показано переливание эритроцитарной мас-
237
сы, кровезаменителей.
Терапевтической лечение заключается в назначении омепразола в течение первых суток в дозе 20-40 мг внутривенно 3 раза в сутки; фамотидина по 10-20 мг или ранитидина по 25-50 мг 4 раза в сутки. При наличии геморрагических эрозий показан вентер по 1-2 г. При отсутствии эффекта от указанной терапии рекомендуется хирургическое лечение.
Профилактика. Соблюдение режима питания, труда и отдыха, требований гигиены. Важным является профилактика рецидивов ЯБ.
Внастоящее время эррадикационная терапия проводится с использованием 3х- и 4х-компонентных схем (таб. 1.57). Из антисекреторных
препаратов, помимо антацидов, гастроцепина, показано назначение Н2- гистаминоблокаторов II (ранитидин, фамотидин) и III поколений (аксид, роксатидин). Их применение целесообразно для непрерывной профилактики на фоне рецидивирующего течения ЯБ, язвенных кровотечений, трудно рубцующихся язв, гиперацидных состояний, эрозивного поражения слизистой нескольких отделов желудочнокишечного тракта. Антисекреторной направленностью обладают блокаторы протонного насоса (омепразол), синтетические простагландины (энпростил, арбопростил), энкефалины (даларгин).
Вкомплексной противорецидивной терапии ЯБ используются регуляторы моторики желудочно-кишечного тракта: прокинетические средства (церукал, мотилиум, цизаприд), эндогенные опиоиды (тримебутин), полипептиды (даларгин), антихолинергические соединения нового поколения (риабол, бускопан). Из ферментных препаратов применяют микросферы панкреатина – Креон. В зависимости от выраженности адаптационно-метеотропного синдрома, противорецидивные циклы лечения включают седативные средства, малые транквилизаторы.
Детям, перенесших хирургическое вмешательство, оформляют инвалидность.
Прогноз серьезный при наличии множественных язвенных дефектов или язв располагающихся ниже луковицы 12 п.к.
238

Вопросы к экзамену. Язвенная болезнь. Этиология. Классификация.
Клинические проявления. Диагностика. Методы выявления пилорического хеликобактера. Лечение язвенной болезни. Осложнения. Клинические проявления. Диагностика. Неотложная помощь при кровотечении и прободении язвы. Показания к хирургическому лечению.
ПОНОСЫ НЕИНФЕКЦИОННОЙ ЭТИОЛОГИИ. ТОКСИКОЗ С ЭКСИКОЗОМ
Понос (диарея) – учащение стула свыше возрастной нормы и появление жидкой консистенции кала. Частота стула у детей грудного возраста в норме при грудном вскармливании составляет 3-5 раз в сутки, при искусственном вскармливании – 1-3 раза. Диарея считается острой, если длительность заболевания не превышает 2-3 недель.
Эпидемиология. Распространенность диарей среди детей очень высокая. На протяжении жизни практически у каждого ребенка отмечаются эпизоды дисфункции кишечника.
Этиология. Основными причинами поносов являются инфекции (вирусы, бактерии и др.). Наиболее частыми причинами поносов неинфекционной этиологии являются заболевания системы пищеварения, пиелонефриты у детей раннего возраста, дисбиозы кишечника, аллергия, заболевания эндокринной и нервной системы, глистные инвазии, муковисцидоз, целиакия, дисахаридазная недостаточность и др. Диарея развивается при усиленной перистальтике кишечника и ускоренном продвижении его содержимого; нарушении всасывания жидкости в кишечнике; усиленной продукции кишечного секрета. Нередко диарея является проявлением заболевания внутренних органов.
Патогенез. В патогенезе любой диареи можно выделить 4 механизма: гиперсекреторный, гиперэкссудативный (инвазивный), гиперосмолярный, г ипер- и гипокинетический. Все механизмы диареи часто сочетаются между собой.
Табл. 1.61. Патогенетическая характеристика диарей
Тип поноса |
Патогенетические |
Особенности |
Возбудители |
|
механизмы |
стула |
|
Гиперсекре- |
Пассивная секре- |
Обильный, во- |
|
торная диа- |
ция води и элек- |
дянистый, в ко- |
Ротавирусы |
рея |
тролитов преобла- |
программе нет |
|
|
дает над всасыва- |
лейкоцитов |
|
239

|
нием |
|
|
|
Гиперэкссу- |
Гиперэкссудация |
Жидкий, не- |
Сальмонеллы, |
|
дативная |
белка в просвет |
обильный, |
шигеллы, кам- |
|
(инвазив- |
кишки с после- |
кровь, слизь, в |
пилобактер, |
|
ная) диарея |
дующим «сбро- |
копрограмме |
некоторые |
|
штаммы ки- |
||||
|
сом» воды и элек- |
лейкоциты |
||
|
шечной палоч- |
|||
|
тролитов |
|
||
|
|
ки и др. |
||
|
|
|
||
Гиперосмо- |
Задержка воды в |
Полифекалия, |
|
|
лярная диа- |
кишечнике в ре- |
стеаторея |
Не выявля- |
|
рея |
зультате накопле- |
|
ются |
|
|
ния осмотически |
|
|
|
|
активных веществ |
|
|
|
Гипер- и |
Нарушение скоро- |
Жидкий или |
|
|
гипокине- |
сти передвижения |
кашицеобраз- |
Не опреде- |
|
тическая |
кишечного содер- |
ный, необиль- |
ляются |
|
диарея |
жимого |
ный |
|
Острые расстройства пищеварения у детей раннего возраста.
Расстройства пищеварения (мальдигистия) – синдром, характеризующейся нарушением пищеварения вследствие дефицита пищеварительных ферментов в желудке, 12 п.к., тонком кишечнике. Клиническая картина синдрома мальдигистии зависит от уровня поражения пищеварительного тракта.
Табл. 1.62. Основные причины расстройств пищеварения у де-
тей
Синдром недостаточности пищеварения
Желудочное |
12 п.к. |
Тонкий кишечник |
Дискинезия желуд- |
Панкреатиты |
Уремия |
ка |
Заболевания печени |
Тиреотоксикоз |
Острый гастрит |
и системы желче- |
Глистные инвазии |
Гастрит при ин- |
выделения |
Энтериты |
фекционных забо- |
Недостаточность |
Нарушение желчеобра- |
леваниях |
желудочного пище- |
зования |
|
варения |
Нарушения желудочного |
|
|
и панкреатического пи- |
|
|
щеварения |
Клиника. Наиболее частыми проявлениями синдрома мальдиги-
240
стии являются: тошнота, рвота, метеоризм, диарея, отрыжка воздухом или пищей, снижение аппетита.
Табл.1.63. Клинические особенности диарей (Струтынский А.В.,
1997)
Вид |
Клинические особенности |
Энтеральные (вос- |
Умеренное учащение стула (до 4-6 раз в сутки), |
паление слизистой |
очень обильные испражнения, в которых содер- |
оболочки тонкой |
жатся остатки непереваренной пищи. Характер- |
кишки) |
на стеаторея («жирный кал»). Диарея нередко |
|
сопровождается болями вокруг пупка |
Колитические (ча- |
Очень частый стул (10-15 раз в сутки), сопрово- |
ще при поражении |
ждающийся тенезмами (болезненными позыва- |
слизистой оболоч- |
ми к дефекации). Испражнения скудные, часто с |
ки дистальных от- |
примесью слизи и крови |
делов кишки) |
|
Желудочные (при |
Умеренное учащение стула (до 4-6 раз в сутки), |
снижении секре- |
испражнения жидкие, темного цвета, с остатка- |
торной функции |
ми непереваренной пищи, нередко с неприят- |
желудка, сопрово- |
ным гнилостным запахом (нарушение перевари- |
ждающихся нару- |
вания белков), со слизью. Диарея часто сопро- |
шениями перевари- |
вождается чувством переполнения и тупыми |
вания белков и бы- |
распирающими болями дистензионного харак- |
стрым опорожне- |
тера в эпигастральной области |
нием желудка) |
|
Панкреатические |
Умеренное учащение стула. Испражнения |
(при снижении |
обильные (полифекалия), кашицеобразные или |
внешнесекреторной |
жидкие, со слизью. Характерны стеаторея и не- |
функции поджелу- |
приятный гнилостный запах. Диарея сопровож- |
дочной железы) |
дается болями в верхней половине живота, ино- |
|
гда опоясывающего характера, метеоризмом, |
|
часто значительным похуданием |
К основным проявлениям острых неинфекционных диарей у детей раннего возраста относят: простую диспепсию, непереносимость белка коровьего молока, функциональную диарею малышей, вторичную лактазную недостаточность.
241
ДИСПЕПСИЯ ПРОСТАЯ заболевание, развивающееся преимущественно у детей первого года жизни. Данный диагноз в настоящее время практикующими педиатрами используется редко.
Этиология: погрешности в питании ребенка (обильное частое кормление, перекорм, недокорм, пища, не соответствующая возрасту, быстрый переход на искусственное вскармливание, перегрузка жиром, углеводами или белком), нарушение режима, ухода (перегревание, отнятие от груди в жаркое время года). Диспепсия чаще наблюдается у ослабленных детей, страдающих экссудативным диатезом, рахитом, гипотрофией. В основе заболевания - снижение ферментативной деятельности желудочно-кишечного тракта, усиление бродильных процессов с образованием большого количества газов, снижение всасывательной функции кишечника.
Клиника. Начало чаще острое; появляется срыгивание, иногда рвота, снижается аппетит. Стул 8-10 раз в сутки, жидкий, с кислым запахом, желто-зеленого цвета с небольшим количеством слизи, в каловых массах белые комочки омыленных жиров (похожие на частички рубленого белка куриных яиц). Выражен метеоризм, поэтому ребенок периодически бывает беспокоен, плачет, после отхождения газов быстро успокаивается. Общее состояние страдает мало, температура нормальная. Интенсивность прибавки веса несколько замедляется.
Лечение. Необходимо выяснить причину, вызвавшую диспепсию, и устранить причины, приведшие к развитию заболевания. В первые день лечения диспепсии можно пропустить одно или два кормления, и обеспечить ребенку обильное питье (см. «оральная регидратация»). В последующие дни количество пищи постепенно доводят до возрастной нормы (под контролем стула).
При длительном употреблении продуктов с повышенным содержанием белка развивается гнилостный вариант диспепсии. В этом случае необходимо ограничить: мясо, рыбу, сыр, творог, бобовые, орехи, яйца, крупы (манную, овсяную, гречневую). Гнилостные процессы подавляют: черника, яблоки, черная смородина, редька, гранат и др.
При избыточном размножении дрожжеподобных грибков из пита-
ния исключают: виноград, свежий хлеб, кефир, сыр.
При бродильной диспепсии не рекомендуют: цельное молоко, кисломолочные продукты, белые каши, картофельное пюре, кисели, бананы, виноград, огурцы.
Медикаментозная терапия должна проводиться под контролем результатов копрограммы. Для лечения часто используют панкреатические ферменты (Креон, мезим форте и др.), пробиотики (линекс, хилак форте, пробиформ и др.) При метеоризме, болях в животе показаны
242
тепло на живот, согревающий компресс, Эспумизан, укропная вода, газоотводная трубка.
Прогноз. При правильном, своевременном лечении течение и исход заболевания благоприятный.
ТОКСИКОЗ С ЭКСИКОЗОМ
Наиболее частыми причинами развития токсикоза с эксикозом являются острые кишечные инфекции с диареей секреторного типа (ротавирусная инфекция, эшерихиоз, кишечные инфекции, вызванные условно-патогенной флорой и др.).
Патогенез кишечного токсикоза
Входные ворота инфекции – ротовая полость. После попадания возбудителя в дистальные отделы толстого кишечника, происходит их размножение и гибель. Микроорганизмы выделяют токсические продукты, которые вызывают морфологические изменения в кишечнике, а при попадании в кровь развитие инфекционного токсикоза.
Ведущим моментом в развитии кишечного токсикоза является потеря жидкости и электролитов с жидким стулом и рвотой из-за увеличенной проницаемости кишечного барьера. Усилению потерь жидкости способствует лихорадка, одышка, рвота. Потери жидкости приводят к уменьшению объема плазмы, внеклеточной сосудистой жидкости, нарушению реологии крови, гиповолемическому шоку.
Важным элементом патогенеза кишечного токсикоза является поражение нервной системы (воздействие токсинов на сосуды мозга), в результате которого формируется симпатикотония. Дисфункция вегетативной нервной системы, непосредственное воздействие токсинов на мышцу сердца приводят к поражению сердечно-сосудистой системы (снижение сократительной способности миокарда, тонуса сосудов, кратковременное повышение АД, развитие коллаптоидных состояний при тяжелом течении заболевания).
Гиперсимпатикотония способствует усилению функции коры надпочечников с последующим развитием централизации и децентрализации кровообращения. В результате распада тромбоцитов выделяется серотонин, что приводит к развитию местного спазма сосудов и усилению циркуляторных расстройств.
Измененный эндотелий сосудов активирует тканевой тромбопластин, что приводит к активации свертывающей системы крови и развитию ДВС-синдрома.
Наряду с токсемией в патогенезе имеют значение местные воспалительные изменения в кишечнике. Воспалительный процесс сопровождается активацией специфической и неспецифической иммуноло-
243
гической реактивности. В некоторых случаях формируется вторичная иммунная недостаточность.
При удовлетворительном состоянии иммунитета заболевание заканчивается выздоровлением.
Исследования. Посев кала, в том числе и на специальные среды, серологическое обследование, копрограмма с обязательным определением рН кала, нагрузочные пробы с лактозой и сахарозой, глюкозой и галактозой, тест с D-ксилозой, биопсия слизистой тонкого кишечника, УЗИ печени и поджелудочной железы, колоноскопия, исследование кала на лямблии, яйца глистов.
Анамнез, клиника. Клинические проявления каждого из заболеваний, сопровождающегося диареей достаточно специфичны. Общими для всех заболеваний с диареями являются: изменения характера стула, развитие обезвоживания, поражение отдельных органов и систем, в том числе и функциональная недостаточность кишечника. Синдром острой кишечной недостаточности проявляется появлением метеоризма, уменьшением частоты стула (или его задержкой), усилением рвоты, нарастанием токсикоза, появлением признаков пареза кишечника.
Табл. 1.64. Степени кишечного токсикоза
При- |
I степень |
II степень |
III степень |
знаки |
токсикоза |
токсикоза |
токсикоза |
ЦНС |
Ирритативно- |
Кома I-II степе- |
Кома II-III сте- |
|
сопорозное нару- |
ни, судороги |
пени |
|
шение сознания |
|
|
Кожа |
Бледнопепельно- |
Бледная, цианоз |
Сероцианотич- |
|
цианотичная окра- |
слизистых |
ная, мрамор- |
|
ска губ и ногтевых |
|
ность, симптом |
|
лож |
|
белого пятна |
Тем- |
39,0-39,5оС, соот- |
До 40 оС, умень- |
Неуправляемая |
пера- |
ношение между |
шение разницы |
гипертермия |
тура |
кожной и ректаль- |
между кожной и |
или гипотермия |
|
ной температурой в |
ректальной темпе- |
|
|
ратурой |
|
|
|
норме |
|
|
|
|
|
|
Пульс |
Умеренная тахи- |
Выраженная |
Относительная |
|
кардия |
тахикардия |
брадикардия |
АД |
Повышение систо- |
Повышение диа- |
Снижение АД |
|
лического АД |
столического АД |
|
ЧДД |
Тахипноэ |
Тахипноэ |
Тахипноэ или |
244

|
|
|
брадипноэ |
Живот |
Парез кишечника |
Парез кишечни- |
Парез кишечни- |
|
|
ка |
ка |
Разме- |
В пределах нормы |
Увеличены в |
Значительно |
ры |
или незначительное |
размерах |
увеличены в |
печени |
увеличение |
|
размерах |
и селе- |
|
||
зенки |
|
|
|
Диу- |
Олигурия |
Олигоанурия |
Анурия, ГУС |
рез |
|
|
|
КОС |
Латентный ацидоз |
Смешанный |
Декомпенсиро- |
|
|
ацидоз |
ванный сме- |
|
|
|
шанный ацидоз |
ДВС- |
Гиперкоагуляция |
Появление кож- |
Гипокоагуляция, |
син- |
|
ного геморраги- |
паренхиматоз- |
дром |
|
ческого синдро- |
ные кровотече- |
|
|
ма |
ния |
Эксикоз (обезвоживание) развивается у детей при быстрой потере массы тела в результате поносов, рвоты, недостаточного поступления в организм жидкости, пареза кишечника и т.д. Эксикоз приводит к потере электролитов. В результате уменьшается объем плазмы, внеклеточной сосудистой жидкости, нарушается реология крови, что приводит к недостаточности кровообращения по типу ангидремического гиповолемического шока. Клиническая картина эксикоза определяется величиной потери массы тела. Выделяют 3 степени дегидратации
(табл. 1.62.)
Степени тяжести эксикоза
Эксикоз I степени: потеря жидкости 50 мл/кг (или 5% от массы тела). Нарушения периферической микроциркуляции отсутствуют.
Эксикоз II степени: потеря жидкости 60-90 мл/кг (6-9% массы тела). Развивается субкомпенсированные нарушения микроциркуляции.
Эксикоз III степени: потеря жидкости составляет 100-150 мл/кг (потеря массы тела 10% и выше). Появляются признаки нарушения центральной гемодинамики.
Табл. 1.65. Характеристика эксикоза у детей
Признак |
I степень |
II степень |
III степень |
Стул |
До 5 раз в су- |
До 10 раз в сутки |
Свыше 10 раз в |
|
тки |
|
сутки |
245
Рвота |
1-2 раза |
Повторная |
Многократная |
Общее |
Среднетяжелое |
Тяжелое |
Очень тяжелое |
состояние |
|
|
|
Жажда |
Умеренная |
Резко выраженная |
Может отсутст- |
|
|
|
вовать |
Эластич- |
Сохранена |
снижена |
Резко снижена |
ность |
|
|
|
тканей |
|
|
|
Слизи- |
Влажные |
Суховатые, слегка |
Сухие |
стые |
|
гиперемирован- |
|
оболочки |
|
ные |
|
Большой |
Норма |
Слегка запавший |
Втянут |
родничок |
|
|
|
Глазные |
Норма |
Мягкие |
Запавшие |
яблоки |
|
|
|
Тоны |
Ясные |
Слегка приглуше- |
Резко приглу- |
сердца |
|
ны |
шены |
АД |
Норма, слегка |
Систолическое |
Снижено |
|
повышено |
норма, диастоли- |
|
|
|
ческое повышено |
|
Тахикар- |
Отсутствует |
Умеренная |
Выраженная |
дия |
|
|
|
Цианоз |
Отсутствует |
Умеренный |
Резко выражен- |
|
|
|
ный |
Сознание, |
Не нарушены |
Возбуждение, или |
Отсутствует |
реакции на |
|
вялость |
|
окружаю- |
|
|
|
щее |
|
|
|
Реакция |
Выражена |
Ослаблена |
Отсутствует |
на боль |
|
|
|
Голос |
Норма |
Ослаблен |
Часто афония |
Диурез |
Сохранен |
Снижен |
Резко снижен |
Дыхание |
Норма |
Умеренное тахипноэ |
«Токсическое» |
Темпера- |
Нормальная или |
Часто повышен- |
Часто ниже нор- |
тура тела |
повышенная |
ная |
мы |
ДВС- |
Отсутствует |
1-я фаза |
2-3-я фазы |
синдром |
|
|
|
рН |
Норма |
7,3 и ниже |
Резко снижен |
ВЕ |
Норма |
Ниже 10 |
Ниже 20 |
246
Существует несколько вариантов потерь жидкости и электролитов при обезвоживании: соледефицитный (гипотонический, внутриклеточный); вододефицитный (гипертонический, тотальная дегидратация); соразмерная потеря воды и солей (изотонический, (внеклеточный)).
Табл.1. 66. Виды дегидратации
Признак |
|
Вариант дегидратации |
|
||
Соледефицитный |
|
Вододефицитный |
|
Соразмерная |
|
|
(гипотонический, |
|
(гипертонический, |
|
потеря воды и |
|
внутриклеточный) |
|
тотальная дегид- |
|
солей (изотониче- |
|
|
|
ратация) |
|
ский, (внеклеточ- |
|
|
|
|
|
ный) |
Особенно- |
Потеря солей, |
|
Потери воды |
|
Соразмерные |
сти обез- |
приток |
|
|
|
потери вода + |
воживания |
воды в клетку |
|
|
|
соли |
Причины |
Поносы, рвоты, |
|
Поносы, рвота, |
|
Поносы, рвота, |
|
ХПН |
|
одышка, усилен- |
|
ятрогения |
|
|
|
ное потоотделе- |
|
|
|
|
|
ние, избыточное |
|
|
|
|
|
введение солей, |
|
|
|
|
|
сахарный диабет |
|
|
Жажда |
отсутствует |
|
выражена |
|
выражена |
Беспокой- |
Не характерно |
|
характерно |
|
выражено |
ство |
|
|
|
|
|
Сухость |
характерно |
|
характерно |
|
выражено |
слизистых |
|
|
|
|
|
Повыше- |
характерно |
|
характерно |
|
Зависит от |
ние темпе- |
|
|
|
|
этиологии |
ратуры |
|
|
|
|
заболевания |
Сухожиль- |
снижены |
|
повышены |
|
Не изменены |
ные реф- |
|
|
|
|
|
лексы |
|
|
|
|
|
Мышечный |
|
|
Снижен |
|
Снижен |
тонус |
|
|
|
|
|
Вялость |
выражена |
|
Не характерна |
|
Не характерна |
Нарушение |
+++ |
|
+ |
|
++ |
сознания |
|
|
|
|
|
Уровень |
снижен |
|
повышен |
|
нормальный |
натрия |
|
|
|
|
|
Общий |
Норма |
|
повышен |
|
Умеренно по- |
247
белок |
|
|
вышен |
Гематокрит |
Повышен на 10- |
повышен |
повышен |
|
12% |
|
|
Гемогло- |
повышен |
повышен |
повышен |
бин |
|
|
|
Диурез |
Олигоанурия |
Снижен |
Повышен или |
|
|
|
снижен |
Диагноз. Необходимо установить причину диареи (кишечные инфекции, неинфекционные причины и др.). При отрицательных результатах посевов кала бактериальная этиология диарей доказывается обнаружением в копрограмме повышенного количества лейкоцитов; результатами серологических исследований.
Выявить нарушения водно-электролитного баланса можно на ос-
новании:
а) дефицита массы тела, развившегося за последние дни; б) выявления клинических проявлений эксикоза;
в) определения гемоконцентрационной триады в плазме крови: гемоглобин, гематокрит, общий белок;
г) измерения почасового, суточного диуреза, относительной плотности мочи;
д) выявления дефицита (избытка) электролитов в крови; е) исследования осмолярности (осмолярность определяется или
прямым методом (измерение температуры замерзающей жидкости)
или по формуле: Сосм = 1,86АNa + Ck + Сглюкозы + С мочевины, где С –
концентрация веществ (натрий, калий, глюкоза, мочевина). Или Сосм =
(СNa + 5) × 2.).
Лабораторные исследования Определение уровней натрия и калия позволяет уточнить вид де-
гидратации.
Уровень гематокрита указывает на степень обезвоживания. ЦВД является суммарным показателем гемодинамики и эффективности работы сердца.
Уровень креатинина свидетельствует о функциональном состоянии почек.
Показатели протеинограммы с одной стороны позволяют говорить о степени дегидратации, а с другой – о нарушениях белкового обмена.
248
Дифференциальный диагноз основных причин острых диарей представлен в табл. 1.67.
Табл. 1.67. Основные причины острых диарей
Понос +
+ боли в правой подвздошной области, |
|
положительные симптомы раздражения |
Аппендицит |
брюшины, рвота, ослабление перисталь- |
|
тики, ↑tо |
|
+ связь с употреблением в пищу молока, |
Аллергия к белку ко- |
рвота, обезвоживание, плохой аппетит, |
ровьего молока |
эозинофилия |
|
+ рвота, обезвоживание, ↑tо, токсикоз, |
Бактериальные диареи |
судороги, нарушение сознания, иногда |
|
кровь в стуле, гной |
|
+ водянистый стул со слизью без приме- |
Вирусные диареи |
си крови,↑tо |
|
+ рвота, увеличение печени, темная моча, |
Вирусный гепатит |
желтуха |
|
+ клиника заболевания, вызвавшего дис- |
Дисбактериоз ки- |
бактериоз, характерные результаты мик- |
шечника |
робиологического исследования кала и |
|
копрограммы |
|
+ боли в животе, ↑tо, дизурия, интоксика- |
Инфекция мочевых пу- |
ция, лейкоцитурия |
тей |
+ боль в животе, рвота, водянистый стул, |
Лактазная недостаточ- |
вздутие живота, гипотрофия, рН кала |
ность |
менее 5,5 |
|
+ хронический ремитирующий энтерит |
Лямблиоз кишечника |
+ стеаторея, рецидивирующий понос, |
Муковисцидоз |
гипотрофия, частые бронхолегочные за- |
|
болевания |
|
+ сильная боль в животе опоясывающего |
|
характера, рвота, лихорадка, положи- |
Острый панкреатит |
тельные симптомы Кача, Мейо-Робсона и |
|
др., связь с травмой, инфекцией |
|
+ анамнез! Рвота, боль в животе, озноб и |
Пищевая токсико- |
лихорадка, водянистый стул, нарушение |
инфекция |
сознания, коллапс |
|
+ плохой аппетит, рвота, увеличение жи- |
|
249
вота в размерах, полифекалия, стеаторея |
Целиакия |
|
|
||||
(возраст – старше 6 мес.) |
|
|
|
|
|||
|
|
Понос у новорожденных детей |
|
|
|||
+ нарушение диеты (!), срыгивание, взду- |
Алиментарные диспеп- |
|
|||||
тие живота, беспокойство, отсутствие |
сии |
|
|
||||
интоксикации |
|
|
|
|
|
|
|
+ упорная рвота, большое количество в |
Врожденная лактазная |
|
|||||
кале воды, отсутствие патологических |
недостаточность |
|
|||||
примесей, рН кала менее 5,5, лактозурия, |
|
|
|
||||
гипотрофия |
|
|
|
|
|
|
|
+ клиника основного заболевания (ОКИ), |
Вторичная лактазная |
|
|||||
вздутие живота, беспокойство, кислый |
недостаточность |
|
|||||
запах кала, отсутствие в копрограмме |
|
|
|
||||
воспалительных изменений |
|
|
|
|
|||
+ меконеальный илеус в анамнезе, рвота, |
Муковисцидоз |
|
|||||
дегидратация, стеаторея, легочные про- |
|
|
|
||||
явления |
|
|
|
|
|
|
|
+ в анамнезе асфиксия, сепсис, кровь в |
|
|
|
||||
стуле, вздутие и напряжение живота, |
|
Некротизирующий энте- |
|
||||
тромбоцитопения, ацидоз, перфорация |
роколит |
|
|
||||
кишок, шок, выявление при рент- |
|
|
|
|
|||
генологическом исследовании пневмото- |
|
|
|
||||
за, уровней жидкости и др. |
|
|
|
|
|||
Табл.1. 68. Дифференциальная диагностика эксикоза |
|
||||||
|
|
|
|
|
|
|
|
Заболе- |
|
Признаки, позво- |
|
Необходимые |
Необходимые |
|
|
вание |
|
ляющие заподоз- |
|
минимальные |
результаты |
|
|
|
|
рить заболевание |
|
исследования |
|
|
|
Адрено- |
|
Рвота с первых не- |
|
Определение в |
Гипонатрие- |
|
|
гени- |
|
дель жизни, гипо- |
|
крови натрия, |
мия, гипо- |
|
|
тальный |
|
трофия, понос, ги- |
|
хлора, калия, |
хлоремия, ги- |
|
|
синдром |
|
пертрофия клитора |
|
17-ОКС, глю- |
перкалиемия, |
|
|
|
|
|
|
козы, ЭКГ, |
повышение 17- |
|
|
|
|
|
|
эндокринолог |
ОКС в крови |
|
|
Гипо- |
|
Постепенная потеря |
|
Оценка показа- |
Дефицит мас- |
|
|
трофия |
|
массы, а затем за- |
|
телей физиче- |
сы тела более |
|
|
|
|
держка роста, сни- |
|
ского развития. |
10%, трофиче- |
|
|
|
|
жение тургора, на- |
|
Определение в |
ские наруше- |
|
|
|
|
личие причины (на- |
|
крови глюко- |
ния кожи и |
|
|
250
|
рушение питания, |
зы, протеино- |
волос, анемия, |
|
|
пороки развития, |
граммы, ко- |
стеаторея, дис- |
|
|
инфекции и др.) |
программы; |
протеинемия |
|
|
|
анализ крови |
|
|
Острая |
Лихорадка, рвота, |
Анализ крови |
Гипонатриемия, |
|
надпочеч- |
снижение АД, на- |
и мочи, глюко- |
гиперкалиемия, |
|
никовая не- |
рушение дыхания, |
за крови, ка- |
гипогликемия, |
|
достаточ- |
олигурия, понос, |
лий, натрий |
резкий лейкоци- |
|
тоз со сдвигом |
||||
ность |
гипотония, сниже- |
|
||
|
влево, снижение |
|||
|
ние массы тела, ко- |
|
||
|
|
в крови уровня |
||
|
ма |
|
||
|
|
кортизола и 17- |
||
|
|
|
ОКС, повы- |
|
|
|
|
шение уровня |
|
|
|
|
АКТГ в крови |
Лечение, задачи лечения: восстановление исходной массы тела (ликвидация эксикоза), коррекция гомеостаза, этиопатогенетическая терапия основного заболевания.
Схема лечения: Обязательное лечение: регидратационная терапия, диетотерапия, восстановление электролитного баланса, коррекция КОС.
Вспомогательное лечение: нормализация белкового обмена, восстановление биоценоза кишечника.
Показания для госпитализации: наличие кишечного токсикоза, эксикоз II-III степени, невозможность проведения лечения в амбулаторных условиях, необходимость проведения углубленного обследования.
Диета назначается с учетом возраста, степени тяжести состояния, особенностей заболевания.
Оральная регидратация
При Э I степени: регидратационную терапию назначают всем больным при выявлении признаков Э. Оральная регидратация проводится в два этапа.
Первичная регидратация - направлена на возмещение дефицита воды и солей, имеющегося на момент начала лечения. Для проведения оральной регидратации используют регидрон, глюкосолан, гастролит и др.
При легкой степени Э назначают внутрь ребенку растворы по 40-50 мл/кг в течение 4-х часов. При Э II степени: оральную регидратацию проводят в объеме 60-90 мл/кг в течение 6 ч.
При Э III степени регидратацию начинают с парентерального введения растворов и продолжают перорально. Общий объем жидкости
251
для регидратации при тяжелом обезвоживании составляет 100-120 мл/кг за 8 часов.
Выбранные растворы дают через короткие промежутки времени малыми порциями. Грудным детям - по 2-3 чайные ложки (или 10-15 мл из рожка), а более старшим детям - 1-2 столовых ложки через каждые 3-5 мин. Первичная оральная регидратация проводится без учета типа дегидратации. Если регидратация еще не наступила, а у ребенка появилась отечность век, следует прекратить введение растворов и поить ребенка кипяченой водой, слабым чаем или рисовым отваром. Когда отек век исчезнет, вновь продолжают прием глюкозо-солевого раствора.
Показателем эффективности первичной регидратации служит исчезновение признаков обезвоживания.
Поддерживающая регидратация направлена на возмещение про-
должающейся потери воды и солей, обусловленной поносом и рвотой. Одновременно с первичной регидратацией проводят компенсацию текущих потерь жидкости из расчета детям в возрасте до 2 лет по 50100 мл, а детям старше 2 лет по 100-200 мл глюкозо-солевого раствора после каждой дефекации или через 20-30 мин после рвоты.
Инфузионная терапия показана в следующих случаях: наличие токсикоза с эксикозом II-III степени, неукротимая рвота, неэффективность оральной регидратации, кома, судороги, признаки гиповолемического шока.
Задачи инфузионной терапии:
1.обеспечение нормального объема водных пространств и секре-
тов;
2.восстановление и поддержание водно-электролитного баланса;
3.восстановление нормальных свойств крови (текучесть, свертываемость, оксигенация);
4.детоксикация, в том числе форсированный диурез;
5.длительное и равномерное введение лекарств;
6.осуществление парентерального питания;
7.нормализация иммунитета.
Варианты венозного доступа:
а) пункция вены; б) венесекция (необходимость непрерывного введения препаратов
в течение 3-7 суток; в) катетеризация крупных вен (бедренная яремная, подключичная);
- необходимость длительного введения препаратов (в течение 1-4 недель).
252
Методы внутривенного введения: прерывистое (струйное), непре-
рывное (капельное) введение растворов с помощью: а) одноразовых капельниц, б) перистальтических и шприцевых насосов.
Препараты для инфузионного введения включают:
Объемозамещающие препараты: а) искусственные плазмозаме-
нители (растворы глюкозы, растворы крахмала, гемодез, реополиглюкин и др.).
б) естественные плазмозаменители: нативная плазма, свежезамо-
роженная плазма, сухая плазма, 5,10, 20% растворы альбумина, криопреципитат, протеин, эритроцитарная масса, взвесь отмытых эритроцитов, тромбомасса, лейкомасса.
Показания для использования препаратов этой группы: возмещение объема циркулирующей крови, возмещение объема циркулирующей плазмы, возмещение объема эритроцитов или других компонентов плазмы, сорбция токсинов, обеспечение реологической функции крови, для получения осмодиуретического эффекта.
Важная особенность действия препаратов этой группы: чем больше их молекулярная масса, тем дольше они циркулируют в сосудистом русле.
Гидрокиэтилкрахмал выпускается в виде 6 или 10% раствора (инфукол, стабизол) имеет довольно высокую молекулярную массу (200-400 кД) и способен циркулировать в сосудистом русле до 8 суток. Основное показание для применения – терапия шока.
Полиглюкин (декстран 60) имеет молекулярную массу 60000 Д. Способен циркулировать в сосудистом русле до 7 суток. Основное показания для применения – лечение шока.
Реополиглюкин (декстран 40) имеет молекулярную массу 40000 Д. Способен циркулировать в сосудистом русле до 1 суток. Применяется для терапии шока. Один из лучших реопротекторов.
Гемодез (6% раствор поливинилового спирта) имеет молекуляр-
ную массу 8000-12000 Д. Время действия – 12 часов. Механизм действия – сорбент, обладает умеренными дезинтоксикационными свойствами, и осмодиуретическим эффектом.
Альбумин – почти идеальное объемозамещающее средство, особенно при шоке. Самый мощный естественный сорбент для гидрофобных токсинов.
Плазма, кровь и ее компоненты – используются при наличии де-
фицита соответствующего компонента в крови.
Кристаллоиды: а) препараты глюкозы 5 и 10% растворы. Имеют осмолярность 278 и 555 мосм/л. Осмолярность этих растворов обеспе-
чивается сахаром, который быстро метаболизируется, что приводит к
253
снижению осмолярности введенного раствора, и как следствие, к угрозе развития гипоосмолярного синдрома.
Физиологический раствор (0,85% раствор хлорида натрия содержит много хлора, по сути, не является физиологическим). Кислый, изоосмолярный.
б) комбинированные кристаллоиды: растворы Рингера, Рингера-
Локка, Хартмана, лактосоль, ацесоль, дисоль, трисоль (содержат ионы натрия, кальция, хлора, лактата) наиболее близки по составу к жидкой части плазмы и адаптированы к лечению детей. Осмолярность 261-329 мосм/л. Изоосмолярные.
При составлении программы инфузионной терапии рекомендо-
вана следующая последовательность действий:
1.Установить диагноз, наличие и степень эксикоза, его вариант, состояние сердечно-сосудистой, мочевыделительной, центральной нервной систем, особенности электролитного обмена.
2.С учетом диагноза определить:
а) цели и задачи инфузионной терапии (дезинтоксикация, регидратация, лечение шока, поддержание водного баланса, восстановление микроциркуляции, диуреза, введение лекарств).
б) методы (струйно, капельно).
в) доступ к сосудистому руслу (пункция, катетеризация, постановка линии).
г) средства инфузионной терапии (капельница, шприцевой насос).
3.Провести расчет жидкости на определенный отрезок времени: 6ч, 12ч, 24 ч.
3.1.Определить собственно объемы инфузионной терапии.
4.Установить избыток или дефицит электролитов.
5.Соотнести расчетную потребность в воде и электролитах с их количеством в инфузионных растворах.
6.Выбрать стартовый раствор для инфузионной терапии.
7.Определить необходимость введения препаратов специального назначения (эритроцитарная масса, плазма, альбумин, плазмозаменители и т. д.).
8.Расчет текущих патологических потерь:
а) точное измерение текущих патологических потерь (взвешивание пеленок, сбор мочи и кала, рвотных масс).
б) ориентировочный расчет текущих (прогнозируемых) патологических потерь по существующим нормативам (см. табл. 1.70).
254
9 . Расчет жидкости возмещения обезвоживания. Внимание! Для проведения инфузионной терапии учитывается только дефицит массы тела, который развился за последние 1-2 дня.
Эксикоз I степени: потеря жидкости 50 мл/кг.
Эксикоз II степени: потеря жидкости 60-90 мл/кг.
Эксикоз III степени: потеря жидкости составляет 100-150 мл/кг. Расчет у детей с нормо- и гипотрофией ведется на фактическую массу тела. При гипертрофии (ожирение) общее количество жидкости у детей на 15-20% меньше, чем у худых детей и одинаковая потеря массы тела у них соответствуют более высокой степени дегидратации.
Общие правила составления программы инфузионной терапии
1.Коллоидные растворы содержат соли натрия и относятся к солевым растворам и их объем должен учитываться в общем объеме солевых растворов.
2.В сумме коллоидные растворы не должны превышать 1/3 общего суточного объема жидкости для инфузионной терапии.
3.У детей младшего возраста соотношение растворов глюкозы и солей составляет 2:1 или 1:1; в старшем возрасте количество солевых растворов увеличивается (1:1 или 1:2).
3.1.Вид дегидратации оказывает влияние на соотношение глюкозосолевых растворов в составе инфузионных сред.
4.Все растворы необходимо разделить на порции («капельницы»), объем которых для глюкозы обычно не превышает 10-15 мл/кг и 7-10 мл для коллоидных и солевых растворов. В емкость для одного капельного введения не должно помещаться больше ¼ рассчитанного на сутки объема жидкости. Более 3-х капельных введений в сутки провести ребенку нереально.
Принципы инфузионной регидратационной терапии
При инфузионной регидратационной терапии выделяют 4 этапа: 1. противошоковые мероприятия (1-3 часа); 2. Возмещение внеклеточного дефицита жидкости (1-2-3 суток); 3. поддержание водноэлектролитного баланса в условиях продолжающихся патологических потерь (2-4 дня и более); парентеральное питание (полное или частичное) или лечебное энтеральное питание.
Расчет объемов жидкостей для инфузионной терапии.
Для поддержания состояния гомеостаза необходимо обеспечить ба-
ланс между вводимой в организм жидкостью и жидкостью, которую организм выводит в виде мочи, пота, кала, с выдыхаемым воздухом. Количество и характер потерь меняется в зависимости от характера заболевания.
255

Количество жидкости, необходимое для возмещения физиологических потерь организма у детей разного возраста, не одинаковое.
Таб.1. 69. Возрастная потребность в жидкости и электролитах
для детей
Возраст |
Потребность в воде в мл/кг |
1-й день жизни |
50-70 |
2-й день жизни |
70-90 |
3-й день жизни |
80-100 |
4-й день жизни |
100-120 |
5-й день жизни |
130 |
С 6-го дня жизни |
130 |
1-й год жизни |
100-140 |
2-й год жизни |
80-120 |
3 года-5 лет |
80-100 |
6-10 лет |
60-80 |
С 10 лет |
50-70 |
|
Электролиты ммоль/кг/сут |
Натрий |
3-5 |
Калий |
1-3 |
Кальций |
0,1-1 (3 ммоль для недоношенного набирающе- |
|
го массу) |
Магний |
0,1-0,7 |
Хлорид |
3-5 |
Фосфат |
0,5-1 (0,25 для недоношенного, набирающего |
|
массу) |
Физиологическая потребность в натрии у детей раннего возраста составляет 3-5 ммоль/кг; у детей старшего возраст 2-3 ммоль/кг;
Потребность в калии равна 1-3 ммоль/кг; Потребность в магнии составляет, в среднем 0,1 ммоль/кг.
Потребность в жидкости и электролитах, необходимых для возмещения физиологических потерь, может быть рассчитана несколькими методами.
Суточную жидкость поддержания (потребность в жидкости) можно рассчитать несколькими способами: 1) на основе учета площади поверхности тела (существует корреляция между этими показателями); 2) энергетическим методом (существует зависимость между энергетическими потребностями и массой тела). Минимальная потребность в
256
воде составляет 100-150 мл/100 ккал; 3) по номограмме Абердина (или таблицам, сделанным на ее основе – табл. 1.69).
При некоторых патологических состояниях потери воды и/или электролитов могут значительно увеличиваться или уменьшаться.
Табл. 1.70. Текущие патологические потери. Состояния, изме-
няющие потребность в жидкости
Состояние |
Потребность в жидкости |
Лихорадка |
Увеличение на 10 мл/кг на каждый градус |
|
повышения температуры |
Гипотермия |
Снижение на 10 мл/кг на каждый градус сни- |
|
жения температуры |
Рвота неукротимая |
Увеличение потребности на 20-30 мл/кг/сут |
Понос |
Увеличиваются на 25-50 мл/кг/сутки |
Сердечная недоста- |
Уменьшение потребности на 25-50% в зави- |
точность |
симости от степени недостаточности |
Отек легких |
Уменьшение потребности до 20-30 мл/кг/сут |
Усиленное потоот- |
Увеличение потребности на 10-25 мл/100 |
деление |
ккал |
Гипервентиляция |
Увеличение потребности до 50-60 мл/100 |
|
ккал |
Повышение влаж- |
Уменьшение потребности на 0-15 мл/100 |
ности воздуха |
ккал |
Почечная недоста- |
Уменьшение потребности до 15-30 |
точность |
мл/кг/сутки |
Парез кишечника |
Увеличение потребности на 25-50 |
|
мл/кг/сутки |
Фототерапия |
Увеличение потребности на 15-30% |
Высокая темпера- |
Увеличение потребности на 50-100% |
тура среды |
|
Повышение мета- |
Увеличение потребности на 25-75% |
болизма |
|
ИВЛ новорожден- |
Уменьшение потребности на 20-30 мл/кг от |
ных (при хорошем |
суточной потребности |
увлажнении) |
|
Для покрытия потребности в жидкости необходимо учесть физиологическую потребность в жидкости (1500-1800 мл/м2) или рассчитанную по таблицам (табл. 1.69), или энергетическим методом и добавить к ним потери жидкости, выявленные у больного.
257

Общие принципы расчета необходимой жидкости:
СЖ = СЖП+ ЖВО+ЖВТПП, где СЖ – рассчитываемая суточная жидкость, СЖП – суточная жидкость поддержания, ЖВО – жидкость возмещения обезвоживания, ЖВТПП - жидкость возмещения текущих патологических потерь.
Противошоковые мероприятия
При шоке показатели центральной гемодинамики необходимо восстановить за 2-4 часа путем введения жидкости в объеме 3-5% от массы тела. Средняя скорость введения растворов не должна превышать 15-20 мл/кг/час.
При децентрализации кровообращения инфузию начинают с введения бикарбоната натрия. Затем вводят 5% раствор альбумина или плазмозамещающие растворы (реополиглюкин, гидроксиэтилкрахмал), а затем или параллельно солевые растворы. Применение растворов глюкозы на данном этапе возможно только после восстановления показателей центральной гемодинамики.
Возмещение внеклеточного дефицита жидкости
Суточная жидкость = суточная жидкость поддержания (СЖП) + ЖВО (жидкость возмещения обезвоживания) + ЖВТПП (жидкость возмещения текущих патологических потерь.
ЖВО + ЖВТПП – это суммарные патологические потери. Рассчитанный объем патологических потерь следует вводить на протяжении 2-3 дней. Следовательно, на первые сутки лечения необходимо взять ½ или 1/3 от рассчитанного объема патологических потерь. Скорость введения жидкости на данном этапе составляет 4-6 мл/кг/час.
Гипертоническая дегидратация (внутриклеточное обезвожива-
ние). Неотложные противошоковые мероприятия (1 фаза). Лечение начните с введения альбумина4 в дозе 5 мл/кг (или физиологический раствор по 20 мл/кг в течение 20-30 минут). Соду вводить в соответствии с показателями КОС, или при наличии признаков децентрализации кровообращения.
2-я фаза (1-24 часа) - снижение уровня Na+ в плазме: вводить глю- козо-солевые растворы (раствор Рингера с 5% глюкозой, Рингер с лактатом и др.) в количестве СЖП + 1/3-1/2 объема жидкости возмещения патологических потерь. Дефицит воды восполнять медленно! (опасность отека мозга). Соотношение глюкозо-солевых растворов у детей в возрасте до 2-х месяцев - 4-6 : 1; в возрасте 2-11 мес. - 4-5 : 1; в воз - расте старше 1-го года - 2-3 : 1. Калий целесообразно добавить в состав инфузионных сред после стабилизации диуреза.
4 При отсутствии альбумина можно использовать плазму.
258
3-я фаза (2-е-3-е сутки): возмещение потерь воды - глюкозосолевые растворы в соотношении 1 : 1 в количестве СЖП + остаток объема жидкости возмещения патологических потерь.
Изотоническая дегидратация. Лечение такое же, как и при гипо-
тонической дегидратации. Неотложные (противошоковые) мероприя-
тия (1 фаза) начать с введения альбумина по 5 мл/кг (или раствор Рингера с лактатом, 0,9% раствор натрия хлорида с 5% раствором глюкозы). При отсутствии выраженных нарушений микроциркуляции альбумин можно заменить солевым раствором.
2-я фаза (1-24 часа): вводить глюкозо-солевые растворы в количестве СЖП + 1/2-1/3 объема жидкости возмещения обезвоживания.
3-я фаза (2-3е сутки): глюкозо-солевые растворы в количестве СЖП + остаток жидкости возмещения патологических потерь. Соду вводить по показателям КОС. Соотношение глюкозо-солевых растворов для детей до 2-х месяцев - 3-4 : 1; в возрасте 2 -11 мес. - 2-3 : 1; в возрасте старше 1-го года - 1 : 1.
Гипотоническая дегидратация. Неотложные (противошоковые)
мероприятия начинайте с введения альбумина в дозе 5 мл/кг.
2-я фаза (1-36 часов): вводите глюкозо-солевые растворы в количестве СЖП + объем жидкости возмещения патологических потерь. Соотношение глюкозо-солевых растворов у детей до 2-х месяцев - 2-3 : 1; в возрасте 2-11 мес. - 1-2 : 1; у детей старше 1-го года 1 : 2-3. Соду вводят по показателям КОС. При бессимптомных гипотонических дегидратациях половину инфузионных растворов вводите в течение 8 часов, а оставшуюся часть - в последующие 16 часов.
При лечении Э необходимо контролировать: 1) ЧСС, 2) ЧД, 3)
температуру тела, 4) АД, ЦВД, 5) массу тела до начала инфузионной терапии, 6) массу тела после окончания инфузионной терапии, 7) гематокрит (ежедневно), 8) общий анализ мочи, 9) уровень диуреза (должен быть не менее 1-1,5 мл/кг в час).
Критерии адекватности терапии эксикоза: восстановление диуреза, уменьшение гематокрита, исчезновение неврологической симптоматики, нормализация деятельности ССС.
Интоксикация – неспецифическая реакция организма на действие
различных по происхождению токсинов, различающаяся относительным динамическим равновесием и определенной стабильностью во времени. Эта реакция представлена комплексом защитноприспособительных реакций организма, направленных на элиминацию токсина из организма.
259
Дезинтоксикационная терапия, по сути, включает в себя весь комплекс лечебных мероприятий, направленных на борьбу с заболеванием, но прежде всего это выведение из организма токсических субстанций, циркулирующих в крови.
Этот вид интенсивной терапии может проводиться с использованием внутренних ресурсов организма ребенка – интракорпораной детоксикации, удаления содержимого с последующим очищением полости ЖКТ, либо путем очищения крови вне организме – экстракорпоральной детоксикации.
Оральная дезинтоксикация – прием во внутрь кипяченой воды, фруктовых отваров, растворов Оралита, Регидрона в дозе 100 мл/кг в сутки.
Инфузионная внутривенная дезинтоксикация проводится с помо-
щью глюкозо-солевых растворов (чаще в соотношении 2:1 или 1:1). Ее объем зависит от степени интоксикации: при I степени половину объема можно ввести внутривенно капельно за 2-3 часа; при II степени этот объем вместе с жидкостью для возмещения плазмы вводят за 4-6 (до 8 часов), а остальную часть – до конца 1-х суток (медленно), при III степени 70-90% суммарного объема жидкости вводят внутривенно равномерно в течение 1-х суток, далее в зависимости от динамики клинических проявлений интоксикации с обязательным добавлением мочегонных средств.
При тяжелой интоксикации и отсутствии органической ОПН показано применение форсированного диуреза с помощью внутривенной инфузии глюкозо-солевых растворов в объеме 1,0-1,5 физпотребности в сочетании с лазиксом в разовой дозе 1-2 мг/кг, маннитолом (10% раствор в дозе 10 мл/кг) с таким расчетом, чтобы объем введенной жидкости был равен диурезу. Скорость введения жидкости – 8-10 мл/кг/час. Для инфузионного введения используют препараты кратковременного действия – раствор Рингера или другие официнальные смеси электролитов в сочетании или с 5%, или с 10% растворами глюкозы. Для удержания необходимого ОЦК в состав инфузии включают реополиглюкин по 10 мл/кг. В том случае, если не происходит желаемого увеличения диуреза, в лечение добавляют лазикс в дозе 1-3 мг/кг. Метод форсированного диуреза противопоказан при наличии сердечной недостаточности, нарушении функции почек.
Для усиления эффекта дезинтоксикации можно использовать: реоглюман, альбумин; энтеросорбенты: смекта, энтеродез, полисорб, энтеросгель, уголь активированный, Карболонг, Полифепан, Холестирамин Альгисорб, СУМС-1.
260

Показаны также средства, улучшающие функцию гепатоцитов (гепатопротекторы) – эссенциале, урсосан, силибинин, лактулоза, орнитин, моторную функцию желчных путей (холеретики, энтерокинетики, спазмолитики) – но-шпа, галидор, мебеверин, т др.
Табл. 1.71. Общая схема дезинтоксикационной терапии (Учай-
кин В.Ф.с соавт., 2005)
Этап терапии |
Степень интоксикации |
||
|
I |
II |
III |
Этиотропная терапия |
|
|
|
Противовирусная терапия и антибиотики |
- |
± |
+ |
|
|
|
|
Гипериммунные препараты |
- |
± |
+ |
Антидоты (при отравлении) |
± |
± |
± |
Восстановление эффективной гемодина- |
|
|
|
мики: нормализация ОЦК, АД, ЦВД, и |
+ |
+ |
+ |
перфузии тканей; создание гемодилюции |
|
|
|
|
|
|
|
Ликвидация гипоксии: |
|
|
|
аэротерапия |
+ |
|
- |
|
|
|
|
Кислородотерапия |
± |
+ |
+, ИВЛ |
Переливание эритроцитарной массы |
- |
± |
± |
Детоксикация: |
|
|
|
Оральная |
+ |
- |
- |
Инфузия, парентеральная |
± |
+ |
+ |
экстракорпоральная |
- |
- |
+ |
Препараты иммуноглобулинов: Пентаглобин, Иммуноглобулин,
иммуноглобулин нормальный для внутривенного введения, Цитотект, Гепатект.
Вопросы к экзамену. Неинфекционная диарея. Острые расстройства пищеварения у детей раннего возраста. Простая диспепсия. Причины. Клиническая картина. Диагностика. Дифференциальный диагноз. Лечение. Профилактика.
Токсикоз с эксикозом. Этиология. Патогенез. Фазы развития. Виды и степень обезвоживания. Клиническая картина. Диагностика. Осложнения. Исходы. Основные направления терапии. Оральная и парентеральная регидратация. Диетотерапия больных с диареями. Профилактика.
261
Глава IX. Заболевания сердечно-сосудистой системы
ОСТРАЯ РЕВМАТИЧЕСКАЯ ЛИХОРАДКА (ОРЛ) -
постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных β-гемолитическим стрептококком группы А (БГСА), в виде системного воспалительного заболевания соединительной ткани с преимущественной локализацией в сердечно–сосудистой системе (кардит), суставах (мигрирующий полиартрит), мозге (хорея) и коже (кольцевидная эритема, ревматические узелки), развивающееся у предрасположенных лиц, главным образом, молодого возраста (7–15 лет), в связи с аутоиммунным ответом организма на антигены стрептококка и перекрестной реактивностью со схожими аутоантигенами поражаемых тканей человека (феномен молекулярной мимикрии).
Эпидемиология. ОРЛ встречается во всех климатогеографических странах мира. По данным ВОЗ (1989) среди детей и подростков в различных странах мира ОРЛ составила 0,3-18,6 на 1000 детского населения.
Распространенность ОРЛ и ревматических пороков сердца в РФ у детей и подростков составляет 0,3-0,8 и 1,3 на 1000 соответственно. Рост первичной заболеваемости в 1989 и в 1994г.г. произошел, преимущественно, в Северо–Кавказском регионе, особенно в республиках Ингушетия и Дагестан.
Этиология, патогенез и патоморфология ОРЛ
ОРЛ развивается после назофарингеальной и скарлатинозной стрептококковой инфекции. Установлено, что ОРЛ развивается в 0,3% случаев после спорадической носоглоточной БГСА инфекции и в 3% случаев – после эпидемической.
Так называемые «ревматические штаммы» А-стрептококка (М-5, М-6, М-18, М-24) обладают высокой контагиозностью. Эти штаммы имеют в составе клеточной стенки специфический белок - М-протеин, который подавляет их фагоцитоз. Кроме того, эти штаммы обладают тропностью к носоглотке и способностью перекрестно реагировать с различными тканями макроорганизма-хозяина (феномен молекулярной мимикрии).
ОРЛ развивается у генетически предрасположенных лиц, имеющих аллоантиген В-лимфоцитов, определяемый моноклональными антителами D8/17, локусы системы HLA (DR5DR7, Cw2Cw3), а также группу крови – А(II) и В (III), фенотип кислой фосфатазы (СС).
262

Для возникновения ОРЛ необходимо длительное персистирование БГСА или его антигенов, обладающих токсическими свойствами (стрептолизины О и S), стрептокиназы, гиалуронидазы, дезоксирибо- нуклеазы-В и др.) в организме. Антигены стрептококка оказывают на сердце прямое или опосредованное (иммунопатологическое) кардиотоксическое действие.
В ответ на А-стрептококковую инфекцию в организме развивается устойчивая гипериммунная реакция с образованием антистрептококковых антител – антистрептолизина – О (АСЛ-О), антистрептогиалуронидазы (АСГ) и др. Антитела и образующиеся иммунные комплексы активируют систему комплемента (особенно С1, С4). Иммунные комплексы в соединении с комплементом (ЦИКи) и антитела разносятся циркуляцией и фиксируются в тканях сердца и сосудах других органов, вызывая их повреждение и высвобождение фармакологически активных веществ, которые играют важную роль в углублении иммунных нарушений. Само по себе иммунное воспаление способствует повреждению тканей. Кроме того, в органах-мишенях развивается сосу- дисто-экссудативная фаза острого воспаления. В фазу неспецифического экссудативного компонента воспаления вырабатывается большое количество иммунорегуляторных цитокинов (ИЛ-2, ИЛ-5, ИЛ-7, ИЛ-10 и др.) которые, связываясь с рецепторами клеток, способствуют клональной пролиферации Т-лимфоцитов и росту числа В- лимфоцитов, в итоге приводя к активации макрофагов и моноцитов.
Активация макрофагов/моноцитов способствует увеличению синтеза провоспалительных цитокинов (ИЛ-1α, ИЛ-1β, ИЛ-6, ИЛ-8,
ФНОα, ФНОβ), обладающих способностью усиливать синтез метаболитов арахидоновой кислоты по липооксигеназному пути и повышать образование лейкотриенов, которые, в свою очередь, приводят к увеличению продукции ИЛ-1 и ФНО. Эти цитокины играют важную роль не только в развитии локального иммунного воспаления при ОРЛ, но и вызывают системные эффекты: повышение температуры тела, нарушение сна, появление генерализованной миалгии, артралгии, головной боли, похудания, синтез острофазовых белков, являющихся показателями остроты/тяжести ревматического процесса. Таким образом, выраженность неспецифического экссудативного компонента воспаления при ОРЛ, исходом которой является системная дезорганизация соединительной ткани и васкулиты с развитием умеренного фиброза, определяет остроту течения ревматического процесса.
β-гемолитический стрептококк группы А
 263
263
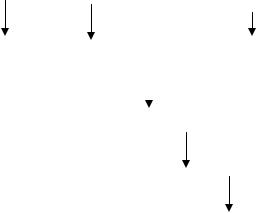
ферменты, токсины |
Образование противострептококковых ан- |
|
тител и формирование иммунных комплексов и |
Повреждение соединительной ткани эндо-, мио-, перикарда, других органов и сосудов по типу гиперчувствительности немедленного типа
Образование |
аутоантител |
к |
|
соединительной |
ткани |
эндо-, |
|
||||||
мио-, перикарда, других органов и систем, сосудов |
|
|
||||
Длительная иммунная реакция по типу гиперчувствительности замедленного типа
Иммунное и неиммунное воспаление эндо-, мио-, перикарда, других органов и сосудов
Рис 1.32. Схема патогенеза ОРЛ
Патоморфологические изменения при ревмокардите бывают двух видов: специфические (гранулёма Ашофф-Талалаева) и неспецифические, с развитием очаговых и диффузных лимфогистиоцитарных и лейкоцитарных инфильтратов.
Ревматическая гранулёма развивается только в трех оболочках сердца. Неспецифические экссудативно-пролиферативные изменения возникают вокруг гранулёмы, а также в сосудах, с развитием васкулита, в том числе в коронарных сосудах (коронарит).
Ревматический процесс дезорганизации соединительной ткани характеризуется 4-я стадиями:
1.стадия мукоидного набухания (единственная обратимая стадия при своевременно начатом лечении);
2.стадия фибриноидного набухания и некроза (может заканчиваться фиброзом миокарда, минуя гранулематозную стадию);
3.стадия формирования гранулёмы Ашофф-Талалаева (гранулёма представляет собой скопление молодых макрофагальных клеток, в центре которых расположены пролифелирующие и гипертрофированные гистиоциты. Макрофаги и гистиоциты расположены вокруг продуктов дезорганизации соединительной ткани и фибриноидных масс
264
(«цветущая» гранулёма). В дальнейшем исчезают фибриноидные глыбки («увядающая» гранулёма), затем происходит рубцевание («рубцующаяся» гранулёма);
4. Стадия склероза (фиброза) характеризуется развитием рубца. Ревматическое поражение оболочек сердца называют ревмокарди-
том и оно чаще представлено сочетанным их поражением. Ревматический эндокардит может быть: простой эндокардит
(вальвулит Талалаева), острый бородавчатый эндокардит, возвратный бородавчатый эндокардит, фибропластический эндокардит.
По частоте поражения клапанов на первом месте находится митральный (65-70%), на втором – одновременное поражение митрального и аортального (25%), на третьем – аортальный (5-10%) .
Ревматический перикардит является признаком высокой активности процесса, бывает серозным или серозно-фибринозным.
Миокардиты чаще бывают экссудативные, очагового или диффузного характера, так как преобладают реакции гиперчувствительности немедленного типа.
Васкулит при ОРЛ может быть экссудативным, экссудативнопролиферативным, продуктивным.
При артрите клиническая манифестация отмечается только при экссудативной форме. Преобладают артриты крупных и средних суставов. В околосуставной ткани формируются очаги фибриноида с лимфо-макрофагальной реакцией (ревматические узелки). Особенностью ревматических артритов является то, что никогда не развиваются анкилозы (как при ревматоидных артритах), так как никогда не поражаются суставные хрящи.
Ревматическое поражение ЦНС отмечается в двух видах:
1.ревматических васкулитов;
2.малой хореи, при которой поражаются ядра стриопаллидум, при этом сосуды не вовлекаются в процесс.
Ревматические васкулиты с поражением ЦНС могут развиваться в любом возрасте, малая хорея – только у детей.
Ревматический гломерулонефрит (ГН) чаще бывает очагового харак-
тера.
При поражении легких иммунное воспаление отмечается в периваскулярной и перибронхиальной соединительной ткани с развитием асептической ревматической серозной или серозно-дескваматозной пневмонии.
В селезенке и лимфатических узлах возникает гиперплазия В-
зависимых зон. При декомпенсации эти иммунные реакции угнетают-
265
ся, лимфатические узлы и селезенка могут быть опустошены (лимфоидное опустошение).
Классификация ОРЛ (Ассоциация ревматологов России 2003, г. Саратов).
Клинические формы: острая ревматическая лихорадка (ОРЛ); повторная ревматическая лихорадка;
клинические проявления: основные: кардит, артрит, хорея, кольцевидная эритема, ревматические узелки.
дополнительные: лихорадка, артралгия, абдоминальный синдром, серозиты.
Исходы: выздоровление, хроническая ревматическая болезнь сердца (ХРБС) без порока сердца; хроническая ревматическая болезнь сердца с пороком сердца и сердечной недостаточностью;
Недостаточность кровообращения: (по Н.Д. Стражеско и В.Х. Василенко) стадии: 0, I, IIА, IIБ, III.
По классификации NYHA функциональные классы: 0, I, II, III, IV. Исследования: общий анализ крови и мочи, протеинограмма, трансаминазы в крови, серомукоид, фибриноген, СРБ, ревматоидный фактор, титры АСЛО, АСГ, анти-ДНК-аза-В, антистрептогиалуронидаза, ЭКГ, ФКГ, ЭХО-КГ с допплеранализом. По показаниям: рентге-
нография суставов, иммунограмма. При вовлечении в процесс сердца показано определение показателей коагулограммы.
Исследования амбулаторно, при приобретенном пороке сердца, приказ МЗ РФ №379: измерение АД, ЭКГ, рентгенография сердца с контрастированием пищевода, ЭХО-КГ, общий анализ крови, СРБ, фибриноген крови. По показаниям: рентгенография легких, протеинограмма, посев крови на стерильность, титры антистрептолизинов О, ФКГ.
Анамнез, клиника. ОРЛ обычно начинается через 2-6 недель после перенесенного стрептококковой ангины или фарингита, сопровождается лихорадкой и интоксикацией.
У детей младшего возраста заболевание обычно манифестирует кардитом, у детей старшего возраста – артритом.
Поражение сердца. Кардит – ведущий синдром ОРЛ (90–95% случаев), который определяет тяжесть течения и исход заболевания. Основополагающим компонентом ревматического кардита считается вальвулит. Внимание! Для первичного ревматического вальвулита не характерны признаки кардиомегалии и застойной сердечной недостаточности.
Клинические признаки вальвулита митрального клапана: глухость первого тона над верхушкой; систолический шум средней интенсивно-
266
сти, жестковатый, «дующего тембра», занимающий ½ - 2/3 систолы, связанный с I тоном, проводящийся экстракардиально.
Клинические признаки вальвулита аортального клапана: диастоли-
ческий шум малой интенсивности и мягкого тембра - «льющийся» шум, примыкающий ко второму тону и занимающий 1/3 – ½ диастолы. Шум лучше выслушивается во втором-третьем межреберье справа от грудины или на середине грудины. Характерно умеренное снижение диастолического и увеличение пульсового АД.
Важнейшая особенность вальвулита при первой атаке ОРЛ – четкая положительная динамика под влиянием активной антиревматической терапии. В преобладающем большинстве случаев на фоне лечения происходит нормализация частоты сердечных сокращений, восстановление звучности тонов, уменьшение интенсивности систолического и диастолического шумов, сокращение границ сердца, исчезновение симптомов недостаточности кровообращения.
Особенностью современного течения ревмокардита является умеренная или слабая манифестация миокардита, который проявляется умеренной тахикардией, ослаблением или приглушением I тона над верхушкой, наличием мягкого систолического шума над верхушкой и в V точке, занимающего ½ систолы, без выраженной кардиомегалии и застойной сердечной недостаточности. Миокардит является постоянным проявлением ревмокардита.
Ревматический эндомиокардит с вовлечением в процесс митрального клапана характеризуется появлением грубого дующего систолического шума, связанного с ослабленным I тоном, который выслушивается на верхушке и проводится в левую подмышечную область, усиливается после физической нагрузки. При поражении аортального клапана появляется диастолический шум вдоль левого края грудины.
Ревматический перикардит возникает при тяжелом кардите, встречается крайне редко (в 2,5% случаев). Отмечается стойкое сердцебиение и одышка в покое, боли в сердце. Боли носят загрудинный и давящий характер. Верхушечный толчок разлитой, границы сердца расширены преимущественно влево и вверх, оба тона значительно приглушены. Может выслушиваться шум трения перикарда (при фибринозном перикардите).
Поражение суставов. Ревматический полиартрит (60–100% слу-
чаев) – мигрирующий полиартрит преимущественно крупных и средних суставов (коленных, голеностопных, реже – локтевых, плечевых, лучезапястных). Артрит, как правило, сочетается с кардитом и реже (10–15% случаев) протекает изолированно. Характерно: симметричность поражения суставов, кратковременность (3-7 дней), быстрая и
267
полная регрессия воспаления под влиянием противовоспалительной терапии, отсутствие остаточных явлений.
Редко возникают другие полисерозиты: плеврит, асептический экссудативный перитонит, гепатит, нефрит и другие проявления.
Поражение ЦНС. Ревматический церебральный васкулит проявляется в виде менингоэнцефалита.
Малая хорея чаще встречается у девочек, в пубертатном периоде, клинически проявляется пентадой синдромов, наблюдающихся в различных сочетаниях: гиперкинезы, мышечная гипотония (вплоть до дряблости мышц с имитацией параличей), нарушение статики и координации, сосудистая дистония и эмоциональная лабильность.
Гиперкинезы проявляются беспорядочными, нестереотипными, насильственными движениями в различных группах мышц. При этом отмечается неловкость движений, невнятность речи, изменения почерка. Чаще гиперкинезы бывают двусторонними, усиливаются при волнении и исчезают во сне. Выполнение координационных проб затруднено. Характерна мышечная гипотония различной степени выраженности. Отмечается неустойчивость настроения плаксивость, раздражительность.
Поражение кожи. Кольцевидная (аннулярная) эритема встречает-
ся у 7-19% больных, в виде бледно-розовых кольцевидных высыпаний на боковых поверхностях туловища, реже на руках и ногах (но не на лице!). Сыпь не возвышается над поверхностью кожи, исчезает при надавливании. Она имеет транзиторный мигрирующий характер, быстро исчезает без остаточных явлений (пигментаций, шелушения, атрофических изменений). Диагностическое значение аннулярной эритемы в настоящее время уменьшилось, так как она нередко возникает при других инфекционно-аллергических заболеваниях.
Табл. 1.81. Критерии Киселя-Джонса, применяемые для диагно-
стики ОРЛ (в модификации АРР, 2003)
Большие |
Малые критерии |
Данные, подтверждающие |
критерии |
|
предшествующую инфек- |
|
|
цию БГСА |
Кардит |
Клинические: |
Положительная культура |
Артрит |
Артралгии |
стрептококка группы А, |
Хорея |
Лихорадка (более 38 оС) |
выделенная из зева, или |
Кольце- |
Лабораторные: (повышение |
положительный тест бы- |
видная эри- |
острофазовых показателей): |
строго определения ан- |
тема |
СОЭ, С-реактивного белка; |
тигена стрептококка |
268
Подкожные |
Инструментальные: |
группы А |
ревматиче- |
Удлинение интервала P-R на |
Повышение или повы- |
ские узелки |
ЭКГ |
шающиеся титры проти- |
|
Признаки митральной и/ или |
вострептококковых ан- |
|
аортальной регургитации |
тител |
|
при ДЭхоКГ |
|
Ревматические узелки – это плотные безболезненные образования размером от нескольких мм до 1-2 см, локализуются у мест прикрепления сухожилий в области коленных, локтевых суставов, в области лодыжек, ахилловых сухожилий, остистых отростков позвонков. У детей встречаются при возвратной РЛ.
Диагноз. Для диагностики ОРЛ применяются диагностические критерии Киселя–Джонса (табл. 1.81). Критерии приведены с учетом последнего пересмотра Американской ревматологической ассоциацией (АКА) (1992г.) и модификаций, предложенных Ассоциацией ревматологов России (АРР) в 2003 г.
Наличие двух больших критериев или одного большого и двух малых в сочетании с данными, документировано подтверждающими
предшествующую инфекцию БГСА, свидетельствуют о высокой вероятности ОРЛ.
Особые случаи:
•Изолированная («чистая») хорея – при исключении других при-
чин (в том числе синдром PANDAS (pediatric autoimmune neuropsychiatric disorders associated with group A streptococcal infections);
•Поздний кардит – растянутое во времени (более 2 месяцев) развитие клинических и инструментальных симптомов вальвулита – при исключении других причин;
•Повторная ОРЛ на фоне хронической ревматической болезни сердца (ХРБС) или без нее.
Критерии активности ревматического процесса. Клинические проявления болезни зависят от степени активности ревматического воспаления. Выделяют три степени активности: минимальную (I), умеренную (II), максимальную (III).
Минимальная степень активности характерна для постепенного
начала ОРЛ, температура тела остается нормальной, при этом лабораторные показатели либо в пределах возрастной нормы, либо имеются незначительные отклонения в части из них. Подтвердить минимальную степень активности возможно при динамическом обследовании больного. Важно помнить, что именно при минимальной степени ак-
269
тивности и затяжном течении ОРЛ клапанный порок формируется в 3- 3,5 раза чаще, чем при высокой степени активности процесса.
Умеренная степень активности характеризуется постепенным началом, субфебрильной температурой тела, умеренным или слабо выраженным кардитом, полиартралгиями, хореей. Рентгенологических отклонений от нормы часто не определяется. Лабораторные показатели активности воспаления изменены умеренно или незначительно. Клапанный порок сердца формируется также чаще, чем при остром течении и высокой степени активности процесса.
Выраженная степень активности проявляется яркими признаками болезни с острым началом, с выраженным экссудативным компонентом воспаления в пораженных органах (полиартрит, панкардит, полисерозит, множественные висцериты), высокой лихорадкой. Картина острого кардита характеризуется расширением полостей сердца и снижением сократительной функции миокарда, что подтверждается инструментальными методами исследования. Лабораторные показатели воспаления и противострептококкового иммунитета значительно выше нормы.
Лабораторные исследования
Для выявления активной БГСА инфекции важно обнаружить повышенные или (что важнее) повышающиеся при повторном исследовании (через 3 недели) титры противострептококковых антител (АСЛ- О, антидезокси-рибонуклеазы В и антистрептогиалуронидазы (АСГ).
Выявление БГСА при бактериологическом исследовании мазка и из зева и носа не позволяет дифференцировать активную инфекцию от стрептококкового носительства.
Рентгенологическое исследование: при вальвулите митрального клапана определяется митральная конфигурация сердца за счет вы-
полнения «талии» сердца ушком левого предсердия и увеличения размеров обеих левых камер сердца. При вальвулите аортального клапана выявляется аортальная конфигурация сердца.
На ЭКГ при эндомиокардите могут быть такие неспецифические признаки, как: синусовая тахиили брадикардия, реже миграция водителя ритма, экстрасистолия, АВ-блокады I–II степени, нарушения процессов реполяризации желудочков. При вальвулите митрального клапана могут быть признаки острой перегрузки левого предсердия; при вальвулите аортального клапана – признаки диастолической перегрузки левого желудочка.
На ДЭхоКГ признаками вальвулита являются рыхлость и утолщение эхосигнала от пораженного клапана, ограничение их подвижности,
270
при тяжелом кардите - снижение фракции выброса левого желудочка
(ниже 60%).
Гематологические сдвиги: лейкоцитоз выше 11×109/л и повышение СОЭ более 20 мм/ч – у больных с умеренной степенью выраженности ОРЛ. Высокий лейкоцитоз и повышение СОЭ более 40 мм/ч характерны для тяжелой степени выраженности ОРЛ.
Также соответствуют степени тяжести заболевания и другие острофазовые показатели: СРБ, серомукоид, диспротеинемия с гипоальбуминемией и гиперглобулинемией.
Внимание! При изолированной малой хорее лабораторные показатели могут быть в пределах возрастной нормы, несмотря на выраженные клинические проявления.
Дифференциальный диагноз
Первичный ревмокардит необходимо дифференцировать с: приоб-
ретенными неревматическими кардитами (вирусные миокардиты),
которые могут возникать в возрасте от 1мес. до 17 лет. В этих случаях в анамнезе отмечается частая связь с вирусной носоглоточной инфекцией (чаще энтеровирусной или аденовирусной), короткий «светлый» промежуток между заболеваниями; наличие в анамнезе предшествующих аллергических заболеваний, особенно у детей младшего возраста; жалобы на сердцебиение (внимание! ЧСС не соответствует степени лихорадки), одышка при физической нагрузке или в покое, кардиалгии, выраженная астенизация. В дебюте заболевания можно выявить повышение температуры до субфебрильных и фебрильных цифр.
Объективно: тоны сердца приглушены на верхушке (преимущественно I тон), часто выявляется экстрасистолия, систолический шум митральной регургитации; при сопутствующем перикардите – шум трения перикарда. При наличии СН: тахикардия, ритм «галопа», слабый пульс, отеки, пастозность, набухание шейных вен, гепатомегалия, влажный кашель (чаще ночной), хрипы в легких.
Гематологические сдвиги могут быть минимальными (лейкоцитоз, повышение СОЭ) или показатели гемограммы могут оставаться без изменений. Отмечается повышение КФК, КФК-МВ, тропонина I, ЛДГ, АсАТ.
На ЭКГ: синусовая тахикардия, экстрасистолия, удлинение интервала PR и QT. Рентгенологически: кардиомегалия, застойные явления в легких. На ДЭхоКГ: глобальная гипокинезия (наиболее типичный признак), систолическая дисфункция левого желудочка (снижение фракции выброса), увеличение конечно-диастолического и конечносистолического размеров левого желудочка, перикардиальный выпот, отсутствие вальвулита.
271
При сравнении с ОРЛ – более медленная положительная динамика клинических и ЭКГ признаков под влиянием терапии (торпидность).
Идиопатический пролапс митрального клапана (ПМК) чаще встре-
чается у девочек, с астеническим телосложением, высоким ростом, имеющими признаки дисплазии соединительной ткани: воронкообразная деформация грудной клетки, гипермобильность суставов, нарушение осанки, сколиоз, готическое нёбо, прогнатизм, миопия, раннее развитие плоскостопия и др. В анамнезе у большинства таких детей отмечается раннее начало ангин, формирование хронического тонзиллита. Жалобы многочисленные, вегетативного характера (головокружение, слабость, сердцебиение, одышка, головная боль, кардиалгии, связанные с эмоциональным перенапряжением, которые проходят самостоятельно или после приема настойки валерианы). Объективно, при аускультации сердца выслушивается систолический щелчок (лучше в вертикальном положении), позднесистолический шум (лучше выслушивается в положении лёжа). Наиболее отчетливо выявляется сочетание систолического щелчка с позднесистолическим шумом после физической нагрузки. Нет клинических признаков сердечной недостаточности, кардиомегалии, тоны сердца звучные.
Гематологические сдвиги отсутствуют, в биохимическом анализе крови нет увеличения острофазовых показателей. На рентгенограмме – малые размеры сердца, выбухание дуги легочной артерии. При ДЭхоКГ – утолщенность «лохматость» створок митрального клапана, выгибание одной или обеих створок в полость левого предсердия, митральная регургитация 1-2 степени (при отсутствии недостаточности митрального клапана).
Малую хорею (в сочетании с поражением сердца, суставов и, особенно изолированную) необходимо дифференцировать с: неврозом навязчивых движений (тиками). В анамнезе у таких д етей – перинатальная (постгипоксическая или посттравматическая) энцефалопатия, психоэмоциональная лабильность, хронические очаги инфекции в носоглотке. Клинически: после острого стресса отмечается возникновение стереотипных и повторяющихся движений мышц лица (подергивание или нахмуривание бровей, мигание, зажмуривание глаз, шмыганье носом, стереотипные жевательные движения) или верхних, реже нижних конечностей, при сохранении нормального мышечного тонуса. Гематологические сдвиги отсутствуют, в биохимическом анализе крови нет увеличения острофазовых показателей. Положительная динамика при лечении седативными препаратами.
Для синдрома PANDAS (pediatric autoimmune neuropsychiatric disorders associated with group A streptococcal infections), характерна пси-
272
хоневрологическая симптоматика. В анамнезе: предшествующая стрептококковая инфекция носоглотки. Клинически: характерно острое начало у детей в возрасте до 12 лет и приступообразное течение; сочетание навязчивых мыслей и навязчивых движений (хореиформных гиперкинезов: быстрых, хаотических движений дистальных частей конечностей и лица).
Параклинически: выделение БГСА в мазке из зева и серологическое подтверждение инфекции (повышение титров антистрептолизина
– О и анти–ДНК–азы В). Назначение адекватной противострептококковой антибиотикотерапии (пенициллины или оральные цефалоспорины) приводит к быстрому и полному выздоровлению.
Ревматический полиартрит необходимо дифференцировать с реактивными артритами, которые развиваются после носоглоточной, кишечной инфекции, инфекции мочевыводящих путей. Клинически: короткий «светлый» промежуток между этими заболеваниями (от нескольких дней до 1-1,5 недель), нередко повышение температуры, моноартриты, чаще крупных или средних суставов нижних конечностей, не характерен «летучий» характер артритов.
Гематологические сдвиги умеренные (лейкоцитоз, повышенная СОЭ). Выделение возбудителей: стрептококков, стафилококков в мазках из зева и носа, хламидий (в мазках из конъюнктивы, в моче), сальмонелл, шигелл, иерсений (в кале) а также серологическое подтверждение перенесенной инфекции. Рентгенологически: признаки артрита, без деструктивных изменений. При проведении этиотропной и противоспалительной терапии - быстрое обратное развитие заболевания, с восстановлением функции, без деформации суставов.
Лечение. Задачи лечения: эрадикация БГСА, подавление активности ревматического процесса, предупреждение формирования приобретенных пороков сердца, купирование застойной недостаточности кровообращения, ликвидация экстракардиальных проявлений заболевания.
Схема лечения. Обязательные мероприятия: соблюдение этапно-
сти лечения, режим, антибиотики, НПВС/гормоны, препараты хинолинового ряда.
Вспомогательное лечение: диета, антигистаминные средства, витаминотерапия.
Показания для госпитализации: все пациенты с ОРЛ.
Режим: постельный на 2-3 недели, до появления стойкой положительной клинической и лабораторно-инструментальной динамики; далее режим расширяется до полупостельного, затем – до тренирующего.
273

Диета – содержание белка не менее 1г/кг массы тела, ограничение поваренной соли. Показано включение в рацион продуктов, содержащих соли калия и магния.
Лечение ОРЛ включает три этапа: стационарное лечение, лечение в местном кардиоревматологическом санатории, лечение в условиях поликлиники (см. «профилактика ОРЛ).
Этиотропная терапия направлена на эрадикацию (уничтожение) БГСА. Всем больным с ОРЛ назначают препараты пенициллина.
Табл. 1.82. Схема применения антибиотиков при непереносимо-
сти некоторых из них
Бензилпенициллин |
макролиды (азитроми- |
Линкозамиды |
в/м, 10 сут; при непе- |
цин, вильпрофен, кла- |
(клиндамицин, |
реносимости пеницил- |
ритромицин, рокситро- |
линкомицин) |
линов: |
мицин, мидекамицин, |
|
|
спирамицин, эритроми- |
|
|
цин); при непереносимо- |
|
|
сти макролидов: |
|
Табл. 1.83. Дозы основных антибиотиков, применяемых при этио-
тропной терапии ОРЛ
Препарат |
Доза, возраст паци- |
Путь введения, кратность, |
|
ента |
длительность |
Бензилпени- |
1,5–4 млн ЕД/сут, |
в/м, в 4 приема, 10 сут. |
циллин |
детям старше 12 лет |
в/м, в 4 приема, 10 сут. |
|
400–600 тыс. ЕД /сут, |
|
|
детям младше 12 лет |
|
Азитромицин |
0,5 г/сут (со 2-го дня |
Внутрь, 1 раз (за 1 час до |
|
– 0,25 г/сут), детям |
еды); в 1-й день; 2-5-й день – |
|
старше 12 лет |
по 0,25 г/сут, 1 раз в день |
|
|
Внутрь, 1 раз (за 1 час до |
|
12 мг/кг/сут, детям |
|
|
младше 12 лет |
еды); 5 сут. |
Кларитроми- |
0,5 г/сут детям стар- |
Внутрь (до еды), в 2 приема, |
цин |
ше 12 лет |
10 сут. |
|
15 мг/кг/сут детям |
Внутрь, в 2 приема, 10 сут. |
|
младше 12 лет |
|
Мидеками- |
1,2 г/сут. детям стар- |
Внутрь (до еды), в 3 приема, |
цин (макро- |
ше 12 лет |
10 сут. |
274
пен) |
50 мг/кг/сут. детям |
Внутрь (до еды), в 3 приема, |
|
младше 12 лет |
10 сут. |
Рокситроми- |
0,3 г/сут. детям стар- |
Внутрь (за 15 мин. до еды), в |
цин |
ше 12 лет |
2 приема, 10 сут. |
|
5 мг/кг/сут. детям |
Внутрь (за 15 мин. до еды), в |
|
младше 12 лет |
2 приема, 10 сут. |
Спирамицин |
6 млн ЕД/сут. детям |
Внутрь, в 2 приема, 10 сут. |
|
старше 12 лет |
|
|
3 млн ЕД/сут. детям |
Внутрь, в 2 приема, 10 сут. |
|
младше 12 лет |
|
Эритромицин |
1,5 г/сут. детям стар- |
Внутрь (за 1 час до еды), в 3 |
|
ше 12 лет |
приема, 10 сут. |
|
40 мг/кг/сут. детям |
Внутрь (за 1 час до еды), в 3 |
|
младше 12 лет |
приема, 10 сут. |
Клиндамицин |
0,6 г/сут. детям стар- |
Внутрь (запивать большим |
|
ше 12 лет |
количеством воды) в 4 прие- |
|
|
ма, 10 сут. |
|
20мг/кг/сут. детям |
Внутрь (запивать большим |
|
младше 12 лет |
количеством воды) в 3 прие- |
|
|
ма, 10 сут. |
Линкомицин |
1,5 г/сут. детям стар- |
Внутрь (за 1-2 часа до еды), в |
|
ше 12 лет |
3 приема, 10 сут. |
|
30 мг/кг/сут. детям |
Внутрь (за 1-2 часа до еды), в |
|
младше 12 лет |
3 приема, 10 сут. |
Патогенетическая терапия (противовоспалительная терапия)
Показания для назначения преднизолона: тяжелый или умеренно выраженный ревмокардит (панкардит), хорея, полисерозиты; максимальная или умеренно выраженная активность воспалительного процесса (СОЭ ≥ 30мм/ч).
Преднизолон назначают по 20 мг/сут (детям старше 12 лет), по 0,7- 0,8 мг/кг/сут (детям младше 12 лет), в 1 прием, утром, до еды, примерно, на протяжении 2-х недель. Далее дозу снижают по 2,5 мг/сут, ка ж- дые 5-7 дней, вплоть до отмены, курс 1,5-2 мес. Сопутствующие препараты при назначении преднизолона: антациды (альмагель, маалокс, вентер) и препараты калия (аспаркам, панангин).
Показания для назначения НПВС (диклофенак): слабовыраженный кардит; ревматический артрит без кардита, минимальная активность процесса (СОЭ < 30 мм/ч), а также: при необходимости в длительном лечении после стихания высокой активности ОРЛ, повторная РЛ на фоне ревматического порока сердца.
275
Симптоматическая терапия включает лечение СН: дигоксин, капотен, фуросемид, гипотиазид, верошпирон.
При лечении малой хореи используют этиотропную, патогенетическую терапию ОРЛ, в сочетании с антипсихотическими средствами и нейроптиками (галоперидол, диазепам), применяют также барбитураты (фенобарбитал), ноотропы (мексидол, фенибут), а также витамины группы В (нейромультивит, мильгамма).
Исход и прогноз РЛ связан с частотой формирования ревматического порока сердца (РПС). Частота формирования РПС после первой атаки ОРЛ у детей составляет 20–25%, причём максимальная частота формирования РПС отмечается в течение первых 3-х лет после ОРЛ. Преобладают изолированные пороки сердца, чаще митральная недостаточность. Реже формируется недостаточность аортального клапана, митральный стеноз и митрально–аортальный порок. У больных, перенесших первую атаку ОРЛ в возрасте 23 лет и старше, сочетанные и комбинированные РПС формируются в 90% случаев. Примерно у 7– 10% детей после перенесенного кардита формируется пролапс митрального клапана.
Дети и подростки, имеющие РПС, относятся к группе среднего риска по возникновению вторичного инфекционного эндокарда.
Первичная профилактика ОРЛ
I этап: общие мероприятия: обеспечение правильного физического развития ребенка; полноценное витаминизированное питание; закаливание с первых месяцев жизни; выполнение комплекса санитарногигиенических правил; борьба со скученностью в школах, детских учреждениях.
II этап - борьба со стрептококковой инфекцией - проводится ран-
няя диагностика БГСА; лечение острого тонзиллита, вызванного БСГА: в/м, однократно - бензатина бензилпенициллин; или внутрь, в течение 10 сут. - амоксициллин, феноксиметилпенициллин, цефадроксил. При непереносимости указанных препаратов назначают макролиды, внутрь, в течение 10 сут. (см. табл. 1.83). При обострении хронического тонзиллита, вызванного БСГА, применяют: внутрь, в течение 10 сут. – амоксициллин/клавуланат, цефуроксим. При непереносимости бета-лактамных антибиотиков: внутрь, в течение 10 сут. – клиндамицин, линкомицин.
Вторичная профилактика РЛ
Проводится экстенциллином, ретарпеном (бензатином бензилпенициллином) в дозе: 600 000 ЕД детям массой тела до 25 кг; 1 200 000 ЕД детям с массой более 25 кг; 2 400 000 ЕД подросткам и взрослым 1 раз в 3 недели или бициллином-1 в той же дозе, но 1 раз в неделю. При
276
непереносимости пенициллинов пролонгированного действия рекомендуется своевременно применять макролиды 10-ти дневным курсом в каждом случае БСГА тонзиллита/фарингита. Длительность бициллинопрофилактики устанавливается индивидуально:
1.у больных, перенесших ОРЛ без кардита (хорея, артрит) - в течение 5 лет или до 18-летнего возраста по принципу «что дольше»;
2.у больных, перенесших ОРЛ с кардитом, без формирования порока – в течение 10 лет или до 25 -летнего возраста по принципу «что дольше»;
3.у больных, перенесших ОРЛ с кардитом, с формированием порока – пожизненно.
Профилактика вторичного инфекционного эндокардита: прово-
дится пациентам с РПС при медицинских манипуляциях в области полости рта, пищевода, дыхательных путей: амоксициллин внутрь 2 г (детям старше 12 лет), 50 мг/кг (детям младше 12 лет), однократно, за 1 час до процедуры или ампициллин в/в или в/м, в той дозе, однократно, за 30 мин. до процедуры.
При непереносимости пенициллинов: клиндамицин внутрь 600 мг (детям старше 12 лет), 20 мг/кг (детям младше 12 лет), однократно, за 1 час до процедуры; цефадроксил или цефалексин внутрь 2г (детям старше 12 лет), 50 мг/кг (детям младше 12 лет), однократно, за 1 час до процедуры или клиндамицин в/в 600 мг (детям старше 12 лет), 20 мг/кг (детям младше 12 лет), однократно, за 30 мин. до процедуры; цефазолин в/в или в/м 1г (детям старше 12 лет), 25 мг/кг (детям младше 12 лет), однократно, за 30 мин. до процедуры.
При непереносимости линкозамидов и цефалоспоринов: азитромицин внутрь 500 мг (детям старше 12 лет), 15 мг/кг (детям младше 12 лет), однократно, за 1 час до процедуры; кларитромицин внутрь 500 мг (детям старше 12 лет), 15 мг/кг (детям младше 12 лет), однократно, за 1 час до процедуры.
Профилактика вторичного инфекционного эндокардита: прово-
дится пациентам с РПС при медицинских манипуляциях в области желудочно-кишечного и урогенитального трактов: амоксициллин внутрь 2 г (детям старше 12 лет), 50 мг/кг (детям младше 12 лет), о д- нократно, за 1 час до процедуры или ампициллин в/в или в/м, в той дозе, однократно, за 30 мин. до процедуры. При непереносимости пенициллинов: ванкомицин в/в капельно, 1г, в течение 1-2 ч, однократно (введение необходимо завершить за 30 мин. до процедуры).
277
Хроническая ревматическая болезнь сердца (ХРБС) -
заболевание сердца, возникающее после ОРЛ и характеризующееся поражением сердечных клапанов в виде поствоспалительного краевого фиброза клапанных створок или формированием порока сердца (стеноз и/или клапанной недостаточности).
Распространенность ХРБС среди детей и подростков составляет 28 и 60 на 100 000 соответственно, среди взрослого населения – 226 на 100 000. Клиническая картина, течение, диагностика, дифференциальный диагноз и исходы при ХРБС практически аналогичны данным, характерным для ОРЛ. Однако существуют и некоторые особенности ХРБС. Так, в частности, при повторных ревматических атаках отмечаются следующие особенности течения процесса:
-уменьшается частота и выраженность экстракардиальных проявлений заболевания;
-увеличивается тяжесть кардиальной патологии, частота развития приобретенных пороков сердца;
-увеличивается количество больных с развитием недостаточности кровообращения при возвратных ревмокардитах. Недостаточность кровообращения нарастает при снижении активности ревматического процесса, на фоне нарастающих дистрофических и склеротических изменений в сердечной мышце;
-медленная нормализация лабораторных, в том числе и иммунологических показателей.
Исходы. Наиболее частым исходом ОРЛ и ХРБС является формирование такого приобретенного порока сердца, как митральная недостаточность. По современным данным недостаточность митрального клапана составляет 61-70% всех пороков ревматического происхождения. На втором месте среди приобретенных пороков сердца стоит изолированная недостаточность аортального клапана (до 10%). Реже формируется более неблагоприятный по гемодинамическим показателям приобретенный порок - стеноз митрального клапана (до 3%). Еще реже, чем стеноз митрального клапана среди приобретенных пороков сердца, встречается изолированный стеноз аортального клапана (до 1%). При ХРБС часто происходит формирование сочетанного приобретенного порока – уже к имеющейся недостаточности аортального клапана, после повторной атаки РЛ, присоединяется стеноз устья аорты.
Недостаточность митрального клапана, как и другие ревматиче-
ские приобретенные пороки сердца, формируется в течение нескольких лет, в среднем от 3 -х до 5-ти. При этом пороке происходит смор-
278
щивание, укорочение и неполное смыкание створок митрального клапана. Изменяется и подклапанный аппарат: укорачиваются сухожильные нити, склерозируются сосочковые мышцы.
Гемодинамика. При недостаточности митрального клапана во время систолы происходит постоянный обратный ток крови из левого желудочка в левое предсердие. Мышца левого предсердия из-за перегрузки гипертрофируется. В дальнейшем происходит дилатация полости левого желудочка и гипертрофия его мышцы. Далее происходит повышение давление в левом предсердии и в малом круге кровообращения. Повышение нагрузки на правый желудочек приводит к его гипертрофии. В последнюю очередь происходит дилатация и гипертрофия правого предсердия.
Недостаточность митрального клапана проходит несколько стадий формирования - от минимальной до максимальной, в зависимости от степени выраженности порока сердца. Особенностью недостаточности митрального клапана является то, что при умеренной степени недостаточности может длительно сохраняться состояние компенсации митрального клапана.
Клиника. I степень недостаточности митрального клапана кли-
нически характеризуется: расширением границ относительной сердечной тупости влево и вверх, аускультативно определяется ослабление I тона, дующий систолический шум органического характера, р. max. – на верхушке сердца.
При II, и, особенно при III степени недостаточности митрального
клапана – отмечается выраженное расширение всех трех границ относительной сердечной тупости, подтверждаемое на рентгенограмме органов грудной полости и ДЭхоКГ, усиление и смещение верхушечного толчка влево и вниз. I тон приглушен, при развитии сердечной недостаточности выслушивается III тон, II тон на легочной артерии акцентуирован. При развитии декомпенсации порока происходит уменьшение акцента II тона на легочной артерии.
Диагноз
Инструментальные методы исследования ДЭхоКГ – (золотой стандарт диагностики порока) позволяет вы-
явить степень недостаточности митрального клапана, морфологические изменения его клапанов.
ЭКГ – признаки перегрузки и гипертрофии различных отделов сердца, аритмии: экстрасистолию, фибрилляцию предсердий.
Осложнениями недостаточности митрального клапана являются фатальные аритмии при декомпенсации порока и инфекционный эндокардит. При тяжелом поражении митрального клапана проводят кла-
279
паносохраняющую операцию – аннулопластику с использованием полужесткого искусственного кольца.
Стеноз левого атрио-вентрикулярного отверстия. Порок чаще всего формируется при атипичном течении РЛ. При митральном стенозе происходит склеивание, а затем срастание соприкасающихся между собой створок митрального клапана. Створки утолщаются, становятся плоскими, укорачиваются. Также происходит утолщение и укорочение подкапанных структур. Клапан приобретает вид воронки, которая суживается у выходного отдела левого желудочка и расширяется в полости левого предсердия.
Гемодинамические нарушения возникают при уменьшении площади митрального отверстия в 2-3 раза. При этом резко затрудняется продвижение крови в диастолу из левого предсердия в левый желудочек, левое предсердие гипертрофируется. Повышенное давление в левом предсердии способствует повышению давления в малом круге кровообращения. В свою очередь легочная гипертензия ведет к гипертрофии правого желудочка, далее к его дилатации и формированию правожелудочковой недостаточности.
Клиника. Наиболее ранним клиническим симптомом этого порока сердца является одышка, особенно при физической нагрузке, из-за развития гипертензии в малом круге кровообращения. В дальнейшем при физической нагрузке могут возникать сухой кашель, иногда с примесью крови и жалобы ребенка на выраженные боли в области сердца, сердцебиение. Нарастает отставание в физическом развитии. Объективно: верхушечный толчок ослаблен, в третьем-четвертом межреберье слева от грудины возможно диастолическое дрожание; границы относительной сердечной тупости расширены вправо и вверх, I тон на верхушке громкий, хлопающий, «пушечный», диастолический шум на верхушке. II тон резко усилен или раздвоен на легочной артерии. САД снижено, снижено пульсовое АД, пульс малого наполнения и напряжения.
Диагноз стеноза левого атрио-вентрикулярного отверстия основывается на данных клинического обследования и подтверждается результатами дополнительных исследований.
Инструментальные методы исследования ДЭхоКГ- (золотой стандарт диагностики порока) позволяет выявить
степень стеноза, дилатацию и гипертрофию правого желудочка, левого предсердия.
280
На рентгенограмме органов грудной полости – кардиомегалия за счет увеличения левого предсердия и правого желудочка, выбухание дуги легочной артерии, признаки легочной гипертензии.
ЭКГ – ЭОС отклонена вправо, признаки гипертрофии левого предсердия и правого желудочка. Ранний признак стеноза - изменение зубца Р: вначале он высокий и широкий, позже он расщепляется в I, II стандартных отведениях и в AVL, в отведениях V1 и V2 зубец Р двухфазный (+,-).
Прогноз для пациентов, имеющих стеноз митрального клапана серьезен, так как адаптационные механизмы левого предсердия и правого желудочка значительно ограничены. При прогрессировании стеноза митрального клапана проводится оперативная коррекция в виде баллонной вальвулопластики или митральной комиссуротомии.
Недостаточность аортального клапана
Изменения гемодинамики при этом пороке связаны с обратным током крови из аорты в левый желудочек в период диастолы из-за неполного смыкания створок аортального клапана. При ревматическом поражении клапана аорты створки его уплотняются, сморщиваются и в диастолу становится невозможным их полное смыкание. В левом желудочке происходит так называемая «тоногенная» дилатация его полости. Повышенная работа левого желудочка ведет к развитию гипертрофии миокарда, которая также как и дилатация являются в начальной стадии порока компенсаторным фактором. При прогрессировании порока высокое диастолическое давление в левом желудочке приводит к застою крови в левом предсердии и повышении в нем диастолического давления. Это, в свою очередь, ведет к формированию гипертензии в малом круге кровообращения. Застойные явления в легких вначале приводят к усиленной работе правого желудочка и далее к недостаточности правых отделов сердца и застою в большом круге кровообращения. При выраженной декомпенсации порока может возникнуть острая левожелудочковая недостаточность.
Клиника. На первом этапе компенсации порока (за счет усиленной работы левого желудочка), пациент жалоб не предъявляет, нет периферических симптомов. Объективно определяется некоторое усиление верхушечного толчка и небольшое расширение левой границы относительной сердечной тупости. Аускультативно в V точке выслушивается нежный, льющийся диастолический шум аортальной недостаточности.
В дальнейшем, при прогрессировании аортальной недостаточности, когда компенсация порока осуществляется главным образом за счет усиленной работы правого желудочка), у пациента возникают жалобы
281
на одышку (из-за гипертензии в малом круге кровообращения), сердцебиения, боли в области сердца сжимающего характера (недостаточность коронарного кровообращения). Из-за значительного уменьшения кровоснабжения головного мозга возникают выраженные головные боли, головокружения, обмороки. Возникают периферические симптомы: псевдокапиллярный пульс (симптом Квинке), высокий и быстрый пульс, феномен «бесконечного» пульса, над бедренной артерией определяется феномен двойного патологического шума Дюрозье. Кожные покровы бледные. При декомпенсации цвет кожи приобретает пепельный оттенок. Отмечается пульсация сонных артерий - «пляска каротид». Может появиться симптом Мюссе – ритмичное покачивание головой синхронно с пульсом. Верхняя граница артериального давления повышается, а нижняя граница падает вплоть до нуля. При этом на нижних конечностях систолическое артериальное давление (САД) может быть значительно выше, чем на нижних. Верхушечный толчок усилен, разлитой, смещен влево и вниз. Границы относительной сердечной тупости значительно расширены влево. Аускультативно: во II межреберье справа - диастолический шум аортальной недостаточности, может выслушиваться грубый систолический шум относительного стеноза аорты. На верхушке – систолический шум относительной недостаточности митрального клапана, иногда – диастолический шум Флинта.
Диагноз
Инструментальные методы исследования Рентгенография органов грудной полости - выявление «аорталь-
ной» конфигурации сердца, с подчеркнутой талией.
ДЭхоКГ - подтверждает диагноз недостаточности аортального клапана.
ЭКГ - отклонение ЭОС влево, признаки гипертрофии миокарда левого желудочка без его систолической перегрузки.
Прогноз. Отличительной способностью данного порока сердца является то, что порок у детей и подростков может быть длительно компенсированным, без возникновения жалоб. В более старшем возрасте, при появлении жалоб у пациента, без хирургического лечения продолжительность жизни может составить 3-5 лет. Протезирование аортального клапана проводится в более ранние сроки аортальной недостаточности; хорошие результаты хирургического лечения у 75% больных сохраняются до 10 лет.
Аортальный стеноз. При ревматизме изолированный стеноз аорты возникает крайне редко, чаще происходит присоединение стеноза
282
аорты к уже имеющейся недостаточности аортального клапана. Стеноз аортального клапана, как и недостаточность аортального клапана, в 3-4 чаще встречается у лиц мужского пола, чем у женского.
Гемодинамика. В результате сращения между собой полулунных створок аортального клапана в области комиссур, создается препятствие оттоку крови из левого желудочка в аорту во время систолы. Развивается концентрическая гипертрофия левого желудочка с незначительным расширением его полости, между аортой и полостью левого желудочка возникает градиент давления, который может достигать 50 мм. рт. ст. и более. Компенсаторно возникает удлинение систолы левого желудочка и брадикардия. Порок может оставаться компенсированным до 15-20 лет, из-за мощной сократительной способности гипертрофированного левого желудочка. Признаки коронарной недостаточности возникают задолго до развития сердечной недостаточности. При декомпенсации возникает снижение сократительной способности левого желудочка, его дилатация, недостаточность кровообращения в малом круге кровообращения, левожелудочковая сердечная недостаточность. При имеющейся выраженной левожелудочковой сердечной недостаточности, при значительном расширении фиброзного кольца митрального клапана возникает недостаточность митрального клапана, так называемая «митрализация» аортального порока, что еще в большей степени вызывает легочную гипертензию. С момента возникновения левожелудочковой недостаточности гибель пациента может наступить в течение 2-3-х лет из-за прогрессирования СН и/или развития фатальной аритмии.
Клиника. При данном виде порока долгое время у пациента отсутствуют жалобы. Они возникают при значительном сужении аортального устья: быстрая утомляемость, слабость при умеренной физической нагрузке, головокружение, обмороки при нагрузке или быстрой перемене положения тела, боли в сердце (из-за коронарной недостаточности), одышка, сначала при физической нагрузке, а затем в покое.
Объективно. Кожа бледная, так называемая «аортальная» бледность – из-за сниженного сердечного выброса и компенсаторной вазоконстрикторной реакции периферических сосудов. При выраженном стенозе аортального клапана пульс слабого наполнения и напряжения. АД: САД - понижено, ДАД – повышено, пульсовое давление – уменьшено. При усиленном сокращении левого желудочка у пациентов может наблюдаться «двойной» верхушечный толчок, в дальнейшем верхушечный толчок не только усилен, но и смещен влево и вниз. На основании сердца определяется систолическое дрожание; граница относительной сердечной тупости смещена влево. Аускультативно – тоны
283

сердца ослаблены, во II межреберье справа от грудины выслушивается грубый громкий систолический шум органического характера, проводится на сосуды шеи и спину. Иногда этот систолический шум приобретает «дистанционный» характер, по шкале Levin – 5 - 6 степени интенсивности, т.е. слышен на расстоянии от больного.
Диагноз
Инструментальные методы исследования ЭКГ – отклонение ЭОС влево, признаки гипертрофии левого желу-
дочка, иногда признаки полной или неполной блокады левой ножки пучка Гиса.
Рентгенография органов грудной полости: в стадии декомпенсации определяется «аортальная» конфигурация сердца, с выраженной талией сердца и постстенотическим расширением аорты, при легочной гипертензии – признаки застоя крови в легких по венозному и артериальному руслу.
ДЭХоКГ – выявляет все признаки, характерные для стеноза аорты. Прогноз. При тяжелом течении порока 25% больных умирают на первом году жизни (у взрослых). Неблагоприятными прогностическими признаками являются такие клинические проявления как, обмороки, боли в сердце ишемического характера, левожелудочковая недостаточность. При появлении этих признаков необходима хирургическая коррекция порока. При протезировании механическими клапанами необходим пожизненный прием антикоагулянтов, при протезировании биологическими протезами – повторная операция по замене клапана
показана через 12-15 лет.
Вопросы к экзамену. Ревматическая лихорадка. Этиология. Современ-
ные взгляды на патогенез заболевания. Значение неспецифического экссудативного компонента воспаления, определяющего остроту течения процесса. Основные критерии диагноза (Киселя-Джонса-Нестерова). Дополнительные критерии диагноза. Критерии активности ревматического процесса. Классификация ревматической лихорадки. Основные клинические проявления: кардит, полиартрит, хорея, аннулярная эритема, ревматические узелки. Острая ревматическая лихорадка. Острая ревматическая болезнь сердца. Клиническая картина. Диагностика. Дифференциальный диагноз. Течение. Исходы. Повторная ревматическая лихорадка. Хроническая ревматическая болезнь сердца. Клиническая картина. Диагностика. Дифференциальный диагноз. Течение. Исходы.
Экстракардиальные поражения при острой и повторной ревматической лихорадке. Клинические проявления. Диагностика. Течение. Этапное лечение ревматической лихорадки. Лечение острого периода. Особенности лечения хореи. Санаторное лечение. Первичная и вторичная профилактика ревматической лихорадки.
Приобретенные пороки сердца: недостаточность митрального клапана, стеноз левого атрио-вентрикулярного284отверстия, недостаточность аортального клапана, аортальный стеноз. Гемодинамические нарушения. Сроки формирования пороков. Клинические проявления. Диагностика. Прогноз.
ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА (ВПС)
Эпидемиология. ВПС выявляют у 5-8 детей на 1000 живорожденных.
Этиология. Установить конкретные причины формирования ВПС у ребенка чрезвычайно трудно. Формирование ВПС связывают с: заболеваниями хромосомного аппарата, неблагоприятными воздействиями факторов внешней среды, внутриутробными инфекциями, неблагоприятными воздействиями во время беременности (курение, алкоголь, наркотики, медикаменты, заболевания матери). Известно, что синдромальные причины при ВПС выявляется у 6-40% детей, а моногенная природа ВПС – у 8%.
Патогенез. Указанные выше факторы в периоде внутриутробного развития приводят к формированию патологических структур сердца, вызывая образование различных дефектов: отсутствие закрытия фетальных коммуникаций, гипертрофии или аплазии желудочков, дефекты клапанного аппарата, неестественные сужения сосудов и т.д. В большинстве случаев к моменту рождения гемодинамика существенно не страдает, и ее декомпенсация появляется через любое время после рождения.
Классификация
Табл. 1.84. Классификация врожденных пороков сердца (по
Marder с дополнениями (Мутафьян О.А. с соавт. ,2005г.))
Особенно- |
Без цианоза |
С цианозом |
|
сти гемоди- |
|
|
|
намики |
|
|
|
|
Дефект межжелудочковой |
Транспозиция магистраль- |
|
|
перегородки (ДМЖП), |
ных сосудов (ТМС), Глав- |
|
Обогаще- |
Дефект межпредсердной |
ный легочной ствол (ГЛС), |
|
перегородки (ДМПП), От- |
Общий артериальный ствол |
||
ние мало- |
крытый артериальный |
(ОАС), |
|
го круга |
проток (ОАП), Аномаль- |
Единственный (общий) же- |
|
кровооб- |
|||
ный дренаж легочных вен |
лудочек сердца (ЕЖС) |
||
ращения |
|||
|
(АДЛВ), Неполная атрио- |
|
|
|
вентрикулярная коммуни- |
|
|
|
кация (неполная АВК) |
|
|
|
|
|
285

Обеднение |
Изолированный стеноз |
Транспозиция магистраль- |
малого |
легочной артерии (ИСЛА) |
ных сосудов + стеноз легоч- |
круга |
|
ной артерии (ТМС +СЛА), |
кровооб- |
|
Тетрада Фалло (ТФ), Три- |
ращения |
|
|
|
куспидальная атрезия, Бо- |
|
|
|
|
|
|
лезнь Эбштейна, Общий |
|
|
артериальный ствол ложный |
|
|
(ОАС ложный) |
Препятст- |
Стеноз аорты (СА), |
|
вие кро- |
Коарктация аорты (КоА) |
|
вотоку в |
|
|
большом |
|
|
круге |
|
|
кровооб- |
|
|
ращения |
|
|
|
|
|
Без суще- |
Декстракардия, Аномалия |
|
ственных |
расположения сосудов, |
|
наруше- |
Сосудистое кольцо - двой- |
|
ний гемо- |
ная дуга аорты (ДДА), Бо- |
|
динамики |
лезнь Толочинова - Роже |
|
|
|
|
Степень легочной гипертензии: Iа, |
САД ЛА/САД Ао, в % |
|
Iб, II, IIIа, IIIб, IV |
До 30; Более 30; Менее 70; Бо- |
|
|
|
лее 70; Менее 100; Более 100 |
Фаза течения порока:
- первичной адаптации; относительной компенсации; терминальная.
Степень недостаточности кровооб- |
или функциональный класс |
ращения: 0, Iа, Iб, IIа, IIб, IIIа, IIIб |
(по NYHA) 0, 1, 2, 3, 4 |
Осложнения: дистрофия, анемия, рецидивирующая пневмония, ин-
фекционный эндокардит, тромбоэмболический синдром, нарушение ритма и проводимости
ВПС, при которых для поддержания жизни ребенка до хирургической коррекции нет необходимости поддерживать фетальную коммуникацию (открытый артериальный проток) называются дуктуснезависимыми, например: дефект межжелудочковой перегородки, дефект межпредсердной перегородки и др.
ВПС, при которых для поддержания жизни ребенка до хирургической коррекции (радикальной или гемодинамической) порока необходимо поддерживать фетальную коммуникацию (открытый артериальный проток) являются дуктус-зависимыми пороками сердца, к кото-
286
рым относятся: атрезия легочной артерии, тотальный аномальный дренаж легочных вен, критический стеноз аорты (клапанный, надклапанный и подклапанный), коарктация или перерыв дуги аорты, транспозиция магистральных артерий и др.
Лечение, задачи лечения: хирургическая коррекция анатомического дефекта, лечение недостаточности кровообращения, купирование и профилактика осложнений.
Схема лечения. Обязательные мероприятия: хирургическое лече-
ние ВПС, лечение недостаточности кровообращения. Вспомогательное лечение: оксигенотерапия, диета, режим, витами-
нотерапия, кардиотрофики, санация очагов хронической инфекции. Показания для госпитализации: необходимость углубленного об-
следования, декомпенсация ВПС, развитие жизнеугрожающих состояний (аритмии, легочная гипертензия).
Лечение недостаточности кровообращения. При развитии не-
достаточности кровообращения показано ограничение соли, покой. Медикаментозное лечение: сердечные гликозиды, мочегонные. Строфантин детям до 2-х лет назначаются в дозе насыщения 0,01 мг/кг, а детям старше 2-х лет - в дозе 0,007 мг/кг. Доза насыщения для коргликона детям до 2-х лет равна 0,013 мг/кг, а детям старше 2-х лет - 0,01 мг/кг. Поддерживающая доза для строфантина и коргликона равна разовой дозе. Доза насыщения для дигоксина детям до 2-х лет равна 0,06-0,07 мг/кг (внутрь) и 0,04 мг/кг (внутривенно). Детям старше 2-х лет доза насыщения равна 0,05-0,06 мг/кг (внутрь) и 0,03-0,04 мг/кг (внутривенно). Поддерживающая доза для дигоксина детям до 2-х лет составляет ¼-1/5 от дозы насыщения, а детям старше 2-х лет - 1/5-1/6.
Противопоказаниями для применения сердечных гликозидов являются брадикардия, АВ-блокада, желудочковая пароксизмальная тахикардия, анурия, коарктация и стеноз аорты, тетрада Фалло.
Допамин (с кардиотоническим эффектом) – 4 мкг/кг/мин и более в течение 4-48 часов и добутамин в дозе 2-10 мкг/кг/мин. При легочном сердце: оксигенотерапия, эуфиллин, блокаторы кальциевых каналов (верапамил, нифедипин, амлодипин), а при любой этиологии недостаточности – ингибиторы АПФ или антагонисты ангиотензина 2 (вальсартан, кандесартан). При задержке натрия и воды – мочегонные (альдактон, фуросемид, гипотиазид и др.).
При ВПС, сопровождающихся уменьшением легочного кровотока применяют: миотропные спазмолитики (дротаверин), β - адреноблокаторы (пропранолол, метопролол, бисопролол).
При недостаточности кровообращения показана оксигенотерапия через «усы» или носоглоточный катетер; при отеке легкого применяет-
287

ся оксигенотерапия в сочетании с пеногасителями.
Профилактика осложнений ВПС: 1) лечение хронической недоста-
точности кровообращения (дигоксин, мочегонные, вазодилататоры). Дозы и схемы препаратов подбираются в специализированном отделении;
2)лечение и профилактика респираторных заболеваний (ИРС-19, рибомунил, Бронхомунал, антибактериальные препараты);
3)лечение анемии (особенности при наличии анемии у детей с синими ВПС препаратами железа, меди, витаминами группы В, фолиевой кислотой для поддержания Hb на уровне 160 г/л и более);
4)обеспечение больных с синими ВПС в межприступном периоде достаточным объемом жидкости (1-1,5 литра), назначение обзидана по 0,5-1 мг/кг/сутки;
5)профилактика инфекционного эндокардита (ранняя диагностика
илечение инфекций у ребенка с ВПС, санация очагов инфекции, профилактическое назначение антибиотиков).
Вопросы к экзамену. Врожденные пороки сердца. Причины. Классифи-
кация. Понятие о дуктус-зависимых и дуктус-независимых пороках сердца.
Врожденные пороки сердца бледного типа
Дефект межжелудочковой перегородки (ДМЖП) – врож-
денный дефект перегородки, возникший вследствие недоразвития межжелудочковой перегородки (МЖП) на различных её уровнях, в результате чего формируется сообщение между левым и правым желудочками.
Эпидемиология. ДМЖП встречается в 1,5–3,5 случаев на 1000 доношенных новорожденных и в 4,5–7 случаях у недоношенных новорожденных. Среди ВПС частота ДМЖП составляет 15-20%. Перимембранозные (в мембранозной части перегородки) дефекты составляют примерно 80% всех ДМЖП. Мышечные дефекты составляют 5-20% изолированных ДМЖП.
Этиология. ДМЖП имеет мультифакториальное происхождение. Генетические факторы риска: высокая частота кардиальных аномалий в генеалогическом анамнезе у родителей. Материнские факторы риска: диабет, фенилкетонурия, алкоголизм матери.
288
Механизм формирования ДМЖП изучен недостаточно. Полагают, что перимембранозный дефект возникает изза нарушенного слияния отделов сердца вследствие транзиторного нарушения кровообращения в развивающейся перегородке; мышечные дефекты – следствие гибели клеток в перегородке.
Гемодинамика зависит от величины ДМЖП, количества, расположения,
Рис. 1.33. Схема ДМЖП продол-
жительности заболевания, степени легочной гипертензии, степени компенсаторной гипертрофии мио-
карда правого и левого желудочков сердца, соотношения сосудистых сопротивлений большого и малого кругов кровообращения.
После рождения, при малых дефектах (0,2–1,0 см) и физиологически высоком сопротивлении сосудов малого круга кровообращения, сброс крови слева-направо небольшой, и осуществляется только в систолу, легочный кровоток превышает системный только в 1,2–1,5 раза. Диастолическая перегрузка левого желудочка, вызывает его гипертрофию.
При средних и больших дефектах (2–3 см) величина сброса крови зависит от разницы сопротивлений в большом и малом кругах кровообращения. Обычно развивается гипертрофия левого желудочка. Повышение давления в левом предсердии и легочных венах благодаря нейрогуморальному механизму (рефлекс Китаева) ведет к спазму легочных сосудов, предохраняющего легкие от «затопления» их кровью. Увеличение легочного сосудистого сопротивления вызывает систолическую перегрузку правого желудочка. Правый желудочек, позже и правое предсердие гипертрофируются.
Анамнез, клиника. При малых дефектах МЖП физическое развитие ребенка не страдает. Систолический шум выслушивается при интеркурентных заболеваниях или случайно в III-IV межреберьях слева от грудины, иррадиирует вправо и влево от грудины, и на спину.
При средних и больших дефектах дети отстают в физическом раз-
витии, у них возникает гипотрофия; у большинства пациентов в анамнезе затяжные и рецидивирующие пневмонии, бронхиты. С первых недель жизни отмечаются признаки недостаточности кровообращения: затруднения при сосании, возникновение одышки, бледности, потливости (за счет выделения кожей задержанной жидкости), перорального цианоза.
289
У детей с большим ДМЖП (из-за гиперволемии малого круга кровообращения) возникает постоянная одышка, усиливающаяся при кормлении, плаче, перемене положения тела.
При физикальном обследовании визуально определяется сердечный «горб», за счет увеличения правого желудочка (грудь Дэвиса). Верхушечный толчок разлитой, усиленный, определяется патологический сердечный толчок, у 2/3 больных - систолическое дрожание в 3-4 межреберье слева от грудины, свидетельствующее о сбросе крови в правый желудочек. Границы относительной сердечной тупости расширены в обе стороны, особенно влево. Выслушивается грубый скребущего тембра интенсивный систолический шум, максимально в 3-4 межреберье слева от грудины и у мечевидного отростка. Характерна иррадиация шума влево и вправо от грудины и на спину. Спонтанное закрытие дефекта наблюдается часто у детей до года и значительно реже после двух лет.
Диагноз ДМЖП основывается на выявлении органического шума максимально в 3-4 межреберье слева от грудины и у мечевидного отростка, признаков недостаточности кровообращения, кардиомегалии, наличия рецидивирующих бронхолегочных заболеваний.
Лабораторные исследования ЭКГ. Определяется отклонение ЭОС вправо, признаки комбиниро-
ванной гипертрофии желудочков.
Рентгенологически выявляется гиперволемия по малому кругу кровообращения, увеличение размеров сердца за счет обоих желудочков и предсердий. Отмечается выбухание дуги легочной артерии по левому контуру сердца.
ДЭхоКГ. Двухмерная ДЭхоКГ с цветовым картированием позволяет определить размер и локализацию ДМЖП. С помощью допплерографии дополнительно получают гемодинамические показатели: давление в правом желудочке, давление в легочной артерии, межжелудочковый градиент.
Дифференциальный диагноз ДМЖП необходимо проводить с пороками, протекающими с обогащением малого круга кровообращения: с первичным ДМПП, АВК, ОАП с легочной гипертензией.
Лечение. Лечение недостаточности кровообращения проводится по общим принципам (см. выше).
Показаниями к хирургической коррекции порока являются сердеч-
ная недостаточность, задержка физического развития, повторные респираторные инфекции. В этих случаях операцию проводят, начиная с первого полугодия жизни. У детей старше года хирургическое вмеша-
290
тельство показано при соотношении легочного и системного кровотоков 2:1 и более.
При больших дефектах без сердечной недостаточности, но с повышением легочного артериального давления по данным допплерографии необходима как можно более ранняя радикальная операция в возрасте до 1-го года.
Проводится пластика заплатой из ксеноперикарда. В последние годы при мышечных, особенно множественных и в некоторых случаях при перимембранозных дефектах используется методика чрезкатетерного закрытия ДМЖП с помощью окклюдера Amplatzer.
Паллиативная операция по сужению легочной артерии проводится только в случае сопутствующих пороков и аномалий, затрудняющих радикальную коррекцию ДМЖП.
Осложнения. При средних и больших дефектах МЖП гиперволе-
мия малого круга кровообращения сопровождается компенсаторным спазмом сосудов легких и повышением давления в легочной артерии. Длительная легочная гипертензия и гиперволемия малого круга кровообращения приводит к морфологическим изменениям в стенке легочных артериол, сосудов мелкого и среднего калибра. Развивается хронический артериит, фиброз и склероз стенок сосудов, их запустевание. В конечной склеротической стадии легочной гипертензии происходит расширение ствола легочной артерии, давление в легочной артерии может превышать 60-70% от системного артериального давления. Давление в правом желудочке повышается и становится больше, чем в левом. Сброс крови через дефект становится перекрестным, а затем право-левым, развивается синдром Эйзенменгера – осложнение тер-
минальной фазы течения ДМЖП средних и больших размеров в перимембранозной части. Для него характерны:
-тяжелая легочная гипертензия с высоким общелегочным сопротивлением;
-веноартериальный сброс крови через дефект («смена шунта») с появлением цианоза;
-расширение ствола легочной артерии и запустевание периферических сосудов малого круга кровообращения; обеднение периферического легочного рисунка на рентгенограмме органов грудной полости
впрямой проекции («синдром ампутации»), выбухание дуги легочной артерии;
Клинически – исчезновение систолического шума и систолического дрожания в третьем-четвертом межреберьях слева от грудины; появление диастолического шума недостаточности клапана легочной артерии (шум Грехема–Стилла); акцент II тона на легочной артерией –
291

признак высокой легочной гипертензии. Появляются признаки хронической гипоксии - деформация фаланг пальцев («барабанные палочки») и ногтей («часовые стекла»).
При небольших дефектах в мышечной части МЖП сброс крови в правый желудочек небольшой и гемодинамической перегрузки малого круга кровообращения не наступает.
Осложнения после операции. Атриовентрикулярные блокады, блокады ножек пучка Гиса. Также возможна недостаточность трикуспидального клапана, реканализация дефекта, остаточная легочная гипертензия, инфекционный эндокардит.
Профилактика. При малых хирургических манипуляциях (удаление зуба, аденотомия, тонзиллэктомия) у непрооперированных больных и после паллиативной и радикальной коррекции порока проводится профилактика инфекционного эндокардита.
Вопросы к экзамену. Дефект межжелудочковой перегородки. Вариант
Толочинова-Роже. ДМЖП в мембранной части. Клинические проявления, сроки выявления. Гемодинамические осложнения порока (синдром Эйзенменгера). Диагностика. Показания к раннему паллиативному варианту хирургического лечения. Сроки проведения радикальной кардиохирургической коррекции порока.
Дефект межпредсердной перегородки (ДМПП) – врожден-
ное аномальное сообщение между двумя предсердиями. Эпидемиология. Частота ДМПП – 0,1-0,53/1000 новорожденных.
Преобладают пациенты женского пола (2:1). Среди всех ВПС ДМПП выявляется у 10-12%.
В зависимости от характера и степени недоразвития первичной и вторичной межпредсердных перегородок и эндокардиальных валиков, выделяют первичные, вторичные дефекты и полное отсутствие межпредсердной перегородки (единственное общее предсердие, трёхкамерное сердце).
Этиология. Первичный ДМПП возникает из-за недоразвития первичной межпредсердной перегородки и сохранения первичного сообщения между предсердиями; это, как правило, большой по размеру дефект (1/3-1/2 часть перегородки), который локализуется в нижней части перегородки. Данный порок наиболее часто сочетается с синдромом Дауна (трисомия 21).
Вторичный ДМПП возникает в результате недоразвития вторичной межпредсердной перегородки и в большинстве случаев находится в центре межпредсердной перегородки. Данный порок часто сочетает-
292
ся с клапанным стенозом легочной артерии. Изолированный вторичный ДМПП часто наследуется по аутосомно-доминантному типу.
Возможны комбинации первичных и вторичных ДМПП. В некоторых случаях происходит формирование единственного предсердия.
Открытое овальное окно (ООО) является межпредсердной коммуникацией, через него во время внутриутробного развития кровь из нижней полой вены направляется непосредственно в левое предсердие.
При рождении давление в левом предсердии выше, чем в правом, клапан овального окна прижимается к овальному окну и возникает его физиологическое закрытие. К концу первого месяца жизни ООО при недоразвитии клапана овального отверстия или его дефекте сохраняется у 7-3%, к году у 2%. ООО обнаруживается у 15% взрослых пациентов.
Гемодинамика. Основой нарушения гемодинамики является сброс крови через дефект слева-направо, из-за большего давления в левом предсердии, чем в правом. Это вызывает объемную перегрузку правого желудочка в диастолу и гиперволемию малого круга кровообращения. У детей раннего во з- раста направление шунта может легко меняться из-за преходящего повышения давления в правом предсердии (при
заболевании органов дыхания, крике, сосании) с возникновением преходящего цианоза.
Длительная объемная перегрузка правых камер сердца приводит к их дилатации и постепенному развитию умеренной гипертрофии правого желудочка.
При ДМПП легочная гипертензия развивается достаточно редко, так как отсутствует прямое влияние нагнетающего эффекта левого желудочка.
Анамнез, клиника. У детей с небольшим первичным дефектом
межпредсердной перегородки порок протекает бессимптомно и выявляется только по наличию шума. Физическое развитие детей нормальное, они занимаются спортом, удовлетворительно переносят нагрузки. Во втором десятилетии жизни могут появиться одышка после физической нагрузки, повышенная утомляемость, головокружения, обмороки. Легочная гипертензия и сердечная недостаточность формируются к 20 годам.
293
У грудных детей выслушивается небольшой систолический шум изгнания слева от грудины. В более старшем возрасте выслушивается расщепление II тона на легочной артерии и небольшой систолический шум во втором-третьем межреберье слева от грудины. Шум связан с функциональным стенозом легочной артерии, возникающим из-за увеличенного кровотока при неизмененном фиброзном кольце легочной артерии.
При большом или среднем по размеру первичном дефекте манифе-
стация порока возможна как в периоде новорожденности (одышка, тахикардия), так и в возрасте 1-2 лет. Отмечается бледность, гипотрофия, умеренное отставание в физическом развитии. Характерна склонность к частым ОРИ, бронхитам и пневмониям.
При осмотре выявляется кардиомегалия с расширением границ относительной сердечной тупости вправо и вверх, реже – влево. Возможна деформация грудной клетки в виде центрального сердечного горба из-за дилатации и гипертрофии правого желудочка. Аускультативно I тон усилен, II тон усилен и расщеплен над легочной артерией, систолический шум средней интенсивности и продолжительности выслушивается во втором-третьем межреберье слева от грудины. У детей старшего возраста дополнительно может выслушиваться короткий диастолический шум относительного стеноза трикуспидального клапана (шум Кумбса), в связи с увеличенным кровотоком через трикуспидальный клапан.
Дети со вторичным ДМПП не имеют клинической симптоматики. У подростков отмечается снижение толерантности к физическим нагрузкам.
У взрослых при ООО возможно формирование право-левого шунта при легочной гипертензии или при сочетании ООО с гипоплазией правого желудочка, со стенозом трикуспидального клапана. При этом через право-левый шунт может возникать парадоксальная эмболия сосудов головного мозга с развитием нарушений зрения, гемиплегией, нечленораздельной речью у больных с тромбозом глубоких вен или повышенной свертываемостью крови.
Первичный ДМПП не подвергается спонтанному закрытию. Спонтанное закрытие небольшого (чаще до 3 мм) вторичного дефекта межпредсердной перегородки возможно как у детей до 1 года, так и в более поздние сроки. ООО может спонтанно закрыться у детей до 2-х лет или может сохраняться в течение всей жизни без каких-либо симптомов заболевания.
Диагноз ДМПП устанавливается при наличии кардиомегалии, наличия систолического шума средней интенсивности и продолжитель-
294
ности во втором-третьем межреберье слева от грудины. В анамнезе частые бронхолегочные и простудные заболевания.
Лабораторные исследования ЭКГ. ЭОС отклонена вправо, признаки гипертрофии правого желу-
дочка, гипертрофия правого предсердия; у 2/3 больных – неполная блокада правой ножки пучка Гиса.
Рентгенологически выявляется усиление легочного рисунка. При больших дефектах в прямой проекции сердце увеличено за счет правого желудочка, талия сердца сглажена за счёт выбухания легочной артерии, в косых и левой боковой выявляется увеличение правых камер сердца.
ДЭхоКГ. Двухмерная ЭхоКГ выявляет перерыв эхосигнала в зоне межпредсердной перегородки, градиент давления между предсердиями; цветное допплеровское картирование определяет направление шунта.
Дифференциальный диагноз необходимо проводить с изолированным стенозом легочной артерии, триадой Фалло, ДМЖП, аномальным дренажом легочных вен, аномалией развития трехстворчатого клапана Эбштейна.
Очень часто возникает вопрос, есть ли отличия между открытым овальным окном (ООО) и ДМПП? В настоящее время детские кардиологи небольшие дефекты межпредсердной перегородки (до 5-6мм), локализующиеся в области овальной ямки обозначают как «ООО», а дефекты более 6мм или при других локализациях – как ДМПП.
Лечение. Показания к хирургической коррекции порока: сердечная недостаточность, отставание в физическом развитии, легочные заболевания. Гемодинамическое показание к операции – соотношение легочного кровотока к системному более чем 2:1. При эффективности консервативной медикаментозной терапии операцию можно отложить до 3-5-летнего возраста (максимально – до 8-10 лет).
Вторичные дефекты закрываются ушиванием; первичные ДМПП закрывают заплатой из аутоперикарда или синтетической ткани с использованием торакотомии и искусственного кровообращения. Эндоваскулярная пластика дефекта с помощью окклюдеров возможна только при вторичном ДМПП размером до 25-40 мм, вокруг которого имеется кайма перегородки, шириной до 10 мм.
Осложнения ДМПП появляются на склеротической стадии легочной гипертензии в виде синдрома Эйзенменгера (легочная гипертензия, с расширением ствола легочной артерии и сменой шунта справаналево, с появлением постоянного цианоза). Характерным для этого состояния является сочетание расширенного ствола легочной артерии
295

и формирование относительного функционального стеноза легочного клапана на фоне возросшего ударного объема правого желудочка. На поздних стадиях ДМПП с синдромом Эйзенменгера происходит дистрофия и склероз миокарда правого желудочка, что приводит к развитию сначала правожелудочковой, а затем тотальной сердечной недостаточности.
Осложнения после операции: острая сердечная недостаточность, нарушения ритма сердца, инфекционный эндокардит, резидуальный шунт.
Возможные осложнения при катетерной окклюзии дефекта: пер-
форация стенки сосуда, окклюзия сосуда, неполное закрытие дефекта, инфекционный эндокардит.
Вопросы к экзамену. Дефект межпредсердной перегородки. Гемоди-
намические нарушения. Сроки выявления. Клиническая картина. Лечение. Исходы.
Открытый артериальный проток (ОАП) – наличие ано-
мального сосудистого сообщения, при котором кровь из аорты поступает в легочную артерию.
Эпидемиология. Частота ОАП – 0,14-0,3/1000 живорожденных. Среди всех ВПС ОАП встречается в 6-7% случаев. ОАП страдают преимущественно девочки. В 5-10% ОАП сочетается с другими ВПС. В одних случаях он рассматривается как компенсирующий порок (при тетраде Фалло, стенозе легочной артерии, предуктальной коарктации аорты, атрезии аорты); в других случаях как порок, усиливающий г е- модинамические нарушения: при постдуктальной коарктации аорты, ДМЖП, ДМПП.
Этиология. В норме ОАП обеспечивает фетальное кровообращение. Обычно проток отходит от дуги аорты, дистальнее отхождения левой подключичной артерии и впадает в легочную артерию в области её бифуркации или вблизи места отхождения левой легочной артерии. Закрывается проток в первые 2 недели жизни. Если этого не происходит, говорят о пороке сердца.
У недоношенных детей формирование ОАП связано с незрелостью дуктальной ткани и повышенной концентрацией простагландинов. У доношенных детей это предположительно связано с хронической гипоксией, внутриутробной задержкой развития.
Гемодинамика. После первого вдоха и раскрытия легочных сосудов давление в легочной артерии быстро снижается при одновремен-
296
ном увеличении давления в большом круге кровообращения. Праволевый сброс крови резко уменьшается. По мере падения общего легочного сопротивления возникает двунаправленный, а затем левоправый поток крови через ОАП. У новорожденных «перекрестный» сброс крови может возникать при плаче, натуживании, сосании, из-за высокого давления в легочной артерии. В первые месяцы жизни левоправый сброс осуществляется только в систолу, в дальнейшем, когда и диастолическое давление в аорте превышает давление в легочной артерии, лево-правый шунт приобретает постоянный систолодиастолический характер, что приводит к той или иной степени легочной гиперволемии.
При длинном и узком протоке сброс крови небольшой, гиперволемия малого круга кровообращения умеренная. Развивается умеренная дилатация левого желудочка, длительно отсутствует легочная гипертен-
зия.
При коротком и широком протоке сброс крови значительный, что приводит к выраженной гиперволемии малого круга кровообращения. «Балластный» объем крови, циркулирующий в малом круге кровообращения, возвращаясь в левые отделы сердца, вызывает перегрузку объемом и дилатацию левого предсердия, левого желудочка и расши-
рение восходящей аорты. Эффективный ударный объем, поступающий на периферию большого круга кровообращения уменьшен на величину сброса в легочную артерию. Кровоток в аорте и большом круге кровообращения имеет «пульсирующий» характер, напоминает кровоток при недостаточности аортального клапана. В сонных артериях в систолу кровоток нормальный, а в диастолу существенно снижается, происходит «диастолическое обкрадывание» мозгового кровотока.
Анамнез, клиника.
При узких и длинных ОАП пациенты развиваются нормально до 5- 6-летнего возраста, когда впервые появляются жалобы и клиническая манифестация порока. Единственным проявлением ВПС у них является непрерывный систолодиастолический шум на основании сердца, с максимумом на легочной артерии. У детей раннего возраста шум может быть только умеренным систолическим.
297
При коротком и широком протоке клиническая симптоматика по-
является в первые месяцы жизни. Отмечается постоянная бледность кожных покровов, в результате синдрома «обкрадывания» большого круга кровообращения. При натуживании, кашле, крике, сосании появляется транзиторный цианоз.
Дети отстают в массе и в физическом развитии, у них часто развиваются рецидивирующие бронхиты и пневмонии. После 3-5 лет наблюдаются обмороки, боли в сердце, сердцебиение, одышка после физической нагрузки.
Область сердца может быть деформирована в виде левостороннего сердечного горба, верхушечный толчок, усилен, разлитой, приподнимающий. У некоторых детей на основании сердца пальпируется систолическое или систолодиастолическое дрожание; границы относительной сердечной тупости расширены влево и вверх.
При аускультации I тон громкий, II тон может быть перекрыт по интенсивности характерным непрерывным интенсивным (4-6 степени по шкале Levin), скребущим систолодиастолическим «машинным» шумом. Максимально шум выслушивается на основании сердца, проводится вдоль левого края грудины, иррадиирует на спину между верхним углом лопатки и позвоночником. При длительном существовании порока с большим сбросом может возникнуть диастолический шум на верхушке сердца из-за митрального стеноза.
Периферический пульс высокий, скачущий. Систолическое артериальное давление (САД) нормальное или повышено, за счет большого выброса в аорту. Диастолическое АД (ДАД) значительно снижено (феномен «бесконечного пульса») за счет одновременного тока крови в легочную артерию и нисходящую аорту, пульсовое АД значительно повышено. Характерна выраженная пульсация сонных артерий («пляска каротид») и сосудов ногтевого ложа («капиллярный пульс»).
Наиболее тяжелыми периодами течения порока являются фаза первичной адаптации порока у новорожденных детей, и терминальная фаза легочной гипертензии у детей старшего возраста, которые сопровождаются выраженной сердечной недостаточностью.
Продолжительность жизни при естественном течении порока 25–40 лет, к 45 годам умирают 42% больных, к 60-годам – 50–70% больных.
Диагноз. ОАП устанавливается при наличии грубого систолического, а затем систоло-диастолического шума во 2-3 межреберье слева, акцента 2 тона над легочной артерией, недостаточности кровообращения, снижение диастолического артериального давления.
Лабораторные исследования
298
ЭКГ. Отклонение электрической оси влево, признаки перегрузки левого желудочка, увеличение левого желудочка, нарушения обменных процессов в миокарде.
Рентгенологически: выявляется усиление легочного рисунка, соответствующее величине артериовенозного сброса, расширение или выбухание ствола легочной артерии. Талия сердца сглажена, увеличены левые отделы сердца.
ДЭхоКГ. При сканировании из высокого парастернального или супрастернального доступа визуализируется проток, направление шунта. По косвенным признакам судят о величине шунта.
Дифференциальный диагноз проводят с ДМЖП, неполной атриовентрикулярной коммуникацией, у старших детей - с сочетанным аортальным пороком.
Лечение. Специфическая консервативная терапия возможна только у недоношенных детей, путем внутривенного введения трех доз за 48 часов ингибитора синтеза простагландинов (индометацина в дозе 0,2; 0,1; 0,1 мг/кг). При отсутствии эффекта через 24 часа возможно дополнительное трехкратное введение препарата в дозе по 0,1 мг/кг с интервалом 24 часа. Результативность лечения – 70 - 80%.
Показанием к хирургическому лечению является наличие ОАП. У маленьких детей прибегают к клипированию сосуда. У старших детей производят перевязку сосуда. Оптимальные сроки операции – от 6-12 месяцев – до 3–5 лет. Послеоперационная летальность составляет менее 1%. Устранение порока проводится и эндоваскулярным методом – с помощью специальных спиралей (при диаметре протока до 3мм); при более крупных отверстиях (до 6 мм) применяют несколько спиралей или специальные окклюдеры.
Осложнения при ОАП. Длительная перегрузка малого круга кровообращения приводит к формированию легочной гипертензии, которая способствует формированию гипертрофии правого желудочка и правого предсердия, смене шунта на право-левый, артериальной гипоксемии, хронической правожелудочковой или тотальной сердечной недостаточности.
При небольших протоках возможно развитие бактериального эндокардита. Редко развивается такое осложнение как аневризма ОАП с её разрывом, тромбозом или инфицированием.
Послеоперационные осложнения: кровоизлияния, повреждения со-
судов, травмирование возвратного ларингеального и диафрагмального нервов, инфекционный эндокардит, застойная сердечная недостаточность.
299

Возможные осложнения транскатетерной окклюзии протока: остаточный шунт, миграция спирали, гемолиз и тромбоз бедренных сосудов, через которые проводился катетер.
Прогноз. После хирургической коррекции порока, при отсутствии осложнений, развитие таких детей нормальное.
У недоношенных детей с большим ОАП часто, в короткие сроки развивается бронхолегочная дисплазия.
Вопросы к экзамену. Открытый артериальный проток. Особенности
гемодинамических нарушений. Клинические проявления. Лечение. Сроки
ипоказания к хирургической коррекции. Прогноз.
Врожденные пороки сердца с препятствием к выбросу из желу-
дочков
Изолированный стеноз легочной артерии (ИСЛА) – ВПС,
при котором происходит обструкция выходного тракта правого желудочка.
Частота ИСЛА составляет - 8–12% от всех ВПС. В сочетании с другими пороками сердца ИСЛА встречается у более 50% всех детей с ВПС.
Различают три основных анатомических варианта порока:
1.Клапанный стеноз легочной артерии (наиболее частый вариант порока), при котором сужение клапана происходит из-за срастания створок по комиссурам. Клапан при этом имеет аномальное строение, например двустворчатый или диспластичный.
2.Подклапанный (инфундибулярный) стеноз выходного отдела правого желудочка. Сужение непосредственно под клапаном легочной
артерии образуется за счёт концентрической гипертрофии мышц выходного отдела правого желудочка или за счёт фиброзно-мышечной перегородки с отверстием различного диаметра.
3. Надклапанный (постклапанный) СЛА составляет 1,4% всех ИСЛА; его часто связывают с синдромом краснухи. После участка сужения часто возникает тонкостенный участок постстенотического расширения легочной артерии.
Гемодинамика. При сужении площади выходного отверстия до 10 мм2 или до 40% от должной величины порок протекает относительно удовлетворительно, без существенных нарушений гемодинамики.
300
При более выраженном сужении компенсаторно возникает гипертрофия правого желудочка и повышение давления в его полости. Повышение давления в правом желудочке вызывает относительную недостаточность трикуспидального клапана, повышение давления в правом предсердии, возникает возможность открытия овального окна. Через ООО происходит праволевый сброс крови, приводящий к
снижению насыщения кислородом артериальной крови.
Степень стеноза с возрастом относительно увеличивается в связи с ростом ребенка и увеличением полостей сердца. При длительном существовании ИСЛА гипертрофированный миокард правого желудочка диффузно склерозирован, нарушен коронарный кровоток.
Легочный кровоток существенно уменьшается при выраженных степенях стеноза и декомпенсации правого желудочка.
При критическом легочном стенозе выраженные нарушения гемодинамики наблюдаются сразу после рождения в виде правожелудочковой недостаточности и артериальной гипоксемии. Системный выброс существенно снижается при резко уменьшенном возврате крови к левым отделам. При открытом овальном окне системный выброс может сохраняться на удовлетворительном уровне.
Анамнез, клиника. Картина порока многообразна и зависит от степени стеноза и выраженности нарушений гемодинамики.
При небольшой обструкции у ребенка жалоб нет, физическое развитие не страдает, цианоз отсутствует. Патология сердца может проявляться только систолическим шумом, который выявляется случайно.
Выраженный стеноз проявляется рано, с жалоб ребенка на одышку и боли в сердце при физической нагрузке. Дети отстают в физическом развитии. У многих образуется правосторонний «сердечный горб»; во II межреберье слева от грудины определяется систолическое дрожание. Границы сердца расширены влево за счёт правого желудочка и вверх. II тон над легочной артерией не определяется; вдоль левого края грудины выслушивается грубый интенсивный систолический шум, с максимумом во втором межреберье слева от грудины, проводящийся на сосуды шеи и на спину. В последующем формируется правожелудочковая недостаточность, появляются симптомы «часовых стекол» и
301
«барабанных палочек». В некоторых случаях возникают головокружения и синкопальные состояния, связанные с аритмиями или ригидным сердечным выбросом в ответ на физическую нагрузку.
Критический легочный стеноз характеризуется ранней правожелудочковой недостаточностью (увеличенная плотная печень, отёки), одышкой, центральным цианозом, синдромом низкого сердечного выброса (угнетение ЦНС, холодные цианотичные конечности, метаболический ацидоз). Недостаточность кровообращения рефрактерна к медикаментозной терапии.
Диагноз ИСЛА устанавливается при выявлении грубого систолического шума изгнания во 2 межреберье слева, и правожелудочковой сердечной недостаточности.
Лабораторные исследования ЭКГ выявляет резкое отклонение ЭОС вправо, гипертрофию мио-
карда правого желудочка и правого предсердия, признаки нарушения коронарного кровотока в правом желудочке.
Рентгенологически при критическом стенозе выявляется обедненный легочный рисунок, при умеренном – он может быть не изменен. При стенозе без шунта (ООО) тень сердца расширена за счет гипертрофии правого желудочка и увеличенного правого предсердия. При клапанном стенозе из-за постстенотического расширения легочной артерии выбухает дуга легочной артерии. Кардиомегалия выявляется у больных, имеющих большой межсистемный сброс или недостаточность трикуспидального клапана.
ДЭхоКГ выявляет турбулентный кровоток на клапане легочной артерии, наличие градиента давления между правым желудочком и стволом легочной артерии. Определяется гипертрофия правого желудочка и межжелудочковой перегородки, нарушение открытия легочного клапана, утолщенные створки которого дугообразно выбухают в легочный ствол. На уровне межпредсердного сообщения возможен сброс справа налево.
Дифференциальный диагноз необходимо проводить с ДМПП, частичным аномальным дренажом легочных вен, триадой Фалло.
Лечение. Медикаментозное лечение малоэффективно. У новорожденных для поддержания легочного кровотока и оксигенации возможно использование простагландинов.
Показания к оперативному лечению порока:
- появление одышки и признаков правожелудочковой сердечной недостаточности при физических нагрузках;
302

- увеличение давления в правом желудочке до 70-80 мм рт. ст. и градиента давления между правым желудочком и легочной артерией до 40-50 мм рт. ст.
Оптимальным для проведения операции является ранний школьный возраст, хуже результаты операции получаются в возрасте до 3-х лет и после 15 лет. При критическом или выраженном стенозе операция сможет быть выполнена по экстренным показаниям уже в первые месяцы жизни. Операции на открытом сердце показаны при выраженной дисплазии клапана, наличии инфундибулярного стеноза, требующего резекции. У пациентов раннего возраста с «критическим стенозом» проводят чрезкожную транлюминальную баллонную вальвулопластику.
Осложнения обусловлены острой правожелудочковой недостаточностью, возникающей в результате неадекватного устранения стеноза. После операции возможно возникновение: рестенозирования легочной артерии, развития клапанной недостаточности легочной артерии.
Прогноз. Дети с легким и умеренным стенозом имеют благоприятный прогноз, стеноз у этих пациентов обычно не прогрессирует. У детей с тяжелым стенозом легочной артерии с возрастом отмечается прогрессирование порока.
В первые 6 месяцев умирают 4% больных, имеющих критическую обструкцию клапана, при естественном течении порока до 15 лет доживает 95% больных. Дальнейшее течение зависит от осложнений: инфекционного эндокардита, сердечной недостаточности.
Вопросы к экзамену. Стеноз легочной артерии. Гемодинамические на-
рушения. Клиническая картина. Диагностика. Лечение. Прогноз.
Стеноз аорты (СА) – ВПС, при котором нарушается отток крови из левого желудочка в большой круг кровообращения в результате наличия препятствия в выходном отделе левого желудочка (инфундибулярный подклапанный стеноз), на уровне клапана (клапанный стеноз), в восходящей части аорты (надклапанный стеноз).
Эпидемиология. Частота СА составляет 0,04-0,48/1000 новорожденных; 2-8% среди всех ВПС и 2,5% среди критических ВПС. Наиболее часто встречается клапанный стеноз (до 70% всех СА); реже – подклапанный (до 20%). Клапанный и надклапанный СА в 3 раза чаще встречаются у мальчиков.
Этиология. Клапанный СА образуется за счёт сужения клапанного кольца или за счёт сращения между собой по комиссурам створок аор-
303
тального клапана, который может быть трехстворчатым, двустворчатым и одностворчатым. При клапанном стенозе может возникнуть постстенотическое расширение аорты.
Подклапанный СА образуется фиброэластической мембраной или фибромышечным валиком, исходящим из межжелудочковой перегородки.
При надклапанном СА чаще встречается сужение аорты по типу «песочных часов», реже - диффузное сужение восходящей аорты на протяжении или сужение фиброзной диафрагмой. Постстенотического расширения аорты обычно не отме-
чается.
Гемодинамика. СА затрудняет выброс крови в аорту. В результате возникает компенсаторная гипертрофия левого желудочка; его усиленная работа создает градиент систолического давления на клапане; позволяющий сохранить достаточный выброс.
При выраженном и длительно существующем стенозе наряду с гипертрофией миокарда левого желудочка возникает дефицит коронарно-
го кровообращения, формируется эндомиокардиальный фиброэластоз. При распространении ишемии на папиллярные мышцы может развиться недостаточность митрального клапана. Турбулентный поток крови обусловливает фиброзирование аортального клапана и часто приводит к формированию аортальной недостаточности с формированием застойной сердечной недостаточности.
У новорожденных с критическим аортальным стенозом в первые дни после рождения может возникнуть синдром низкого сердечного выброса. При резком снижении артериального давления кровь поступает в большой круг кровообращения из легочных артерий через ОАП. Возникает центральный цианоз, симулирующий «синий» порок. При синдроме низкого сердечного выброса из-за отсутствия выраженной гипертрофии левого желудочка градиент давления на аортальном клапане бывает небольшим, что создает иллюзию небольшого стеноза.
Различают три степени СА:
- небольшой СА – градиент систолического давления менее 40 мм рт. ст., градиент среднего давления менее 20 мм рт. ст.;
304
-умеренный СА – градиент систолического давления до 75 мм рт. ст., градиент среднего давления до 50 мм рт. ст.;
-выраженный СА – градиент систолического давления более 75 мм
рт. ст., градиент среднего давления более 50 мм рт. ст.; Анамнез, клиника. Клинические признаки клапанного СА могут
проявиться в любом возрасте.
При небольшом СА порок может протекать бессимптомно и проявляться только систолическим шумом с максимумом во втором-третьем межреберье справа от грудины; который хорошо проводится на сосуды шеи.
При умеренном СА отмечается повышенная утомляемость, приступы сердцебиения, снижение толерантности к физическим нагрузкам.
При выраженном СА дополнительно появляются обморочные состояния (из-за нарушения периферического кровотока), боли в сердце, связанные с относительной коронарной недостаточностью гипертрофированного миокарда при интенсивной нагрузке. При СА возможна внезапная смерть из за острой коронарной недостаточности и аритмий.
Сердечная недостаточность долго не проявляется из-за хороших компенсаторных возможностей левого желудочка. Однако если она развилась, состояние больных и прогноз жизни резко ухудшаются, летальный исход возможен в пределах 2-3 лет.
Объективно – область сердца не изменена, границы относительной сердечной тупости в пределах возрастной нормы, т.к. развивается концентрическая гипертрофия левого желудочка (уменьшение объёма камеры сердца без её расширения). Пальпаторно: систолическое дрожание во втором межреберье справа от грудины при клапанном и надклапанном стенозе и в третьем-четвёртом межреберье слева – при подклапанном стенозе. Аускультативно – грубый «скребущего» характера систолический шум во втором межреберье справа от грудины при клапанном и надклапанном стенозе и в третьем-четвёртом межреберье слева – при подклапанном стенозе. Шум хорошо проводится на сосуды шеи.
Систолическое артериальное давление и пульсовое давление снижается по мере прогрессирования стеноза. В соответствии с этим снижается наполнение пульса. При надклапанном стенозе выявляется феномен асимметрии артериального давления между правой и левой руками более 10 мм рт. ст. При этом артериальное давление на правой руке значительно выше, чем на левой.
Диагноз СА устанавливается при наличии систолического дрожания во втором и в третьем-четвёртом межреберье справа от грудины,
305
грубого «скребущего» характера систолического шума во втором и в третьем-четвёртом межреберье слева межреберье справа от грудины.
Лабораторные исследования ЭКГ. При тяжелом клапанном СА выявляется:
-гипертрофия левого желудочка;
-систолическая перегрузка и перенапряжение миокарда левого желудочка по типу strain: депрессия сегмента ST более 2 мм в левых о т- ведениях и инверсия зубца Т.
Депрессия сегмента ST и зубца Т, возникающая или усиливающаяся при физической нагрузке, свидетельствует о развитии умеренного градиента давления между левым желудочком и аортой. При умеренных и легких стенозах ЭКГ обычно нормальная.
Рентгенологически при тяжелом СА и левожелудочковой сердеч-
ной недостаточности выявляется усиление легочного рисунка по венозному руслу. В прямой проекции сердце имеет характерную «аортальную» конфигурацию - хорошо выражена талия сердца, верхушка закруглена и приподнята над диафрагмой.
При клапанном СА по правовому контуру определяется постстенотическое выбухание восходящей аорты. Во 2-ой косой проекции определяется увеличение левого желудочка за счёт наслоения заднего контура сердца на позвоночник и расширение восходящей аорты.
ДЭхоКГ при клапанном СА выявляет выбухание створок в просвет аорты с турбулентным потоком крови через клапан.
При подклапанном СА выявляется фиброзная или фиброзномышечная обструкция выводного отдела левого желудочка.
При надклапанном СА определяется обструкция в виде «песочных часов» с уменьшением восходящего отдела аорты, при наличии фибромышечной диафрагмы, диаметр восходящего отдела аорты не изменен, в просвете сосуда определяется мембрана сразу над синусами Вальсальвы.
Ранним признаком развивающейся сердечной недостаточности является диастолическая дисфункция левого желудочка.
Дифференциальный диагноз проводят с КоА, СЛА, ДМЖП,
ДМПП, с гипертрофической кардиопатией – идиопатическим гипертрофическим субаортальным стенозом, с приобретенным стенозом аортального клапана.
Лечение. Показанием к операции являются:
- «критический» СА у детей раннего возраста с систолическим градиентом давления в системе «левый желудочек - аорта» более 80 мм рт. ст. (III стадия), с клиническими проявлениями левожелудочковой или тотальной сердечной недостаточности;
306
-выраженный стеноз с градиентом систолического давления от 50
–до 80 мм рт. ст. (II стадия) с жалобами на ангинозные боли в сердце, обмороками и синкопальными состояниями, возникающими при физической нагрузке.
У новорожденных при критическом СА проводят медикаментозную терапию, до стабилизации состояния (ИВЛ, мочегонные, допамин 6-8 мкг/кг/мин). При дуктус-зависимом кровообращении проводят инфузию простагландинов группы Е и далее баллонную дилатацию клапанного стеноза.
При клапанном СА баллонная вальвулопластика или вальвулотомия по комиссурам на открытом сердце являются паллиативными, т.к. после этого клапан часто становиться несостоятельным в плане его запирательной функции и со временем прогрессирует аортальная недостаточность. У 50-70% больных в дальнейшем проводится протезирование клапана.
При подклапанном СА проводится полная резекция фиброэластической мембраны, а при фибромышечном стенозе – резекция фиброзной ткани с частичной миотомией. При развитии аортальной недостаточности у пациентов в возрасте 10-21 года проводится протезирование аортального клапана.
При надклапанном СА проводится аортотомия и резекция места надклапанной обструкции. При диффузном сужении аорты проводится реконструктивная операция.
Осложнения до операции: прогрессивный стеноз устья коронар-
ных артерий; инфекционный эндокардит; внезапная смерть. Осложнения после операции: прогрессирование послеоперацион-
ной недостаточности аортального клапана, рестеноз, инфекционный эндокардит, недостаточность кровообращения, летальный исход операции при диффузном надклапанном сужении аорты, ятрогенный дефект межжелудочковой перегородки, атриовентрикулярный блок.
Прогноз. При легком и умеренном надклапанном стенозе жизненный прогноз благоприятный. При тяжелом надклапанном стенозе послеоперационная выживаемость составляет за 15 лет 85%.
При субаортальном стенозе внезапная сердечная смерть у неоперированных больных наблюдается у 2-10% больных. При естественном течении субаортального стеноза более, чем у 60% развивается аортальная регургитация. Субаортальный стеноз может вновь появиться после успешно проведенной хирургической резекции.
Поздняя послеоперационная смертность возникает при резидуальном субаортальном стенозе и повторных хирургических вмешательствах. Высокая частота рецидивов (10–50% за 10-летний период) наблю-
307

дается, если у пациента градиент субаортальной обструкции до операции превышал 50 мм рт. ст.; если возраст пациента менее 10 лет.
Вопросы к экзамену. Стеноз аорты. Гемодинамические нарушения.
Клиническая картина. Диагностика. Лечение. Прогноз.
Коарктация аорты (КоА) – ВПС при котором имеется сужение или полный перерыв аорты, наиболее часто в области перешейка, немного дистальнее отхождения левой подключичной артерии. В 2% случаев расположение КоА бывает в грудном отделе аорты на уровне диафрагмы или в брюшном отделе на уровне почек.
Эпидемиология. КоА встречается в 6-15% от всех ВПС, как изолированный порок, и в сочетании с другими ВПС (чаще всего с двустворчатым аортальным клапаном, аортальным стенозом, ДМЖП). КоА выявляется в 3–5 раз чаще у мальчиков. У каждого четвертого пациента с КоА имеется аномалия ЖКТ, мышечной, скелетной и мочевыделительной систем.
Этиология. Согласно гемодинамической теории КоА возникает в результате уменьшения потока крови через дугу и перешеек аорты.
Во внутриутробном периоде перешеек получает относительно меньшее количество крови. Нисходящая аорта получает кровь из правого желудочка через артериальный проток. Левый желудочек снабжает кровью восходящую аорту и брахиоцефальные артерии, и лишь небольшая часть крови поступает к перешейку.
Такие ВПС как ДМЖП, двустворчатый аортальный клапан, аортальный стеноз уменьшают левожелудочковый объём и также приводят к формированию КоА. Этим объясняется частое сочетание КоА с этими ВПС.
Если к 2,5-3 месяцам жизни ребенка диаметр перешейка не превысит 80% от диаметра нисходящей аорты на уровне диафрагмы, то это рассматривается как КоА.
По отношению к ОАП различают три варианта локализации КоА в области перешейка:
1.предуктальный – проксимальнее места отхождения ОАП;
2.юкстадуктальный – на уровне отхождения ОАП;
3.постдуктальный - дистальнее места отхождения ОАП.
При постдуктальной КоА протяженность участка сужения может быть чуть больше 1мм, в виде «песочных часов». При предуктальной КоА протяженность участка сужения чаще бывает 1-2 см, по типу г и- поплазии перешейка аорты.
308
Гемодинамика. Перегрузка левого желудочка при КоА развиваться постепенно или остро, что приводит к его гипертрофии. У 15-20% детей грудного возраста дополнительно развивается эндомиокардиальный фиброэластоз из-за гипертрофии желудочков с развитием относительной коронарной недостаточности и хронической ишемии миокарда. При остром развитии клиники КоА быстро развиваются застойные явления и шок.
При постепенном развитии КоА компенсаторно формируются артериальные коллатерали (подключичные, межреберные, внутренние грудные и др.). Коллатеральное кровообращение улучшает выживаемость больных.
В организме ребенка устанавливается два режима кровообращения: проксимальнее и дистальнее места сужения аорты.
Проксимальнее места сужения аорты возникает артериальная гипертензия. Повышается САД, ДАД и среднее гемодинамическое артериальное давление. Величина артериального давления может достигать 200 мм рт. ст. Это обусловлено не только механическим фактором – нарушением оттока крови из восходящей аорты, но и действием вазоренального фактора – активацией ренин-ангиотензин- альдостероновой системы на фоне почечной ишемии. Также активируется симпатическая нервная система, приводящая к увеличению числа сердечных сокращений и артериального давления. Повышается уровень вазопрессина, который способствует задержке свободной жидкости в организме и повышает ОЦК. Из-за перегрузки сопротивлением вслед за гипертрофией левого желудочка, возникает гипертрофия левого предсердия.
Дистальнее места сужения аорты устанавливается режим арте-
риальной гипотензии. САД в сосудах нижней половины тела и нижних конечностях становится равно или ниже, чем в сосудах верхних конечностей. Однако ДАД может быть повышенным во всех участках аорты, а пульсовое артериальное давление – уменьшенным. По мере взросления ребенка коллатеральные сосуды претерпевают изменения. Они становятся широкими, извитыми. Извилистость межреберных артерий приводит к деформации краёв нижних ребер (узуры). Возникают аневризмы аорты, подключичных артерий, сосудов головного мозга.
При сочетании КоА и ОАП изменения гемодинамики зависят от степени стеноза аорты, локализации и ширины ОАП.
При постдуктальной КоА создается высокий градиент давления между аортой и легочной артерией, что приводит к большому сбросу крови через ОАП и гиперволемии малого круга кровообращения. Бы-
309
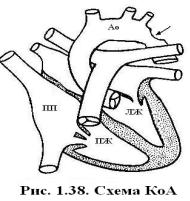
стро развивается лёгочная гипертензия. В этом случае также быстро развивается систолическая артериальная гипертензия. ДАД снижено из-за большого лево-правого шунта.
При предуктальной КоА и ОАП шунт лево-правый, также развивается гиперволемия малого круга кровообращения. Смена шунта на право-левый возможна при высокой лёгочной гипертензии и выраженной КоА. При этом развивается цианоз нижней половины туловища и нижних конечностей.
При сочетании КоА с ДМЖП сброс крови в правый желудочек большой и лёгочная гипертензия развивается быстрее и принимает злокачественный характер. САД в восходящей аорте длительно остается умеренно повышенным из-за уменьшения её кровенаполнения.
Сочетание КоА с фиброэластозом эндомиокарда сопровождается выраженной кардиомегалией за счёт дилатации и гипертрофии левого желудочка и левого предсердия, ранней, рефрактерной к терапии недостаточности кровообращения, нарушениями ритма сердца, тромбоэмболическими осложнениями.
Анамнез, клиника зависят от степени КоА, сопутствующих аномалий, сроков появления артериальной гипертензии, осложнений коарктации аорты. Кроме того, клиническая картина порока сильно различается у больных раннего воз-
раста и у более старших детей. Большинство детей с КоА рож-
дается с нормальной массой тела или с умеренной пренатальной гипотрофией. Рано появляются признаки сердечной недостаточности: быстрая утомляемость при кормлении, беспокойство, бледность. При гиперволемии малого круга кровообращения отмечаются рецидивирующие пневмонии. Одышка резко выражена, в легких выслушиваются стойкие мелкопузырчатые застойные хрипы. Верхушечный тол-
чок усилен, разлитой. Границы относительной сердечной тупости расширены в поперечнике. Второй тон усилен над легочной артерией, при сердечной недостаточности часто возникает трёхчленный ритм галопа. Шумовая симптоматика при КоА у грудных детей не характерна, особенно при сердечной недостаточности. Во втором-третьем
310
межреберье слева от грудины может выслушиваться систолический или систолодиастолический шум ОАП.
На радиальных, сонных и локтевых артериях пульс хорошего наполнения и напряжения, а на бедренных артериях и на сосудах тыла стопы у 2/3 больных пульсация резко ослаблена или отсутствует. Однако при дифференцированном цианозе пульс на ногах и бедренных артериях может быть лишь умеренно ослабленным (при выраженной предуктальной КоА и смене шунта на право-левый). САД на руках на 30-60% выше нормы, артериальное давление на ногах снижено.
У старших детей КоА часто обнаруживается случайно в школьном возрасте при измерении артериального давления. До выявления артериальной гипертензии дети обычно жалоб не предъявляют и развиваются в соответствии с возрастом. Характерны жалобы на боль и слабость в мышцах нижних конечностей, иногда на судороги в икроножных мышцах, особенно после интенсивных физических нагрузок связанные с синдромом артериальной гипотензии в нижней половине тела. При физической нагрузке также отмечаются сжимающие и колющие боли в сердце из-за коронарной недостаточности и ишемии гипертрофированного левого желудочка.
САД на верхних конечностях превышает возрастную норму на 3080% и значительно повышается после физической нагрузки. ДАД повышенно умеренно. Пульсовое давление значительно увеличено до 80100 мм рт. ст. Из-за артериальной гипертензии развивается ангиопатия сетчатки.
САД на ногах снижается на 20-40 мм рт. ст. и становиться меньше, чем на руках. ДАД остается нормальным, пульсовое давление значительно снижено. Верхушечный толчок резко усилен, приподнимающий. Границы относительной сердечной тупости умеренно расширены влево и вверх за счёт левого желудочка и левого предсердия. Второй тон над аортой усилен за счёт гипертензии в восходящей аорте. Выслушивается средней интенсивности систолический шум вдоль левого края грудины. Шум проводится на сосуды шеи и на спину между л е- вой лопаткой и позвоночником на уровне II-V грудных позвонков (т.е. на уровне КоА), особенно при задержке дыхания на выдохе.
Диагноз КоА устанавливается при выявлении артериальной гипертензии, снижении АД на нижних конечностях, наличии средней интенсивности систолического шума вдоль левого края грудины.
Лабораторные исследования ЭКГ выявляет признаки перегрузки левого желудочка с явлениями
его субэндокардиальной ишемии, отклонение ЭОС влево. Сочетание КоА с другими ВПС проявляется усилением гипертрофии левых или
311
правых отделов сердца в зависимости от характера порока и степени легочной гипертензии. Относительно часто выявляются признаки перегрузки левого или правого предсердий.
Рентгенологические признаки у детей старшего возраста включают узурацию нижних краев ребер. Сердце может иметь шаровидную конфигурацию с приподнятой верхушкой. У детей грудного возраста отмечаются признаки кардиомегалии, венозного застоя в легких. Сердце в основном имеет «аортальную» конфигурацию, но может быть и овоидной формы.
ДЭхоКГ визуализирует область сужения аорты, определяет градиент давления в участке сужения сосуда, выявляет сопутствующие сердечные аномалии.
Дифференциальный диагноз КоА проводят с гипертрофической кардиомиопатией, артериальной гипертензией, клапанным стенозом аорты.
Лечение. Основным показанием к операции у грудных детей является наличие КоА с недостаточностью кровообращения. До операции проводится терапия дигоксином, при низком сердечном выбросе – допамином, при застойной сердечной недостаточности – диуретиками. У новорожденных с предуктальной КоА применяют простагландины группы Е для сохранения открытого артериального протока.
У детей старшего возраста до операции артериальную гипертензию корригируют β-адреноблокаторами. Постоперативная гипертензия устраняется путем в/в введения нитропруссида или β- адреноблокаторов - эсмолола. Многие пациенты после операции нуждаются в продолжении гипотензивной терапии несколько месяцев или лет ингибиторами АПФ, иногда в комбинации с β-адреноблокаторами.
Операция заключается в резекции суженного участка аорты с анастомозом конец-в-конец.
Осложнения. КоА является «пожизненным» заболеванием, осложнения могут наблюдаться как до операции, так и через много лет после хирургического лечения. Наиболее частые осложнения: рекоарктация аорты, аневризма аорты, мозговые аневризмы с разрывом и высокой смертностью, паралич, гипертрофическая кардиомиопатия у новорожденных детей с критическим сужением аорты, аритмии, инфекционный эндокардит.
Прогноз. Изолированная КоА приводит к смерти у более 40% детей в течение первого года жизни. При сочетании КоА с другими ВПС умирают до 90% детей, несмотря на медикаментозную терапию. Основные причины смерти – недостаточность кровообращения и почечная недостаточность.
312

У детей, у которых не была выполнена хирургическая коррекция порока средняя продолжительность жизни составляет 35 лет. Меньше, чем 20% без хирургической коррекции доживает до 50 лет. Факторы, которые влияют на смертность: возраст пациента, масса тела, наличие или отсутствие значимых сердечно-сосудистых аномалий, артериальная гипертензия, внутричерепные кровоизлияния, разрыв или расслоение аортальной стенки, инфекционный эндокардит, застойная сердеч- но-сосудистая недостаточность.
Если КоА устранена хирургическим путем в возрасте до 14 лет, то 20-летняя выживаемость составляет 91%; если – после 14 лет – 79%.
После хирургической коррекции КоА 97–98% пациентов имеют СН I степени (I ФК по NYHA), так как у них наблюдается нарушенная диастолическая функция и гипертрофия левого желудочка, несмотря на хорошие гемодинамические показатели в покое.
Во время беременности у женщин с неоперированной КоА высокий риск осложнений как у матери так и у плода. Материнская смертность составляет в этих случаях 3–8%.
Даже, если КоА была своевременная устранена, у беременной сохраняется высокий риск расслоения аорты, разрыва церебральных аневризм в третьем триместре беременности из-за гемодинамических и гормональных изменений в этот период.
Все беременные женщины, у которых в анамнезе была КоА, представляют собой группу риска по течению беременности. Наличие значительной КоА, в том числе резидуальной или повторной, является противопоказанием к беременности.
Вопросы к экзамену. Коарктация аорты. Гемодинамические наруше-
ния. Клиническая картина. Диагностика. Лечение. Прогноз.
Полная транспозиция магистральных сосудов (ПТМС) –
ВПС, при котором аорта отходит от морфологически правого желудочка и несёт венозную кровь к тканям организма, а легочная артерия отходит от морфологически левого желудочка и несёт артериальную кровь к лёгким.
Эпидемиология. Частота ПТМС составляет 12-20% среди всех ВПС, и 23% среди критических ВПС. ПТМС чаще обнаруживается у мальчиков. С большой частотой ПТМС сопутствуют ДМЖП, стеноз легочной артерии, аномалии коронарного кровообращения.
313
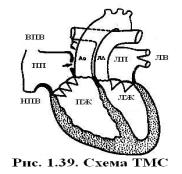
Гемодинамика. Во внутриутробном периоде, в отсутствии функционирования малого круга кровообращения ПТМС практически не влияет на развитие плода. Ребенок рождается в срок, с хорошим весом.
После рождения, при данном пороке аорта, отходящая от правого желудочка, несёт венозную кровь, которая, пройдя системный круг, возвращается через полые вены в правое предсердие. Артериальная
кровь лёгочной артерии, отходящей от левого желудочка, пройдя через лёгкие, возвращается в левое предсердие. Большой и малый круг кровообращения разобщены. В большом круге кровообращения постоянно циркулирует кровь с низким содержанием кислорода, а в малом круге кровообращения – с высоким. Жизнь возможна при наличии коммуникаций между ними: ОАП, ДМЖП, ДМПП. Шунтирование крови при ТМС всегда двухстороннее. При рождении в связи с падением лёгочного сосудистого сопротивления происходит веноартериальный сброс крови через ОАП. Резко возрастает объём циркулирующей крови в малом круге кровообращения, что приводит к сбросу крови слева направо через ДМПП. Двунаправленный сброс крови происходит при наличии ДМЖП: справа налево - во время систолы и слева направо – во время диастолы. При сопутствующем стенозе лёгочной артерии или высокой лёгочной гипертензии шунтирование через ДМЖП происходит в другом порядке: слева направо – в систолу и справа налево – в диастолу. Значительная гиперволемия малого круга кровообращения возникает при большом диаметре ОАП или ДМЖП. При наличии ДМЖП у больных с ПТМС высокая лёгочная гипертензия развивается быстрее (уже к 3-4месяцам), чем при бледных пороках с обогащением малого круга кровообращения и быстро приобретает склерозирующий характер.
Компенсаторно у пациентов с ПТМС развивается полицитемия, полиглобулия, коллатеральное кровообращение через бронхиальные сосуды лёгких, увеличивается объём циркулирующей крови. В связи с тем, что правый желудочек функционирует в режиме большого круга кровообращения, против высокого периферического сопротивления в аорте, он значительно гипертрофируется. Гипертрофия левого желудочка наступает позже из-за увеличенного легочного кровотока и перегрузки объёмом. Более быстрая и выраженная гипертрофия левого
314
желудочка наступает при сопутствующем стенозе лёгочной артерии. Однако все эти механизмы не могут компенсировать выраженной артериальной гипоксемии и гипоксии.
У больных с ПТМС существует резкий контраст между газовым составом крови в легочных венах и аорте. В крови, оттекающей от легких рО2 составляет 100-110 мм рт. ст., рСО2 – 15-25 мм рт. ст. В большого круга кровообращения рО2 крови составляет 35–37 мм рт. ст., рСО2 – около 45 мм рт. ст. Поэтому уже через несколько часов после рождения ребенка развивается дефицит кислорода, возрастают анаэробный метаболизм и продукция лактата, истощаются запасы гликогена. Развиваются метаболический ацидоз и нарушения функции клеток.
Анамнез, клиника. ПТМС, проявляется уже в роддоме цианозом. Тяжесть цианоза зависит от количества коммуникаций. Самый тяжёлый цианоз («чугунный») отмечается при наличии только ООО. Быстро прогрессирует гипотрофия и отставание в физическом и психомоторном развитии. Появляются признаки хронической гипоксии – изменения концевых фаланг пальцев и ногтей («барабанные палочки» и «часовые стёкла»). Кардиомегалия развивается к месячному возрасту из-за гипертрофии и дилатации правого желудочка. Границы сердца расширены в поперечнике. У более старших детей развивается центральный сердечный горб. Определяется систолическое дрожание. I тон на верхушке громкий, II – акцентирован, особенно при ДМЖП. Шум проявляется не всегда в первые дни жизни, и соответствует по топике сопутствующей коммуникации. При ТМС с ДМЖП и подклапанным стенозом лёгочной артерии, так же как и при тетраде Фалло, могут наблюдаться гипоксемические кризы. Генез этих кризов, как и при тетраде Фалло, связан со спазмом мышц выходного отдела левого желудочка, при котором резко нарушается и без того сниженный легочный кровоток и усиливается гипоксемия. Развивается ранняя рефрактерная сердечная недостаточность.
Диагноз ПТМС основывается на выявлении у ребенка с цианозом и недостаточностью кровообращения кардиомегалии, органических шумов различной локализации (компенсирующие ВПС).
Лабораторные исследования ЭКГ: ЭОС отклонена вправо. Отмечаются признаки гипертрофии
правого желудочка и правого предсердия. При наличии ДМЖП и ОАП
– определяются признаки гипертрофии левого желудочка. Рентгенологически при ПТМС легочный рисунок чаще всего уси-
лен по артериальному руслу, особенно при ТМС в сочетании с ДМЖП и ОАП. Определяется кардиомегалия (по форме сердце чаще напоми-
315
нает «яйцо, лежащее на боку»). Сосудистый пучок в переднезадней проекции узкий, в боковой – широкий. При сочетании ТМС с ДМЖП и подклапанным стенозом легочной артерии лёгочный рисунок обеднён. Оба желудочка увеличены, однако кардиомегалия менее выражена, чем при большом ДМЖП и гиперволемии малого круга кровообращения.
ДЭхоКГ выявляет аорту, отходящую от правого желудочка и лёгочную артерию, отходящую от левого желудочка. Нередко обнаруживаются сопутствующие аномалии: ДМЖП, ОАП, стеноз легочной артерии, аномалии коронарного кровообращения.
Дифференциальный диагноз необходимо проводить с тетрадой Фалло, атрезией лёгочной артерии, общим артериальным стволом, тотальным аномальным дренажом лёгочных вен.
Лечение ПТМС на первом этапе направлено на предупреждение закрытия ОАП, особенно при ТМС с ДМЖП и обструкцией выводного тракта левого желудочка (проводится инфузия простагландина Е1). Также важно корригировать метаболический ацидоз и анемию, сердечную недостаточность, объем циркулирующей крови.
У новорожденных с выраженной гипоксемией проводится паллиативная операция под контролем ультразвука – закрытая атриосептостомия с помощью специального баллона (процедура Рашкинда) для увеличения межпредсердного сообщения. В случаях ригидной межпредсердной перегородки возможно применение ножевой атриосептостомии или дилатация отверстия баллоном высокого давления. Показанием для радикальной оперативной коррекции является сам порок с выраженной гипоксемией.
К вмешательствам, полностью устраняющим гипоксемию, относятся операция анатомической коррекции порока (артериальное переключение с реимплантацией венечных артерий, операция Жатене) и операция Мастарда и Сеннинга (предсердное переключение или гемодинамическая коррекция) в пределах первого месяца жизни. При наличии ДМЖП или лёгочного стеноза нагрузка на левый желудочек сохраняется. Поэтому анатомическая коррекция с закрытием ДМЖП возможна и в более поздние сроки (в 3-6 мес.).
Операция по предсердному переключению заключается в том, что в условиях искусственного кровообращения и регулируемой гипотермии проводится атрисептопластика. При этом создается канал для дренирования крови из легочных вен и коронарного синуса через трикуспидальный клапан в правый желудочек, а крови из полых вен через митральный клапан – в левый желудочек, переводя ПТМС в корригированную.
316

У детей более старшего возраста с ДМЖП и выраженным легочным стенозом выполняют операцию Растелли. Коррекция заключается в том, что создается внутрисердечный «туннель» для оттока крови из левого желудочка в аорту и имплантируется кондуит между правым желудочком и лёгочным стволом.
Осложнение. После гемодинамической коррекции (предсердное переключение) системным остаётся правый желудочек. При данном типе операции не бывает долговременного хорошего результата. В условиях высокого давления насосная функция правого желудочка постепенно снижается, нарушается функция трикуспидального клапана, и при этом часто возникают нарушении ритма.
Прогноз. 30% детей с ПТМС умирают на первой неделе, 50% - в периоде новорожденности и 90% - в течение первого года жизни, до двух лет доживают не более 7% больных. При сочетании ПТМС с большим ДМЖП и умеренным стенозом лёгочной артерии (что является наилучшей корригирующей комбинацией), при естественном течении порока больные доживают до 4-5 лет. Основными причинами смерти являются тяжёлая гипоксия и ацидоз, сердечная недостаточность, застойно-бактериальные пневмонии.
Вопросы к экзамену. Транспозиция магистральных артерий. Анатоми-
ческие варианты порока. Гемодинамические нарушения. Сроки выявления. Клиническая картина. Диагностика. Сроки хирургического лечения.
Врожденные пороки сердца с цианозом
Тетрада Фалло (ТФ) – многокомпонентный ВПС, включающий в себя стеноз выводного отдела правого желудочка, ДМЖП, декстрапозицию аорты и гипертрофию правого желудочка.
Эпидемиология. Частота ТФ составляет 11-13% среди всех ВПС по клиническим данным, и 4% среди критических ВПС. ТФ входит в десятку наиболее распространённых ВПС. В 40% случаев ТФ сочетается с другими сердечными аномалиями.
Этиология. В основе нарушений эмбриогенеза лежит ротация артериального конуса против часовой стрелки и смещение конусной перегородки вперед и влево. Это не позволяет соединиться аорте с межжелудочковой перегородкой (МЖП) и формирует ДМЖП, а устье аорты оказывается расположенным над МЖП («сидящая верхом» над перегородкой аорта). Кроме того, смещение конусной перегородки вперёд и влево приводит к сужению и обструкции выходного тракта правого желудочка.
317
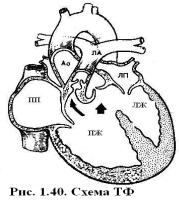
Декстрапозиция аорты при ТФ является не истинной, а вторичной и рассматривается как смещение её устья вправо по отношению к межжелудочковой перегородке. При этом фактически аорта часто отходит не только от левого, но и правого желудочка.
Гипертрофия правого желудочка формируется как компенсаторный механизм из-за систолической перегрузки сопротивлением.
Гемодинамика. Из четырёх компонентов порока определяющим является степень стеноза выходного отдела правого желудочка. Наиболее частым вариантом обструкции правого желудочка выявляется изолированный инфундибулярный стеноз. Реже отмечается сочетание инфундибулярного стеноза и клапанного стеноза лёгочной артерии. Стенозирование легочной артерии расценивается как умеренное при уменьшении диаметра устья лёгочной артерии и её ствола менее 80% диаметра устья аорты.
При уменьшении этих параметров менее 50% диаметра аорты – как тяжёлый стеноз.
При умеренной выраженности стеноза, из-за малого сопротивления кровотоку сосудов лёгких, кровь из правого желудочка поступает в лёгочную артерию и не сбрасывается в аорту и в левый желудочек через ДМЖП. На начальных этапах течения порока из-за более высокого давления в левом желудочке возможен лево-правый сброс крови через ДМЖП. По мере роста ребенка на первом году жизни, увеличения размеров камер сердца и ударного объёма крови, значительно возрастает относительная степень стеноза лёгочной артерии. Это приводит к существенной систолической перегрузке сопротивлением правого желудочка, и он гипертрофируется. При большом ДМЖП систолическое внутрижелудочковое давление в нём сравнивается с давлением в левом желудочке. К 6 -10 месяцем жизни сначала появляется транзиторный сброс крови справа налево (при крике, натуживании, сосании), а затем формируется постоянный право-левый шунт с развитием артериальной гипоксемии. Величина шунта в зависимости от степени стеноза может составлять от 30% до 80% минутного объёма малого круга кровообращения. При этом развивается гиповолемия малого круга кровообращения. Левое предсердие из-за недогруженности малого круга кровообращения гипоплазировано.
318
В фазе первичной адаптации при значительном стенозе лёгочной артерии, выживаемость детей зависит от наличия ОАП, через который кровь из аорты поступает в малый круг кровообращения и степени развития коллатерального кровообращения.
При ТФ существует также и гемическая компенсация артериальной гипоксемии за счёт высокой полицитемии (эритроцитемии) и увеличения содержания гемоглобина.
При физической нагрузке увеличивается минутный объем кровотока и венозный возврат крови к правому желудочку, что ещё больше увеличивает степень относительного стеноза и способствует большему сбросу крови справа налево через шунт. Это приводит к усилению гипоксемии.
При длительном существовании некорригированного порока из-за высокого давления в правом желудочке и дистрофических изменений в миокарде (обычно после 3-6 лет) возможно развитие сердечной недостаточности.
Анамнез, клиника. На внутриутробное развитие плода ТФ не оказывает существенного влияния, дети рождаются с нормальной длиной и массой тела. В первые 4-6 недель у них нет ни цианоза, ни отдышки, сосание и прибавка в массе тела удовлетворительные. Первым признаком порока может быть систолический шум легочного стеноза или шум незаращенного ОАП. После 6-8 недель появляются одышка и бледность при сосании и плаче. Цианоз вначале транзиторный, после года цианоз быстро нарастает и у 60-70% больных становится постоянным и тотальным. Его интенсивность варьирует от бледнофиолетового до сине-малинового или чугунно-синего. Цианоз не связан с недостаточностью кровообращения, а обусловлен повышенным содержанием в артериальной крови восстановленного гемоглобина.
Хроническая гипоксия органов приводит к их дисфункции, отставанию в физическом и умственном развитии. У большинства больных имеются изменения концевых фаланг конечностей в виде «барабанных палочек» и ногтей в виде «часовых стёкол». Также часто встречаются нарушения со стороны костно-мышечной системы: уплощение грудной клетки, сколиоз, неправильный рост зубов, слабо развитая мышечная масса.
При физикальном обследовании пульс удовлетворительного наполнения, САД умеренно снижено. Во втором-третьем межреберье пальпируется систолическое дрожание, возможна эпигастральная пульсация. Границы сердца могут быть умеренно расширенными в поперечнике. Первый тон не изменен, второй тон ослаблен над лёгочной артерией (из-за гиповолемии малого круга кровообращения). Во
319
втором-третьем межреберье слева выслушивается грубый, скребущий систолический шум лёгочного стеноза. Шум проводится на сосуды шеи и в межлопаточное пространство.
Шум ДМЖП в третьем-четвёртом межреберье слева от грудины может быть очень умеренным или вообще не выслушиваться из-за малого градиента давления между желудочками. На спине в межлопаточном пространстве может выслушиваться систолодиастолический шум коллатерального кровотока.
Характерным клинико-гемодинамическим синдромом при ТФ яв-
ляется одышечно-цианотический приступ. Первые приступы возника-
ют на 3-6 месяце жизни, и учащаются к 1-3 годам. Внезапно, после физической или эмоциональной нагрузки возникает резко выраженная одышка (до 70-80 в 1 минуту у детей младшего возраста), усиливается тотальный тёмно-фиолетовый цианоз. Возможно развитие комы и судорог.
Приступы различны по тяжести и продолжительности – от 10-15 секунд до 2-3 мин и обычно спонтанно прекращаются. После приступа больные жалуются на резкую слабость. Иногда отмечаются нестойкие гиперкинезы. В редких случаях могут быть тяжелые нарушения мозгового кровообращения и летальный исход.
Генез приступов связывают с мышечным спазмом в инфундибулярном отделе правого желудочка, который приводит к почти полной обструкции выходного тракта и сбросу всей венозной крови через ДМЖП и резчайшей гипоксемии. К 4-6 годам частота и интенсивность приступов уменьшается или они полностью исчезают.
Диагноз ТФ устанавливается у детей с тотальным цианозом, оды- шечно-цианотическими приступами и выслушиванием шумов в сердце органического характера.
Лабораторные исследования ЭКГ. ЭОС отклонена вправо. Признаки гипертрофии правого же-
лудочка, а затем правого предсердия.
Рентгенологически при ТФ определяется форма сердца в виде «деревянного башмачка». Сердце, как правило, небольших размеров из-за отсутствия дилатации полостей. Лёгочный рисунок обеднён.
ДЭхоКГ позволяет выявить ДМЖП, смещение аорты, стеноз лёгочной артерии, степень его выраженности, увеличение толщины межжелудочковой перегородки и передней стенки правого желудочка. При ДЭхоКГ обнаруживается турбулентный поток крови через ДМЖП и в лёгочной артерии, градиент давления между правым желудочком и лёгочной артерией.
320
Дифференциальный диагноз необходимо проводить с атрезией лёгочной артерии, общим артериальным стволом, аномалией Эбштейна, единственным желудочком сердца, двойным отхождением магистральных сосудов от правого желудочка.
Лечение при ТФ направлено на коррекцию гипотрофии, анемии, улучшение реологических свойств крови (назначение антиагрегантов и антикоагулянтов). При одышечно-цианотическом приступе проводят оксигенотерапию, подкожно вводят кордиамин, промедол, капельно трансфузию «поляризующей смеси», при судорогах – ГОМК; при развитии гипоксической комы – анаприлин. Для профилактики гипоксических приступов назначают β-адреноболкаторы (обзидан, индерал, анаприлин). При некупирующемся одышечно-цианотическом приступе экстренно проводят паллиативную операцию – наложение систем- но-лёгочного анастомоза.
Радикальную операцию, как правило, выполняют в сроки от 6 месяцев до 3-х лет. Цель операции – закрыть ДМЖП и устранить обструкцию выходного отдела правого желудочка. Некоторые кардиохирурги прибегают к радикальной операции до 3-6 месяцев, независимо от симптоматики.
Осложнения. При ТФ возможны такие осложнения как абсцесс головного мозга, кровоизлияние в головной мозг, бактериальный эндокардит.
Осложнения радикальной операции: остаточный стеноз лёгочной артерии, реканализация ДМЖП, нарушения ритма и проводимости, в том числе внутрижелудочковые (полная блокада правой ножки пучка Гиса, частичная блокада левой ножки пучка Гиса). При развитии полной АВ-блокады – проводится имплантация электрокардиостимулятора.
Прогноз. Средняя продолжительность жизни неоперированных больных с ТФ –12 лет. На первой неделе жизни погибают около 6% больных; к концу первого года жизни – до 25%; к 40 годам – 95%. В старшем возрасте основные причины смерти - сердечная недостаточность, аритмии, внезапная смерть. Паллиативные операции хоть и удлиняют продолжительность жизни, однако не улучшают прогноз.
После радикальной операции, проведенной без послеоперационных осложнений, прогноз у пациентов удовлетворительный. Послеоперационная выживаемость к 36 годам составляет 85%.
321

Вопросы к экзамену. Тетрада Фалло. Анатомические составляющие
порока. Гемодинамические нарушения. Сроки выявления. Клиническая картина. Причины отсутствия сердечной недостаточности. Изменения показателей периферической крови. Диагностика. Сроки выявления цианоза. Лечение. Купирование одышечно-цианотических приступов. Показания к кардиохирургической коррекции.
Атрио-вентрикулярная коммуникация, открытый атриовен-
трикулярный канал (АВК) – ВПС, составными компонентами которого являются первичный дефект межпредсердной перегородки, расщепление створок митрального и трикуспидального клапанов, дефект межжелудочковой перегородки.
Порок может быть частичным и полным. При полной АВК определяются оба септальных дефекта и единый атриовентрикулярный клапан. При частичной АВК – первичный ДМПП с разделенными отверстиями для митрального и трикуспидального клапанов, которые сформированы на одном уровне (в норме трикуспидальный клапан смещён верхушке сердца). АВ-клапаны, при этом варианте порока, прикреплены к верхнему краю межжелудочковой перегородки. Расщепление створки митрального клапана может быть в виде небольшого диастаза или доходить до её основания. От краев расщепления нередко отходят дополнительные хорды, прикрепленные к межжелудочковой перегородке, также возможны аномалии папиллярных мышц.
Эпидемиология. Частота АВК среди всех ВПС составляет 3-4%, и 6% среди критических ВПС. У 60-70% детей с АВК выявляется полная форма порока, 50% этих больных
имеют синдром Дауна.
Гемодинамика. При частичной АВК нарушения гемодинамики определяются регургитацией на митральном клапане и шунтированием крови через дефект межпредсердной перегородки. В большинстве случаев имеется большой сброс крови слева направо, гиперволемия малого круга кровообращения и объемная перегрузка обоих желудочков. В период систолы желудочков происходит обратный
322
сброс крови из левого желудочка в левое предсердие из-за недостаточности митрального клапана, а затем из левого предсердия в правое предсердие через ДМПП.
Умеренная легочная гипертензия может быть следствием как постоянной гиперволемии в малом круге кровообращения, так и венозного застоя при малых размерах ДМПП, приводящих к повышенному давлению в левом предсердии. Высокая легочная гипертензия развивается на поздних стадиях заболевания.
При полной форме АВК нарушения гемодинамики определяются недостаточностью атриовентрикулярных клапанов и шунтированием крови через дефекты межпредсердной и межжелудочковых перегородок. При этой форме порока нагрузка на сердце возникает уже внутриутробно и может приводить к появлению сердечной недостаточности и водянке плода. Из-за большого лево-правого сброса крови, которая вновь поступает в легочную артерию, развивается объемная перегрузка правых и левых отделов сердца. Давление в правом и левом желудочках рано становится равным, что приводит к раннему развитию высокой легочной гипертензии.
Клиника. При частичной форме АВК клиническая симптоматика определяется в первую очередь степенью митральной недостаточности. При её небольшой величине порок протекает как простой ДМПП, но проявляется в более ранние сроки. При значительной регургитации клапана, уже в периоде новорожденности могут появиться признаки выраженной сердечной недостаточности, возникают ОРИ, со склонностью к затяжному течению, дети с первых месяцев жизни отстают в физическом развитии. При общем предсердии у детей развивается умеренный цианоз.
При физикальном обследовании определяется левосторонний сердечный горб, систолическое дрожание в IV межреберье и/или над верхушкой сердца. Аускультативно выслушивается два шума: шум относительного стеноза лёгочной артерии во II межреберье слева от грудины (шум изгнания) и на верхушке и вдоль левого края грудины систолический шум митральной недостаточности.
При полной форме АВК основное ухудшение наступает к концу первого месяца жизни, когда снижается резистентность легочных сосудов и нарастает легочный кровоток. Сразу после рождения ребенка отмечается быстрая утомляемость при кормлении, потливость, нарастают признаки сердечной недостаточности. Дети отстают в физическом развитии, у них возникают повторные ОРИ и пневмонии. Как правило, рано формируется сердечный горб. При нагрузке происходит кратковременная смена шунта на право-левый сброс крови, что сопро-
323
вождается появлением цианоза. При физикальном обследовании, пальпаторно определяется систолическое дрожание. Аускультативно – тоны сердца усилены, при развитии высокой легочной гипертензии выслушивается акцент второго тона над легочной артерией, вдоль левого края грудины грубый систолический шум (дефект межжелудочковой перегородки), систолический шум клапанной недостаточности, проводящийся в левую аксилярную область. Однако шум недостаточности митрального клапана может быть перекрыт шумом ДМЖП.
Высокая легочная гипертензия (синдром Эйзенменгера) развивается уже к концу первого года жизни, а концу второго возникают необратимые изменения в сосудах лёгких. Особенно подвержены этим изменениям больные с трисомией по 21 паре хромосом - болезни Дауна в связи с тем, что АВК сочетается с хронической бронхолегочной патологией. Причинами смерти при АВК являются тяжелая сердечная недостаточность, высокая легочная гипертензия, фатальные аритмии.
Диагноз АВК можно заподозрить при наличии сердечной недостаточности, горба, грубых систолических шумов, цианоза.
Лабораторные исследования ДЭхоКГ. Диагностика частичной и полной формы АВК в основном
основывается на данных ДЭхоКГ. При частичной форме АВК определяется первичный ДМПП, атриовентрикулярные клапаны расположены на одном уровне, расщепление передней створки митрального клапана и регургитация на нем. Количественно оценивается давление в правом желудочке и лёгочной артерии и степень регургитации на митральной клапане. При полной АВК также выявляется полная морфологическая и гемодинамическая характеристика порока: первичный ДМПП, ДМЖП, наличие общего атриовентрикулярного клапана (со створкой, пересекающей межжелудочковую перегородку). Определяется направление шунта, давление в правом желудочке и лёгочной артерии и степень регургитации на митральном и трикуспидальном клапанах.
Рентгенологически при частичной форме АВК лёгочный рисунок варьирует; характерно его усиление, как по артериальному, так и по венозному руслу. Форма сердца различна. Выраженная митральная недостаточность сопровождается увеличением левого предсердия и левого желудочка. При небольшой степени преобладают признаки увеличения правого предсердия. При полной форме АВК легочный рисунок значительно усилен по артериальному руслу, меньше - по венозному. Могут выявляться признаки высокой лёгочной гипертензии, тень сердца увеличена в размерах за счёт всех камер сердца.
324
ЭКГ при частичной форме АВК выявляет отклонение электрической оси влево, в том числе и у новорожденных. Левограмма чаще всего сочетается с признаками перегрузки правого желудочка. В случае значительной недостаточности митрального клапана начинают преобладать признаки перегрузки левого предсердия и левого желудочка.
При полной форме АВК обнаруживают отклонение электрической оси сердца влево в сочетании с выраженными перегрузками обоих желудочков и левого предсердия.
Дифференциальный диагноз неполной формы АВК проводят с врожденной митральной недостаточностью, с полной формой АВК. При полной форме АВК – с большим дефектом межжелудочковой перегородки, единственным желудочком сердца.
Лечение. Медикаментозное лечение при АВК направлено на купирование признаков сердечной недостаточности с включением в схему лечения дигоксина, при необходимости – ингибиторов АПФ и мочегонных препаратов.
Плановое хирургическое вмешательство при неполной форме АВК показано в возрасте 1-2 лет. При выраженной митральной недостаточности или общем предсердии – хирургическая коррекция проводится раньше. Коррекция заключается в пластике дефекта межпредсердной перегородки и реконструкции расщепленных створок митрального и трикуспидального клапанов.
Хирургическое лечение при полной форме АВК возможно только в раннем возрасте (чаще в первые месяцы жизни), до развития синдрома Эйзенменгера. Суть радикальной операции состоит в том, что проводится разделение общего атриовентрикулярного канала на митральную и трикуспидальную части, закрытие одной или двумя заплатами септальных дефектов.
Осложнения. При выраженных формах порока высока вероятность быстрого развития сердечной недостаточности, возникновений нарушений ритма сердца, инфекционного эндокардита.
Прогноз при АВК остается неудовлетворительным. При естественном течении порока в течение первых шести месяцев жизни погибает до 27% больных, до конца первого года жизни – 40%. В течение последующих четырёх лет умирают ещё 10%. В единичных случаях больные доживают до зрелого возраста, однако являются тяжелыми инвалидами.
После адекватно выполненной радикальной операции, при полном АВК в раннем детстве, в последующие годы жизни требуются повторные операции по реконструкции атриовентрикулярных клапанов. Прогноз определяется размерами ДМПП и степенью митральной недоста-
325
