
Материаловедение
.pdf2.6. Полупроводниковые соединения |
71 |
да на акустических фононах. К нему добавляется неполярное рассеяние на оптических фононах. При переходе к соединениям (чистые образцы), имеющим ионную составляющую связи, начинает преобладать рассеяние носителей заряда на поляризационных фононах. Поэтому можно ожидать уменьшения µL при переходе от элементарных полупроводников к соединениям изоэлектронного ряда. Однако в наиболее обширных изоэлектронных рядах α-Sn и Ge подвижность электронов µn сначала растет, а лишь затем начинает резко падать (табл. 2.6). Для того чтобы объяснить этот факт, необходимо иметь в виду, и это очень существенно, что при сравнении подвижностей носителей в разных кристаллах следует учитывать, что на их величину, кроме степени ионности соединения, также влияет и масса носителей заряда, и сама зонная структура кристалла [6]. Какой из факторов окажется преобладающим, часто трудно предсказать.
В соединениях AIIIBV максимум подвижности µ 78000 см2/В · с наблюдается у InSb, в AIIBVI максимум µ 2300 см2/В · с наблюдается у HgTe, в AIBVII максимум µ 50 см2/В · с наблюдается у AgI. Во всех этих трех соединениях q оказывается минимальным или близким к минимальному значению эффективных зарядов, характерных для соответствующей группы соединений, поэтому полярное рассеяние в них минимально. Таким образом, в каждой из групп соединений ANB8−N максимум подвижности наблюдается вблизи минимального значения q , а при переходе от AIIIBV к AIIBVI и далее к AIBVII величина максимальной подвижности падает с увеличением равновесной ионности соединения, так что и относительная полярность связи q , и равновесная ионность определяют величины подвижности электронов в полупроводниковых соединениях с ковалентно-ионной межатомной связью.
Подвижности дырок во всех соединениях ANB8−N, как правило, не превышают их величин в полупроводниках IVA подгруппы. В изоэлектронных рядах, приведенных в табл. 2.6, подвижность дырок резко уменьшается при переходе от элементарных полупроводников к соединениям и далее продолжает уменьшаться с ростом степени ионности соединения.
2.6.6.Химические связи в полупроводниках, производных
от ANB8−N
Для развития прикладной полупроводниковой электроники требуется получение полупроводниковых материалов с заданными свойствами. В рамках обычного эмпирического подхода с этой целью синтезируют большое число кристаллов разного состава, изучают их свойства и находят тот

72 |
Глава 2. Основы теории химической связи |
материал, который обладал бы заданными параметрами. В такой ситуации, естественно, весьма желательно сформулировать некоторые критерии, которые давали бы возможность, не затрачивая больших средств и времени на изготовление огромного числа разных кристаллов, заранее исключить из рассмотрения те материалы, которые не являются полупроводниками или не обладают требуемыми свойствами. Проще всего решения этой проблемы можно достичь используя теорию химической связи. Несмотря на то, что значения кристаллохимических параметров этой теории, как правило, не являются строго определенными, знание основных закономерностей изменения физико-химических свойств известных полупроводников с изменением этих параметров позволяет в ряде случаев синтезировать аналоги известных материалов с заранее прогнозируемыми свойствами.
Анализируя химическую связь в полупроводниках, Музер и Пирсон [25] ввели понятие о некоторой специфической «полупроводниковой связи»,18 основной составной частью которой является ковалентная связь, обеспечивающая полупроводниковые свойства кристаллов. Они пришли к выводу, что для образования этой связи в элементарных полупроводниках необходимо наличие полностью заполненных s- и p-орбиталей в валентных оболочках всех атомов. В полупроводниковых бинарных соединениях достаточно, чтобы хотя бы один из двух связанных атомов обладал заполненными s- и p-валентными орбиталями. Присутствие пустых «металлических» орбиталей у другого атома, входящего в состав соединения, не уничтожает полупроводниковых свойств, если эти атомы не связаны друг с другом. Связи в полупроводниках должны образовывать одно-, двухили трехмерную решетку, простирающуюся на весь кристалл.
Принимая во внимание выводы Музера и Пирсона и учитывая накопленный при исследовании полупроводников опыт, установили, что большинство бинарных полупроводников подчиняются следующим эмпирическим закономерностям.
1. Полупроводник должен содержать в своем составе атом элемента, принадлежащего к IVA–VIIA подгруппам периодической системы. Поясним это правило.
Это правило эквивалентно требованию присутствия в полупроводниковом соединении атомов B, у которых валентная оболочка будет заполняться полностью и которые, как правило, имеют большую электроотрицательность, чем электроотрицательность атомов A. При этом предполагается, что у атомов A возможно наличие свободных «металлических»
18На самом деле химические связи в полупроводниках, конечно же, смешанные.
2.6. Полупроводниковые соединения |
73 |
орбиталей. Принцип полного заполнения валентной зоны соединения не нарушается, если атомы A непосредственно не связаны друг с другом. Однако наличие свободных «металлических» орбиталей может вызвать образование резонансной связи (см. ниже). В этом случае число ближайших соседей, с которыми образуется химическая связь, у атомов B будет превышать их валентность.
2. В полупроводнике для валентных электронов выполняется соотношение, называемое правилом Музера-Пирсона:
ne/NB + NBB = 8, |
(2.10) |
где ne — суммарное число валентных электронов на атом или молекулу (число валентных электронов, участвующих в образовании связи), NB — число атомов B (анионов из IVA–VIIA группы) в молекуле, NBB — число связей, образуемых B атомами между собой. Определение NBB требует знания кристаллической структуры соединения.
3.Разность электроотрицательностей, входящих в состав полупроводниковых соединений элементов, должна быть менее 0.8–1. Это требование связано с тем, что степень ионности связи пропорциональна разности электроотрицательностей. Увеличение степени ионности связи приводит, как мы выяснили ранее, к увеличению Eg и к уменьшению µn,p, то есть переходу к диэлектрикам.
4.Большинство полупроводников подчиняются еще и правилу нормальной валентности: для бинарных соединений AKa BLb
Ka = (8 − L)b, |
(2.11) |
где K и L — валентности элементов A и B, соответственно, в соединении AaBb, а a и b — числа, определяющие стехиометрический состав соединения.
Легко проверить, что эти правила выполняются во всех рассмотренных выше полупроводниковых соединениях ANB8−N. Например,
GaAs (AIIIBV): ne = 8; NB = 1; NBB = 0; ne/NB + NBB = 8 CdTe (AIIBVI): ne = 8; NB = 1; NBB = 0; ne/NB + NBB = 8 CuBr (AIBVII): ne = 8; NB = 1; NBB = 0; ne/NB + NBB = 8
Приведенные простые эмпирические закономерности оказались полезными с точки зрения прогнозирования полупроводниковых производных от известных полупроводниковых соединений, в частности большой группы полупроводников сложного состава (твердые растворы, бинарные, тройные и др. соединения), производной от ANB8−N.
74 |
Глава 2. Основы теории химической связи |
Поскольку далее мы будем рассматривать не только соединения, производные от ANB8−N, но и твердые растворы, то необходимо дать определения понятиям «соединение» и «твердый раствор».
Все однофазные (см. гл. 4) твердые кристаллические тела представляют собой либо соединения, либо твердые растворы.
1. Соединения.
Соединение определяется стехиометрической формулой, с помощью которой задается строгое соотношение между числами атомов элементов, входящих в состав соединения. Также отличительным признаком соединения является наличие у него определенной кристаллической решетки, отличной от решеток элементов, из которых оно образовано. Например, соединение InSb имеет кубическую решетку, а элементы, из которых оно образовано имеют: In — тетрагональную решетку, а Sb — ромбоэдрическую. Для соединения характерно строгое расположение атомов, из которых оно состоит, в элементарной ячейке. Например, кристаллическая решетка InSb (структурный тип сфалерит) состоит из двух г.ц.к.-подрешеток, сдвинутых относительно друг друга на 1/4 объемной диагонали, каждая из которых заполняется своим сортом атомов: одна — In, другая — Sb.
2. Твердые растворы.
Понятие «твердый раствор» было введено по аналогии с жидкими растворами, так как в твердых растворах для атомов растворяемого вещества характерно случайное расположение атомов в решетке растворителя, как в жидкостях, а не строго определенное, как в соединениях. Взаимодействующие вещества (растворитель и растворяемое вещество) могут иметь как неограниченную, так и ограниченную растворимость друг в друге с разной степенью этого ограничения и разной температурной зависимостью предела растворимости (см. гл. 4 и гл. 8). Таким образом, твердые растворы существуют не при определенном численном соотношении своих компонентов, а в интервале концентраций, величина которого определяется пределом растворимости. Кроме того, при образовании твердого раствора тип кристаллической решетки растворителя сохраняется, хотя постоянная решетки изменяется.
Таким образом, твердые растворы — это твердотельные двухили многокомпонентные однородные системы переменного состава (например, типа AxB1−x), в которых атомы компонентов, смешиваясь в различных соотношениях (0 ≤ x ≤ 1), образуют общую кристаллическую решетку, характерную для одного из компонентов.
На основе растворителя — химического элемента — возможны два типа твердых растворов:
2.6. Полупроводниковые соединения |
75 |
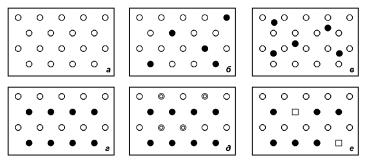
Рис. 2.22. Типы твердых растворов: а — растворитель; б — раствор замещения; в — раствор внедрения; г — растворитель; д — раствор замещения; е — раствор вычитания. а, б, в — растворитель–химический элемент, г, д, е — раствори- тель–соединение AB. ◦ — атомы A, • — атомы B, — атомы C, — незанятые узлы.
а) Растворы замещения: атомы растворяемого элемента занимают позиции атомов растворителя в узлах решетки, то есть замещают их (рис. 2.22,б). Примером может служить твердый раствор Ge–Si.
б) Растворы внедрения: атомы растворяемого элемента занимают междоузельные позиции в решетке растворителя, внедряясь между атомами последнего (рис. 2.22,в). Примеры: Ge(Li), Si(Li).
Если твердые растворы образуются на основе соединений, то кроме растворов замещения (рис. 2.22,д) и внедрения образуются еще и
в) Растворы вычитания: один из элементов, образующих соединение, присутствует в количестве, превышающем формульное, но при этом занимает в решетке соединения присущие ему позиции, а соответствующая часть позиций другого элемента остается вакантной (рис. 2.22,е). Например, Ni49Sb51, In2Te3.
Обратимся вновь к вопросу о полупроводниковых производных от ANB8−N с алмазоподобной структурой. Заметим, что помимо четырех общих закономерностей для бинарных полупроводников, для алмазоподобных выполняется следующее правило: в них на каждый атом в среднем приходится четыре валентных электрона и химические связи строятся на sp3-гибридных орбиталях. Поскольку правило Музера-Пирсона определяется суммарным числом валентных электронов и кристаллической структурой вещества, то это дает возможность получать новые вещества, обладающие полупроводниковыми свойствами, из полупроводниковых соединений AB, замещая часть атомов A или (и) B элементами
76 |
Глава 2. Основы теории химической связи |
из той же подгруппы с учетом остальных правил для сохранения полупроводниковых свойств. Практически это замещение осуществляется следующим образом. Возьмем два полупроводниковых соединения, например, с разными металлическими компонентами AC и BC, в которых элементы A и B находятся в одной и той же подгруппе периодической системы. «Смешивание» этих двух соединений приведет к образованию твердого раствора A1−xBxC в области его существования. Область существования — это часть фазовой диаграммы (см. гл. 4), в которой образуется непрерывный ряд твердых растворов и которая имеет тем большую протяженность, чем меньше различия между периодами решеток смешиваемых соединений и чем меньше различия между степенями ионности химических связей, то есть чем меньше различие между разностями электроотрицательностей в смешиваемых соединениях.
Примерами твердых растворов с замещением компонента A могут быть:
AlAs + GaAs → AlxGa1−xAs для соединений AIIIBV,
CdTe + HgTe → CdxHg1−xTe для соединений AIIBVI.
Выполнение закономерностей, характерных для полупроводников, в том числе и правила Музера-Пирсона, и сохранение алмазоподобной структуры для результирующих твердых растворов очевидно, так как в них, как и в исходных соединениях, реализуются смешанные кова- лентно-ионные sp3-гибридные связи.
Как показывает опыт, при «смешении» полупроводниковых соединений с одинаковыми атомами A и разными атомами B, расположенными в одной и той же подгруппе периодической системы, также образуются полупроводниковые твердые растворы. Например, GaSb1−yAsy (GaSb+GaAs) и CdSe1−yTey (CdSe+CdTe). При таком замещении также очевидно выполнение всех закономерностей, приведенных выше, и сохранение алмазоподобной структуры.
Возможно одновременное замещение сразу двух компонент соединения атомами из соответствующих групп периодической системы с образованием четверного твердого раствора. Например, (GaAs)1−x(InP)x (GaAs+InP).
Практическая важность получения подобных материалов для полупроводниковой электроники заключается в возможности, как правило, монотонного изменения за счет изменения состава ширины запрещенной зоны Eg от максимальной до минимальной величин, определяемых шириной запрещенных зон смешиваемых соединений (рис. 2.23). Таким образом, можно получить ряд кристаллов с непрерывно меняющейся Eg
2.6. Полупроводниковые соединения |
77 |
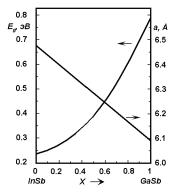
Рис. 2.23. Зависимость ширины запрещенной зоны Eg и параметра решетки от состава твердого раствора In1−xGaxSb.
и даже кристаллы, в которых Eg меняется от точки к точке. Период кристаллической решетки обычно линейно зависит от состава (концентрации растворенного компонента). Такая зависимость называется правилом Вегарда. Концентрационная зависимости подвижности носителей, времени их жизни, интенсивности излучательной рекомбинации и оптического поглощения в твердых растворах прямозонных полупроводниковых материалов описываются плавными кривыми между значениями, характерными для составляющих их компонентов. В твердых растворах, образованных прямозонным и непрямозонным полупроводниковыми материалами, в области составов, где происходит изменение зонной структуры, наблюдаются резкие изменения свойств.
Далее следует обратить внимание на то, что в правиле Музера-Пир- сона оговаривается только число B атомов элемента, входящего в состав полупроводника, а роль A атомов сводится к добавлению электронов в суммарное число валентных электронов ne. Это позволяет предполагать, что можно посредством замены компонента A в исходном соединении получать не только полупроводниковые твердые растворы, производные от соединений ANB8−N, но и другие бинарные, тройные и более сложные полупроводниковые соединения, но уже, возможно, со структурой, производной от алмазоподобной. В этом случае замещающие элементы выбираются из групп периодической таблицы, отличных от той, в которой расположен замещаемый атом A, однако при этом должны удовлетворяться общие закономерности образования полупроводников (см. выше).
Ниже приведены ряды соединений, получающихся из ANB8−N при горизонтальном замещении, с примерами полупроводниковых соединений
78 |
Глава 2. Основы теории химической связи |
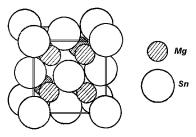
Рис. 2.24. Структура Mg2Sn (антифлюорита).
соответствующих типов.
1. AIVBIV
2. AIIIBV
3. AIIBVI
4. 3AIIBVI
→ |
A2IIBIV |
Mg2(Si,Ge,Sn,Pb); |
|
I |
V |
(Li,Rb,Cs)3(Sb,Bi); |
|
→ AI3BVI |
|||
→ |
A2B |
(Cu,Ag)2(O,S,Se,Te); |
|
III |
VI |
(Al,Ga,In)2(O,S,Se,Te)3 |
|
→ A2 |
B3 |
||
Рассмотрим, как в приведенных примерах реализуется ковалентная связь и какое влияние на кристаллическую структуру оказывает горизонтальное замещение компонента A в соединениях ANB8−N.
Соединения с резонансной связью
В соединениях первого типа наиболее электроотрицательный элемент IVA подгруппы играет роль компонента B. Рассмотрим этот тип замещения на примере соединения Mg2Sn. Mg2Sn кристаллизуется в структуре антифлюорита, которая показана на рис. 2.24. Видно, что эта структура отличается от структуры алмаза, а в молекуле два атома A и число валентных электронов в расчете на один атом меньше 4 (8/3 < 4). Тем не менее, Mg2Sn является полупроводником, а правила нормальных валентностей (K = 2; a = 2; L = 4; b = 1), Музера-Пирсона (ne = 8; NB = 1; NBB = 0) и остальные общие полупроводниковые закономерности выполняются.
В структуре антифлюорита каждый атом олова окружен восемью атомами магния, а каждый атом Mg — четырьмя атомами Sn, расположенными в вершинах тетраэдра. Атомы олова образуют плотноупакованную (гранецентрированную кубическую) решетку, все тетраэдрические пустоты которой (вместо половины в алмазоподобных структурах) заняты атомами магния. Формально можно рассматривать связи у Sn как sp3-гибридные с удвоенным числом атомов Mg.

2.6. Полупроводниковые соединения |
79 |
Рис. 2.25. а — Схема образования резонансных (кратность связи 1/3) ковалентных связей в Mg2Sn; б — локальное окружение атомов Sn в структуре антифлюорита и схемы виртуальных тетраэдрических связей.
Для описания таких структур было введено понятие о резонансной или кратной ковалентной связи. Используя все свои валентные электроны, каждый атом Sn образует четыре ковалентные sp3-гибридные связи, которые испытывают поворотный резонанс между восемью положениями. Таким образом, каждый атом Sn образует 8 «полусвязей» с соседними атомами Mg, заполняя тем самым его и свои s- и p-оболочки, причем свою до конца (до 8 электронов), а оболочки атомов Mg — только наполовину (рис. 2.25,а). Поскольку каждый атом Mg использует свои два электрона для насыщения «полусвязей» с четырьмя соседними атомами Sn, то для образования связи Mg–Mg уже не остается электронов и, в результате, выполняются условия образования «полупроводниковой связи».
Таким образом, реальное кубическое окружение атома Sn можно представить как результат наложения двух виртуальных тетраэдрических, и при этом считается, что 4 электрона олова попеременно взаимодействуют с двумя группами атомов Mg (в каждой по четыре, см. рис. 2.25,б). Кратность связи показывает, что общее число валентных электронов на атом в молекуле меньше четырех, то есть число полных sp3-гибридных связей атома B меньше числа соседей A. Численно кратность связей определяется отношением числа полных ковалентных связей к числу ближайших соседей, то есть в случае Mg2Sn равна 1/2 (4/8).
Аналогичные выводы о появлении резонансных связей можно сделать относительно соединений третьего типа, в которых число валентных электронов на атом также меньше четырех.19
Такой же подход к образованию химических связей применим и для
19В соединениях AI2BVI схема образования резонансных связей однотипна и аналогична схеме, характерной для соединений AII2 BIV, однако кристаллизуются они не только в структуре антифлюорита, что связано с индивидуальными особенностями образующих соединение элементов.
80 |
Глава 2. Основы теории химической связи |
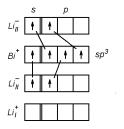
Рис. 2.26. Схема образования резонансных (кратность связи 1/2) ковалентных связей в Li3Bi.
соединений второго типа, но с небольшими усложнениями. Типичный представитель соединений второго типа — Li3Bi. В структуре этого соединения атомы висмута образуют кубическую плотную упаковку, а атомы Li размещаются в двух различных положениях в пустотах этой решетки. Две трети атомов лития (положение LiII) занимают все тетраэдрические пустоты, образуя вместе с атомами Bi структуру типа антифлюорита, а оставшаяся треть атомов Li (LiI) занимает октаэдрические пустоты в подрешетке Bi.
Схема образование ковалентных связей в соединении Li3Bi показана на рис. 2.26. Вследствие перехода по одному электрону от атомов Bi и LiI к атомам LiII, каждый из последних имеет по два электрона и в антифлюоритной решетке (LiII)2Bi может наблюдаться резонанс того же типа, что и в Mg2Sn. Этот пример показывает, как некоторые атомы, не принимая активного участия в образовании полупроводниковой связи, поставляют необходимые для ее реализации электроны. Таким образом, в Li3Bi наблюдаются одновременно как электронные переходы, так и поворотный резонанс.
Соединения с дефектной структурой
Кроме полупроводников, структура которых является производной от структуры алмаза и которые образуются путем заполнения дополнительных мест в этой решетке, существуют полупроводники с дефектными структурами на основе структур сфалерита и вюртцита. Это соединения четвертого типа. Они образуются при замене атомов A из II подгруппы на атомы из III подгруппы и изменении их числа с трех на два для сохранения общего числа электронов в молекуле. С точки зрения правила нормальной валентности и правила Музера-Пирсона такое изменение роли не играет — в обоих случаях ne = 24, NB = 3, NBB = 0. Однако число валентных электронов на атом становится больше 4 (24/5 = 4.8). Такая ситуация приводит к образованию дефектной тетраэдрической структу-
