
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
Выход по току
Выход по току – это отношение практически полученной массы продукта (Gпр.) в процессе электролиза к теоретически возможной (GT), рассчитанной по закону Фарадея:
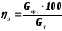 (2.2.15)
(2.2.15)
В соответствии с первым законом Фарадея масса вещества (GТ), полученная при электролизе, пропорциональна количеству пропущенного электричества (Q) т.е., силе тока (I) и времени электролиза ():
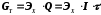 (2.2.16)
(2.2.16)
где Эх – электрохимический эквивалент вещества, (г/Ач), который определяется по формуле:
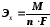 (2.2.17)
(2.2.17)
М – молярная масса вещества, г/моль;
n – число электронов, участвующих в электродной реакции;
F – число Фарадея, 26,8 Ач/моль-экв.
I – сила тока, А
- время электролиза, ч
Для гидроксида натрия, хлора и водорода электрохимические эквиваленты соответственно равны (г/Ач):
 (2.2.18)
(2.2.18)
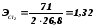 (2.2.19)
(2.2.19)
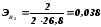 (2.2.20)
(2.2.20)
Удельный расход электроэнергии
Теоретический расход электроэнергии на 1000 г целевого продукта(WT) рассчитывают по формуле:
 ,
Вт·ч/кг
(2.2.21)
,
Вт·ч/кг
(2.2.21)
где UT – теоретическое напряжение разложения, равное разности равновесных потенциалов анода и катода; для хлорида натрия в условиях промышленного электролиза UT = 2,1 - 2,2 В.
Подставляя в формулу (2.2.21) значение GT из (2.2.16) и сократив I, , получим:
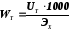 ,
Вт·ч/кг
(2.2.22)
,
Вт·ч/кг
(2.2.22)
На практике напряжение на электролизной ванне (Uпр.) значительно выше теоретического напряжения разложения, т. к. в реальных условиях необходимо учитывать перенапряжение на аноде и катоде, падение напряжения на диафрагме, в электролите, контактах и т. д. Кроме того, количество полученного продукта меньше теоретического, эту разницу учитывает выход по току. Поэтому удельный расход электроэнергии (WУД) равен:
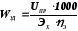 ,Вт·ч
/кг
(2.2.23)
,Вт·ч
/кг
(2.2.23)
где Э – в долях единицы.
В соответствии с уравнением (2.2.23) удельный расход электроэнергии пропорционален напряжению на ванне и обратно пропорционален выходу по току. Поэтому все мероприятия, направленные на увеличение выхода по току и снижение напряжения на ванне, приводят к снижению удельного расхода электроэнергии.
Коэффициент использования электроэнергии
По существу коэффициент использования электроэнергии (N) является долей полезного использования электроэнергии, количественно его выражают как отношение теоретического расхода электроэнергии на единицу массы целевого продукта к фактическому расходу, выраженное в процентах:
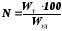 %
(2.2.24)
%
(2.2.24)
С учетом (2.2.22) и (2.2.23), получим:
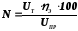 %
(2.2.25)
%
(2.2.25)
Степень использования электроэнергии тем выше, чем больше выход по току и ближе значения практического и теоретического напряжений. Поскольку выход по току для процесса получения гидроксида натрия изменяется на практике незначительно (93 - 98%), основной вклад в коэффициент использования электроэнергии вносит напряжение на ванне. Оно складывается из разности равновесных потенциалов анода (Ea) и катода (Ek) (35 - 42%), перенапряжений на аноде (а) и катоде (k) (23 - 6%), падения напряжения на диафрагме (Uд) (4-6%), в электролите (UЭ) (10 - 15%), на электродах и контактах (UК, 2 - 5%).
Uпр. = (Ea - Ek) + (а + k )+ UЭ + UК + UД (2.2.26)
В процессе работы эти соотношения могут изменяться, особенно в случае нарушения режимов процесса и возникновения неполадок: износ электродов, забивание диафрагмы, окисление контактов и др.
