
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
3.2.3. Теоретические основы процесса
Химия, равновесие и выбор катализатора. Образование 1,3-бутадиена из этанола описывается общим уравнением
2С2Н5ОН
 С4Н6
+ 2Н2О
+ Н2
-
80 кДж/моль
(3.2.1)
С4Н6
+ 2Н2О
+ Н2
-
80 кДж/моль
(3.2.1)


Термодинамические расчеты показывают, что образование 1,3-бутадиена возможно при сравнительно низких температурах. Как видно из графика (рис. 3.2.1), при повышении температуры равновесный выход дивинила растет и при температуре 330 ОС приближается к стехиометрическому. Одновременно с основной реакцией термодинамически разрешено протекание параллельных и последовательных побочных реакций. В результате побочных реакций получаются углеводороды (алканы, алкены и арены), а также кислородсодержащие соединения: спирты, альдегиды, эфиры и кетоны. Алкены и арены в свою очередь полимеризуются и конденсируются с образованием продуктов уплотнения - твердых углистых веществ. Уравнение (3.2.1) – суммарное. Механизм процесса должен включать разные по природе элементарные стадии: отщепление водорода - дегидрирование, отщепление воды – дегидратацию, для образования дополнительных связей С–С необходима реакция конденсации (как один из возможных вариантов). В основу выбора активного и селективного катализатора была положена идея о том, что он должен содержать компоненты, способные ускорять перечисленные реакции (стадии). Лучшим катализатором оказалась система, предложенная С.В. Лебедевым, включающая кислотный катализатор дегидратации на основе Al2O3, катализатор дегидрирования – ZnO и основной оксид – MgO, катализатор конденсации. При этом механизм может быть представлен следующим образом.
Первой стадией превращения этилового спирта в 1,3-бутадиен является его дегидрирование:
ZnO
I. 2СН3–СН2ОН 2СН3–СНО + 2Н , 2Н Н2 (3.2.2)
где Н - адсорбированный на поверхности катализатора водород
Далее в результате альдольной и кротоновой конденсации образуется кротоновый альдегид
MgO Al2O3
II. 2СН3–СНО СН3–СН(ОН)–СН2–СНО
Al2O3
СН3–СН=СН-СНО +Н2О (3.2.3)
Кротоновый альдегид восстанавливается адсорбированным на поверхности оксида цинка атомарным водородом в кротиловый спирт (молекулярный водород плохо активируется оксидом цинка):
ZnO
III. СН3–СН=СН–СНО + 2Н СН3–СН=СН–СН2ОН (3.2.4)
Кротиловый спирт дегидратируется с изомеризацией в 1,3-бутадиен:
Al2O3 Al2O3
IV. СН3–СН=СН–СН2ОН СН3–СН=С=СН2
– H2O
Al2O3
СН2=СН-СН=СН2 (3.2.5)
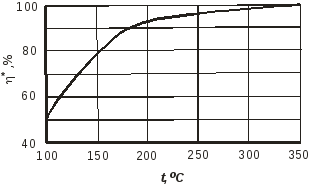
Рис.3.2.1 Зависимость равновесного выхода (*) 1,3-бутадиена от температуры.
В связи с тем, что синтез бутадиена сопровождается образованием большого количества различных побочных продуктов (до шестидесяти), процесс необходимо проводить в присутствии селективного катализатора.
3.2.4. Выбор оптимального технологического режима.
Основными факторами, влияющими на процесс получения бутадиена, являются катализатор, температура и время контактирования.
Активность катализатора и селективность процесса зависит от соотношения количеств оксидов, входящих в состав катализатора. Изменение этого соотношения почти не влияет на качественный состав получаемых продуктов, но зато сильно отражается на их количествах. Увеличение содержания в катализаторе оксида цинка выше определенной величины приводит к образованию избыточных количеств этаналя. При повышенных концентрациях этаналя, кротонового и других альдегидов будут интенсивно протекать последовательные реакции конденсации с образованием олигомерных продуктов. Повышение против нормы содержания оксида алюминия ускоряет образование этилена и диэтилового эфира (этоксиэтана), получающихся дегидратацией этанола:
С2Н5ОН С2Н4 + Н2О (3.2.6)
2С2Н5ОН (С2Н5)2О + Н2О (3.2.7)
Влияние состава катализатора (мольного соотношения Al2O3 : ZnO) на выходы 1,3-бутадиена и побочных продуктов иллюстрирует рис. 3.2.2. Правильный выбор состава катализатора позволяет проводить все превращения этанола в 1,3-бутадиен с большой скоростью и в одну технологическую стадию.
Несмотря на присутствие катализатора, побочные реакции протекают в заметной степени, и поэтому синтез бутадиена относят к сложным каталитическим процессам.
При получении 1,3 бутадиена наблюдается довольно быстрое падение активности катализатора. Образующиеся за счет побочных превращений 1,3-бутадиена, других непредельных углеводородов и альдегидов продукты уплотнения отлагаются на активных центрах катализатора, что затрудняет диффузию паров спирта к его поверхности. Процесс регенерации катализатора состоит в пропускании через него воздуха или воздуха с водяным паром при температуре 500-550ОС. При этом продукты уплотнения выгорают и катализатор вновь становится активным.
Многократная регенерация при повышенных температурах вызывает постепенное изменение кристаллической структуры катализатора и необратимое падение его активности. В этом случае катализатор заменяют свежим.

Рис.3.2.2 Зависимость выходов 1,3-бутадиена и побочных продуктов от соотношения Al2O3 и ZnO в катализаторе, [MgO] = const: 1 - С4Н6, 2 - С2Н4, 3 - СН3СНО.
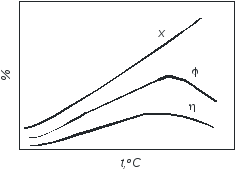
Рис.3.2.3 Зависимость степени превращения спирта (Х), селективности процесса() и выхода 1,3-бутадиена () от температуры.
Температура. Для каталитического процесса выбор температуры определяется, как правило, температурным интервалом, в котором активен применяющийся катализатор. Для катализатора С.В.Лебедева оптимальный температурный диапазон 350 – 400 ОС. Проведенный в этих условиях синтез 1,3-бутадиена представляет собой обратимый смещённый процесс (см. рис. 3.2.1). Влияние температуры связано с двумя моментами, имеющими место при любом сложном химическом процессе. При температурах ниже оптимального диапазона, выход целевого дивинила ниже максимального за счёт недостаточно высокой степени превращения этанола и невысокой селективности (катализатор недостаточно активен, и скорость побочных превращений исходного реагента соизмерима со скоростью основной реакции). При температурах выше оптимального диапазона выход целевого продукта уменьшается за счёт опережающего ускорения реакций превращения исходного реагента (этанола) и 1,3-бутадиена.
Так 1,3-бутадиен при повышенной температуре олигомеризуется с образованием низкополимерных продуктов, в частности димера бутадиена (4-винилциклогексена):
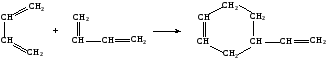
Зависимость степени превращения спирта, выхода бутадиена и селективности процесса от температуры представлена на рис. 3.2.3. По мере повышения температуры растет конверсия спирта, так как увеличиваются скорости всех возможных реакций в соответствии с их энергиями активации на данном катализаторе. Влияние температуры на выход и селективность образования 1,3-бутадиена характеризуется кривыми с максимумами в сравнительно узком диапазоне температур. Ниже оптимальных температур выход 1,3-бутадиена и селективность процесса малы вследствие относительно небольшой скорости основной реакции, выше - в основном за счет ускорения последовательных реакций дальнейших превращения дивинила.
Время контактирования. Кривые зависимости выхода и селективности образования дивинила и конверсии спирта от времени контактирования имеют тот же характер, что и соответствующие кривые зависимости от температуры. Вначале увеличение времени пребывания исходного вещества в зоне катализатора повышает количество этанола, разлагающегося с образованием бутадиена. При увеличении времени контакта сверх оптимального начинают преобладать вторичные изменения 1,3-бутадиена и превращения этанола в других направлениях. Оптимальное время контактирования тесно связано с температурой. Его выбирают таким образом, чтобы степень превращения этанола была бы невелика, во избежание протекания побочных (главным образом последовательных) реакций. Небольшая степень превращения сырья вызывает необходимость проведения процесса по циркуляционной схеме, причем возможен возврат в процесс не только непрореагировавшего спирта, но и получающегося промежуточного продукта - ацетальдегида (этаналя).
