
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
3.3.5. Описание лабораторной установки
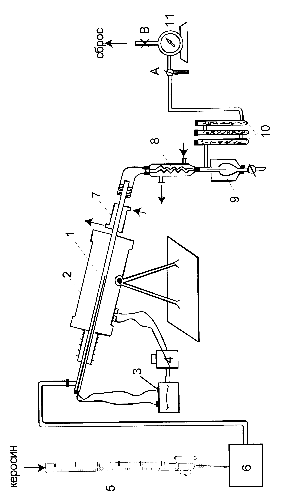
Схема установки представлена на рис. 3.3.4. Реактор пиролиза – полая стальная трубка 1 – помещен в электрическую печь 2 . нужную температуру (~700 °С) реакционной зоны задают, контролируют и поддерживают с помощью терморегулятора 3 и ЛАТРа 4. Сырье поступает в реактор из градуированной бюретки 5 с помощью насоса – микродозатора 6. Продукты пиролиза охлаждаются в воздушном и водяном холодильниках 7, 8. Сконденсировавшиеся жидкие продукты – смола пиролиза – собираются в приемнике 9, погруженном в баню со льдом и задерживаются в фильтрах 10. Первые два фильтра по ходу парогазовой смеси заполнены стеклянной ватой, третий – активированным углем. Объем газообразных продуктов пиролиза измеряют газовым счетчиком 11.
Рис. 3.3.4 Схема лабораторной установки для пиролиза фракций нефти.
3.3.6. Порядок проведения опыта
1. Взвешивают фильтры и присоединяют их так, чтобы последним по ходу парогазовой смеси был фильтр с активированным углем. Проверяют соединение установки с коллектором выхлопных газов.
2. Взвешивают колбу с пробкой для конденсата (смолы пиролиза).
3. Заливают керосиновую фракцию в градуированную бюретку 5.
4. Подают воду в холодильник 8 и загружают лед в баню, охлаждающую приемник конденсата 9.
5. Включают в электросеть ЛАТР и терморегулятор.
6. После выхода реактора на постоянный режим (температура ~700 °С) фиксируют уровень керосина в бюретке 5 и начальные показания газового счетчика 11.
7. Включают насос-микродозатор 6. В случае подачи керосина через капельную воронку установка вместо бюретки 5 и насоса 6 содержит капельную воронку. В этом случае взвешивают колбу с керосином до опыта, затем заливают керосин в воронку, плотно закрывают пробкой и устанавливают заданный расход (капли в минуту). Расход керосина контролируют каждые 5 минут. По окончании опыта закрывают кран подачи керосина и сливают его остаток в ту же колбу, которую еще раз взвешивают. По разности определяют расход керосина за данное время.
8. Во время опыта через каждые 5 минут записывают в Табл. 3.3.2 соответствующие показания (уровень керосина в бюретке, температуру в реакторе, показания газосчетчика).
9. Во время эксперимента лаборант отбирает пробу газа через трехходовой кран А для хроматографического анализа
10. По истечении заданного преподавателем времени прекращают подачу керосина. Через 10 - 15 мин выключают электрообогрев печи и фиксируют конечные показания газосчетчика. Затем перекрывают подачу воды в холодильник и отсоединяют установку от коллектора выхлопных газов с помощью зажима В.
11. Взвешивают фильтры и конденсат. Последний сливают из приемника в подготовленную колбу.
Исходные и экспериментальные данные
Дата __.______.____г.
Характеристики сырья:
а) темп. пределы выкипания
керосиновой фракции _____оС
б) средняя молекулярная масса _____
в) плотность _____г/мл
Средняя температура процесса _____ оС
Продолжительность опыта _____мин
Атмосферное давление _____мм.рт.ст.
Температура в лаборатории _____ оС
Объем реакционной зоны аппарата _____мл
Таблица 3.3.2
