
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
1.2. Основные технологические критерии эффективности
Для оценки качества ХТП используют количественные технологические показатели: степень превращения сырья, селективность образования и выход продукта, производительность реактора или установки, интенсивность работы реактора или катализатора, расходные коэффициенты по реагентам, другим веществам (в ходе ХТП расходуются катализаторы, инерты и т.д.) и энергии. Эти показатели характеризуют степень совершенства ХТП.
Рассмотрим основные показатели на примере реакции (1.18), которую будем считать основной реакцией ХТП.
aA + bB = pP (1.18)
1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
Количества реагента могут быть выражены в единицах массы, молях, в мольных потоках (количество молей вещества, поступающее в реактор или выходящее из реактора в единицу времени) и, даже, в единицах объема, взятых при одинаковых условиях (температуре и давлении).
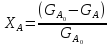 ;
;
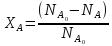 (1.19)
(1.19)
где
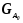 и
и
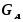 - массы введенного и непрореагировавшего
реагента А, соответственно;
- массы введенного и непрореагировавшего
реагента А, соответственно;
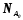 и
и
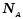 – те же величины, выраженные в молях.
– те же величины, выраженные в молях.
Если объем реакционной системы остается постоянным в ходе ХТП, то во всех расчетах количества веществ могут быть заменены их молярными концентрациями. При использовании формул (1.19) степень превращения получают в долях единицы. Умножив полученное значение на сто процентов, получим величину Х в процентах.
1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
Эквивалентная формулировка: - Выход продукта по данному реагенту – это отношение количества продукта, полученного практически, к количеству этого продукта, которое должно быть получено из введенного количества данного реагента в соответствии с уравнением реакции.
Обе формулировки выражаются одной формулой. Для уравнения (1.18) выходы продукта Р на реагенты А и В выражаются формулами (1.20).
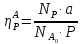
(1.20)
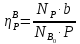
где
 ,
,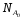 и
и
 количества молей продукта Р,
полученное в реакции (1.18), и реагентов
А
и В,
введенные в реакционную систему,
соответственно, а,
b
и p
– стехиометрические коэф- фициенты
реакции (1.18).
количества молей продукта Р,
полученное в реакции (1.18), и реагентов
А
и В,
введенные в реакционную систему,
соответственно, а,
b
и p
– стехиометрические коэф- фициенты
реакции (1.18).
Для уточнения связи формулы (1.20) с двумя формулировками определения выхода перепишем ее для реагента А в двух видах: (1.21) – для первой формулировки, (1.22) – для второй.
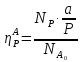 (1.21)
(1.21)
 (1.22)
(1.22)
Выражение
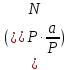 в
формуле (1.21) – это количество молей
реагента А, из которого образуется NP
молей продукта Р в соответствии с
уравнением (1.18) и т.д.
в
формуле (1.21) – это количество молей
реагента А, из которого образуется NP
молей продукта Р в соответствии с
уравнением (1.18) и т.д.
Выход можно рассчитывать для каждого из продуктов по любому из реагентов (а если необходимо, то и по всем реагентам основной реакции). Чаще выход рассчитывают для наиболее ценного (целевого) продукта на наиболее дорогой из реагентов.
Например, в синтезе метанола из синтез-газа наряду с основной (1.23) идут побочные реакции (1.24 - 1.26).
СО + 2Н2 = СН3ОН (1.23)
2СО + 2Н2 = СН4 + СО2 (1.24)
СО + 3Н2 = СН4 + Н2О (1.25)
2СН3ОН = СН3ОСН3 + Н2О (1.26)
Выход метанола (ηCH3OH) в соответствии со стехиометрией уравнения (1.23) по оксиду углерода(II) рассчитывают по формуле (1.27), а по водороду – по формуле (1.28).
 (1.27)
(1.27)
 (1.28)
(1.28)
где
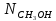 –
полученное количество молей метанола,
–
полученное количество молей метанола,
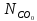 и
и
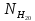 –
введенные в систему количества молей
СО
и Н2.
–
введенные в систему количества молей
СО
и Н2.
Аналогичным образом может быть рассчитан выход по каждому из побочных продуктов. Очевидно, что практический выход не может превышать равновесный выход при условиях проведения процесса.
Для процессов, в которых нельзя выделить одну стехиометрическую реакцию образования целевого продукта и поэтому нельзя рассчитать выход описанным способом, определяют показатель, который также называют выходом или массовым выходом и который представляет собой отношение массы полученного продукта к массе затраченного сырья. Например, выход этилена для процесса пиролиза фракций нефти находят как отношение массы этилена к массе поступившей в реактор фракции нефти.
1.2.3 Селективность – важнейший показатель сложного ХТП, характеризующий эффективность превращения сырья в целевой продукт.
Селективность образования продукта по реагенту (φ) – это отношение количества этого реагента, превратившегося в продукт, к общему количеству превратившегося реагента.
В отличие от выхода, селективность учитывает только превратившийся реагент, поэтому этот показатель более чувствителен к соотношению различных направлений химического превращения. Для реакции (1.18) селективность образования продукта Р по реагентам А и В выразится формулами (1.29) и (1.30), в знаменателе которых, в отличие от формул для выхода (1.21) и (1.22), количество превращенного реагента. Символом N обозначены мольные количества веществ или мольные потоки (для открытых систем, работающих в стационарном режиме).
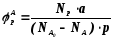 (1.29)
(1.29)
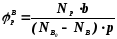 (1.30)
(1.30)
Для селективности, также как для выхода, есть второе определение: селективность – это отношение количества полученного практически продукта, к количеству этого продукта, которое должно было быть получено из прореагировавшего количества реагента в соответствии со стехиометрией реакции, по которой образуется этот продукт.
Если продукт образуется по нескольким реакциям, то селективность, как правило, рассчитать нельзя.
Селективность, рассчитанную по формулам (1.29,1.30) называют интегральной в отличие от дифференциальной селективности.
Дифференциальной
селективностью
(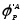 )
образования продукта Р
по реагенту А
называют отношение скорости расходования
реагента А
на образование продукта Р
к суммарной скорости превращения А.
Рассчитывают дифференциальную
селективность как отношение скоростей
образования продукта и расходования
реагента, умноженное на обратное
отношение стехиометрических коэффициентов
(1.31 для реакции 1.18). Член
)
образования продукта Р
по реагенту А
называют отношение скорости расходования
реагента А
на образование продукта Р
к суммарной скорости превращения А.
Рассчитывают дифференциальную
селективность как отношение скоростей
образования продукта и расходования
реагента, умноженное на обратное
отношение стехиометрических коэффициентов
(1.31 для реакции 1.18). Член
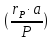 в уравнении (1.31) равен скорости
расходования А
на образование Р.
в уравнении (1.31) равен скорости
расходования А
на образование Р.
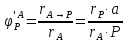 (1.31)
(1.31)
Например, для реакции синтеза метанола (1.23) интегральную селективность образования метанола по СО и по Н2 рассчитывают по формулам (1.32) и (1.33), соответственно.
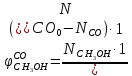 (1.32)
(1.32)
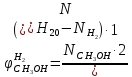 (1.33)
(1.33)
1.2.4. Взаимосвязь степени превращения реагента, выхода и интегральной селективности образования продукта по этому реагенту легко получить, перемножив выражения для степени превращения (1.19) и селективности (1.29). Сократив одинаковые члены в числителе и знаменателе, получим (1.34) (сравнить с (1.21)).
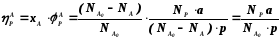 (1.34)
(1.34)
Очевидно,
что для простых ХТП селективность равна
единице (100%)
для всех продуктов единственной реакции
(стехиометрического уравнения). В этом
случае выход каждого из продуктов
реакции по любому из реагентов равен
степени превращения этого реагента
(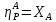 ).
).
В случае сложных ХТП для получения высокого выхода необходимо иметь высокие значения и степени превращения, и селективности. Если процесс протекает с полным превращением реагента, то выход продуктов по этому реагенту равен селективности образования каждого из продуктов по данному реагенту.
Например, в контактном окислении аммиака весь поступающий в процесс аммиак реагирует, превращаясь в оксид азота и побочные продукты. Выход оксида азота на аммиак в этом случае равен селективности образования NO по аммиаку.
1.2.5. Производительность аппарата. Производительность аппарата (П) - это масса (или объем) выработанного целевого продукта за единицу времени:
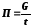 (кг/ч,
т/ч,
(кг/ч,
т/ч,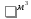 /ч)
/ч)
где G – масса (или объем) продукта, полученная за время t/
1.2.6. Интенсивность работы аппарата. Интенсивностью работы аппарата (I) называют его производительность, отнесенную к какой-либо величине, характеризующей размеры данного аппарата. Обычно производительность относят к объему аппарата V или к площади его сечения S:
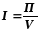 (кг/м3ч),
(кг/м3ч),
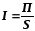 (кг/м2ч)
(кг/м2ч)
В каталитических процессах рассчитывают интенсивность работы катализатора, для чего массу полученного за единицу времени целевого продукта относят к объему катализатора Vk:
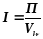 (кг
(кг ч)
ч)
