
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
3.1.10. Задание
1. Провести процесс получения формальдегида с записью всех данных по прилагаемой форме.
2. Определить содержание формальдегида в формалине и провести анализ полученного газа.
3. Составить приближенный материальный баланс контактного аппарата на заданный преподавателем базис.
4. Рассчитать на основании экспериментальных данных и материального баланса основные показатели процесса:
-
полученное при проведении опыта соотношение между О2 и СН3ОН (от стехиометрии);
-
время контактирования, сек;
-
степень превращения метанола, %;
-
выход формальдегида, %;
-
селективность образования формальдегида, %;
-
расходные коэффициенты по метанолу;
-
интенсивность работы катализатора, кг/м3ч;
3.1.11. Техника безопасности
Метанол ядовит и огнеопасен. При попадании в организм 10 мл метилового спирта наступает необратимая потеря зрения. Пролитый на кожу метанол нужно немедленно смыть водой. Формальдегид ядовит. Он раздражает слизистые оболочки дыхательных путей.
Библиографический список.
1. Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза, 3-е изд. -М.: Химия, 1981.-608 с.
2. Огородников С.К. Формальдегид. -Л.: Химия, 1984.-280 с.
3.2. Получение 1,3-бутадиена (дивинила)
из этанола по методу С.В. Лебедева
3.2.1. Цель работы.
Ознакомить с основными закономерностями сложного многостадийного процесса, в котором используют полифункциональный катализатор; рассчитать и интерпретировать полученные технологические критерии и параметры процесса.
3.2.2. Введение
Дивинил
(1,3-бутадиен СН2=СН-СН=СН2)
- первый член гомологического ряда
углеводородов с сопряженной двойной
связью, бесцветный газ со специфическим
запахом, конденсирующийся в жидкость
при - 4,3ОС
(атмосферное давление). С воздухом
1,3-бутадиен образует взрывоопасные
смеси в пределах концентраций 2,0 - 11,5 %
объемн., его химические свойства
определяются наличием сопряженных
двойных связей. Дивинил является основным
мономером для производства синтетических
каучуков. При сополимеризации дивинила
со стиролом, метилстиролом и акрилонитрилом
образуется макромолекула, в которой
1,3-бутадиен связывается в 1,4 или 1,2
положениях: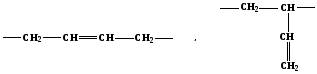
Особенно ценные свойства имеет цис-бутадиеновый каучук, получаемый полимеризацией дивинила преимущественно в 1,4-положении с цис-расположением атомов водорода при двойной связи:

В СССР в 40-х годах получил широкое распространение синтез 1,3-бутадиена из этанола по способу С.В.Лебедева. В настоящее время ввиду использования сравнительно дорогого сырья, низких показателей и сложности разделения продуктов в этом синтезе, основными методами производства 1,3-бутадиена являются дегидрирование н-бутана и н-бутена, а также выделение бутадиена из продуктов пиролиза фракции нефти. Поэтому данная лабораторная работа имеет главным образом методическое значение.
