
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
1.2.7. Материальный баланс хтп.
Материальный баланс ХТП является следствием закона сохранения массы вещества (а точнее – следствием сохранения элементов при химических превращениях). Это означает, что масса веществ, поступивших на технологическую операцию - приход, равна массе полученных веществ - расходу. Материальный баланс должен соблюдаться для ХТП всех типов: синтеза, разделения, очистки целевых продуктов. Данные о материальном балансе позволяют дать оценку целесообразности осуществления процесса в заданных условиях. Эти данные нужны как при проектировании новых, так и при анализе работы существующих производств. По данным материального баланса рассчитывают технологические показатели процесса: выход целевого продукта, степень превращения сырья, селективность процесса, расходные коэффициенты по сырью и т.д. Материальный баланс является необходимым элементом при расчете энергетического и эксергетического балансов.
Материальный баланс сводят, пользуясь уравнениями основной и побочных реакций. Когда учитывают не все происходящие побочные реакции и полученные побочные продукты, а лишь наиболее важные из них, материальный баланс имеет приблизительный характер. Существуют три основные формы составления материального баланса. В виде системы уравнений, таблицы и поточной диаграммы.
Уравнение материального баланса в общем виде:
GAO + GBO + ... = GR + ...+ GD +...+ GA + GB + G,
где GAO , GBO - массы исходных реагентов (сырья).
GR - масса целевого продукта,
GD - масса побочного продукта,
GА , GВ - массы непрореагировавших веществ,
G - невязка баланса.
Невязка баланса является следствием потерь сырья и продуктов при проведении процесса, неточности эксперимента и расчета, а также принятых допущений.
Чаще всего материальный баланс процесса представляют в виде таблицы:
|
Приход |
Расход |
|||||
|
Наименование |
Масс. ед. |
% масс. |
Наименование |
Масс. ед. |
% масс. |
|
|
Реагент А |
... |
... |
Целевой продукт R |
... |
... |
|
|
Реагент В |
... |
... |
Побочный продукт D |
... |
... |
|
|
|
|
|
Реагент А (остаток) |
... |
... |
|
|
|
|
|
Реагент В (остаток) |
... |
... |
|
|
|
|
|
Невязка |
... |
... |
|
|
Всего |
... |
100 |
Всего |
... |
100 |
|
В таблицу материального баланса, кроме обязательных масс и массовых процентов введенных и получающихся веществ, включают еще и объемы веществ, находящихся в газовой фазе, приведенные к нормальным условиям. Массовые проценты в столбце “Расход” рассчитывают по отношению к сумме масс введенных реагентов в столбце “Приход”, т.е. массу всех введенных реагентов принимают за 100%. Может случиться, что из-за погрешностей эксперимента и допущений, принятых при расчете, масса полученных веществ окажется больше массы введенных. Тогда невязка баланса будет иметь отрицательное значение. Материальный баланс составляют на заданный базис. Обычно базисом является масса сырья или целевого продукта (кг, т) или продолжительность процесса (ч, сутки). В лабораторных исследованиях составляют баланс за время проведения опыта.
В дальнейшем производят пересчет на заданный базис, пользуясь коэффициентом пересчета. Коэффициент пересчета показывает, во сколько раз нужно изменить массы веществ, входящих в материальный баланс, при переходе на другой базис. Так, если в материальном балансе, составленном за время проведения опыта, получили GR грамм целевого продукта, а заданный базис расчета - 1000 г целевого продукта, коэффициент пересчета равен 1000 / GR.
В названии таблицы материального баланса указывают, для какого процесса и реактора произведен расчет, а также принятый базис расчета.
Поточная диаграмма это блок-схема (рис.1.3). Материальные потоки изображают в виде полос, ширина которых пропорциональна массе в выбранном масштабе. Основным преимуществом данного способа изображения является его наглядность.

Рис.1.3. Поточная диаграмма колонны синтеза аммиака:
1 - свежий газ;
2 - циркулирующий газ;
3 - жидкий аммиак и растворенные в нем газы;
4 - отдувочные газы
1.2.8. Расходные коэффициенты по сырью. К основным показателям ХТП относятся расходные коэффициенты, характеризующие затраты сырья, воды, топлива, электроэнергии, пара на единицу массы целевого продукта. В связи с большим вкладом затрат на реагенты (сырье) в себестоимость продуктов в химической технологии особое значение имеют расходные коэффициенты по реагентам. Различают теоретические и практические расходные коэффициенты. Теоретический расходный коэффициент стех рассчитывают, пользуясь стехиометрическим уравнением, описывающим химическое превращение (1.18):
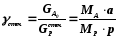



где
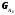 и
и
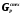 - массы реагента и продукта из уравнения
реакции
- массы реагента и продукта из уравнения
реакции
MA и MP - молекулярные массы реагента и продукта
а и р - стехиометрические коэффициенты.
Теоретический расходный коэффициент характеризует минимальный расход сырья на получение единицы массы продукта.
Практический
расходный коэффициент
отражает реальный расход поступившего
в процесс сырья на получение единицы
массы продукта, т.е. его рассчитывают
как отношение массы поступившего в
процесс сырья
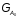 к массе получившегося продукта GР:
к массе получившегося продукта GР:
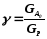
Расходные коэффициенты рассчитывают по всем реагентам. Практические расходные коэффициенты всегда больше стехиометрических из-за неполноты превращения сырья, а также из-за расходования сырья на побочные реакции. Данные для расчета практических расходных коэффициентов берут из материального баланса процесса. Практический расходный коэффициент по реагенту можно найти, зная теоретический расходный коэффициент и выход целевого продукта по этому реагенту:
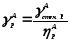
где
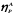 - выход Р
по реагенту А
в долях единицы.
- выход Р
по реагенту А
в долях единицы.
