
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
3.1.5. Описание лабораторной установки
Лабораторная установка состоит из трех основных элементов: испарителя-смесителя 1, контактного аппарата 2 и «закалочного» холодильника-поглотителя 3 (рис. 3.1.3). Воздух, подаваемый компрессором 11, поступает через диафрагму 5, перепад давления на которой измеряют с помощью дифференциального манометра 10, в нижнюю часть испарителя-смесителя 1. Сверху в него из бюретки 12 дозирующим насосом 9 подают метанол. Спирт по внутренней трубке попадает в нижнюю часть испарителя, испаряется на нагретой металлической стружке и, смешавшись с воздухом, проходит насадку из стеклянной ваты для улавливания капель неиспарившегося спирта. Испаритель имеет внешний электрообогрев, интенсивность нагрева регулируют с помощью терморегулятора 6. Нагретая спирто-воздушная смесь поступает в контактный аппарат 2. Внутри аппарата на сетке помещен катализатор - серебро, нанесенное на пемзу. Контактный аппарат изготовлен из хромоникелевой стали или кварца и снабжен внешним электрообогревом для предварительного подогрева катализатора. Интенсивность нагрева реактора регулируют с помощью терморегулятора 7. Температуру реакционной зоны измеряют термопарой. Продукты контактирования из контактного аппарата поступают в закалочный холодильник-поглотитель 3. Парогазовая смесь проходит по змеевику, охлаждаемому водой, в нижнюю часть, где барботирует через слой дистиллированной воды. В воде растворяются формальдегид, непрореагировавший метанол, муравьиная кислота. Для более полного поглощения метанола и формальдегида парогазовую смесь пропускают через слой воды в склянке Дрекселя 4. Несконденсировавшиеся и нерастворившиеся газы проходят газосчетчик 8, с помощью которого измеряют их расход и объем, и поступают в линию сброса в вытяжной шкаф.
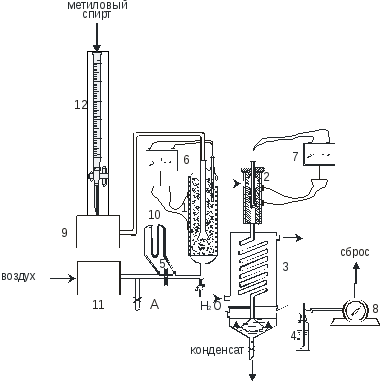
Рис. 3.1.3 Схема лабораторной установки для получения формальдегида: 1 - испаритель; 2 - контактный аппарат; 3 - холодильник-поглотитель; 4 - дрексель-поглотитель; 5 - диафрагма; 6, 7 - терморегуляторы; 8 – газосчетчик; 9 - дозирующий насос; 10 – дифференциальный манометр; 11 - компрессор; 12 - бюретка .
3.1.6. Предварительные расчеты
Рассчитывают расход воздуха в л/ч при температуре и давлении в лаборатории по заданному расходу абсолютного метанола и заданному проценту от стехиометрического количества кислорода. Расчет ведут по реакции (3.1.1), т.е. считают, что по стехиометрии на 1 моль поступающего в контактный аппарат метанола приходится 0,5 моля кислорода (11,2 л кислорода или 53,3 л воздуха при нормальных условиях).
3.1.7. Порядок проведения опыта
Водный раствор метанола в количестве 100 мл заливают в бюретку 12. В нижнюю часть поглотителя 3 и в склянку Дрекселя 4 наливают по 100 мл дистиллированной воды. Включают подачу охлаждающей воды в холодильный аппарат 3.
Включают электрообогрев испарителя 1 и контактного аппарата 2. С помощью терморегуляторов 6 и 7 поддерживают следующие температуры:
а) в испарителе 90 10ОС;
б) в контактном аппарате в момент начала подачи спирта 250 10ОС, а в течение опыта 500 - 700ОС.
При открытом зажиме А включают компрессор 11. Количество подаваемого воздуха регулируют тем же зажимом А, а контролируют с помощью дифференциального манометра 10 и газосчетчика 8. Для измерения расхода воздуха необходимо сделать несколько замеров объема воздуха, поступающего в установку в течение 1 мин. С помощью зажима А установить расчетный расход воздуха.
По достижении необходимых температур в испарителе и контактном аппарате и установления необходимого расхода воздуха начинают подавать спирт. Расход спирта контролируют по изменению объема спирта в бюретке за определенные интервалы времени (5 мин). Момент начала подачи спирта в испаритель (после заполнения шланга, идущего от насоса 9) фиксируют как время начала опыта. Продолжительность опыта 40 – 60 мин. (задается преподавателем). Во время проведения опыта непрерывно следят за ходом процесса и с момента начала опыта через каждые 5 мин записывают в таблицу: скорости подачи спирта (изменение объема спирта в бюретке 12) и воздуха (по дифференциальному манометру 10), значения температуры в испарителе и контактном аппарате (высвечиваются на шкалах терморегуляторов 6 и 7, соответственно), скорость выделения контактного газа (показания газосчетчика 8) (см. Табл. 3.1.1).
Скорости подачи воздуха и спирта в ходе опыта должны оставаться постоянными и соответствовать расчетным значениям. Скорость выделения контактного газа не должна отличаться от скорости подачи воздуха более чем на 10 – 15 % (почему?). Обо всех отклонениях от режима необходимо как можно быстрее сообщить преподавателю.
В ходе опыта с помощью лаборанта или преподавателя необходимо провести хроматографический анализ состава контактного газа (см. ниже).
По истечении времени опыта фиксируют конечные показания (см. выше), прекращают подачу спирта (выключают насос 9) и через 5 минут перестают подавать воздух (выключают компрессор 11). Эти «лишние» пять минут подачи воздуха необходимы для продувки системы от паров формальдегида, метанола и реакционных газов. Выключают нагрев испарителя и контактного аппарата и ждут 15 - 20 мин для охлаждения контактного аппарата до 100 - 150С.
Формалин из поглотителя 3 сливают в мерную колбу на 250 мл. Слабым раствором формалина, образовавшимся в склянке Дрекселя, промывают поглотитель 3. Промывные воды сливают в ту же колбу, доводят до метки дистиллированной водой, тщательно перемешивают и определяют количество полученного формальдегида титрованием в присутствие солянокислого гидроксиламина (методику см. ниже).
