
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
3.3.4. Выбор оптимального технологического режима
Сырье. Виды сырья, используемого в мировом производстве этилена, и их доля в общем балансе производства этилена следующие:
|
Сырье |
Этан |
Пропан |
Бутан |
Бензин Темп. пределы выкипания 35-180оС |
Газойль Темп. пределы выкипания 140-350 оС |
|
Доля, % |
36 |
11 |
3 |
47 |
3 |
Лучшим сырьем являются алканы, поскольку с повышением содержания водорода в исходных углеводородах выход алкенов возрастает. Так суммарный выход этилена и пропилена при использовании в качестве сырья этана, пропана и бензина составляет 80%, 68%, 47%, соответственно.
Температура. Температура является важнейшим параметром процесса. Поскольку реакции инициирования цепи сильно эндотермичны, их константы равновесия быстро возрастают с ростом температуры. Напротив, реакции обрыва цепи сильно экзотермичны, что обуславливает быстрое понижение соответствующих им констант равновесия с ростом температуры. Реакции продолжения цепи почти не обладают тепловыми эффектами, и соответствующие им константы равновесия практически не зависят от температуры. В общем, чем выше температура, тем вероятнее образование свободных радикалов.
Наблюдаемая энергия активации распада углеводородов большая величина. Для этана она примерно 200 кДж/моль. Энергии активации реакций инициирования, продолжения цепи и обрыва цепи составляют 351, 46, 40 кДж/моль, соответственно. С повышением температуры скорости реакций инициирования цепи и, следовательно, скорость образования свободных радикалов быстро возрастают. Напротив, скорости реакций обрыва цепи, приводящих к гибели свободных радикалов, мало зависят от температуры. Поэтому повышение температуры будет способствовать увеличению скоростей желательных реакций, приводящих к образованию целевых алкенов (этилена и пропилена).
Температура влияет и на вторичные реакции пиролиза. Так, повышение температуры увеличивает роль реакций распада по сравнению с реакциями конденсации алкенов, поскольку энергия активации реакций распада значительно выше. Общая закономерность состоит в том, что с повышением температуры возрастает выход газа и кокса и снижается выход жидких продуктов (рис 3.3.2).
Современные установки по получению этилена работают при температурах от 750°С (мягкий режим пиролиза) до 900°С (жесткий режим пиролиза) в зависимости от требуемого отношения этилена к высшим алкенам. При повышении температуры газ пиролиза обогащается термодинамически более стабильными веществами - низшими углеводородами и водородом. Содержание алканов С3 и С4 непрерывно уменьшается с повышением температуры, и при 900°С они почти полностью исчезают.
Суммарное количество алкенов вначале увеличивается, но затем снижается за счет вторичных реакций распада и конденсации, проходя через максимум при 650 - 800° С. Наблюдается и максимум содержания в газе отдельных алкенов. Для сохранения целевых продуктов пиролиза - этилена и пропилена - от дальнейших превращений проводят «закалку» (резкое охлаждение) продуктов пиролиза от 700 - 850°С до 350 - 400°С. «Закалку» осуществляют в котле-утилизаторе, где за счет тепла продуктов реакции образуется пар высокого давления 10 - 12 МПа, который после перегрева используют для привода турбокомпрессоров.
Время пребывания сырья в реакционной зоне.
Этилен и пропилен являются продуктами распада углеводородов, как содержащихся в сырье, так и получающихся в качестве первичных продуктов разложения сырья. Расходуются этилен и пропилен в процессе на образование аренов по реакции диенового синтеза. Зависимость выходов этилена, пропилена и жидких продуктов пиролиза от времени пребывания в реакционной зоне дана на рис. 3.3.3. Как видно из рисунка, кривые выхода этилена и пропилена проходят через максимум, что характерно для процессов, в которых целевой продукт расходуется на последовательные побочные реакции. При этом выход жидких продуктов уменьшается. Необходимо отметить, что время пребывания сырья в реакционной зоне и температура процесса в известных пределах могут компенсировать друг друга. При температурах 700 - 750°С оптимальное время пребывания - 2 с, при повышении температуры до 800 - 850°С оно уменьшается до - 0,3 с. На современных установках производства этилена большой единичной мощности (450 тыс. т/год) пиролиз бензиновых фракций осуществляют при 800 - 850оС и времени пребывания сырья ~0,3 с рециркуляцией образующихся в процессе этана, а также пропана и н-бутана. При этом выход этилена повышается на 3 - 17%.
Давление. Как отмечалось выше, для уменьшения доли реакций конденсации целесообразно проводить процесс пиролиза при пониженном давлении. Это достигается добавлением к сырью инертного разбавителя. В качестве разбавителя применяют водяной пар. Он сравнительно дешев, легко отделяется конденсацией от продуктов пиролиза, взаимодействует с коксом, отлагающимся на стенках реактора, по реакции:
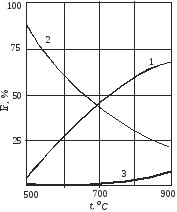
Рис.3.3.2 Зависимость выходов продуктов пиролиза бензиновой фракции нефти от температуры: 1 - газ, 2 - жидкие продукты, 3 - кокс.
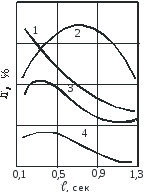
Рис.3.3.3 Зависимость выходов продуктов пиролиза бензиновой фракции при 810 ОС и атмосферном давлении от времени пребывания сырья в реакционной зоне: 1 - жидкие продукты, 2 - этилен, 3 - пропилен, 4 - бутадиен.
С + Н2О = СО + Н2
Обычно бензиновые фракции разбавляют водяным паром, составляющим 20 - 50% от массы сырья. При пиролизе бензиновых фракций нефти, разбавленных водяным паром, выход газа колеблется от 55 - 70% (мягкий режим) до 80 - 95% (жесткий режим). Выходы этилена составляют 25% и 30% соответственно. Выход смолы пиролиза при мягком режиме – 30 - 45%, при жестком - 5 - 20%. Смола содержит арены, алкены и диеновые углеводороды. Выход кокса в процессе пиролиза составляет 1 - 2%. (Выход в данном случае – это отношение массы соответствующего продукта к массе исходных углеводородов.)
