
- •Основы химической технологии Лабораторный практикум Москва 2013
- •Раздел 1 Основные понятия и технологические критерии эффективности химико-технологических процессов
- •1.1. Классификация химико-технологических процессов.
- •1.2. Основные технологические критерии эффективности
- •1.2.1 Степень превращения (степень конверсии) реагента (х) – это отношение количества превращенного реагента к введенному в реакционную систему количеству этого реагента.
- •1.2.2 Выходом продукта по данному реагенту называют отношение количества реагента, превратившегося в данный продукт, к количеству этого реагента, введенного в систему.
- •1.2.7. Материальный баланс хтп.
- •1.3. Технологические параметры хтп
- •1.3.1. Время пребывания исходных веществ в реакционной зоне.
- •Раздел 2 Технология неорганических веществ
- •2.1. Каталитическое окисление аммиака
- •2.1.2. Введение
- •2.1.3. Теоретические основы процесса Химия процесса и равновесие.
- •Кинетика процесса.
- •2.1.4. Выбор оптимального технологического режима.
- •2.1.5. Схема лабораторной установки
- •2.1.6. Порядок проведения опыта
- •1. Подготовка колб для отбора газовых проб.
- •2. Техника проведения эксперимента.
- •Экспериментальные и расчетные данные
- •Контроль процесса
- •Анализ газовых фаз
- •Технологические расчеты
- •2.1.7. Задание
- •2.1.8. Техника безопасности
- •Материальный баланс контактного аппарата для окисления аммиака
- •Библиографический список
- •2.2. Электрохимическое получение гидроксида натрия, хлора и водорода диафрагменным методом
- •2.2.2. Введение
- •2.2.3. Теоретические основы процесса
- •Электродные реакции и термодинамика процесса электролиза водного раствора хлорида натрия в диафрагменной ванне.
- •Электродные реакции и потенциалы разряда ионов
- •Кинетика электродных процессов.
- •Выход по току
- •Удельный расход электроэнергии
- •Коэффициент использования электроэнергии
- •Конверсия сырья
- •2.2.4. Выбор оптимального технологического режима
- •Состав электролита
- •Материал электродов
- •Диафрагма
- •2.2.5. Экспериментальная часть
- •Исходные данные
- •Предварительные расчеты
- •Порядок выполнения работы
- •Экспериментальные данные
- •Контроль процесса Определение концентрации щелочи в католите.
- •1. В связи с техническими сложностями измерения объема подаваемого электролита и анализа всех продуктов при расчёте материального баланса делаем следующие допущения:
- •2. Последовательность расчета материального баланса
- •Материальный баланс процесса электролиза
- •Расчет технологических показателей
- •Технологические показатели процесса электролиза
- •2.2.6. Задание
- •2.2.5.Техника безопасности
- •Библиографический список
- •2.3. Контактное окисление оксида серы (IV)
- •2.3.2.Введение
- •2.3.3. Теоретические основы процесса
- •2.3.4. Выбор технологического режима.
- •Зависимость равновесного выхода η* от состава исходной газовой смеси
- •Зависимость равновесного выхода от температуры при различном давлении
- •2.3.5. Расчетная часть Исходные данные
- •2.3.6. Расчет материального баланса.
- •Показатели процесса окисления оксида серы (IV)
- •2.3.7. Задание
- •Приложение Расчёт степени превращения so2 в so3 (степени контактирования)
- •Библиографический список
- •Раздел 3
- •3.1.3. Теоретические основы процесса.
- •Снон(адс) сн2о (газ)
- •3.1.5. Описание лабораторной установки
- •3.1.6. Предварительные расчеты
- •3.1.7. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Технологические параметры и критерии процесса
- •Экспериментальные данные
- •3.1.8. Контроль процесса
- •3.1.9. Расчет материального баланса контактного аппарата.
- •Материальный баланс контактного аппарата для получения формальдегида.
- •3.1.10. Задание
- •3.2.3. Теоретические основы процесса
- •3.2.5. Описание лабораторной установки.
- •3.2.6. Порядок проведения опыта.
- •Исходные и экспериментальные данные
- •Объем спирта, поступившего в реактор _____мл
- •Контроль процесса
- •Экспериментальные результаты опыта.
- •Данные хроматографического анализа контактного газа
- •3.2.7. Расчет материального баланса реактора
- •Материальный баланс реактора синтеза бутадиена.
- •3.2.8. Задание
- •3.3.3. Теоретические основы процесса
- •Усредненные энергии связей
- •Механизм превращения углеводородов в процессе пиролиза
- •3.3.4. Выбор оптимального технологического режима
- •3.3.5. Описание лабораторной установки
- •3.3.6. Порядок проведения опыта
- •Исходные и экспериментальные данные
- •Экспериментальные данные проведения опыта
- •3.3.7. Расчет материального баланса пиролиза
- •Материальный баланс реактора пиролиза керосиновой фракции.
- •3.3.8. Задание
- •Библиографический список.
- •Раздел 4 Приложение
- •4.1. Хроматографический анализ
- •Характеристики хроматографических пиков
- •Прикладной катализ Химия и технология гомогенного катализа
2.1.5. Схема лабораторной установки
Схема представлена на рис 2.1.6. Газообразный аммиак из баллона 1 через ротаметр 2 поступает в смеситель 3. Ротаметр 2 не калиброван и является лишь индикаторным прибором, регистрирующим заданный расход аммиака (h мм). Расход аммиака регулируется вентилем А. Воздух подается с помощью воздуходувки 4, очищается от масла в фильтре 5, заполненном стеклянной ватой, затем поступает в смеситель 3. Расход воздуха замеряется ротаметром 6 и регулируется вентилем Б. Аммиачно-воздушная смесь поступает в верхнюю часть контактного аппарата 7 и проходит через комбинированный катализатор (одну платиновую сетку и слой оксидного катализатора). Полученные нитрозные газы по нижней трубке направляют на нейтрализацию.
Контактный аппарат состоит из трех частей: верхнего стального конуса, футерованного алюминием; средней цилиндрической части и нижнего конуса, изготовленного из хромоникелевой стали. С целью снижения потерь тепла аппарат снаружи покрыт теплоизоляцией. Между фланцами верхнего конуса и цилиндрической частью зажат фланец катализаторной корзины 8 для таблеток неплатинового катализатора. Над корзиной укреплена платиновая сетка. Для измерения температуры в зоне катализатора в качестве датчика используют термопару 9. В верхний конус контактного аппарата вмонтирована платиновая спираль 10, которая разогревается электрическим током от сети через ЛАТР: сила тока контролируется амперметром. Аппарат имеет смотровое стекло 11 для наблюдения за разогреванием катализатора. Трубка с краном В служит для отбора аммиачно-воздушной смеси, поступающей в контактный аппарат, трубка с краном Г - для отбора нитрозных газов. Трубка с краном Д необходима для слива слабой азотной кислоты, образующейся при частичной конденсации влажных нитрозных газов.
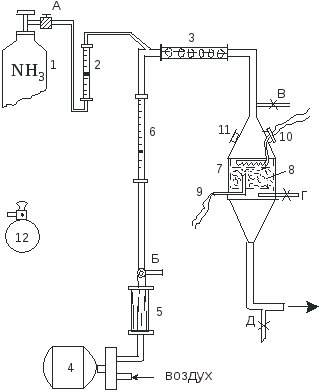
Рис.2.1.6 Схема лабораторной установки для окисления аммиака: 1 – баллон; 2,6 – ротаметры; 3 – смеситель; 4 – воздуходувка; 5 – фильтр; 7 – контактный аппарат: 8 – катализаторная корзина; 9 – термопара; 10 – спираль; 11 – смотровое окно; 12 – колба для отбора пробы газа.
2.1.6. Порядок проведения опыта
1. Подготовка колб для отбора газовых проб.
1.1 Круглодонные колбы с пришлифованными пробками должны быть вымыты. Горловины колб и шлифы очищают от остатков смазки фильтровальной бумагой, наносят на шлиф пробки и горловину вакуумную смазку и тщательно притирают (шлифы после смазки и притирания должны быть совершенно прозрачными).
1.2. В колбу, предназначенную для анализа аммиачно-воздушной смеси, наливают из бюретки 25 мл 0,1 н раствора серной кислоты и 3 капли индикатора метилового красного. В другую колбу, предназначенную для анализа нитрозных газов, наливают 25 мл 0,1 н раствора гидроксида натрия и добавляют 3 капли того же индикатора. Затем пробки на колбах вновь притирают.
1.3. Колбы помещают поочередно в защитное устройство из металлической сетки и откачивают воздух вакуумным насосом до момента закипания жидкости. После этого поворачивают пробку так, чтобы отверстие в ней не совпадало с отверстием в горлышке колбы.
1.4. Взвешивают колбы на электронных весах.
