
- •Лекция №1 зміст, предмет та задачі дисципліни.
- •Лекция №2-4 природные α-аминокислоты. Строение классификация стереоизомерия химические свойства
- •Лекция №5 белки. Общие сведения, функции белков
- •Белки общие сведения.
- •2. Функции белков,содержание белков в органах и тканях
- •Лекция № 6-9. Физико-химические свойства белков, их структурная организация, классификация белков
- •1. Физико-химические свойства белков. Понятие структурной организации белков
- •2. Первичная и вторичная структура белка
- •3. Третичная и четвертичная структура белка
- •4. Классификация белков, химия простых белков, природные пептиды
- •Лекция № 10-12. Особенности белкового обмена, переваривание белков.
- •1. Особенности белкового обмена
- •2. Особенности переваривания белков, эндопептидазы
- •3. Переваривание белков в желудке и кишечнике
- •4. Всасывание продуктов гидролиза белков
- •5. Амины
- •Лекция № 13-15. Обезвреживание аммиака в организме, орнитиновый цикл, специфические пути обмена аминокислот.
- •1. Обезвреживание аммиака в организме
- •2. Специфические пути обмена аминокислот
- •Лекция № 16-18. Сложные белки хромопротеины и нуклеопротеины
- •1. Определение хромопротеинов. Гемо- и флавопротеины
- •2. Нуклеопротеины и липопротеины
- •3. Фосфопротеины и гликопротеины
- •Свойства иммуноглобулинов человека
- •Лекция № 19-21. Химический состав и структура нуклеиновых кислот
- •1. Химический состав нуклеиновых кислот
- •2. Особенности структуры нуклеиновых кислот
- •3. Первичная структура нуклеиновых кислот
- •4. Вторичная и третичная структура нуклеиновых кислот
- •Лекция № 22. Обмен нуклеиновых кислот
- •1. Общие представления об обмене нуклеопротеидов
- •Лекция 23-26 биосинтез днк
- •Лекция №27 биосинтез рнк, биогенез мрнк, биосинтез и распад гемоглобина
- •Биосинтез рнк, биогенез мРнк
- •3. Биогенез тРнк и рРнк, синтез рнк на матрице рнк
- •Распад нуклеиновых кислот
- •Биосинтез гемоглобина
- •Лекция № 28. Общие требования к синтезу белка
- •1. Составные части белоксинтезирующей системы, рибосомы и аминоацил-тРнк-синтетазы
- •2. Транспортные и матричные рнк, природа генетического кода
- •Лекция № 29. Синтез и постсинтетическая модификация белка
- •1. Синтез белка и его транспорт через мембраны
- •2. Транспорт синтезированных белков через мембраны
- •3. Регуляция синтеза белка
- •Лекция № 30-31. Понятие о ферментах, их химическая природа и строение
- •1. Понятие о ферментах, их химическая природа и строение
- •2. Активный центр ферментов
- •3. Изоферменты
- •Лекция № 32. Механизм действия ферментов
- •1. Механизм действия ферментов
- •2. Кинетика ферментативных реакций
- •Лекция № 34-35. Основные свойства ферментов и факторы, определяющие их активность
- •1. Основные свойства ферментов,
- •2. Активирование и ингибирование ферментов
- •3. Регуляция активности ферментов, определение активности ферментов
- •Лекция № 36. Классификация и номенклатура ферментов
- •Лекция №37-38 липиды загальні відомості, будова, класифікація хімічні властивості
- •Лекция №39-40 глицериды фосфолипиды
- •Лекция№41 жирные кислоты
- •Лекция №42 эйкозаноиды
- •Лекция №43-45 биосинтез насыщенных жирных кислот
- •Лекция №46 биосинтез триглицеридов
- •Лекция №47 метаболизм фосфолипидов
- •Лекция №48-49 биосинтез холестерина
- •Лекция №50 метаболизм кетоновых тел
- •Лекция №51-52 окисление жирных кислот
- •Лекция №53-54 углеводы строение, классификация, химические свойства
- •В животных тканях содержатся следующие моносахариды:
- •Лекция №55 переваривание и всасывание углеводов
- •Лекция №56-57 синтез и распад гликогена
- •Лекция №58-59 Тема: Биологическое окисление
- •Лекция № 60-61 гликолиз
- •Лекция№ 62 аэробный метаболизм пирувата
- •Лекция №63-64 глюконеогенез
- •Лекция 65-67 Цикл Трикарбоновых кислот.
- •Лекция № 68-69 пентозофосфатный путь окисления углеводов
- •Лекция №70 регуляция метаболизма углеводов
- •Лекция №71-72. Тема: взаимосвязь обмена белков, нуклеиновых кислот, углеводов и липидов
- •Литература
Лекция № 16-18. Сложные белки хромопротеины и нуклеопротеины
1. Определение хромопротеинов. Гемо- и флавопротеины
Хромопротеины — сложные белки, состоящие из простого белка и окрашенного небелкового компонента. Среди них выделяют гемопротеины, магнийпорфирины и флавопротеины. Хромопротеины участвуют в фотосинтезе, клеточном дыхании, окислительно-восстановительных реакциях, обеспечивают перенос кислорода и углекислого газа, свето- и цветовосприятие и др.
Гемопротеины — это хромопротеины, содержащие в качестве простетической группы железо. К ним относятся гемоглобин и его производные, миоглобин, ферменты (система цитохромов, каталаза и пероксидаза) и хлорофиллсодержащие белки. Гемоглобин — сложный белок, содержащий в качестве белкового компонента глобин, а в качестве простетической группы — гем. Гем одинаков у всех видов гемоглобина, его основу составляет порфириновое кольцо.
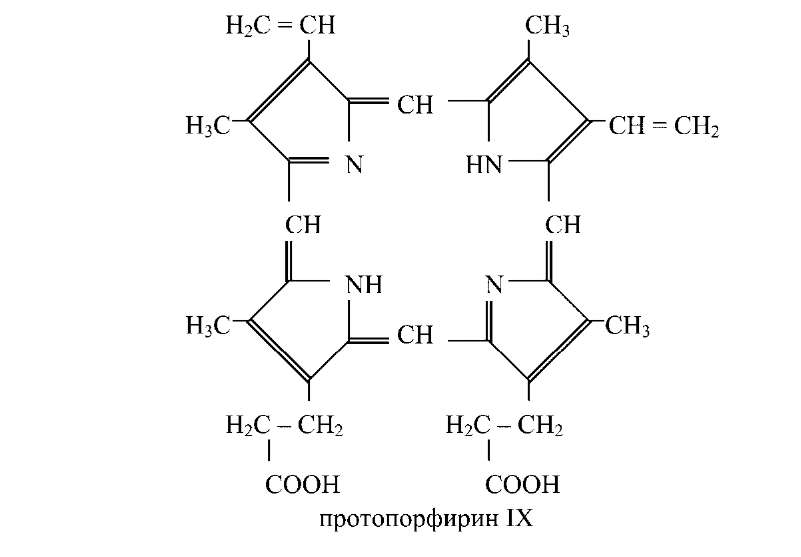

Железо связано с двумя атомами азота молекулы протопор фирина ковалентно и с двумя — координационными связями.
Гем в виде гемпорфирина является простетической группой гемоглобина и его производных, миоглобина, каталазы, пероксидазы и цитохромов b, c и c1. В цитохромах a и a3 гем содержится в виде формилпорфирина. На каждые четыре молекулы гема приходится 1 полипептидная цепь. В молекуле гемоглобина взрослого человека HbA (с англ. adult — «взрослый») содержатся четыре полипептидных цепи, составляющих белковую часть молекулы — глобин: две Р-цепи по 141 аминокислотному остатку и две α-цепи по 146 аминокислотных остатков. В крови взрослого человека также содержится HbA2, состоящий из двух δ-цепей и двух α-цепей, а в крови новорожденного — HbF (80%), состоящий из двух α-цепей и двух γ-цепей.
Существует ряд аномальных гемоглобинов, возникающих вследствие мутаций генов: HbC, HbDa, HbDe, HbE, HbG, HbG
HbI, HbM, HbO и HbS. Болезни гемоглобинов — гемоглобинозы — подразделяются на гемоглобинопатии (в основе лежит наследственное нарушение структуры цепи гемоглобина) и талассемии (обусловлены наследственным нарушением синтеза цепи гемоглобина). Классический пример наследственной гемоглобинопатии — серповидно-клеточная анемия, при которой HbS деформирует эритроциты, принимающие форму серпа, и приводит к массивному гемолизу. В результате соединения молекулярного кислорода с гемоглобином образуется оксигемоглобин. Кислород присоединяется к гему при помощи координационной связи железа. Присоединение одной молекулы кислорода к гему облегчает присоединение последующей. Гемоглобин также легко связывается с угарным газом с образованием карбоксигемоглобина и с оксидами азота с образованием метгемоглобина, содержащего ионы Fe. Накопление этих видов гемоглобина в крови приводит к снижению снабжения тканей кровью. Метод качественного определения производных гемоглобина — исследование их спектров поглощения. Трансферрины (сидерофилины) — сложные белки, характеризующиеся способностью специфично, прочно и необратимо связывать ионы Fe и других переходных металлов. Трансферрин сыворотки крови транспортирует ионы Fe в ретикулоциты, где происходит синтез гемоглобина.
Флавопротеины — сложные белки, простетические группы которых представлены изоаллоксазиновыми производными — флавинмононуклеотидом (ФМН) и флавинадениндинуклеотодом (ФАД). Флавопротеины входят в состав ферментов, катализирующих окислительно-восстановительные реакции в клетке (оксидоредуктаз). К ним относятся ксантиноксидазы, альдегидоксидазы, сукцинатдегидрогеназы, дигидрооротатдегидрогеназы, ацил-КоА-дегидрогеназы и транспортирующего электроны флавопротеина.
