- •Лекция №1 зміст, предмет та задачі дисципліни.
- •Лекция №2-4 природные α-аминокислоты. Строение классификация стереоизомерия химические свойства
- •Лекция №5 белки. Общие сведения, функции белков
- •Белки общие сведения.
- •2. Функции белков,содержание белков в органах и тканях
- •Лекция № 6-9. Физико-химические свойства белков, их структурная организация, классификация белков
- •1. Физико-химические свойства белков. Понятие структурной организации белков
- •2. Первичная и вторичная структура белка
- •3. Третичная и четвертичная структура белка
- •4. Классификация белков, химия простых белков, природные пептиды
- •Лекция № 10-12. Особенности белкового обмена, переваривание белков.
- •1. Особенности белкового обмена
- •2. Особенности переваривания белков, эндопептидазы
- •3. Переваривание белков в желудке и кишечнике
- •4. Всасывание продуктов гидролиза белков
- •5. Амины
- •Лекция № 13-15. Обезвреживание аммиака в организме, орнитиновый цикл, специфические пути обмена аминокислот.
- •1. Обезвреживание аммиака в организме
- •2. Специфические пути обмена аминокислот
- •Лекция № 16-18. Сложные белки хромопротеины и нуклеопротеины
- •1. Определение хромопротеинов. Гемо- и флавопротеины
- •2. Нуклеопротеины и липопротеины
- •3. Фосфопротеины и гликопротеины
- •Свойства иммуноглобулинов человека
- •Лекция № 19-21. Химический состав и структура нуклеиновых кислот
- •1. Химический состав нуклеиновых кислот
- •2. Особенности структуры нуклеиновых кислот
- •3. Первичная структура нуклеиновых кислот
- •4. Вторичная и третичная структура нуклеиновых кислот
- •Лекция № 22. Обмен нуклеиновых кислот
- •1. Общие представления об обмене нуклеопротеидов
- •Лекция 23-26 биосинтез днк
- •Лекция №27 биосинтез рнк, биогенез мрнк, биосинтез и распад гемоглобина
- •Биосинтез рнк, биогенез мРнк
- •3. Биогенез тРнк и рРнк, синтез рнк на матрице рнк
- •Распад нуклеиновых кислот
- •Биосинтез гемоглобина
- •Лекция № 28. Общие требования к синтезу белка
- •1. Составные части белоксинтезирующей системы, рибосомы и аминоацил-тРнк-синтетазы
- •2. Транспортные и матричные рнк, природа генетического кода
- •Лекция № 29. Синтез и постсинтетическая модификация белка
- •1. Синтез белка и его транспорт через мембраны
- •2. Транспорт синтезированных белков через мембраны
- •3. Регуляция синтеза белка
- •Лекция № 30-31. Понятие о ферментах, их химическая природа и строение
- •1. Понятие о ферментах, их химическая природа и строение
- •2. Активный центр ферментов
- •3. Изоферменты
- •Лекция № 32. Механизм действия ферментов
- •1. Механизм действия ферментов
- •2. Кинетика ферментативных реакций
- •Лекция № 34-35. Основные свойства ферментов и факторы, определяющие их активность
- •1. Основные свойства ферментов,
- •2. Активирование и ингибирование ферментов
- •3. Регуляция активности ферментов, определение активности ферментов
- •Лекция № 36. Классификация и номенклатура ферментов
- •Лекция №37-38 липиды загальні відомості, будова, класифікація хімічні властивості
- •Лекция №39-40 глицериды фосфолипиды
- •Лекция№41 жирные кислоты
- •Лекция №42 эйкозаноиды
- •Лекция №43-45 биосинтез насыщенных жирных кислот
- •Лекция №46 биосинтез триглицеридов
- •Лекция №47 метаболизм фосфолипидов
- •Лекция №48-49 биосинтез холестерина
- •Лекция №50 метаболизм кетоновых тел
- •Лекция №51-52 окисление жирных кислот
- •Лекция №53-54 углеводы строение, классификация, химические свойства
- •В животных тканях содержатся следующие моносахариды:
- •Лекция №55 переваривание и всасывание углеводов
- •Лекция №56-57 синтез и распад гликогена
- •Лекция №58-59 Тема: Биологическое окисление
- •Лекция № 60-61 гликолиз
- •Лекция№ 62 аэробный метаболизм пирувата
- •Лекция №63-64 глюконеогенез
- •Лекция 65-67 Цикл Трикарбоновых кислот.
- •Лекция № 68-69 пентозофосфатный путь окисления углеводов
- •Лекция №70 регуляция метаболизма углеводов
- •Лекция №71-72. Тема: взаимосвязь обмена белков, нуклеиновых кислот, углеводов и липидов
- •Литература
Лекция №2-4 природные α-аминокислоты. Строение классификация стереоизомерия химические свойства
α-Аминокислоты являются мономерными единицами биополимеров - пептидов и белков. Белки - основа всего живого. Функции белков в природе многообразны. Это ферменты и гормоны, выполняющие регуляторную функцию, структурные белки (кератин, коллаген), транспортные (гемоглобин), защитные (иммуноглобулины). Некоторые аминокислоты используются как лекарственные средства, например, глутаминовая кислота - при заболеваниях ЦНС, метионин - для лечения заболеваний печени, цистеин - как радиопротектор, а также в глазной практике.
В природе в свободном и связанном виде обнаружены сотни аминокислот, 20-25 из них постоянно встречаются во всех белках.
Строение и классификация природных α-аминокислот
Общая формула α-аминокислот (исключение - пролин и оксипролин):
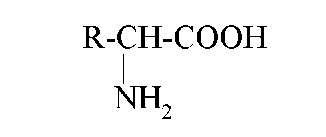
В основном используют тривиальные названия α- аминокислот. В биохимии часто пользуются сокращенными трехбуквенными названиями.
Согласно общей формуле, аминокислоты отличаются лишь строением радикала, в соответствии с чем они классифицируются на алифатические, ароматические и гетероциклические. Среди алифатических аминокислот в зависимости от наличия в радикале функциональной группы выделяют подгруппы гидрокси- и серосодержащих аминокислот.
Примеры алифатических аминокислот:

Примерами ароматических аминокислот являются фенилаланин и тирозин:
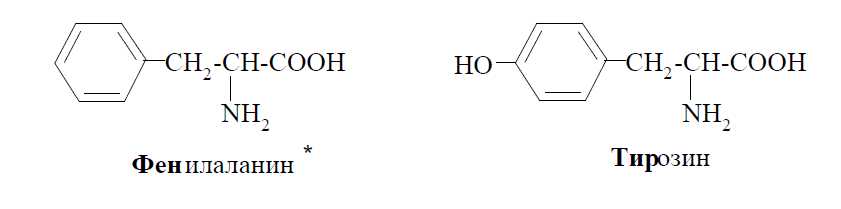
К гетероциклическим аминокислотам относятся:
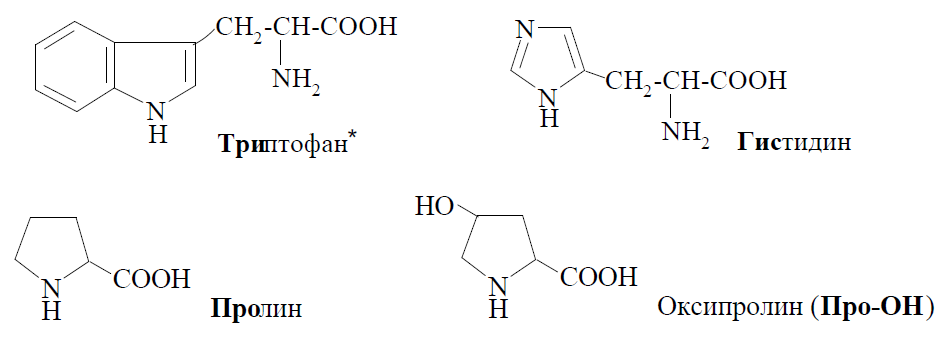
В зависимости от соотношения количества карбоксильных и аминогрупп в молекулах различают нейтральные (моноаминомонокарбоновые) - глицин, аланин и др., кислые (моноаминодикарбоновые) - аспарагиновая, глютаминовая кислоты, основные (диаминомонокарбоновые) аминокислоты - лизин, орнитин, аргинин.
Природа радикала в молекулах аминокислот значительно влияет на свойства белков. Например, наличие полярных групп (-SH, NH2, -OH, COOH, фенольного гидроксила) увеличивает растворимость белков. Кроме того, эти группы принимают участие в образовании связей, формирующих пространственную структуру белка. За счет карбоксильной и аминогруппы многие ферменты обеспечивают кислотный или основный катализ ряда биохимических процессов. Большинство α-аминокислот синтезируется в организме, но некоторые организм не способен синтезировать, они должны поступать с пищей. Эти аминокислоты называют незаменимыми, в норме их восемь: валин, лейцин, изолейцин, треонин, метионин, фенилаланин, триптофан, лизин.
Стереоизомерия α-аминокислот
Все α-аминокислоты, за исключением глицина, имеют в своей структуре хотя бы один хиральный центр, значит, для них характерна оптическая изомерия. Например, аланин существует в виде пары энантиомеров:
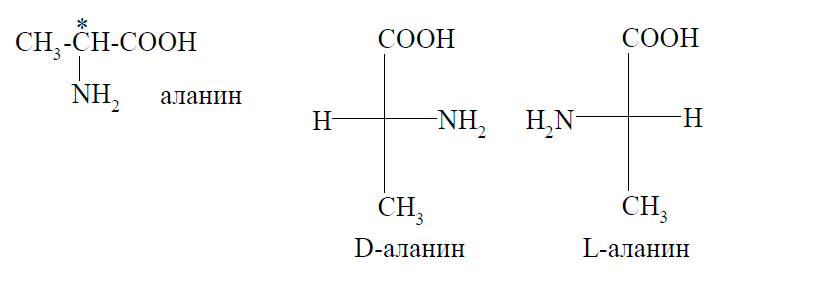
Относительная конфигурация стереоизомеров определяется в сравнении с конфигурационным стандартом - стереоизомерами глицеринового альдегида.
Все α-аминокислоты, участвующие в построении молекул белков животных и человека, имеют L-конфигурацию. D-аминокислоты встречаются в некоторых грибах и микроорганизмах.
α-Аминокислоты представляют собой кристаллические вещества с высокой температурой плавления, растворимые в воде, но не растворимые в неполярных растворителях. Эти свойства результат того, что и в кристаллическом состоянии, и в водных растворах аминокислоты существуют в виде биполярных ионов (цвиттер-ионов). Возможность образования биполярных ионов связана с амфотерностью аминокислот, в молекулах которых присутствуют и кислотные COOH-группы, и основные NH2-группы. Близость этих групп у α-аминокислот облегчает переход протона от карбокисльонй группы.
Практически α-аминокислоты в водном растворе существуют в виде равновесной смеси из цвиттер-ионов, катионной и анионной форм:
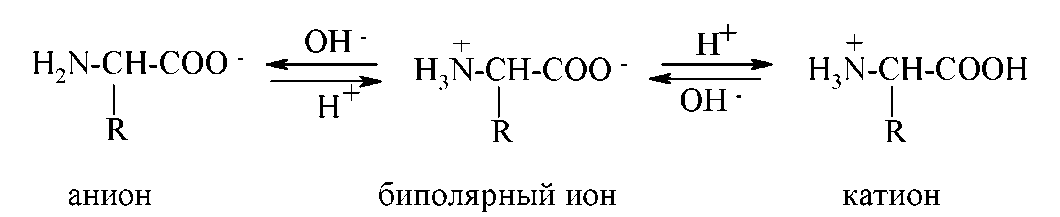
Положение такого равновесия существенно зависит от pH среды: в сильнокислой среде (pH=1-2) преобладает катионная форма, в сильнощелочной (pH=13-14) - анионная.
Если поместить раствор аминокислоты в электрическое поле, то в кислых растворах она будет мигрировать к катоду, а в щелочных - к аноду. При некотором значении pH, характерном для данной аминокислоты, она не будет перемещаться в электрическом поле. При этом значении pH, называемом изоэлектрической точкой (ИЭТ, pI), аминокислота существует в виде биполярного иона и в целом электронейтральна. Итак, изоэлектрическая точка аминокислоты - это то значение pH раствора, при котором большинство молекул данной аминокислоты существуют в виде биполярных ионов, а концентрации анионной и катионной форм минимальны и равны. Изоэлектрическая точка зависит от соотношения кислотных и основных групп в молекуле: pI кислых аминокислот имеет значение <7, pI основных аминокислот >7.
При пропускании электрического тока через раствор, содержащий смесь аминокислот, каждая из них будет двигаться к катоду или аноду со скоростью, зависящей от природы аминокислоты и pH среды. Это явление используют для разделения и анализа смеси аминокислот методом электрофореза.
Химические свойства Являясь амфотерными соединениями, аминокислоты реагируют и с кислотами, и с щелочами:
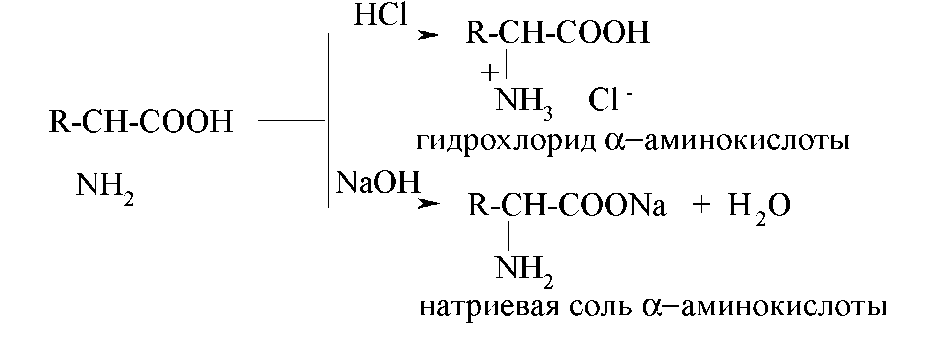
Характерной особенностью α-аминокислот является способность образовывать комплексные соли с ионами тяжелых металлов:
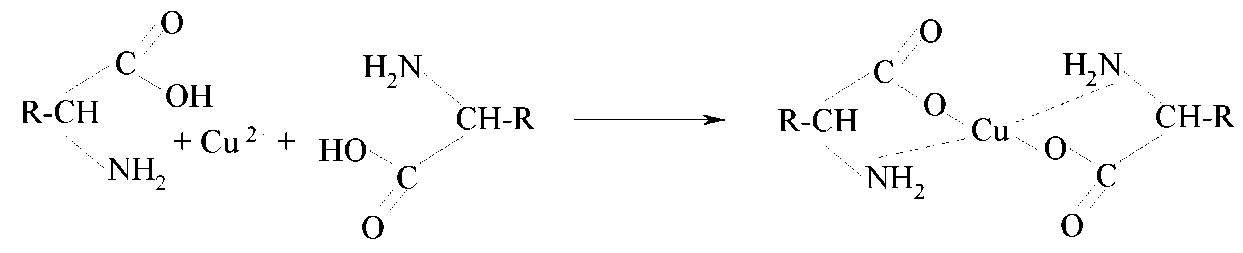
Медные соли аминокислот нерастворимы в воде, имеют интенсивное синее окрашивание. Эта реакция используется для обнаружения α-аминокислот.
Другой общей качественной реакцией α-аминокислот является их взаимодействие с нингидрином с образованием продукта сине-фиолетового цвета:
Как
карбоновые кислоты,
α-аминокислоты
образуют сложные эфиры при взаимодействии
со спиртами и хлорангидриды при
взаимодействии с тионилхлоридом или
хлоридами фосфора: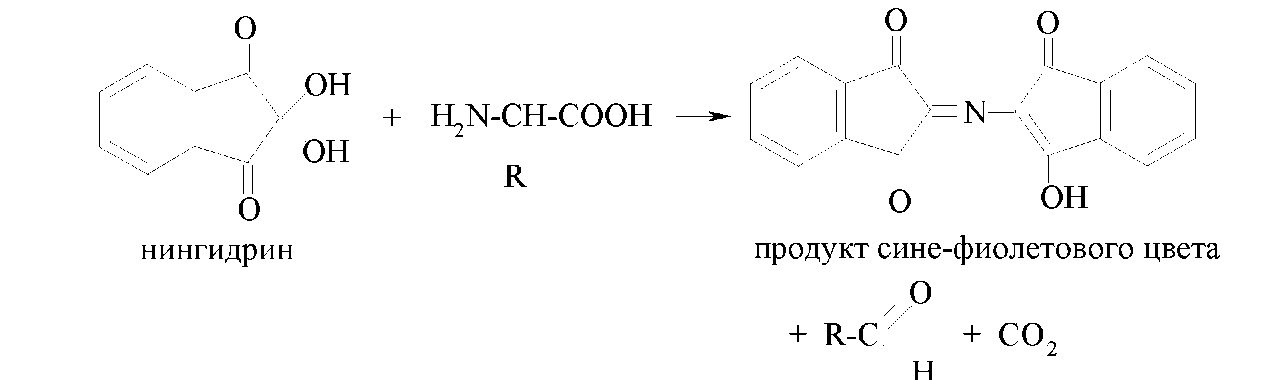
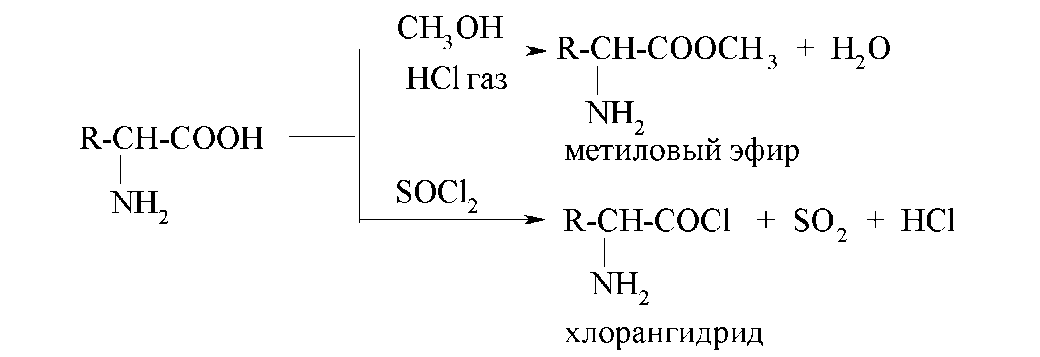
Сложные эфиры α-аминокислот летучи, они имеют сравнительно низкие температуры кипения. Это их свойство используется для разделения смеси аминокислот в белковых гидролизатах (эфирный метод Фишера). С этой целью аминокислоты сначала этерифицируют, а потом подвергают перегонке.
За счет аминогруппы α-аминокислоты подвергаются реакциям ацилирования и алкилирования, взаимодействуют с оксо- соединениями. Так, при ацилировании аминокислоты уксусным ангидридом образуется N-ацетильное производное. При взаимодействии с формальдегидом образуется продукт нуклеофильного присоединения - N-метилольное производное, которое достаточно устойчиво (с другими оксосоединениями протекает реакция нуклеофильного присоединения-отщепления).
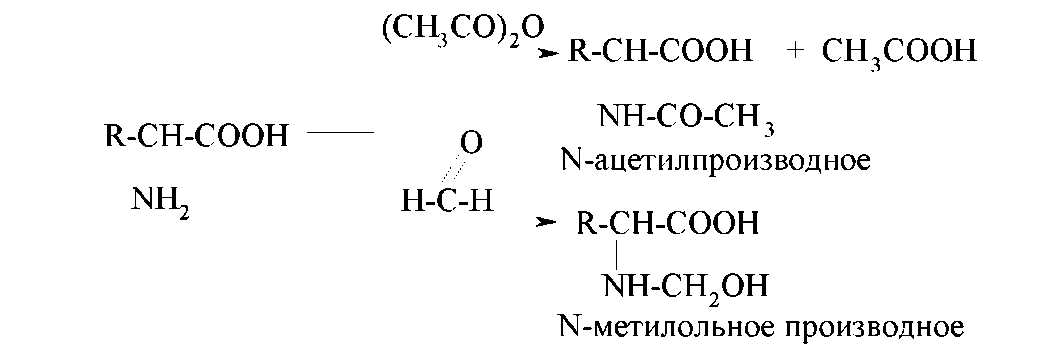
Реакцию ацилирования раньше использовали для защиты аминогруппы в синтезе пептидов. Реакция с формальдегидом лежит в основе метода количественного анализа аминокислот (метод формольного титрования, метод Зеренсена). Сущность метода формольного титрования заключается в следующем: до взаимодействия с формальдегидом растворы большинства аминокислот имеют реакцию, близкую к нейтральной; N-метилольное производное проявляет кислотные свойства и может быть оттитровано раствором щелочи с известной концентрацией.
Как первичные алифатические амины α-аминокислоты подвергаются действию азотистой кислоты с образованием соответствующих α-оксикислот и выделением азота:
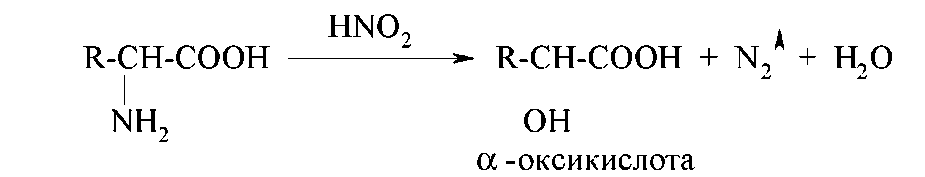
Эту реакцию называют реакцией дезаминирования in vitro. Ее используют и как качественную реакцию для доказательства наличия первичной алифатической аминогруппы (наблюдают выделение пузырьков газа), и для количественного анализа (метод Ван-Слайка) - по объему выделившегося азота рассчитывают количество аминокислоты, вступившей в реакцию.
Специфическим свойством α-аминокислот является их способность к декарбоксилированию при нагревании в присутствии гидроксида бария:
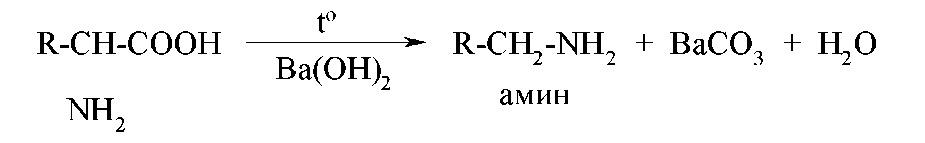
Рассмотренные выше реакции характерны для всех α- аминокислот.
Существуют также реакции на определенные группы аминокислот.
Серосодержащие аминокислоты (цистеин цистин, метионин) обнаруживают по реакции с ацетатом свинца (реакция Фоля).
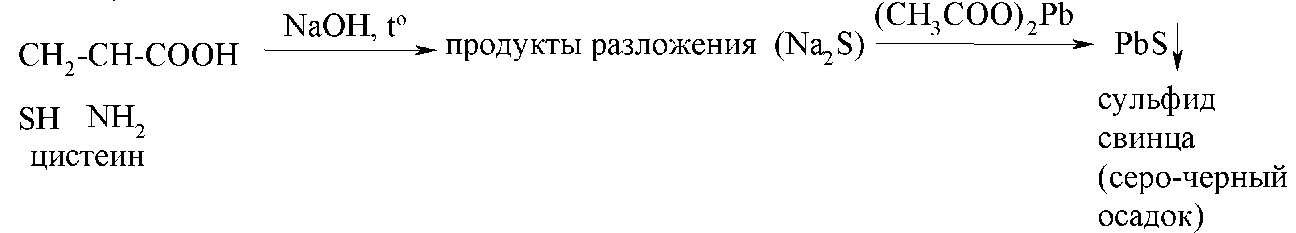
При нагревании с щелочью серосодержащие аминокислоты разлагаются, одним из продуктов разложения является сульфид натрия. При дальнейшем добавлении ацетата свинца образуется осадок сульфида свинца серо-черного цвета.
Для обнаружения
ароматических
аминокислот
используют так называемую
ксантопротеиновую реакцию.
При нагревании этих аминокислот (или
белков, в структуре которых присутствуют
их остатки) с концентрированной азотной
кислотой образуются продукты нитрования
желтого цвета, которые в щелочной
среде приобретают оранжевую окраску: