- •Лекция №1 зміст, предмет та задачі дисципліни.
- •Лекция №2-4 природные α-аминокислоты. Строение классификация стереоизомерия химические свойства
- •Лекция №5 белки. Общие сведения, функции белков
- •Белки общие сведения.
- •2. Функции белков,содержание белков в органах и тканях
- •Лекция № 6-9. Физико-химические свойства белков, их структурная организация, классификация белков
- •1. Физико-химические свойства белков. Понятие структурной организации белков
- •2. Первичная и вторичная структура белка
- •3. Третичная и четвертичная структура белка
- •4. Классификация белков, химия простых белков, природные пептиды
- •Лекция № 10-12. Особенности белкового обмена, переваривание белков.
- •1. Особенности белкового обмена
- •2. Особенности переваривания белков, эндопептидазы
- •3. Переваривание белков в желудке и кишечнике
- •4. Всасывание продуктов гидролиза белков
- •5. Амины
- •Лекция № 13-15. Обезвреживание аммиака в организме, орнитиновый цикл, специфические пути обмена аминокислот.
- •1. Обезвреживание аммиака в организме
- •2. Специфические пути обмена аминокислот
- •Лекция № 16-18. Сложные белки хромопротеины и нуклеопротеины
- •1. Определение хромопротеинов. Гемо- и флавопротеины
- •2. Нуклеопротеины и липопротеины
- •3. Фосфопротеины и гликопротеины
- •Свойства иммуноглобулинов человека
- •Лекция № 19-21. Химический состав и структура нуклеиновых кислот
- •1. Химический состав нуклеиновых кислот
- •2. Особенности структуры нуклеиновых кислот
- •3. Первичная структура нуклеиновых кислот
- •4. Вторичная и третичная структура нуклеиновых кислот
- •Лекция № 22. Обмен нуклеиновых кислот
- •1. Общие представления об обмене нуклеопротеидов
- •Лекция 23-26 биосинтез днк
- •Лекция №27 биосинтез рнк, биогенез мрнк, биосинтез и распад гемоглобина
- •Биосинтез рнк, биогенез мРнк
- •3. Биогенез тРнк и рРнк, синтез рнк на матрице рнк
- •Распад нуклеиновых кислот
- •Биосинтез гемоглобина
- •Лекция № 28. Общие требования к синтезу белка
- •1. Составные части белоксинтезирующей системы, рибосомы и аминоацил-тРнк-синтетазы
- •2. Транспортные и матричные рнк, природа генетического кода
- •Лекция № 29. Синтез и постсинтетическая модификация белка
- •1. Синтез белка и его транспорт через мембраны
- •2. Транспорт синтезированных белков через мембраны
- •3. Регуляция синтеза белка
- •Лекция № 30-31. Понятие о ферментах, их химическая природа и строение
- •1. Понятие о ферментах, их химическая природа и строение
- •2. Активный центр ферментов
- •3. Изоферменты
- •Лекция № 32. Механизм действия ферментов
- •1. Механизм действия ферментов
- •2. Кинетика ферментативных реакций
- •Лекция № 34-35. Основные свойства ферментов и факторы, определяющие их активность
- •1. Основные свойства ферментов,
- •2. Активирование и ингибирование ферментов
- •3. Регуляция активности ферментов, определение активности ферментов
- •Лекция № 36. Классификация и номенклатура ферментов
- •Лекция №37-38 липиды загальні відомості, будова, класифікація хімічні властивості
- •Лекция №39-40 глицериды фосфолипиды
- •Лекция№41 жирные кислоты
- •Лекция №42 эйкозаноиды
- •Лекция №43-45 биосинтез насыщенных жирных кислот
- •Лекция №46 биосинтез триглицеридов
- •Лекция №47 метаболизм фосфолипидов
- •Лекция №48-49 биосинтез холестерина
- •Лекция №50 метаболизм кетоновых тел
- •Лекция №51-52 окисление жирных кислот
- •Лекция №53-54 углеводы строение, классификация, химические свойства
- •В животных тканях содержатся следующие моносахариды:
- •Лекция №55 переваривание и всасывание углеводов
- •Лекция №56-57 синтез и распад гликогена
- •Лекция №58-59 Тема: Биологическое окисление
- •Лекция № 60-61 гликолиз
- •Лекция№ 62 аэробный метаболизм пирувата
- •Лекция №63-64 глюконеогенез
- •Лекция 65-67 Цикл Трикарбоновых кислот.
- •Лекция № 68-69 пентозофосфатный путь окисления углеводов
- •Лекция №70 регуляция метаболизма углеводов
- •Лекция №71-72. Тема: взаимосвязь обмена белков, нуклеиновых кислот, углеводов и липидов
- •Литература
Лекция№41 жирные кислоты
Жирные кислоты—алифатические карбоновые кислоты—в организме могут находиться в свободном состоянии (следовые количества в клетках и тканях) либо выполнять роль строительных блоков для большинства классов липидов.
В природе обнаружено свыше 200 жирных кислот, однако в тканях человека и животных в составе простых и сложных липидов найдено около 70 жирных кислот, причем более половины из них в следовых количествах. Практически значительное распространение имеют немногим более 20 жирных кислот. Все они содержат четное число углеродных атомов, главным образом от 12 до 24. Среди них преобладают кислоты, имеющие С16 и С18 (пальмитиновая, стеариновая, олеиновая и линолевая). Нумерацию углеродных атомов в жирно-кисло3тной цепи начинают с атома углерода карбоксильной группы. Примерно 3/4 всех жирных кислот являются непредельными (ненасыщенными), т. е. содержат двойные связи. Ненасыщенные жирные кислоты человека и животных, участвующие в построении липидов, обычно содержат двойную связь между (9-м и 10-м атомами углеводородов); дополнительные двойные связи чаще бывают на участке между 11-м атомом углерода и метильным концом цепи. Своеобразие двойных связей природных ненасыщенных жирных кислот заключается в том, что они всегда отделены двумя простыми связями, т. е. междуними всегда имеется хотя бы одна метиленовая группа (—СН=СН— —СН2—СН=СН—). Подобные двойные связи обозначают как «изолированные».
Систематическое название жирной кислоты чаще всего образуется путем добавления к названию углеводорода окончания – овая. Насыщенные кислоты при этом имеют окончание – ановая (например, октановая кислота — систематическое название, каприловая кислота—тривиальное название), а ненасыщенные кислоты —еновая (например, октадеценовая кислота — систематическое название, олеиновая кислота—тривиальное название) (табл. 6.1; 6.2).
Таблица Физиологически важные насыщенные жирные кислоты
Тривиальное название |
Систематическое название (IUPAC) |
Брутто формула |
Рациональная полуразвернутая формула |
Нахояедение |
Т.пл. |
рКа |
Масляная кислота |
Бутановая кислота |
C3H7COOH |
CH3(CH2)2COOH |
Сливочное масло |
-8 °С |
4,82 |
Капроновая кислота |
Гексановая кислота |
C5H11COOH |
CH3(CH2)4COOH |
Нефть |
-4 °С |
4,85 |
Каприловая кислота |
Октановая кислота |
C7H15COOH |
CH3(CH2)6COOH |
|
17 0C |
4,89 |
Пеларгоновая кислота |
Нонановая кислота |
C8H17COOH |
CH3(CH2)7COOH |
|
12,5 °С |
4.96 |
Каприновая кислота |
Декановая кислота |
C9H19COOH |
CH3(CH2)8COOH |
Кокосовое масло |
31 °С |
|
Лауриновая кислота |
Додекановая кислота |
С11Н23СООН |
СН3(СН2)10СООН |
|
43,2 °С |
|
Миристиновая кислота |
Тетрадекановая кислота |
C13H27COOH |
CH3(CH2)12COOH |
|
53,9 °С |
|
Пальмитиновая кислота |
Гексадекановая кислота |
C15H31COOH |
CH3(CH2)14COOH |
|
62,8 °С |
|
Маргариновая кислота |
Гептадекановая кислота |
С16Н33СООН |
CH3(CH2)15COOH |
|
61,3 °С |
|
Стеариновая кислота |
Октадекановая кислота |
C17H35COOH |
CH3(CH2)16COOH |
|
69,6 °С |
|
Арахиновая кислота |
Эйкозановая кислота |
C19H39COOH |
CH3(CH2)18COOH |
|
75,4 °С |
|
Бегеновая кислота |
Докозановая кислота |
C21H43COOH |
СН3(СН2)20СООН |
|
|
|
Лигноцериновая кислота |
Тетракозановая кислота |
C23H47COOH |
CH3(CH2)22COOH |
|
|
|
Церотиновая кислота |
Гексакозановая кислота |
С25Н51СООН |
СН3(СН2)24СООН |
|
|
|
Монтановая кислота |
Октакозановая кислота |
С27Н55СООН |
СН3(СН2)2бСООН |
|
|
|
Таблица Физиологически важные ненасыщенные жирные кислоты
Тривиальное название |
Систематическое название (IUPAC) |
Брутто формула |
IUPAC формула (с карб.конца) |
Рациональная полуразвернутая формула |
Лауроолеиновая кислота |
цис-9-додеценовая кислота |
С11Н21СООН |
12:1Δ9 |
CH3-CH2- СН=СН-(СН2)7-СООН |
Миристоолеиновая кислота |
цис-9-тетрадеценовая кислота |
C13H25COOH |
14:1Δ9 |
CH3-(CH2)3- СН=СН-(СН2)7-СООН |
Пальмитолеиновая кислота |
цис-9-гексадеценовая кислота |
C15H29COOH |
16:1 Δ9 |
CH3-(CH2)5- СН=СН-(СН2)7-СООН |
Олеиновая кислота |
цис-9-октадеценовая кислота |
C17H33COOH |
18:1 Δ9 |
CH3-(CH2)7- СН=СН-(СН2)7-СООН |
Элаидиновая кислота |
транс-9-октадеценовая кислота |
C17H33COOH |
18:1 Δ9 |
CH3-(CH2)7- СН=СН-(СН2)7-СООН |
Цис-вакценовая кислота |
цис-11-октадеценовая кислота |
C17H33COOH |
18:1 Δ11 |
CH3-(CH2)5- СН=СН-(СН2)9-СООН |
Транс-вакценовая кислота |
транс-11-октадеценовая кислота |
C17H33COOH |
18:1Δ11 |
CH3-(CH2)5- СН=СН-(СН2)9-СООН |
Гадолеиновая кислота |
цис-9-эйкозеновая кислота |
C19H37COOH |
19:1 Δ9 |
CH3-(CH2)9- СН=СН-(СН2)7-СООН |
Гондоиновая кислота |
цис-11 -эйкозеновая кислота |
C19H37COOH |
20:1Δ11 |
CH3-(CH2)7- СН=СН-(СН2)9-СООН |
Эруковая кислота |
цис-9-доказеновая кислота |
C21H41COOH |
22:1Δ9 |
CH3-(CH2)H- СН=СН-(СН2)7-СООН |
Нервоновая кислота |
цис-15-тетракозеновая кислота |
C23H45COOH |
23:1Δ15 |
CH3-(CH2)7- CH=CH-(CH2)13-COOH |
Линолевая кислота |
цис,цис-9,12-октадекадиеновая кислота |
C17H31COOH |
18:2Δ9,12 |
CH3(CH2)-(CH2- СН=СН)2-(СН2)7-СООН |
γ-линоленовая кислота |
цис,цис,цис-6,9,12- октадекатриеновая кислота |
C17H29COOH |
18:3Δ9,12,15 |
CH3-(CH2)-(CH2-СН=СН)3-(СН2)6-СООН |
а-линоленовая кислота |
цис,цис,цис-9,12,15-октадекатриеновая кислота |
C17H29COOH |
18:3Δ9,12,15 |
СН3-(СН2-СН=СН)3-(СН2)7-СООН |
Арахидоновая кислота |
цис-5,8,11,14-эйкозотетраеновая кислота |
C19H31COOH |
20:4Δ5,8,11,14 |
СН3-(СН2)4-(СН=СН-СН2)4-(СН2)2-СООН |
В соответствии с систематической номенклатурой количество и положение двойных связей в ненасыщенных жирных кислотах часто обозначают с помощью цифровых символов: например, олеиновую кислоту как 18:1;9, линолевую кислоту как 18:2;9,12, где первая цифра—число углеродных атомов, вторая — число двойных связей, а следующие цифры — номера ближайших к карбоксилу углеродных атомов, вовлеченных в образование двойной связи.
В специальной литературе жирные кислоты часто изображают в виде зигзагообразной вытянутой линии, отражающей жесткость валентного угла атомов углерода в 111° для насыщенной и в 123° — для двойной связи. Однако такая конформация является условной и справедлива только для случая, когда жирная кислота находится в кристаллическом состоянии. В растворах жирно-кислотная цепь может образовывать бесчисленное количество конформаций вплоть до клубка, в котором имеются и линейные участки различной длины в зависимости от числа двойных связей. Клубки могут слипаться между собой, образуя так называемые мицеллы. В последних отрицательно заряженные карбоксильные группы жирных кислот обращены к водной фазе, а неполярные углеводородные цепи спрятаны внутри мицеллярной структуры. Такие мицеллы имеют суммарный отрицательный заряд и в растворе остаются суспендированными благодаря взаимному отталкиванию.
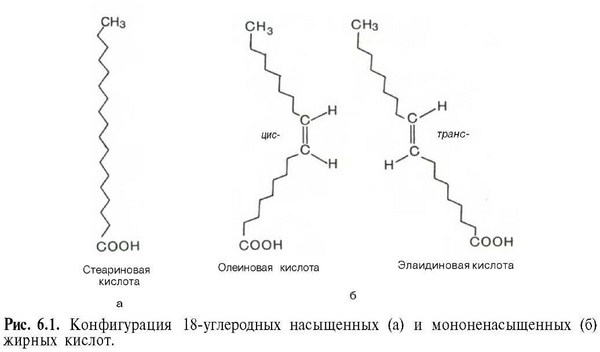
Известно также, что при наличии двойной связи в жирнокислотной цепи вращение углеродньгх атомов относительно друг друга ограничено. Это обеспечивает существование ненасыщенных жирных кислот в виде геометрических изомеров (рис. 6.1), причем природные ненасыщенные жирные кислоты имеют цис-конфигурацию и крайне редко транс-конфигурации. Считают, что жирной кислоте с несколькими двойными связями цис-конфигурация придает углеводородной цепи изогнутый и укороченный вид. По этой причине молекулы этих кислот занимают больший объем, а при образовании кристаллов упаковываются не так плотно, как транс-изомеры. Вследствие этого цис-изомеры имеют более низкую температуру плавления (олеиновая кислота, например, при комнатной температуре находится в жидком состоянии, тогда как элаидиновая — в кристаллическом). Цис-конфигурация делает ненасыщенную кислоту менее стабильной и более подверженной катаболизму.